22 серпня, 2015
Синдром увеличения лимфатических узлов у детей

Довольно часто педиатры сталкиваются с проблемой увеличения периферических лимфатических узлов. Данное состояние в клинической практике часто называют лимфаденопатией. Синдром лимфаденопатии (ЛАП) встречается при большой группе различных заболеваний и представляет собой увеличение лимфатических узлов (ЛУ) одной или нескольких групп, в основном за счет гиперплазии фолликулов лимфоидной ткани. Увеличение лимфоузлов может быть начальным симптомом реактивных состояний, а может и свидетельствовать о первичной локализации в них злокачественных процессов. На современном этапе недостаточно поставить диагноз ЛАП, необходима также тщательная его расшифровка с целью не только определить генез заболевания и принять единственно правильное решение по ведению больного, но и обнаружить первичный патологический процесс, то есть идентифицировать ЛАП. Возникает вопрос: свидетельствует ли лимфаденопатия о каком-нибудь патологическом состоянии в организме ребенка или же это вариант нормы? Ведутся дискуссии по поводу пальпируемых зон ЛУ, а также их нормальных размеров.
В целом, увеличение ЛУ в 70% случаев носит не злокачественный, а доброкачественный характер (реактивный процесс, системные инфекции). Увеличение лимфатических узлов, наблюдающееся менее двух недель или более года, без прогрессирующего изменения их размеров очень редко свидетельствует о злокачественном процессе. Как правило, лимфатические узлы уменьшаются на протяжении нескольких недель или месяцев. При определенных обстоятельствах лимфоузел может оставаться слегка увеличенным в течение многих лет. В этом случае его увеличение не служит поводом для беспокойства. Тревогу должно вызывать прогрессирующее беспричинное увеличение лимфоузла в течение нескольких недель.
Для понимания патогенеза лимфаденопатиии следует напомнить, что лимфоидная система – это часть иммунной системы, которая выполняет множество функций. Лимфатический узел – это своего рода биологический фильтр, который задерживает патогенные микроорганизмы и клетки злокачественных опухолей. Рассматривая с этой позиции увеличение ЛУ, нужно ответить на вопрос – увеличение лимфатического узла произошло вследствие локальной проблемы или это системный ответ с вовлечением других лимфоидных органов? Таким образом, увеличение ЛУ – это показатель наличия иммунного ответа.
Что же следует считать нормой для лимфатического узла? Нормальные ЛУ мягко-эластической консистенции, бобовидной или округлой формы, с гладкой поверхностью, безболезненные, умеренно подвижные, не спаянные с окружающими тканями, кожа над ними не изменена. Относительно их размеров общего мнения не существует, но практика показывает, что многое зависит от локализации ЛУ – поверхностные шейные, подчелюстные, подмышечные – до 1,5-2,0 см, паховые – до 3 см. Но существуют «опасные зоны», где любой пальпируемый ЛУ подозрителен (например, надключичные зоны – для злокачественных поражений, локтевой ЛУ – для феллиноза [болезнь кошачей царапины], левая подмышечная область у детей до 1 года – БЦЖ-лимфаденит [осложнение после прививки против туберкулеза вакциной из штамма Mycobacterium bovis BCG]).
Для унифицированной оценки состояния ЛУ разными специалистами (педиатром, гематологом, инфекционистом и др.) необходимо пользоваться общепринятой характеристикой, которая позволяет оценить следующие моменты:
- Локализацию увеличенных ЛУ – название группы и характер поражения (одно- или двустороннее).
- Размеры и формы ЛУ – величина описывается только в метрических единицах – сантиметры или миллиметры (нельзя сравнивать ЛУ с фруктами, ягодами, орехами, зерном и т. п.). ЛУ имеет два размера – поперечный и продольный, отсюда определяется и форма ЛУ – округлая, когда продольный размер равен поперечному (может быть указан один размер – диаметр), или овальная, когда продольный размер больше поперечного (указываются оба размера).
- Количество – если в каждой группе пальпируется не больше 2 ЛУ, то принято говорить о единичных ЛУ, если пальпируется 3 ЛУ и более, то говорят о множественных ЛУ.
- Консистенция – ЛУ может быть эластичный, плотный, мягкий, указывается наличие флюктуации.
- Болезненность – определяется в покое и при пальпации.
- Связь с окружающими тканями – нормальные ЛУ не спаяны друг с другом и с окружающими тканями, подвижны.
- Состояние кожных покровов над ЛУ – возможны гиперемия, отечность (симптомы воспаления), наличие венозной сети (свидетельствует о дополнительном шунтовом кровотоке, что характерно для специфического процесса), выраженность капиллярной сети (сопутствует хроническим очагам инфекции), свищи.
- Наличие компрессионного синдрома – сдавление крупных венозных стволов, в первую очередь верхней полой вены, – синдром верхней полой вены; сдавление трахеи и крупных бронхов – кашель и одышка; сдавление пищевода – дисфагия (нарушение прохождения пищи).
Обязательно исследование других лимфоидных органов (лимфоглоточное кольцо Вальдеера, печень и селезенка, тимус). Исследование этих органов дает представление о наличии системного процесса.
ЛУ можно распределить на поверхностные (периферические) и глубокие. Для исследования у здорового и больного ребенка наиболее доступны многочисленные группы периферических ЛУ, располагающихся в подкожно-жировой клетчатке, по ходу мышц и крупных сосудов. Различают следующие зоны (области, регионы) периферических ЛУ:
- шейная – формируется подчелюстной, шейными, надключичной, заушной, затылочной группами ЛУ;
- подмышечная – группа подмышечных ЛУ;
- локтевая (кубитальная) – группа кубитальных ЛУ;
- торакальная – группы ЛУ по краю большой грудной мышцы;
- паховая – группа паховых ЛУ;
- подколенная – группа подколенных ЛУ.
До 7-летнего возраста в норме пальпируются пять групп ЛУ: передне- и заднешейные, подчелюстные, подмышечные, паховые. У здорового ребенка старше 7 лет могут быть доступны пальпации 3 группы ЛУ: передне-, заднешейные и подчелюстные при сохранении характеристик нормального ЛУ, и только у 1,5-2% остаются доступными для пальпации паховые и подмышечные ЛУ.
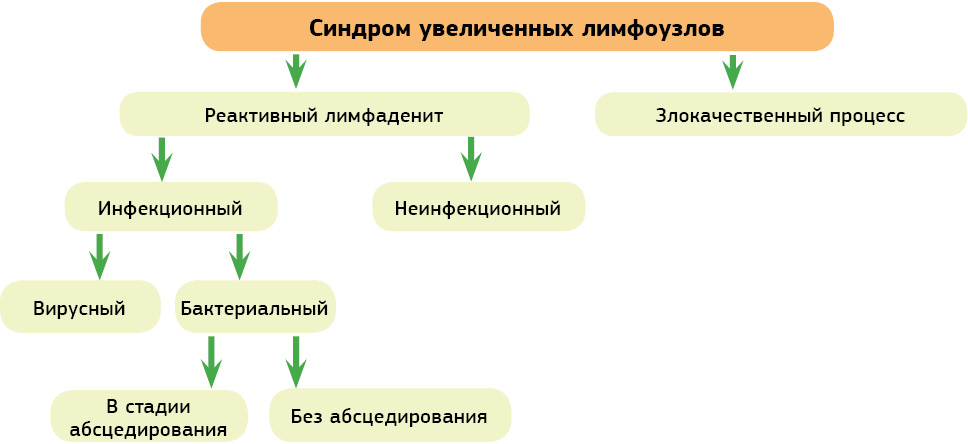
Следует остановиться на проблеме использования терминов «лимфаденит» и «лимфаденопатия». С нашей точки зрения, некорректно использовать термин «лимфаденопатия», так как это не дает понимания причины синдрома увеличенных лимфоузлов, а следовательно, и правильной тактики лечения. Более удобно использовать разделение синдрома увеличенных лимфоузлов на реактивный лимфаденит и на увеличение лимфоузлов злокачественного происхождения (рис. 1).
Отсюда и возникает вопрос – всегда ли при увеличенных лимфоузлах целесообразно лечение антибиотиками и когда есть показания к оперативному лечению?
Как правило, основная жалоба родителей – это наличие опухолевидного образования в определенных зонах. Чаще это заднебоковые и переднебоковые поверхности шеи, затылочные, подмышечные, паховые зоны, реже – надключичные, локтевые. Поэтому необходимо помнить о путях лимфооттока от различных органов, что помогает сузить спектр заболеваний при постановке окончательного диагноза. Наиболее частые и типичные причины увеличения ЛУ разных локализаций рассмотрены в таблице 1.
Таблица 1. Причины увеличения лимфатических узлов у детей [С. Твист, М. Линк, 2002]
|
Инфекции |
Бактериальные: Staphylococcus aureus, β-гемолитический стрептококк группы А, возбудители бруцеллеза, туляремии, болезни кошачьей царапины (Bartonella henselae) Вирусные: инфекционный мононуклеоз (вирус Эпштейна – Барр), цитомегаловирус, вирус иммунодефицита человека, вирусы краснухи, кори Микобактерии: M. tuberculosis, атипичные микобактерии Протозойные: токсоплазма, малярийный плазмодий Грибковые: возбудители гистоплазмоза, кокцидиомикоза, аспергиллеза |
|
Аутоиммунные заболевания |
Ювенильный ревматоидный артрит, системная красная волчанка, сывороточная болезнь |
|
Болезни накопления |
Болезнь Нимана – Пика, болезнь Гоше |
|
Медикаментозные |
Противосудорожные препараты (фенитоин), аллопуринол, изониазид |
|
Поствакцинальные |
Вакцинация БЦЖ и др. |
|
Злокачественные опухоли |
Лимфомы, лейкозы, метастазы солидных опухолей (нейробластома, рабдомиосаркома, опухоли щитовидной железы, назофарингеальный рак) |
|
Гистиоцитозы |
Гистиоцитоз из клеток Лангерганса, гемофагоцитарные синдромы, синусовый гистиоцитоз с массивной лимфаденопатией (болезнь Розаи – Дорфмана) |
|
Иммунодефицитные состояния |
Хроническая гранулематозная болезнь, дефицит адгезии лейкоцитов |
|
Другие |
Саркоидоз, болезнь Кавасаки, болезнь Кастлемана, болезнь Кикучи |
При выявлении опухолевидного образования в типичных зонах лимфооттока небходимо ответить на несколько вопросов:
- лимфоузел ли это вообще;
- если это ЛУ, то каковы его характеристики (форма, размер, консистенция, болезненность, подвижность, одиночный или конгломерат, поражение региона или диффузный характер);
- процесс локальный или системный;
- есть ли вовлечение других лимфоидных и паренхиматозных органов, легких, кожи.
Чаще всего увеличиваются шейные ЛУ вследствие анатомических особенностей этого региона (проблемы ЛОР-органов; стоматологические проблемы; основной лимфодренаж в кровеносное русло происходит именно на шее).
Пальпируемое образование в области шеи – довольно частая находка при осмотре детей. Для более четкой диагностики обязательно ультразвуковое исследование (УЗИ). Заболевания, способные проявляться наличием объемного образования в области шеи [А. Леун, В. Робсон, 2004]:
- эпидемический паротит – отек локализуется в области угла нижней челюсти, тогда как шейные ЛУ расположены под ней;
- киста подъязычной области – локализуется между подъязычной костью и яремной вырезкой грудины, при глотании или высовывании языка движется вверх;
- киста жаберной щели – гладкое флюктуирующее образование, расположенное по нижнему переднему краю грудинно-ключично-сосцевидной мышцы;
- фиброз грудинно-ключично-сосцевидной мышцы – плотное веретеноподобное образование, возникшее вследствие перинатального кровоизлияния в мышцу с последующим фиброзом; подвижно в горизонтальном и не подвижно в вертикальном направлении. Как правило, сопровождается кривошеей;
- шейные ребра – ортопедическая аномалия, как правило, двусторонняя; образование плотное и неподвижное. Диагноз подтверждается при рентгенологическом исследовании;
- кистозная гигрома – многополостная выстланная эндотелием киста мягкой консистенции, сжимающаяся при надавливании, содержит лимфатическую жидкость, просвечивается при диаскопии;
- гемангиома – врожденная сосудистая аномалия, выявляющаяся в родах или сразу после них; обычно красного или синюшного цвета;
- ларингоцеле – мягкое кистозное образование, выдающееся из гортани через тироидную мембрану и увеличивающееся при выполнении пробы Вальсальвы (натуживание на выдохе при закрытом носовом и ротовом отверстии). Может вызывать затруднение дыхания и хрипоту;
- дермоидная киста – расположенная по средней линии киста, содержащая плотные и кистозные фрагменты;
- новообразования щитовидной железы.
При клиническом обследовании ведущую роль играет пальпация лимфатических узлов. Рекомендуем такой порядок обследования ЛУ (сверху вниз):
- затылочная область, далее заушная область и заднешейный регион;
- приушные, подбородочные, подчелюстные, затем переднешейный регион, надключичные области;
- подмышечные области, опускаясь вниз на 15-20 см вдоль боковых поверхностей грудной клетки;
- локтевые сгибы;
- паховые области (начиная от лобка, параллельно паховым складкам в бедренных треугольниках);
- подколенные сгибы.
Минимальный рекомендуемый план обследования включает проведение общего анализа крови.
Таким образом, 1-й шаг – это оценка клинических признаков и результатов общего анализа крови.
После этого следует решить вопрос, к какому шагу следует перейти далее:
- использовать тактику наблюдения («watch and wait»);
- назначить терапию антибиотиками;
- провести более глубокое клиническое обследование:
- развернутый анализ крови с оценкой количества тромбоцитов и анализ мочи;
- УЗИ лимфоузлов региона поражения, лимфоузлов других регионов;
- УЗИ брюшной полости;
- УЗИ тимуса;
- рентгенография органов грудной клетки в 2 проекциях (прямой и правой боковой);
- далее по показаниям, в зависимости от направления дифференциального диагноза, проведение компьютерной (КТ) или магнитно-резонансной томографии (МРТ), костно-мозговая пункция, определение маркеров инфекций, иммунологические исследования и т.д.
Выявление дополнительных признаков при первичном осмотре больных:
- обязательное исследование периферической крови при первичном обращении больного;
- диагностический поиск с учетом выявленных дополнительных признаков;
- наблюдение за больными в течение 2-4 недель при «остром» увеличении ЛУ;
- назначение антибиотиков только в случаях доказанной бактериальной инфекции;
- нецелесообразность назначения глюкокортикоидов при неясных лимфаденопатиях;
- строгие показания к биопсии лимфатического узла (плотные, безболезненные ЛУ размером более 2 см2).
Однако существует еще целый ряд тревожных признаков, которые по отдельности или в сочетании могут ускорить принятие решения врачом о проведении первичной открытой биопсии ЛУ:
- размеры ЛУ более 2 см2;
- увеличение размеров ЛУ в течение 2 недель без явных причин;
- отсутствие уменьшения размеров ЛУ в течение 4-6 недель;
- отсутствие «нормализации» размеров ЛУ в течение 8-12 недель;
- отсутствие уменьшения размеров ЛУ после 1-2 курсов антибактериальной терапии;
- отсутствие признаков инфекции ЛОР-органов и стоматологических проблем;
- изменения на рентгенограммах органов грудной клетки;
- наличие общих симптомов (лихорадка, потеря веса, артралгии, гепатоспленомегалия), высыпаний на коже.
До установления точного диагноза пациентам с синдромом увеличенных лимфоузлов не назначают гормональные препараты, цитостатики, физиотерапевтические процедуры.
При наличии данных о локальном воспалительном характере увеличения ЛУ (острый лимфаденит) можно начинать антибактериальную терапию.
Если же лечение неэффективно или изначально есть подозрение на системный инфекционный процесс, следует провести соответствующие исследования (например, на наличие антител к возбудителю псевдотуберкулеза, иерсиниоза, токсоплазмоза; цитомегаловирусной инфекции или вируса Эпштейна – Барр). Коррекция лечения производится при получении соответствующих результатов; при необходимости проводится консультация инфекциониста.
В план обследования необходимо включать и проведение реакции Манту (хотя интерпретация результатов возможна только на основе анализа клинических данных, эпидемиологического анамнеза, данных о предыдущих результатах постановки этой пробы, результатов рентгенографии органов грудной клетки и, иногда, гистологической картины после биопсии). При необходимости проводится консультация фтизиатра.
При подозрении на злокачественный процесс необходимо провести костно-мозговую пункцию; при отрицательном результате анализа материала – открытую биопсию ЛУ, КТ региона поражения, органов грудной клетки и брюшной полости с внутривенным контрастированием.
Бактериальный лимфаденит – болезненное увеличение лимфоузла вследствие прямого действия инфекционного агента на ткань лимфоузла (чаще реактивного характера), то есть чаще всего имеется причина (например, периодонтит, подчелюстной лимфаденит). В зависимости от вирулентности флоры и реактивности организма возникают симптомы той или иной степени выраженности – боль, отек, местная и системная гипертермия.
Стадии развития лимфаденита (табл. 2):
- стадия инфильтрации – на этом этапе эффективна антибактериальная терапия;
- стадия абсцедирования – на этом этапе необходимо хирургическое лечение.
Таблица 2. Дифференциальная диагностика лимфаденита в стадии инфильтрации и абсцедирования
|
Лимфаденит в стадии инфильтрации |
Лифаденит в стадии абсцедирования |
|
|
Боль |
Постоянная, ноющая |
Усиливается больше к вечеру и ночью, может быть пульсирующей |
|
Местная гипертермия |
Нет |
Да |
|
Системная гипертермия |
Субфебрилитет или фебрилитет |
Фебрилитет или гектическая лихорадка |
|
Локальный отек мягких тканей |
Нет |
Есть |
|
Рамягчение, флюктуация тканей лимфоузла |
Нет |
Есть |
|
Изменения общего анализа крови |
Умеренный лейкоцитоз (с/без сдвига формулы влево) |
Выраженый лейкоцитоз (со сдвигом формулы влево) |
|
Картина УЗИ |
Отек и инфильтрация тканей лимфоузла |
Появление жидкостных очагов в ткани лимфоузла и окружающих тканях |
|
Лечение |
Антибиотикотерапия |
Хирургическое |
При обследовании и лечении детей до 1 года с лимфаденитами необходимо помнить, что у них легко возникает аденофлегмона. Это обусловлено анатомическими особенностями строения лимфоузла – в этом возрасте капсула лимфоузла неплотная, имеет «поры», поэтому воспалительный экссудат легко проникает в окружающие ткани (подкожно-жировую клетчатку), что способствует быстрому местному распространению процесса и нагноению. Поэтому важно вовремя отдать ребенка в руки хирургов. Ответ на терапию возможно контролировать с помощью УЗИ (повторное исследование через 5-7 дней; необходимо обращать внимание на УЗИ-признаки абсцедирования, так как под действием антибиотиков может образоваться «холодный абсцес»). При хорошем ответе на антибактериальную терапию достаточно 7-10-дневного курса, при недостаточном необходимо сменить препарат через 3-5 дней на антибиотик другой группы. Если же и после 2 курсов антибактериальной терапии лимфоузел не уменьшается, то следует рассмотреть возможность проведения открытой биопсии. Показания к открытой биопсии ЛУ:
- проведенное обследование дает основание для постановки диагноза злокачественного заболевания;
- размеры ЛУ больше 2,5 см и проведенное обследование не позволило определить диагноз;
- заболевание персистирует или прогрессирует, несмотря на предпринимаемую антибактериальную терапию (Е.В. Самочатова, 2004).
Проблема пункции лимфоузлов. Особенно следует обратить внимание на низкую диагностическую ценность тонкоигольной аспирационной биопсии лимфоузла. Несмотря на то, что в литературе этот метод широко описан, его практическое значение и целесообразность вызывают сомнения.
Показания к пункции лимфоузла ограничены такими ситуациями: наличие подозрения на абсцедирование лимфоузла (пункция дает ответ на вопрос: есть гной или нет?). Пункцию необходимо проводить достаточно толстой иглой, т. к. тонкая игла закупориваеться густым гноем и фибрином и при проведении тонкоигольнй аспирации в шприце может ничего не оказаться.
При получении гноя следует раскрыть и дренировать гнойник, при отсутствии – пункционный материал необходимо отправить на цитологическое исследование, провести бактериоскопию и посев на микрофлору (до получения результатов проводится антибактериальная терапия). Иногда в таких ситуациях получают ложноположительный ответ на наличие атипических клеток. Это обусловлено тем, что при выраженом воспалительном процессе лимфоидная ткань приобретает «извращенные» морфологические признаки (даже гистологического исследования в таких случаях иногда недостаточно для определения природы заболевания – приходится обращаться к иммуногистохимическим и цитохимическим методикам). Вторая причина ложноположительных ответов – «crush-синдром» клеток (при аспирации тканевого материала в шприц под большим разрежением через тонкую иглу происходит повреждение клеток, что симулирует атипизм этих клеток). Ложноположительные цитологические результаты приводят к необоснованным биопсиям (часто при инфекции вирусом Эпштейна – Барр, аутоиммунных заболеваниях, иммунодефицитах). Установление окончательного диагноза злокачественной опухоли возможно только после гистологического заключения!
Заподозрить злокачественное поражение можна чаще по клинической картине, потому и чаще проводят открытую биопсию лимфоузла, минуя тонкоигольную аспирационную биопсию. Если же проведена пункция и обнаружены атипичные клетки в пунктате – это все равно показание к открытой биопсии лимфоузла. Кроме того, достаточно большая доля ложноотрицательных результатов при тонкоигольных биопсиях (когда злокачественное поражение есть, но в аспирате цитолог не увидел атипичных клеток) обусловлена тем, что часто на начальних стадиях онкопроцесса распределение опухолевых клеток в ткани лимфоузла происходит не диффузно, а очагово, и если игла не попала в очаг поражения – атипичных клеток в пунктате не будет. Ложноотрицательные результаты очень опасны тем, что затягивается время постановки правильного диагноза, что при онкопатологии может привести к фатальным результатам.
Поэтому считаем, что тонкоигольная биопсия для установления окончательного диагноза показана очень ограниченому количеству пациентов при наличии опытного цитолога и возможности применить дополнительные цитологические методы исследования (цитохимический или цитогенетический).
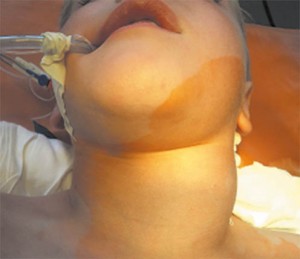 Рисунок 2. Лимфогранулематоз (пакет лимфоузлов на шее слева). Ребенок подготовлен к биопсии лимфоузлов шеи
Рисунок 2. Лимфогранулематоз (пакет лимфоузлов на шее слева). Ребенок подготовлен к биопсии лимфоузлов шеиБиопсия лимфоузла позволяет ответить на многие вопросы, а свести к минимуму риск ошибки при проведении этой процедуры позволяют следующие правила (рис. 2):
- следует проводить биопсию самого большого лимфоузла;
- предпочтительней проводить биопсию того лимфоузла, который увеличился раньше;
- биопсию следует проводить эксцизионным методом (удаляется весь лимфоузел без нарушения его целостности);
- по возможности, если это не приведет к отрицательным последствиям, проводят биопсию нескольких лимфоузлов;
- если есть несколько регионов поражения, следует проводить биопсию в каждом регионе (для точного стадирования и определения объема лучевой и химиотерапии). Реже верификацию состояния лимфоузлов разных регионов поражения можно проводить по схеме: открытая биопсия первичного региона поражения + аспирационная биопсия (при тяжелом состоянии больного и других противопоказаниях);
- рекомендовано проведение интраоперационной костно-мозговой пункции (если не была произведена ранее) и/или трепан-биопсии костного мозга;
- при подозрении на злокачественный процесс желательно проведение иммуногистохимического исследования биопсийного материала.
Эти правила касаются биопсии лимфоузлов как наружной, так и внутренней локализации (внутрибрюшных, внутригрудных).
Несмотря на широкий арсенал медикаментозных средств, которые активно рекламируются и используются большинством врачей для лечения лимфаденитов, хочется отметить, что единственным доказанным эффективным средством лечения банального острого лимфаденита есть системное применение антибиотиков. От применения десенсибилизирующих средств, витаминов и «лимфотропных» препаратов следует воздерживаться в виду их неэффективности. От тепловых процедур необходимо отказаться! Тепловые процедуры значительно увеличивают частоту нагноений. Да и, в принципе, не наблюдается позитивного эффекта от применения «балластных» препаратов и местных тепловых процедур и при системных процессах, а уж тем более при злокачественных, аутоиммунных и других заболеваниях, которые приводят к увеличению лимфатических узлов.
Следует помнить, что увеличение лимфоузлов может иметь «наружную» локализацию и скрытую (ЛУ средостения, брюшной полости). Напомним, что любое увеличение интраабдоминальных или внутригрудных лимфоузлов должно настораживать.
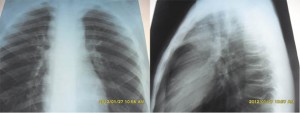 Рисунок 3. Данные рентгенографии: расширение тени средостения за счет конгломерата увеличенных лимфоузлов, поражение переднего средостения
Рисунок 3. Данные рентгенографии: расширение тени средостения за счет конгломерата увеличенных лимфоузлов, поражение переднего средостенияУвеличение внутригрудных лимфоузлов более характерно для злокачественных лифопролиферативных заболеваний (лимфома, лейкоз, метастазы других опухолей) – при этих патологиях в подавляющем большинстве случаев увеличиваются лимфоузлы передне-верхнего средостения, а лимфоузлы корня легкого – реже. При туберкулезном адените чаще увеличиваются лимфоузлы корня легкого (инфицирование туберкулезом происходит воздушно-капельным путем, микобактерии туберкулеза оседают в бронхах или альвеолах, поэтому реагируют регионарные ЛУ, а именно ЛУ корня легкого). Но в любом случае увеличение внутригрудных ЛУ – это тревожный признак. Обычно такая ситуация выявляется рентгенологически (обязательно получение снимков в 2 проекциях – прямой и правой боковой) (рис. 3). Далее диагноз подтверждается данными УЗИ средостения (переднего ретростернального пространства и заднего – со стороны спины паравертебрально), КТ-исследования (нативного и с контрастированием) (рис. 4).
При подозрении на онкологический процесс и в отсутствие периферической лимфаденопатии необходима оценка состояния паренхиматозных органов, проведение костно-мозговой пункции, иногда – торакотомии с биопсией ЛУ (возможно, торакоскопически). В некоторых случаях удается трансъюгулярная медиастинотомия с биопсией всего пакета ЛУ. При диагностике туберкулеза обязательна оценка состояния легочной паренхимы, необходимо проведение посева мокроты с бактериоскопией (иногда бронхоскопией со смывами) и оценка реакции Манту. При наличии плеврита также исследуется плевральная жидкость.
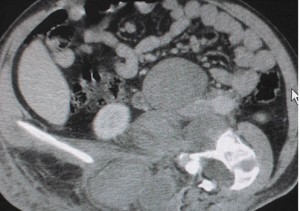
Внутрибрюшная лимфаденопатия чаще всего (в 70% случаев) обусловлена инфекционным процессом – группа бактериальных кишечных инфекций (тифо-паратифозная группа, иерсиниоз и т. д.) и вирусных инфекций (например, мононуклеоз). Остальные случаи – это злокачественные поражения лимфоузлов (лимфомы, метастазы внутрибрюшных опухолей).
Для внутрибрюшной лимфаденопатии более оправдана следующая тактика: УЗИ-контроль; антибиотикотерапия; серологическое и бактериологическое исследование на наличие специфического возбудителя (при его выявлении – соответствующее лечение); УЗИ-контроль через 5-7 дней. Если серологическая и бактериологическая диагностика не дали результата и внутрибрюшная лимфаденопатия сохраняется на протяжении 21 дня, то показана костно-мозговая пункция, КТ-исследование и открытая биопсия (возможно, лапароскопически) с гистологическим исследованием.
Литература
1. Дмитриев В.В., Лазутин Ю.Н., Нестерова Ю.А., Старжецкая М.В., Козель Ю.Ю., Сугак Е.Ю. К вопросу о дифференциальной диагностике доброкачественных и злокачественных лимфаденопатий у детей // Материалы III съезда онкологов и радиологов СНГ, ч. II. – 2004, Мн. – с. 389.
2. Ефименко М.В. Обзор литературы по основам иммунологии // http://www. primer.ru/immu-nologia
3. Киреев А. Исцеление крови. – М.: Ч.А.О. и К, 2001. – 94 с.
4. Козарезова Т.И., Кувшинников В.А., Волкова Л.И., Василевский И.В. Лимфаденопатии у детей (клиника, диагностика, дифференциальная диагностика, тактика ведения больных). Уч. – метод. рекомендации. – Мн.: МЗ РБ, 1996. – 45 с.
5. Козарезова Т.И., Волкова Л.И., Климкович Н.Н. Диагностический алгоритм лимфаденопатий у детей // Материалы I съезда детских онкологов и гематологов России. – Москва. – 1997. – с. 4.
6. Козарезова Т.И., Волкова Л.И., Климкович Н.Н. Некоторые аспекты лечения реактивных (вторичных) лимфаденопатий у детей //Детская онкология. – 1997, № 3-4. – с. 7.
7. Левин Ю.М. Хочешь жить? Сумей выжить. Серия «Эндоэкологическая медицина» . – М., 2001. – 120 с.
8. Мацеха Е.П., Бишарова Г.И. Алгоритм дифференциальной диагностики заболеваний лимфатических узлов у детей // Материалы III съезда онкологов и радиологов СНГ, ч. II. – 2004, Мн. – с. 400.
9. Назаренко О.Р. Сравнительная ценность эхографии в оценке состояния органов брюшной полости у детей с острым лимфобластным лейкозом// Автореф. дис. ... канд. мед. наук: М., 1997. – 24 с.
10. Румянцев А.Г., Чернов В.М., Делягин В.М. Синдром увеличенных лимфатических узлов как педиатрическая проблема // Лечащий врач. – 1998, № 3. – с. 18-23.
11. Сапин М.Р. Анатомия человека, М., « Медицина», 2001. – 428 с.
12. Тарасова И.С. Клинико-гематологическая характеристика детей при различных дозовых радиационных нагрузках // Автореф. дис. … канд. мед. наук: М., 1997. – 25 с.
13. Чернов В.М., Финогенова Н.А., Шахталин В.В., Сидорович Г.И. Структура гематологической заболеваемости детей в г. Клинцы Брянской области // В кн.: Медицинские аспекты влияния малых доз радиации на организм детей и подростков, Обнинск – Москва. – 1992. – с. 92-95.
14. Avaliani Z., Burkadze G. The Morphological Changes in Lymph Nodes during Clinical and Experimental Lymphadenopathy of Different Genesis // Annals of biomedical research and education. – 2003, Vol. 3. – P. 12-14.
15. Bazemore A.W., Smucker D.R. Lymphadenopathy and Malignancy // American Family Physician. – 2002, Vol. 66. – P. 2103-2113.
16. Bertho N., Adamski H., Toujas L., Debove M., Davoust J., Quillien V. Efficient migration of dendritic cells toward lymph node chemokines and induction of TH1 responses require maturation stimulus and apoptotic cell interaction// Blood. – 2005, Vol. 106. – P. 1734-1741.
17. Bezabih M., Mariam D.W., Selassie S.G. Fine needle aspiration cytology of suspected tuberculous lymphadenitis // Cytopathology. – 2002, Vol. 13. – P. 284-290.
18. Binet H., Van Vooren J.P., Thys J.P., Heenen M., Parent D. Tuberculous inguinal and crural lymph nodes // Dermatology. – 1998, Vol. 196. – P. 459-460.
19. Black C., Zavod M.B.. Gosselin B.J. Haemophilus influenzae lymphadenopathy in a patient with agammaglobulinemia: clinical-histologic-microbiologic correlation and review of the literature // Archives of Pathology and Laboratory Medicine. – 2005, Vol. 129. – P. 100-103.
20. Bolliger C.T., Mathur P.N., Beamis J.F. ERS/ATS statement on interventional pulmonology: European Respiratory Society / American Thoracic Society// European Respirator Journal. – 2002, Vol. 19. – P. 356-373.
21. Cetinkaya E., Yildiz P., Altin S., Yilmaz V. Diagnostic Value of Transbronchial Needle Aspiration by Wang 22-Gauge Cytology Needle in Intrathoracic Lymphadenopathy // Chest. – 2004, Vol. 125. – P. 527-531.
22. Chen Yu., Savargaonkar P., Fuchs A, Wasserman P. Role of flow cytometry in the diagnosis of lymphadenopathy in children // Diagnostic Cytopathology. – 2002, Vol. 26. – P. 5-9.
23. Crystal R.G. Sarcoidosis. In: Fauci A.S., Braunwald E., Isselbacher K.J. Harrison’s principles of internal medicine: 14th ed. New York, NY: McGraw Hill. – 1998. – P. 1922-1928.
24. Dangman B.C., Albanese B.A., Kocia M. Cat scratch disease with fever of unknoun origin: imaging features and association with new causative agent Rochalimea henselae // Pediatrics. – 1995, Vol. 5. – Р. 767-771.
25. Ellison E., LaPuerta P., Martin S.E. Supraclavicular masses: results of a series of 309 cases biopsied by fine needle aspiration // Head Neck. – 1999, Vol. 21. – P. 239-246.
26. Espinal M.A., Laszlo A., Simonsen L. Global trends in resistance to antituberculosis drugs // New England Journal of Medicine. – 2001, Vol. 344. – P. 294-1303.
27. Ferrer R. Lymphadenopathy: differential diagnosis and evaluation // American Family Physician. – 1998, Vol. 58. – P. 1313-1323.
28. Flexman J. Bortanella henselae is a causative agent of cat scratch disease in Australia // Journal of Infection. – 1995, Vol. 31. – P. 241-245.
29. Fritscher-Ravens A., Soehendra N., Schirrow L. Role of transesophageal endosonography-guided fine-needle aspiration in the diagnosis of lung cancer // Chest. – 2000, Vol. 117. – P. 339-345.
30. Garpestad E., Goldberg S., Herth F. CT fluoroscopy guidance for transbronchial needle aspiration: an experience in 35 patients // Chest. – 2001, Vol. 119. – P. 329-332.
31. Giordano D., Magaletti D.M., Clark E.A. Nitric oxide and cGMP protein kinase (cGK) regulate dendritic-cell migration toward the lymph-node-directing chemokine CCL19 // Blood. – 2006, Vol. 107. – P. 1537-1545.
32. Habermann T.M., Steensma D.P. Lymphadenopathy // Mayo Clinic Proceedings. – 2000, Vol. 75. – P. 723-732.
33. Herth F.J., Becker H.D., Ernst A. Ultrasound-guided transbronchial needle aspiration: an experience in 242 patients // Chest. – 2003, Vol. 123. – P. 604-607.
34. Ioachim H.L., Ratech H. Ioachim's Lymph Node Pathology: Williams & Wilkins, 3rd edition, 2002. – 624 p.
35. Johnson L.B., Pasumarthy A., Saravolatz L.D. Parvovirus B19 infection presenting with necrotizing lymphadenitis// American Journal of Medicine. – 2003, Vol. 114 (4). – P. 340-341.
36. Karadeniz C., Oguz A., Ezer U., Ozturk G., Dursun A. The etiology of peripheral lymphadenopathy in children // Pediatric Hematology/Oncology. – 1999, Vol. 16. – P. 525-531.
37. Karie S., Izzedine H., Beaufils H., Charlotte F., Launay-Vacher V., Deray G. Lymphadenopathy and proteinuria // Nephrology Dialisis/Transplantation. – 2004, Vol. 19. – P. 739-741.
38. Kelly C.S., Kelly R.E. Lymphadenopathy in Children // Pediatric Clinics of North America. – 1998, Vol. 45. – P. 875-888.
39. Kelly C.S., Kelly R.E.Jr. Lymphadenopathy in children // Pediatric Clinics of North America. – 1998, Vol. 45. – P. 875-888.
40. Kojima M., Nakamura S., Sugihara S., Sakata N., Masawa N. Lymph node infarction associated with infectious mononucleosis: report of a case resembling lymph node infarction associated with malignant lymphoma // International Journal of Surgery Pathology. – 2002, Vol. 10 (3). – P. 223-226.
41. Kоrholz D., Gobel U. Lymphoknotenvergrеungen im Kindesalter // Kinderheilkunde – 2003, Vol. 143 – P. 1023-1033.
42. Larsen S.S., Krasnik M., Vilmann P. Endoscopic ultrasound guided biopsy of mediastinal lesions has a major impact on patient management // Thorax. – 2002, Vol. 57. – P. 98-103.
43. LeBlanc K., Devereaux B.M., Imperiale T.F., Kesler K., DeWitt J.M., Cummings O., Ciaccia D., Sherman S., Mathur P., Conces D., Brooks J., Chriswell M., Einhorn L., Collins E. Endoscopic Ultrasound in Non-Small Cell Lung Cancer and Negative Mediastinum on Computed Tomography // American Journal of Respirator Critical Care Medicine. – 2005, Vol. 171. – p. 177-182.
44. Leung A.K.C., Robson W.L.M. Childhood cervical lymphadenopathy // Journal of Pediatric Health Care. – 2004, Vol. 18 (1). – P. 3-7.
45. Nasuti J.F., Gupta P.K., Baloch Z.W. Clinical implications and value of immunohistochemical staining in the evaluation of lymph node infarction after fine-needle aspiration // Diagnostic Cytopathology. – 2001, Vol. 25 (2). – P. 104-107.
46. Pehme L., Hollo V., Rahu M., Altraja A. Tuberculosis During Fundamental Societal Changes in Estonia With Special Reference to Extrapulmonary Manifestations // Chest. – 2005, Vol. 127. – P. 1289-1295.
47. Rabkin C.S. AIDS and cancer in the era of highly active antiretroviral therapy (HAART) // European Journal of Cancer. – 2001, Vol. 37. – P. 1316-1319.
48. Ramesh V., Misra R.S., Beena K.R., Mukherjee A. A study of cutaneous tuberculosis in children // Pediatric Dermatology. – 1999, Vol. 16. – P. 264-269.
49. Roberts K.B., Tunnessen W.W. Lymphadenopathy. In: Signs and Symptoms in Pediatrics. 3rd ed. Lippincott, Williams, and Wilkins, 1999. – P. 63-72.
50. Rosai J. Lymph nodes (Chapter 21) // Ackerman's Surgical Pathology: Mosby – yearbook, 8th edition. – 1998, Vol.2. – 1739-1741.
51. Roy S. Cervical Lymphadenopathy // Lecture at annual CME Masters of Pediatrics Conference: University of Miami School of Medicine, 2005, Miami Beach.
52. Saif M.W. Diagnosis and treatment of Kaposi's sarcoma // Resid Staff Physician. – 2001, Vol. 47. – P. 19-24.
53. Singh M.K., Solanki R.N., Shah N.J., Tanna D., Patel D.R., Desail I.M. Angioimmunoblastic Lymphadenopathy with Dysproteinemia: Thoracic Involvement // The Indian Journal of Chest. – 2004, Vol. 46. – P. 125-128.
54. Small E.J., Torti F.M. Testes. In: Abeloff MD, ed. Clinical oncology. 2d ed. New York: Churchill Livingstone, 2000. – P. 1912.
55. Steel B.L., Schwartz M.R., Ramzy I. Fine needle aspiration biopsy in the diagnosis of lymphadenopathy in 1,103 patients. Role, limitations and analysis of diagnostic pitfalls // Acta Cytologica. – 1995, Vol. 39. – P. 76-81.
56. Stein D.L., Haramati L.B., Spindola-Franco H., Friedman J., Klapper P.J. Intrathoracic Lymphadenopathy in Hospitalized Patients With Pneumococcal Pneumonia // Chest. – 2005, Vol. 127. – P. 1271-1275.
57. Strauchen J.A., Miller L.K. Lymph node infarction. An immunohistochemical study of 11 cases // Archive Pathology of Labor Medicine. – 2003, Vol. 127 (1). – P. 60-63.
58. Terra R., Louis I., Le Blanc R., Ouellet S., Zuiga-Pflucker J.C., Perreault C. T-cell generation by lymph node resident progenitor cells // Blood. – 2005, Vol. 106. – P. 193-200.
59. Tsang W.Y., Chan J.K. Spectrum of morphologic changes in lymph nodes attributable to fine needle aspiration // Human Pathology. – 1992, Vol. 23 (5). – P. 562-565.
60. Vaccher E., Spina M., Tirelli U. Clinical aspects and management of Hodgkin's disease and other tumours in HIV-infected individuals // European Journal of Cancer. – 2001, Vol. 37. – P. 1306-1315.
61. Vassilakopoulos T.P., Pangalis G.A. Application of a prediction rule to select which patients presenting with lymphadenopathy should undergo a lymph node biopsy // Medicine (Baltimore). – 2000, Vol. 79. – P. 338-347.
62. Vayner N., Coret A., Polliack G. Mesenteric lymphadenopathy in children examined by US for chronic and/or recurrent abdominal pain // Pediatric Radiology. – 2003, Vol. 16. – P. 278-284.
63. von Bergwelt-Baildon M., Shimabukuro-Vornhagen A., Popov A., Klein-Gonzalez N., Fiore F., Debey S., Draube A., Maecker B., Menezes I., Lee M.N., Schultze J.L. CD40-activated B cells express full lymph node homing triad and induce T-cell chemotaxis: potential as cellular adjuvants // Blood. – 2006, Vol. 107. – P. 2786-2789.
64. Wakely P.E. Jr. Fine-needle aspiration cytopathology in diagnosis and classification of malignant lymphoma: accurate and reliable? // Diagnostic Cytopathology. – 2000, Vol. 22. – P. 120-125.
65. Wildi S.M., Judson M.A., Fraig M., Fickling W.E., Schmulewitz N., Varadarajulu S., Roberts S.S., Prasad P., Hawes R.H., Wallace M.B., Hoffman B.J. Is endosonography guided fine needle aspiration (EUS-FNA) for sarcoidosis as good as we think? // Thorax. – 2004, Vol. 59. – P. 794-799.
66. Yasufuku K., Chhajed P.N., Sekine Y. Endobronchial ultrasound using a new convex probe: a preliminary study on surgically resected specimens // Oncology Report. – 2004, Vol. 11. – P. 293-296.
67. Yasufuku K., Chiyo M., Sekine Y., Chhajed P.N., Shibuya K., Iizasa T., Fujisawa T. Real-time Endobronchial Ultrasound-Guided Transbronchial Needle Aspiration of Mediastinal and Hilar Lymph Nodes // Chest. – 2004, Vol. 126. – P. 122-128.
68. Zwischenberger J.B., Savage C., Alpard S.K. Mediastinal transthoracic needle and core lymph node biopsy: should it replace mediastinoscopy? // Chest. – 2002, Vol. 121. – P. 1165-1170.