29 травня, 2020
Глюкокортикоїди в ревматології: коли, кому і як довго?
 Коли змінюється світ, змінюємося і ми. Соціальна дистанція на сьогодні потрібна для збереження здоров’я громадян в умовах пандемії. Саме тому освітні процеси продовжуються у новому веб-форматі, що відповідає ситуації. Громадське об’єднання «Всеукраїнська асоціація ревматологів України» теж відчинило свої двері на сайті Rheumahub.org.ua. Відтепер у нас є можливість спілкуватися онлайн. Ви можете ставити запитання, надавати пропозиції щодо обговорення актуальних тем, знайомитись із новинами. У межах вебінару було розглянуте найактуальніше питання сучасної ревматології – кому, коли і в яких дозах призначати глюкокортикоїди (ГК). Своєю думкою з цього приводу поділилася старший науковий співробітник відділу некоронарогенних хвороб серця та клінічної ревматології ННЦ «Інститут кардіології імені М.Д. Стражеска» НАМН України (м. Київ), к. мед. н. Олена Олексіївна Гарміш.
Коли змінюється світ, змінюємося і ми. Соціальна дистанція на сьогодні потрібна для збереження здоров’я громадян в умовах пандемії. Саме тому освітні процеси продовжуються у новому веб-форматі, що відповідає ситуації. Громадське об’єднання «Всеукраїнська асоціація ревматологів України» теж відчинило свої двері на сайті Rheumahub.org.ua. Відтепер у нас є можливість спілкуватися онлайн. Ви можете ставити запитання, надавати пропозиції щодо обговорення актуальних тем, знайомитись із новинами. У межах вебінару було розглянуте найактуальніше питання сучасної ревматології – кому, коли і в яких дозах призначати глюкокортикоїди (ГК). Своєю думкою з цього приводу поділилася старший науковий співробітник відділу некоронарогенних хвороб серця та клінічної ревматології ННЦ «Інститут кардіології імені М.Д. Стражеска» НАМН України (м. Київ), к. мед. н. Олена Олексіївна Гарміш.
Ревматоїдний артрит
Особливі «стосунки» ревматоїдного артриту (РА) і ГК розпочалися 21 вересня 1948 р. під час першої ін’єкції кортизону хворій на РА. Жінка, яка сиділа в інвалідному візку, одужала впродовж тижня. За свідченням Едварда Кендалла, «вона вийшла з лікарні у веселому настрої та відправилася на тригодинний шопінг» (Kendall, 1948). Декілька років тривав період захоплення «диво-терапією». ГК застосовували у великих дозах та необмежено у часі, що досить швидко спровокувало розвиток тяжких ускладнень, а саме синдрому Іценко – Кушинга. Через десять років використання медична спільнота того часу визнала ГК небезпечними препаратами для лікування РА. Вже у 1960 р. російський емігрант та видатний американський лікар Джозеф Бунім писав, що «у жодному разі ГК не можуть бути застосовані як ініціальні агенти для терапії РА» (Bunim, 1960).
Період «забуття» ГК у терапії РА тривав майже 30 років, доки в 1995 р. Джон Кирван не опублікував результати дослідження запобіжного ефекту низьких доз ГК на суглобову деструкцію (Kirwan, 1995). У рекомендаціях Європейської протиревматичної ліги (EULAR) тимчасове системне застосування ГК у хворих на РА вперше було запропоноване в 2007 р., тоді як у рекомендаціях Американського коледжу ревматологів (ACR) – лише у 2015 р., майже через десятиліття.
У 2010 р. з’явився популярний сучасний термін «міст-терапія», а в 2016 р. робочою групою EULAR тривале застосування ГК у дозі ≤5 мг/добу в більшості пацієнтів було визнано безпечним (Strehl, 2016) та співставним за показником «перевага/ризик» із синтетичними та біологічними хворобомодифікуючими препаратами (ХМП) (Bijlsma, 2016). Крім того, у той же проміжок часу вже було накопичено достатньо доказів щодо хворобомодифікуючого ефекту ГК, особливо при ранньому РА. Все це привело до виникнення так званого «наукового ренесансу» обґрунтованого застосування ГК при ревматичних захворюваннях (РЗ), а особливо при РА.
Проте, незважаючи на чисельні сучасні наукові публікації та міжнародні рекомендації щодо місця ГК при РЗ, у рутинній практиці це питання лишається невирішеним. Для лікаря-ревматолога остаточно не з’ясовані питання тривалості лікування, своєчасності та закономірності зниження дози і повної відміни ГК. Немає окремих докладних рекомендацій щодо особливостей їхнього застосування при різних РЗ. У наявних рекомендаціях терапія ГК зазвичай регламентується одним пунктом, де зазначено лише загальні принципи, і немає відповіді на більшість конкретних клінічних питань. З одного боку, лікарі уникають системного призначення низьких доз, а з іншого – зловживають необґрунтовано частим використанням депо-форм ГК. Така тактика не може забезпечити «лікування до досягнення мети» за сучасною концепцією, а зумовлює лише епізодичне покращення симптомів та розвиток побічних реакцій (ПР), іноді загрозливих і необоротних.
Актуальні рекомендації ACR щодо системного застосування ГК при РА
Рекомендації ACR (2015) (Singh, 2015):
1. Рекомендації для пацієнтів із симптоматичним раннім РА:
- пункт 6: якщо зберігається помірна/висока активність хвороби незважаючи на прийом синтетичних та біологічних ХМП, до лікування необхідно додати ГК;
- пункт 7: у разі загострення слід розпочати прийом ГК коротким курсом у найменших дозах.
2. Рекомендації для пацієнтів із пізнім РА:
- пункт 11: За наявності помірної/високої активності хвороби незважаючи на прийом синтетичних та біологічних ХМП до терапії варто додати ГК;
- пункт 12: у разі загострення РА під час прийому синтетичних та біологічних ХМП потрібно використовувати ГК коротким курсом у найменших дозах (надавати перевагу таблетованим формам).
Рекомендації EULAR (2019)
На початку 2020 р. було опубліковано оновлені рекомендації EULAR від 2019 р. щодо менеджменту хворих на РА із застосуванням синтетичних та біологічних ХМП (Smolen, 2020). Покроковий алгоритм представлено на рисунку 1.
Рис. 1. Алгоритм ведення пацієнтів із РА відповідно до рекомендацій EULAR (2019) із застосуванням синтетичних і біологічних ХМП
Насамперед варто звернути увагу на виділення важливих з практичної точки зору факторів несприятливого перебігу. На сучасному етапі лікування РЗ неможливо уникнути тривалого моніторингу кількості болючих та припухлих суглобів, оскільки лише вони адекватно відображають ефективність лікування.
Слід зазначити, що найбільш вагомими в рутинному клінічному огляді факторами несприятливого перебігу є велика кількість припухлих суглобів та неефективність двох ХМП.
Фактори несприятливого перебігу РА за рекомендаціями EULAR (2019)
- Постійна помірна/висока активність згідно з індексами, які включають оцінку болючих та припухлих суглобів незважаючи на прийом ХМП
- Підвищення швидкості осідання еритроцитів (ШОЕ), С-реактивного білка (СРБ)
- Велика кількість припухлих суглобів
- Позитивний ревматоїдний фактор та/або антитіла до циклічного цитрулінового пептиду, особливо у високих титрах
- Ранні ерозії
- Неефективність ≥2 ХМП
Згідно з новими рекомендаціями, ГК можна призначати як міст-терапію:
- первинно після встановлення клінічного діагнозу РА;
- у разі загострення;
- при заміні базисного препарату;
- за неможливості використання іншої терапії.
Безпечним вважається застосування низьких доз протягом певного часу (до шести місяців), необхідного для досягнення ремісії. Перевагу надають стабільному прийому ГК у таблетованій формі перед епізодичним парентеральним використанням препаратів тривалої дії. В науковій літературі немає даних щодо введення бетаметазону та дексаметазону в/м для лікування РА. Також не дозволене призначення ГК тривалої дії частіше ніж один раз на три місяці.
Рекомендації щодо доз і тривалості прийому ГК базуються на результатах декількох сучасних досліджень при ранньому РА: tREACH (Нідерланди, 2014), CareRA (Бельгія, 2015), IDEA (Велика Британія, 2014) та ESPOIR (Франція, 2017).
Оптимальною схемою за даними двох досліджень виявилася комбінація метотрексату (МТХ) із низькими або середніми дозами ГК. Цільовою є доза МТХ 25 мг/тиждень, яка поступово підвищується за стандартною схемою на 2,5‑5 мг/місяць зі стартової дози 10‑15 мг/тиждень. Доза МТХ залежить від індивідуальної переносимості, за неможливості підвищити її до максимально ефективної для досягнення ремісії доцільно додати другий ХМП, підвищити дозу або продовжити термін прийому ГК.
Внаслідок аналізу ефективності різних схем прийому ГК варто зауважити, що стартову дозу 15 мг/добу протягом місяця із поступовою відміною через 10 тижнів можна рекомендувати пацієнтам із помірною активністю РА без системних проявів. У разі високої активності РА, наявності системних ознак, факторів несприятливого перебігу та швидко прогресуючого ерозивного процесу після прийому стартової дози 15‑30 мг/добу доцільно проводити тривалішу терапію ГК у низьких дозах (<7,5 мг/добу до шести місяців).
Застосування високих доз (>30 мг/добу) не супроводжується підвищенням ефективності та викликає вдвічі більше ПР. Продовження прийому ГК до моменту розвитку максимальної терапевтичної ефективності ХМП (шість місяців) має певні переваги перед призначенням коротких курсів за потребою (у разі загострення) (Bakker, 2012; Schett, 2016).
У 2019 р. було представлено попередні результати випробування NORD-STAR, яке, на мою думку, є вирішальним у визначені місця ГК в лікуванні РА. У дослідження були включені 812 пацієнтів із високою активністю РА в середньому через сім днів після встановлення діагнозу. Хворі були розподілені на чотири групи прийому препаратів, які включали в себе представників усіх наявних класів ХМП, за виключенням ритуксимабу. Всі учасники отримували МТХ у дозі 25 мг/тиждень вже через місяць після початку лікування. Пацієнти першої групи додатково приймали преднізолон 20 мг/добу із поступовим зниженням до 5 мг/добу протягом дев’ятьох тижнів, другої – блокатор фактора некрозу пухлини (ФНП), третьої – абатасепт, четвертої – блокатор інтерлейкіну (ІЛ)-6. Головним висновком є відсутність різниці в ефективності всіх наведених схем лікування.
Таким чином, при ранньому РА комбінація ГК із МТХ або іншим синтетичним ХМП за ефективністю дорівнює комбінації МТХ з біологічним агентом, але є більш обґрунтованою з точки зору фармакоекономіки.
Ревматична поліміалгія
Принципи лікування РПМ згідно з рекомендаціями ACR (2015) (Dejaco, 2015):
1. Для кожного пацієнта із РПМ необхідно скласти індивідуальний план лікування, враховуючи активність захворювання, супутні патології, уподобання хворого.
2. Нестероїдні протизапальні препарати (НПЗП)) не призначають для лікування РПМ. Замість них необхідно призначати ГК одразу після встановлення діагнозу. Застосування НПЗП коротким курсом можливе лише за наявності інших супутніх захворювань (остеоартрозу тощо). Специфічних рекомендацій щодо прийому анальгетиків немає.
3. Монотерапія ГК з індивідуальним підбором дози і тривалості застосування є базисною терапією при РПМ.
4. Добова доза ГК приймається вранці одноразово, за винятком індивідуальних потреб (інтенсивний нічний біль тощо).
5. Початкова доза ГК у період індукції ремісії знаходиться в діапазоні 12,5‑25 мг/добу в еквіваленті за преднізолоном і не повинна бути більшою ніж 30 мг/добу.
6. Ефективність метилпреднізолону (МП) у лікуванні РПМ дорівнює ефективності преднізолону.
7. Після досягнення терапевтичного ефекту рекомендовано знижувати дозу:
A. Початкове зниження: до 10 мг/добу протягом 4‑8 тижнів.
B. Терапія загострень: підвищити дозу до попередньої та знижувати поступово (4‑8 тижнів) до тієї, на якій відбулося загострення.
C. У разі досягнення ремісії: знижувати дозу МП на 1 мг один раз на чотири тижні; преднізолону – на 1,25 мг один раз на чотири тижні або на 2,5 мг один раз на 10 тижнів до повної відміни за наявності збереження ремісії. Зниження дози можливо проводити в альтернуючому режимі, наприклад 10/7,5 мг через день, 7,5/5 мг через день і т.д. При РПМ строго не рекомендовано приймати подвійну дозу ГК через день.
8. Мінімальна тривалість лікування становить 12 місяців і може продовжуватись до п’яти років. Факторами ризику загострень є жіноча стать, ШОЕ понад 40 мм/г та наявність периферичного артриту. Можливість підняти руки за голову в дебюті РПМ є предиктором менш тривалого прийому ГК (Morton, 2019).
9. За індивідуальнї потреби можливе додавання МТХ до ГК як на етапі індукції ремісії, так і протягом підтримуючого лікування, особливо у пацієнтів із ризиком чи наявністю загострень або ГК-асоційованих ПР (Dejaco, 2015).
Тривалість прийому та швидкість знижування дози в період розвитку та підтримання ремісії розраховується індивідуально залежно від активності хвороби та наявності факторів ризику ГК-залежних ПР. Для визначення активності РМП використовують запропонований у 2012 р. індекс активності ревматичної поліміалгії (рис. 2) і критерії ремісії та загострення, визначені методом Делфі (табл. 1). Через брак часу у разі звичайного прийому розрахунок індексів є складним завданням, але моніторування окремих показників у динаміці може допомогти лікареві визначитись із дозою та терміном використання ГК. Одним із важливіших показників активності й факторів прогнозу є можливість підняти руки за голову.
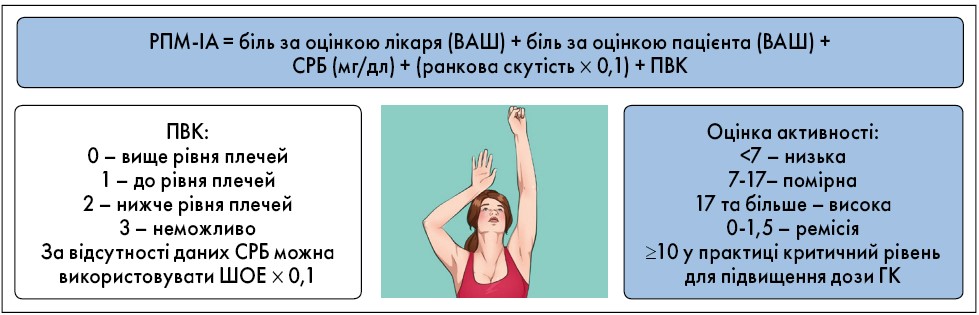 Рис. 2. Індекс активності ревматичної поліміалгії
Рис. 2. Індекс активності ревматичної поліміалгії
Примітки: ІА – індекс активності, ВАШ – візуально-аналогова шкала, СРБ – С-реактивний білок, ПВК – підйом верхніх кінцівок.
Адаптовано за B.F Leeb, H.A. Bird, 2004.
 Системний червоний вовчак
Системний червоний вовчак
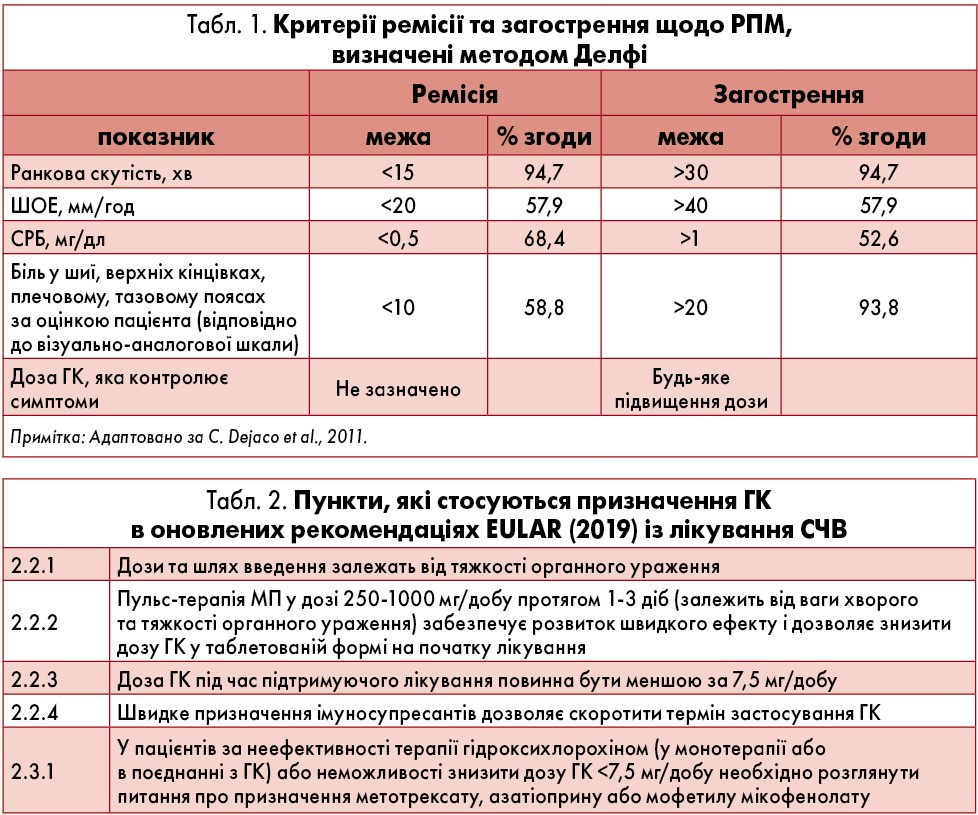
У 2019 р. опубліковані новітні рекомендації з лікування системного червоного вовчака (СЧВ). Загальні принципи щодо використання ГК перегукуються із сучасною стратегією лікування РА і передбачають два підходи (Fanouriakis, 2019) (табл. 2):
Пульс-терапія МП у різних дозах (залежно від активності захворювання та ваги хворого), яка, завдяки швидкому негеномному ефекту ГК, дозволяє надалі застосовувати нижчі стартові дози ГК per os із можливістю їхнього зниження та відміни. Високі дози МП в/в (250‑1000 мг/добу три дні) зазвичай використовують у разі розвитку гострих, загрозливих для життя станів (як-то нефрит, нейролюпус тощо) після виключення інфекцій (Ruiz-Arruza, 2018; Ruiz-Irastorza, 2017).
Ініціація імуносупресивної терапії (МТХ, азатіоприн, мофетилу мікофенолат) одночасно із призначенням ГК у таблетках для швидкого зниження їхньої дози та можливої відміни надалі.
За наявності персистуючої активності або загострення позаниркових проявів слід вирішити питання про призначення белімумабу. У разі рефрактерного перебігу та тяжкого органного ураження можна застосовувати ритуксимаб.
Метою лікування є ремісія/низька активність хвороби та упередження загострень за всіма органами й системами на тлі прийому мінімальної дози ГК. За необхідності хронічного підтримуючого лікування ГК не рекомендовано перевищувати дозу 7,5 мг/добу. За умов ремісії та/або контролю симптомів за допомогою имуносупресивної терапії бажано відмінити ГК.
Новітні настанови пропонують скористатися можливістю повної відміни ГК у хворих на СЧВ. Але, на мою думку, це тільки початок тривалого шляху щодо визначення умов, за яких ми можемо це робити. Створення конкретних рекомендацій із цього приводу та визначення поняття ремісії для РА зайняло майже десятиліття.
Хочу звернути увагу на останню публікацію результатів клінічного дослідження щодо відміни підтримуючої дози ГК у пацієнтів із ремісією СЧВ протягом року (Mathian, 2020). Тривалість дослідження становила 12 місяців, 61 пацієнтові відмінили преднізолон у дозі 5 мг/добу, а 63 продовжили прийом. Отримані результати свідчать про необхідність застосування зваженого підходу до відміни ГК у хворих на СЧВ. У групі без підтримуючого прийому ГК загострення спостерігалося в чотири рази частіше, а тяжке загострення за індексом BILAG – у вісім разів. Автори підкреслюють, що прийом низької дози ГК дозволяє підтримувати ремісію протягом тривалого часу.
За даними 12-річного спостереження за китайською когортою понад 11 тис. пацієнтів із СЧВ було продемонстровано суттєву різницю в кількості та якості ПР залежно від дози преднізолону (Chen, 2018). Так, доза, більша за 10 мг/добу порівняно із меншою асоціювалася з суттєвим підвищенням ризику остеонекрозу, остеопорозу, бактеріальних інфекцій та порушень сну (рис. 3). Але найголовнішою відмінністю при застосуванні дози більш ніж 10 мг/добу була частота розвитку такого ускладнення, як вторинний синдром Кушинга, ризик виникнення якого підвищувався у 62 рази; до речі, він не супроводжувався ожирінням, що може ускладнювати своєчасну діагностику.
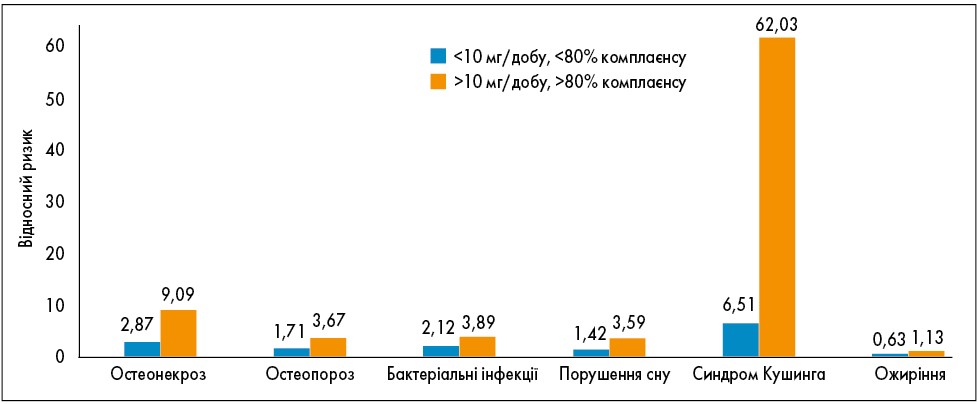
Рис. 3. Кумулятивний ризик розвитку побічних ефектів ГК у пацієнтів із СЧВ залежно від дози та тривалості прийому преднізолону
Примітка: Адаптовано за H.-L. Chen et al., 2018.
Вже понад 60 років такий представник класу ГК, як МП залишається найбільш безпечним серед ГК при тривалому використанні в лікуванні РЗ. Його протизапальна активність перевищує активність преднізолону, а побічні ефекти за деякими показниками є меншими. Оригінальнім представником МП є препарат Медрол, який зареєстрований майже у 100 країнах світу та виробляється компанією Pfizer Inc., що представлена в Україні «Пфайзер Експорт Бі.Ві.»
Підбиваючи підсумки, слід зазначити, що дозу, тривалість прийому, лікарську форму та шлях введення ГК у будь-якому випадку безпосередньо визначає лікар з огляду на індивідуальний клінічний сценарій та дані останніх наукових досліджень і рекомендацій.
Список літератури знаходиться в редакції
Надруковано за підтримки Представництва «Пфайзер Експорт Бі.Ві.»
PP-DEM-UKR‑0021
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 2 (69) 2020 р.



