25 липня, 2020
Рак і вагітність
Рак у період вагітності хоча і є рідкісним випадком, та, як показали деякі епідеміологічні дослідження, його частота в останні роки зростає. Зокрема у данському реєстрі зафіксовано збільшення частки раку, пов’язаного з вагітністю, з 5,4 (n=572) до 8,3% (n=1052) протягом 30 років. Найпоширенішими пухлинами є меланома, рак шийки матки та грудної залози [1]. Підвищення захворюваності на рак у період вагітності не можна пояснити лише збільшенням материнського віку. За даними австралійського дослідження, присвяченого раку, пов’язаного з вагітністю, протягом 14 років повідомлено про 1798 випадків пухлин, 499 – під час вагітності та 1299 – у післяпологовий період, що дає змогу встановити частоту захворюваності на рак приблизно 137,3 на 100 тис. вагітностей [2]. За цей період спостерігалося статистично значуще зростання частки злоякісних захворювань, пов’язаних із вагітністю, і збільшення кількості матерів віком старше 35 років з 13,2 до 23,6%. Однак віком можна пояснити збільшення захворюваності лише на 14%. Дані про післяпологовий період (до 12 міс після пологів) були включені у це дослідження з огляду на затримку діагностики під час вагітності.
В італійському популяційному дослідженні, присвяченому раку, пов’язаному з вагітністю, встановлено, що найпоширенішою пухлиною був рак грудної залози (32%, n=479), а ризик розвитку раку, пов’язаного з вагітністю, значно підвищується з віком – з 60 випадків на 100 тис. у жінок молодших 30 років до 265 на 100 тис. у жінок старших 40 років [3]. Меланому, рак грудної та щитоподібної залози частіше виявляли серед населення Австралії, ніж інших країн, а частота раку шийки матки та яєчника у цій популяції була нижчою [2]. У міжнародному аналізі когорти 1170 жінок, у яких діагностовано рак у період вагітності, визначено, що найпоширенішими інвазивними пухлинами у них були рак грудної залози (39%, n=462), рак шийки матки (13%, n=147), лімфома (10%, n=113), рак яєчника (7%, n=88) та лейкоз (6%, n=68) [4]. За даними популяційного дослідження, проведеного у Швеції, найпоширенішою пухлиною у період вагітності була меланома (25%, n=232), далі – пухлини грудної залози (15%, n=139), шийки матки (15%, n=139) та яєчника (6%, n=54) [5].
Зміни у лікуванні вагітних, хворих на рак, та, відповідно, результати такого лікування відображені в міжнародному когортному дослідженні [3]. За кожні п’ять років дослідження (1996-2016 рр.) частота лікування збільшувалася на 10% (95% довірчий інтервал 5-15), а застосування хіміотерапії – на 31% (95% довірчий інтервал 20-43). Частота народжуваності зростала, а передчасних пологів – зменшувалися. Виживаність матерів була зіставна з такою у невагітних, що лікувалися від раку, покращувався розвиток плода, новонароджених і дітей раннього віку. Таким чином, лікування з приводу онкологічного захворювання у період вагітності можливе, часто – без істотної загрози безпеці матері чи плода.
Діагностика
Діагностика онкологічних захворювань життєво важлива для успішного лікування незалежно від наявності вагітності. Діагностика раку у період вагітності, на жаль, часто затримується; частково тому, що багато симптомів подібні до симптомів вагітності, включаючи нудоту/блювання, зміни грудей, біль у животі, анемію та втому. Зміни грудної залози та вагітна матка можуть ускладнити фізикальний огляд. Крім того, клініцист може бути більш нерішучим при призначенні відповідних досліджень через побоювання, що результати лабораторних тестів можуть бути неточними а радіологічне обстеження – шкідливим. Через рідкісне виникнення рак може не враховуватися в диференційній діагностиці. Ця затримка діагностики може призвести до запізнілого виявлення хвороби, призначення комплексного лікування та поганого прогнозу [6].
Лабораторне тестування
Пухлинні маркери слід застосовувати з обережністю через їх підвищення під час вагітності. Чутливість і специфічність пухлинних маркерів у період вагітності можуть бути нижчими [7]. Фізіологічні зміни та супутні зміни часто використовуваних лабораторних показників можуть ускладнити встановлення діагнозу онкологічного захворювання у період вагітності. Рівень гемоглобіну та гематокриту зазвичай нижчі, тоді як вміст лужної фосфатази та лактатдегідрогенази, як правило, у період вагітності вищі. Рівень CA 15-3 (маркер раку грудної залози), CA 125 (маркер раку епітелію яєчника) й альфа-фетопротеїну (маркер герміногенних пухлин) під час вагітності фізіологічно підвищується [8, 9].
Візуалізаційні обстеження
Візуалізаційні дослідження для діагностики та стадіювання раку можуть створити конфлікт між користю для матері та ризиком для плода. Тому під час вибору відповідної методики візуалізації потрібно враховувати такі аспекти:
- безпека плода;
- ризик метастазування;
- життєздатність плода.
Радіоактивне опромінення вище 100 мГр асоціюється з вадами розвитку плода та пухлинами у дітей [10]. Якщо необхідне рентгенологічне дослідження, слід забезпечити належне екранування живота. Мамограму складно інтерпретувати через фізіологічну гіперсудинність і щільність тканини грудної залози [11]. Комп’ютерну томографію не рекомендується проводити у період вагітності через неприйнятні кумулятивні дози опромінення та контрастності [12]. Використання позитронно-емісійної томографії у період вагітності є дискусійним через ризик радіоактивного опромінення плода [13].
Ультразвукове дослідження як інструмент для діагностики та стадіювання використовується у всьому світі. Це неінвазивний метод діагностики, який допомагає виконувати прицільну біопсію грудної залози та лімфатичних вузлів.
Магнітно-резонансна томографія безпечна у всіх триместрах вагітності. Це візуалізаційне обстеження вибору для діагностики та стадіювання [14].
Гістопатологічне дослідження тканин забезпечує встановлення остаточного діагнозу та стадіювання пухлини. Патоморфолога завжди слід інформувати про вагітність пацієнтки, щоб уникнути неправильного оцінювання змін тканин, пов’язаних із вагітністю [15]. Окрім змін у тілі матки та яєчниках, вагітність по-різному впливає на доброякісні стани, які можуть імітувати злоякісні пухлини.
Окремі пухлини
Рак шийки матки
Рак шийки матки найкраще діагностується за допомогою цитологічного дослідження на ранніх термінах вагітності. Він може проявлятися аномальними кровотечами, виділеннями з піхви та болем у животі. У вагітних рак шийки матки I стадії виявляють втричі частіше, ніж у невагітних із таким захворюванням [17].
Лікування преінвазивної хвороби (від CIN1 до CIN3) може бути відкладено до 6-8 тижнів після пологів. Однак рекомендується проводити кольпоскопію в кожному триместрі для оцінювання розміру ураження та прогресування захворювання. Виконання кольпоскопії у період вагітності може бути складним через посилення васкуляризації та збільшення генітального набряку [18].
Негайно розпочати лікування вагітних, незалежно від гестаційного віку плода, з інвазивним раком потрібно за наступних показань [19]:
- задокументовані метастази в лімфатичних вузлах;
- прогресування захворювання під час вагітності;
- вибір пацієнткою припинення вагітності.
При раку шийки матки IA1 стадії можна застосовувати конізацію, яку найкраще проводити між 12-м та 20-м тижнями вагітності [19]. Термін «біопсія монети» (coin biopsy) іноді використовують щоб підкреслити, що розріз не повинен бути глибоким для уникнення ушкодження плодових оболонок. Це найкраще проводити в операційній при адекватному наркозі. Профілактичний цервікальний серкляж (cerclage) може бути варіантом як запобігання передчасним пологам, так і лікування інтраопераційної кровотечі.
На стадіях IA2-IB1 (менше 2 см) раку шийки матки може проводитися конізація або проста трахелектомія, оскільки поширення пухлини в параметрій спостерігається менш ніж в 1% жінок. Проста трахелектомія є менш складною процедурою і визначається як висічення шийки матки на 1 см вище від межі пухлини [20]. Однак необхідно оцінити стан лімфатичних вузлів за допомогою лапароскопічної лімфаденектомії таза перед консервативним хірургічним втручанням. У разі позитивного статусу лімфатичних вузлів пацієнтці слід рекомендувати негайне лікування. Лапароскопічну лімфаденектомію найкраще проводити до 20-го тижня вагітності [17, 19]. У других настановах рекомендується проводити це лікування до 22‑25-го тижнів вагітності [19].
Абдомінальну та вагінальну радикальну трахелектомію також виконували під час вагітності з різними результатами вагітності. Абдомінальна радикальна трахелектомія є технічно складнішою і пов’язана зі значною втратою крові та тривалими операціями (3,5-7,5 години, медіана 5,3 години) [21]. Акушерський результат поганий, а отже – радикальна трахелектомія у період вагітності не рекомендується [19].
При пухлинах шийки матки ІB1 стадії розміром понад 2 см можна призначати неоад’ювантну хіміотерапію з тазовою лімфаденектомією або без неї. Хіміотерапія є відносно безпечною у другому триместрі, хоча існує вищий ризик передчасних пологів, передчасного розриву плодових оболонок та обмеження росту плода. Неоад’ювантна хіміотерапія сприяє стабілізації пухлини до досягнення зрілості плода, завдяки чому можна виконати кесарів розтин і радикальну гістеректомію. У жінок із великим терміном вагітності
Пологи шляхом кесаревого розтину є кращим вибором розродження при наявності об’ємних пухлин. Вагінальне розродження супроводжується значним ризиком катастрофічних кровотеч та імплантаційного метастазування у місці піхвових розривів або епізіотомічного рубця. При місцево-поширених пухлинах слід уникати поперечного кесаревого розтину нижнього сегмента через ризик розрізання або розриву тканини пухлини. Класичний розріз дозволить мінімізувати втрату крові та уникнути ушкодження великих пухлинних судин.
У разі небажаного збереження вагітності або запущеної пухлини рекомендується переривання вагітності та традиційне лікування. На початку гестації (менше 12 тижнів) мимовільний аборт відбувається після опромінення тазової ділянки. У другому триместрі гістеротомія з подальшою хіміотерапією є бажаною тактикою лікування, оскільки виникає менша кількість акушерських ускладнень.
Рак грудної залози
Рак грудної залози є найпоширенішим злоякісним захворюванням, яке виявляють під час вагітності та у післяпологовий період. Труднощі діагностики можуть бути пов’язані зі змінами грудної залози у період вагітності та ускладненим виявленням пухлини протягом першого року після пологів. Рак грудної залози під час вагітності, як правило, має такі характеристики: більший розмір новоутворення, позитивний статус лімфатичних вузлів, II або III стадія, високодиференційований інвазивний протоковий рак, переважно ER/PR/HER2/neu-негативний [23, 24]. Прогноз визначається характеристиками пухлини та затримкою початку лікування, а не тільки вагітністю.
При підозрі на рак грудної залози під час вагітності не слід допускати затримку діагностики. Мамографія та ультразвукове дослідження грудних залоз – найкращі методи візуалізації; мамографія має чутливість понад 80%, незважаючи на пов’язані з вагітністю зміни [25]. Ультразвукове дослідження можна використовувати для оцінювання ступеня захворювання грудних залоз і лімфатичних вузлів та для проведення біопсії [26]. Трепанобіопсія є бажаною процедурою. Досвід застосування магнітно-резонансної томографії у період вагітності обмежений, а введення контрастної речовини, посилене гадолінієм, протипоказане у першому триместрі, оскільки вона проникає через плаценту. У нещодавно проведеному дослідженні показано 98% чутливість магнітно-резонансної томографії грудної залози в діагностиці раку грудної залози, пов’язаного з вагітністю, що дало змогу змінити режим лікування у 28% жінок [27]. Необхідні комплексні поетапні дослідження, оскільки рак грудної залози у період вагітності може бути виявлений у запущеній стадії. Рентгенографія грудної клітки з екрануванням живота для оцінювання легень та ультразвукове дослідження печінки є безпечними. Сканування кісток можна проводити після пологів, але за наявності симптомів, безпечним методом є безконтрастна магнітно-резонансна томографія скелета [25].
Модифікована радикальна мастектомія з аксилярним стадіюванням – це лікування вибору в першому триместрі. Ад’ювантну хіміотерапію можна розпочати у другому триместрі та провести променеву терапію після пологів [28, 29]. Органозбережні операції можна безпечно виконати у другому та третьому триместрах. Досвід використання біопсії сторожових лімфатичних вузлів у період вагітності обмежений. Синій барвник протипоказаний, але технецій‑99м застосовувати безпечно. Ад’ювантну хіміотерапію за режимами на основі антрацикліну (наприклад, різними комбінаціями циклофосфаміду, доксорубіцину та флуорурацилу) можна розпочати у другому та третьому триместрі. Недостатньо даних, щоб рекомендувати таксани, але паклітаксел можна використовувати після першого триместру, якщо є відповідні показання. Трастузумаб протипоказаний, оскільки повідомлялося про олігогідрамніон/ангідрамніон на фоні такого лікування. Гормонотерапія, включаючи тамоксифен, інгібітори ароматази та аналоги лютеїнізуючого гормону, протипоказана у період вагітності через високий ризик формування вроджених вад. Якщо пацієнтка завагітніла під час лікування тамоксифеном, слід рекомендувати переривання вагітності [28, 29].
Рак яєчника
Пухлини яєчників не є рідкістю у період вагітності і фіксуються приблизно від 1 на 600 до 1 на 1500 вагітностей. Більшість із них є доброякісними і лише 1-3% можуть бути злоякісними. Найбільш частими злоякісними пухлинами яєчників є герміногенні пухлини, за якими ідуть стромальні пухлини статевого канатика, пограничні пухлини та інвазивні епітеліальні пухлини [30]. Найпоширенішим симптомом є біль у животі або тазовій ділянці. Одна третина випадків раку яєчника діагностується випадково. Більшість пухлин виявляють на І стадії, середній вік хворих – 25,8 року, при герміногенних пухлинах та інвазивному епітеліальному раку – 31,6 року, середній розмір пухлини – 18 та 12 см відповідно [31, 32].
Трансвагінальне та ультразвукове дослідження живота мають високу чутливість та специфічність у діагностиці пухлин яєчників, однак найкращу діагностичну точність має магнітно-резонансна томографія [33]. Магнітно-резонансна томографія (без контрастування) та дифузно-зважена візуалізація корисні при оцінюванні ступеня перитонеального поширення хвороби та метастазів у лімфатичних вузлах. Визначення пухлинних маркерів не доцільне, оскільки рівень СА 125, альфа-фетопротеїну та бета-хоріонічного гонадотропіну у період вагітності підвищений. Вміст інгібіну В, антимюллерового гормону, HE4, СА 19-9 та лактатдегідрогенази не підвищується, і їх можна використовувати для діагностики пухлин при вагітності.
Рак яєчника на ранній стадії у другому та третьому триместрах вагітності можна лікувати хірургічно – хірургічне стадіювання, сальпінговаріоектомія, оменектомія, перитонеальна біопсія та оцінювання підозрілих лімфатичних вузлів. Як лапароскопія, так і лапаротомія є прийнятими процедурами. Слід уникати розриву яєчника та витікання його вмісту. Хіміотерапію на основі паклітакселу/карбоплатину безпечно призначати у другому та третьому триместрі при епітеліальному раку яєчника, однак її потрібно припинити до 37-го тижня, щоб уникнути мієлосупресії у новонародженого. Бевацизумаб не рекомендується застосовувати. Вагінальне розродження є оптимальним варіантом при раку яєчника на ранній стадії, який лікується хірургічним шляхом. При герміногенних пухлинах яєчників режим BEP вважається занадто токсичним через значне обмеження росту плода та високу частоту неонатальних ускладнень. Паклітаксел і цисплатин слід вводити щотижня відповідно до рекомендацій ESMO [29]. Поширені пухлини (III та IV стадій), виявлені в першому та на початку другого триместру, потребують хірургічного лікування та проведення ад’ювантної хіміотерапії. У кінці другого та третього триместрів призначають неоад’ювантну хіміотерапію до досягнення зрілості плода. Можливим є кесарів розтин із подальшим повним циторедуктивним хірургічним втручанням. Хоча результати вагітності хороші, недоношеність, втрата плода через хірургічні ускладнення й обмеження росту плода все ж трапляються. Онкологічні результати відповідають таким у невагітних [34].
Лікування раку у період вагітності
Променева терапія
Променева терапія у вагітної пацієнтки повинна ретельно плануватися. Радіолог і фізик повинні мінімізувати прямі та непрямі джерела радіації для плода. Доза плода не має перевищувати 50-100 мГр [35]. Ризики для плода в різні періоди розвитку узагальнені в таблиці.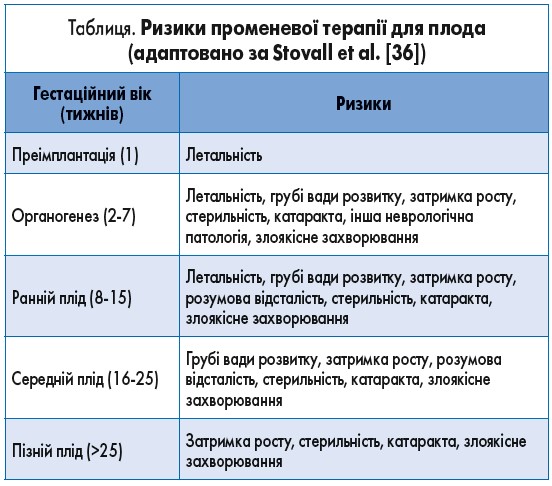
Розсіювання та просочування променів викликають занепокоєння навіть при належному екрануванні (хоча воно здатне мінімізувати ризик). Захист матки, особливо на пізніх термінах вагітності, може бути утруднений через важкість матеріалів, що використовуються для цього. Деякі акушери рекомендують регулярно проводити клінічне та ультразвукове обстеження, щоб визначити передлежання плода з метою виведення голови плода з потенційного поля променевої терапії.
Хіміотерапія
Після першого триместру вагітності застосування більшості хіміотерапевтичних засобів є відносно безпечним. Трансплацентарне проникнення хіміотерапевтичних препаратів істотно відрізняється: деякі агенти, такі як паклітаксел, мають низький рівень проникнення через плаценту, антрацикліни – проміжний, карбоплатин – високий [8, 9]. Незважаючи на це, введення карбоплатину після 12-14 тижнів вагітності, здається, мало шкодить плоду, що розвивається [37].
Трастузумаб, як правило, протипоказаний при вагітності через наявність HER2-рецепторів на нирках плода, що призводить до оліго- або ангідрамніозу та гіпоплазії легень плода. Антифолати, такі як метотрексат, також протипоказані.
Ризик розвитку вроджених вад безпосередньо пов’язаний із гестаційним віком. До 12-го тижня вагітності існує ризик формування вад очей, вух і системи крові; ризик значно знижується після повного органогенезу.
Хіміотерапія може спричинити значне зниження вироблення материнської крові, що призводить до низького рівня тромбоцитів та ризику значного інфікування. Застосовуючи хіміотерапію, слід ретельно планувати термін пологів. Розродження не повинне плануватися протягом 3 тижнів після хіміотерапії. З цієї причини хіміотерапію не слід проводити після 37-го тижня вагітності, враховуючи ризик спонтанних пологів.
Тривале спостереження за дітьми, народженими від матерів, які отримували хіміотерапію у період вагітності, не свідчить про підвищений ризик вроджених порушень або затримки психічного розвитку. Кількість дітей, яких спостерігають тривалий час, ще невелика, і дані слід трактувати обережно. Потенційні ризики включають порушення серцевої функції у дітей, які зазнають впливу антрациклінів у внутрішньоутробний період. Антрацикліни зазвичай використовують для лікування раку грудної залози, вони чинять безпосередній вплив на серцеву функцію. В одному із досліджень під час спостереження 17 дітей після застосування антрациклінів не було виявлено електро- або ехокардіографічних змін.
Хірургічне лікування
У період вагітності операція з приводу онкологічного захворювання може бути показана для діагностики, лікування та стадіювання. Хірургічне втручання є невідкладним, але не екстреним, його можна відкласти до досягнення зрілості плода без шкоди для загальних результатів лікування. Як правило, хірургічні процедури найкраще проводити у другому триместрі для запобігання мимовільному перериванню вагітності [38, 39].
Операція у другому триместрі технічно менш складна, ніж у третьому, через розмір матки. Коли операцію проводять після 28-го тижня вагітності, слід вводити токолітики для запобігання передчасним пологам, а кортикостероїди – для підвищення легеневої зрілості. Маніпуляції з маткою слід звести до мінімуму. Однобічна або двобічна оваріоектомія може бути проведена безпечно після першого триместру вагітності. Якщо це можливо, віддають перевагу регіонарній анестезії перед загальною через потенційний ризик аспірації [40].
Бічний нахил під час операції може допомогти запобігти аортокавальному стисненню [41]. Пацієнтка має надати згоду на екстрений кесарів розтин у третьому триместрі, якщо виникне загроза ускладнень у плода. Лікувальне хірургічне втручання можна проводити в будь-якому триместрі вагітності.
Поширення пухлини на плаценту та плід
Метастазування у плаценту і плід зустрічається рідко. Найбільш схильними до метастазування у плаценту є меланома та гематологічні злоякісні захворювання. У всіх випадках, коли можливе поширення пухлини на плаценту, її слід ретельно обстежити під час гістологічного дослідження. Новонародженого слід ретельно оглянути та регулярно обстежувати на предмет ознак метастазування.
Консультування
Рак у період вагітності становить як психологічну, так і біологічну дилему, оскільки лікування має бути спрямоване на порятунок двох життів: матері та плода. Мультидисциплінарний підхід може допомогти зменшити страждання пацієнтки та її родини. Важливо, щоб акушер, онколог, педіатр і психотерапевт взяли на себе провідні ролі. Пацієнтка та її родина мають брати активну участь у процесі прийняття рішень, що сприятиме підвищенню впевненості та підтримці.
Повідомлення поганих новин
Отримати погані новини болісно для будь-якого пацієнта [42]. Консультація завжди має включати інформацію про перебіг вагітності та вплив захворювання на матір і дитину [43]. При цьому слід дотримуватися певних рекомендацій [42]:
- оцінити психічний стан пацієнтки;
- забезпечити конфіденційність;
- виділити достатньо часу для оцінювання ситуації;
- бути чесними;
- надавати точну інформацію;
- проявити співпереживання;
- упорядкувати присутність членів родини;
- представляти обґрунтовані варіанти лікування;
- інформувати про інші підтримуючі послуги;
- чітко вказати, що пацієнтка ухвалює остаточне рішення щодо її лікування;
- коротко пояснити процес, за допомогою якого встановлено діагноз;
- використовувати різноманітні способи передачі інформації, наприклад, друковані та відеоматеріали.
Консультація з приводу прогнозу
Для прийняття рішень щодо лікування пацієнти потребують інформації про прогноз. Більшість пацієнтів хочуть отримати конкретну та чесну інформацію про прогноз:
- специфічну інформацію (середня виживаність);
- загальну інформацію («я думаю, що ваші шанси хороші»);
- статистичну інформацію (середній часові інтервали);
- винятки (виживаність vs шанси).
Реалістичний і чесний підхід має важливе значення для підтримки та впевненості пацієнта. Надання занадто великого обсягу інформації за допомогою медичних термінів, приховування новин, хибне заспокоєння та патерналістичний підхід, ігнорування занепокоєнь пацієнта знижують його впевненість [44]. Основою спільного прийняття рішень є обмін інформацією – чітко, на основі доказів неупередженого характеру, з належним урахуванням цінностей, турбот, переконань і життєвих пріоритетів пацієнта.
Botha M.H., Rajaram S., Karunaratne K. Cancer in pregnancy. Int J Gynecol Obstet. 2018; 143 (suppl. 2): 137-142. DOI: 10.1002/ijgo.12621.
Список літератури знаходиться в редакції.
Переклав з англ. Назар Лукавецький
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 3 (64) 2020 р.


