25 липня, 2020
Інтенсифікація терапії цукрового діабету 2 типу: перша фіксована комбінація інсуліну гларгіну та агоніста рецептора глюканоподібного пептиду‑1
Поширеність цукрового діабету (ЦД) в Україні збільшилася за останнє десятиріччя на 50 відсотків, у 2016 р. на діабет хворіло вже понад 1,2 млн осіб. У США на діабет страждає понад 29 млн – приблизно 9% від усього населення Сполучених Штатів.
Крім того, приблизно 86 млн дорослої популяції (>33% населення США) мають предіабет, стан, який значно збільшує ризик розвитку діабету. Згідно з останніми тенденціями щодо старіння американської нації протягом наступних кількох десятиліть, поширеність діабету, за прогнозами, до 2050 року зросте до 1 з 3 дорослих особи.
Американська діабетична асоціація (ADA) і Американська асоціація клінічних ендокринологів (AACE) видали схожі керівництва щодо лікування пацієнтів ЦД 2 типу, хоча документ ADA характеризується більш консервативним підходом. З огляду на чинники пацієнта, ADA рекомендує підтримувати рівень HbA1c <7,0%, тоді як AACE цільовим вважає значення HbA1c ≤6,5%. Більш строгі вимоги до рівня HbA1c – <6,5% або <8,0% – ADA рекомендує для конкретних груп: нещодавно діагностованих пацієнтів молодого віку та літніх осіб із множинними супутніми захворюваннями відповідно.
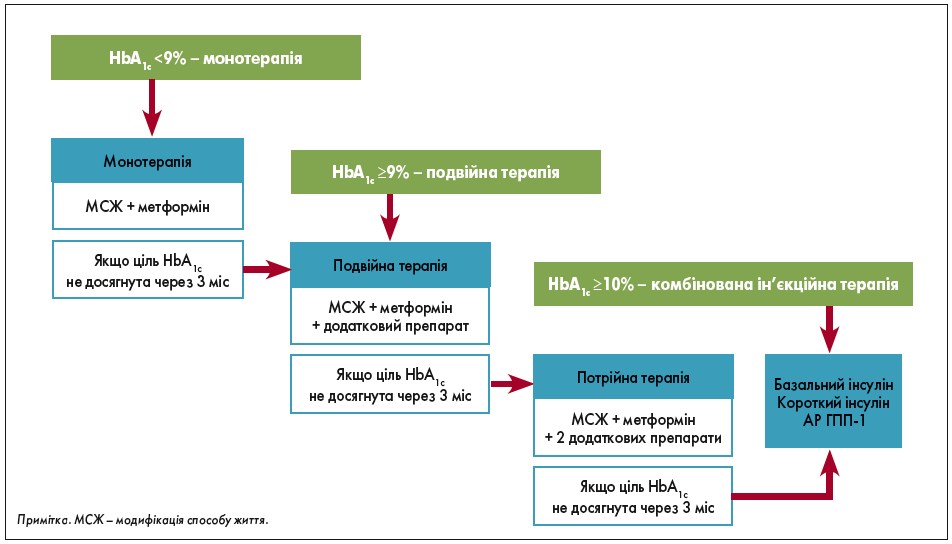
Усі пацієнти, в яких ЦД 2 типу був діагностований нещодавно, мають отримати консультацію щодо зміни способу життя, передусім поліпшення харчування й збільшення фізичної активності та фізичних вправ. Більшість хворих мають почати терапію з метформіну, якщо відсутні протипоказання. Реакцію пацієнта слід оцінювати не пізніше ніж через 3 міс після початку терапії, і якщо рівень HbA1c не досяг цільових значень, ADA і AACE пропонують аналогічні поетапні підходи за загальною схемою:
- інтенсифікація до подвійної терапії метформіном та додатковим препаратом;
- подальше посилення до потрійної терапії з двома додатковими препаратами;
- подальша інтенсифікація доін’єкційної терапії базальним інсуліном (БІ) або агоністом рецептора (АР) глюканоподібного пептиду‑1 (ГПП‑1) у пацієнтів, які ще не використовують ін’єкційний препарат.
Кожен крок переглядається через 3 міс для визначення відповіді на лікування. У будь-який момент клініцисти мають розглянути можливість комбінованої ін’єкційної терапії з БІ плюс АР ГПП‑1 або прандіальним інсуліном, якщо пацієнти, які використовують БІ, досягли своїх цільових рівнів глюкози в плазмі натще (ГПН), але рівні HbA1c залишаються вище цільових значень (рис. 1).
Рис. 1. Схема лікування ЦД різними видами терапії
 У своїй доповіді на черговому засіданні «Школи ендокринолога» завідувачка кафедри ендокринології Львівського медичного університету ім. Данила Галицького, доктор медичних наук, професор Аліна Мечиславівна Урбанович докладно розповіла про такий клінічний випадок.
У своїй доповіді на черговому засіданні «Школи ендокринолога» завідувачка кафедри ендокринології Львівського медичного університету ім. Данила Галицького, доктор медичних наук, професор Аліна Мечиславівна Урбанович докладно розповіла про такий клінічний випадок.
Пацієнтка 58 років, з індексом маси тіла (ІМТ) 26,8 кг/м², хворіє на ЦД 2 типу протягом 6 років та отримує БІ 2 роки. Інсулін призначили через 4 роки перебігу захворювання в зв’язку з прогресуванням діабетичної ретинопатії. На сьогодні в пацієнтки наявні такі супутні захворювання: діабетична ретинопатія, проліферативна ст. Діабетична полінейропатія нижніх кінцівок. Гіпертонічна хвороба 2 ст., ІІ ст. На момент звернення рівень ГПН – 12 ммоль/л, постпрандіальна глікемія (ППГ) – 13,0 ммоль/л, HbA1c – 9,5%. Було призначено терапію: інсулін НПХ – 18 Од вранці, 9 Од ввечері, метформін 2000 мг/добу.
Тут треба зробити деяке пояснення. Проблема «недотитрації» інсуліну та недосягнення цільового рівню HbA1c актуальна не лише для України, а й для західноєвропейських систем охорони здоров’я. Приблизно 50-70% пацієнтів із ЦД 2 типу на базальній інсулінотерапії не досягають рівня HbA1c ≤7% після 1-го року лікування, що призводить до макро- та мікросудинних ускладнень. Затримка інтенсифікації терапії на 1 рік у пацієнтів із ЦД 2 типу при рівні HbA1c >7% суттєво підвищує ризик серцево-судинних (СС) катастроф (рис. 2). 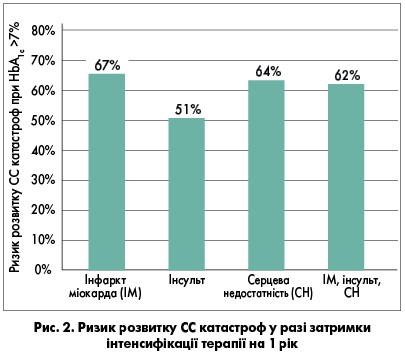
У 2018 р. ADA були розроблені індивідуалізовані цілі терапії ЦД 2 типу. Тому кожен лікар має чітко встановлювати цільовий рівень як глікемії, так і HbA1c для кожного свого пацієнта. Максимальний цільовий показник HbA1c може складати 8% у пацієнтів із тяжкими гіпоглікеміями в анамнезі, короткою очікуваною тривалістю життя, наявністю мікро- та макросудинних ускладнень, тяжких супутніх захворювань, а також у хворих, в яких важко досягти цілі, незважаючи на навчання самоконтролю діабету, відповідний моніторинг рівня глюкози та ефективні дози цукрознижувальних препаратів (ЦЗП), включно з інсуліном. У більшості дорослих не вагітних пацієнтів треба намагатися досягти цільового рівня HbA1c <7%, ГПН – 4,4-7,2 ммоль/л, ППГ (глікемія через 2 год після їжі) – <10 ммоль/л (табл.). 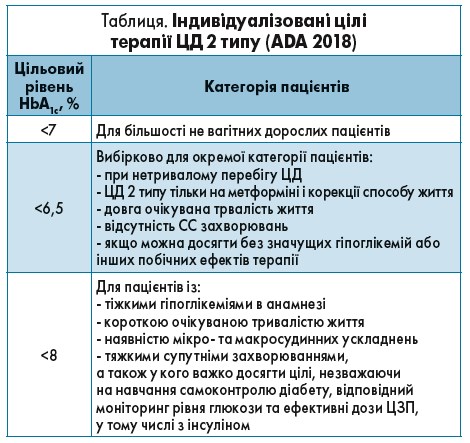
Необхідно слідкувати за варіабільністю глікемії в пацієнтів. На жаль, сьогодні це вдається зробити лише в частки хворих на ЦД 2 типу, і тому нам залишається контроль тільки трьох ключових параметрів: HbA1c, ГПН і ППГ. Щодо останнього параметру, то його контроль є дуже важливим фактором у хворих на діабет 2 типу.
ППГ складає майже 50% від підвищеної глікемії впродовж доби. Безперечно, на цей показник впливають певні чинники, як-от: рівень глікемії перед їдою, склад їжі, а також – наскільки збережена секреція інсуліну. Неабияке значення має й те, яку терапію застосовує пацієнт, чи немає проблем з евакуацією їжі зі шлунку, як абсорбується глюкоза в тонкому кишечнику, як проходить метаболізм глюкози в печінці і переферичній крові.
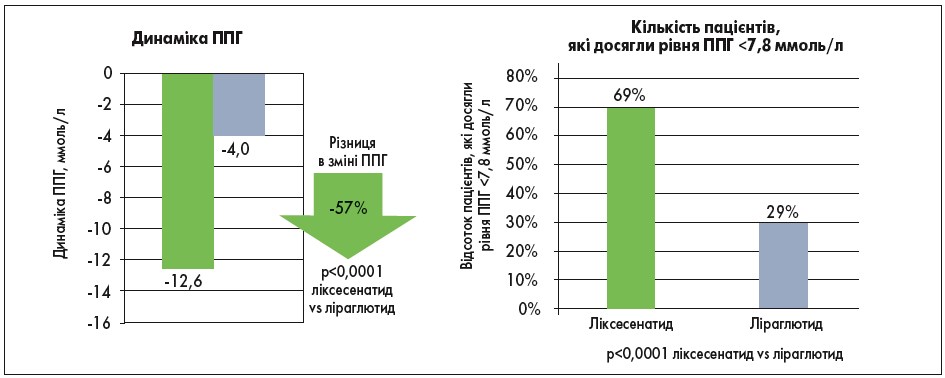
Ліксисенатид, який крім інсуліну гларгіну входить до складу препарату Соліква (виробник «Санофі-Авентіс Дойчланд ГмбХ», Німеччина), є агоністом ГПП‑1 прандіальної дії і тому найбільш виражено впливає на ППГ. Він діє вдвічі ефективніше, ніж ліраглютид, який теж є аналогом людського ГПП‑1. Результати прямого порівняльного дослідження ефективності ліксисенатиду і ліраглютиду в лікуванні пацієнтів із ЦД 2 типу (Kapitza C., Forst T. et al., 2013), яке тривало 28 днів, показують, що різниця в зміні ППГ при застосуванні ліксисенатиду, якщо порівняти з ліраглютидом, складає 57% (рис. 3). Ліраглютид, своєю чергою, вираженіше знижав рівень ГПН, ніж ліксисенатид (-1,3 ммоль/л проти 0,34 ммоль/л відповідно). Профілі безпеки та переносимості обох препаратів були зіставні.
Рис. 3. Динаміка ППГ і кількість пацієнтів, які досягли цільових рівнів ППГ після закінчення 28 днів терапії
Отже, повернемося до згаданої клінічної ситуації. Передусім лікарю необхідно визначити глікемічні цілі, у нашому випадку це HbA1c ≤7%, ГПН – 4,4-7,2 ммоль/л, ППГ – <10 ммоль/л. Для цього лікар має застосувати терапію згідно з рекомендаціями міжнародних гайдлайнів (рис.1). Оскільки кожен лікар, який призначає лікування, підбирає такі препарати, які б не спровокували гіпоглікемію в пацієнта, доповідачкою було порекомендовано призначити пацієнтці комбінацію інсуліну та АР ГПП‑1, щоб досягти цільових рівнів глікемії, запобігти гіпоглікеміям, а також для комфортного тривалого застосування терапії та підвищення якості життя.
Уже згаданий препарат Соліква поєднує в собі два різних компоненти з різними механізмами дії зниження рівня глюкози. Інсулін гларгін – це пролонгований БІ, націлений на рівні ГПН, імітує фізіологічну секрецію інсуліну, забезпечує його безпіковий рівень протягом 24 годин. Ліксисенатид, АР ГПП‑1, приймають 1 раз на день. Цей препарат підвищує рівень інсуліну та знижує секрецію глюкагону, залежного від глюкози таким чином, що мінімізує ризик гіпоглікемії, асоційованої з лікуванням. Ліксисенатид також уповільнює спорожнення шлунка, знижуючи швидкість, з якою глюкоза після їжі входить у кровообіг, і тим самим зменшує відхилення ППГ (рис. 4). Крім того, ліксисенатид продемонстрував СС безпеку при тривалому застосуванні. У дослідженні ELIXA за участю пацієнтів із високим СС ризиком, зумовленим нещодавніми СС подіями, які вимагали госпіталізації, одноразова ін’єкція ліксисенатиду в дозі 20 мкг в якості додаткової протиглікемічної терапії протягом 25 міс не поступалася в ефективності плацебо для комбінованого випадку СС смерті, нефатального ІМ, нефатального інсульту. У липні 2016 р. ліксисенатид був затверджений у США як доповнення до дієти та фізичних вправ при лікуванні пацієнтів із ЦД 2 типу. 
Клінічна ефективність препарату була доведена в програмі низки клінічних досліджень під назвою LixiLan. Результати, які було отримано в 30-тижневому рандомізованому контрольованому багатоцентровому клінічному дослідженні ефективності та безпеки препарату Соліква проти інсуліну гларгіну 100 Од/мл у пацієнтів із ЦД 2 типу та недостатнім глікемічним контролем на тлі терапії пероральними ЦЗП в комбінації з БІ, продемонстрували, що завдяки використанню препарату Соліква майже вдвічі більше пацієнтів досягли цільового рівня HbA1c. Водночас у групі терапії інсуліном гларгіном цільового рівня досягли лише 29,6% учасників дослідження. Крім того, у хворих на ЦД 2 типу, які приймали Солікву, виявлені кращі показники ППГ та зниження маси тіла в середньому на 0,7 кг, тоді як застосування інсуліну гларгіну призвело до підвищення ваги тіла в середньому на 0,7 кг (рис. 5).
У дослідженні LixiLan-L продемонстровано, що при застосуванні Солікви, якщо порівнювати з терапією інсуліном гларгіном, більшість пацієнтів досягали цільового рівня HbA1c <7% без збільшення ваги тіла та без документованих гіпоглікемій. Але Соліква – це препарат, який буде корисним не лише у хворих на ЦД 2 типу з ожирінням. Він є ефективним практично у всіх пацієнтів із ЦД 2 типу, незалежно від їхнього ІМТ. Прийом Солікви дав можливість майже 80% осіб з ІМТ <30 кг/м2 досягти цільових рівнів HbA1c. Серед пацієнтів із ЦД 2 типу й ожирінням цільових рівнів глікемії в дослідженні LixiLan досягли 70%.
Перевагами препарату Соліква є його висока результативність без набору ваги й збільшення ризику гіпоглікемії, можливість робити лише 1 ін’єкцію на добу, відсутність негативних явищ з боку шлунково-кишкового тракту (ШКТ), а також те, що препарат титрується як БІ.
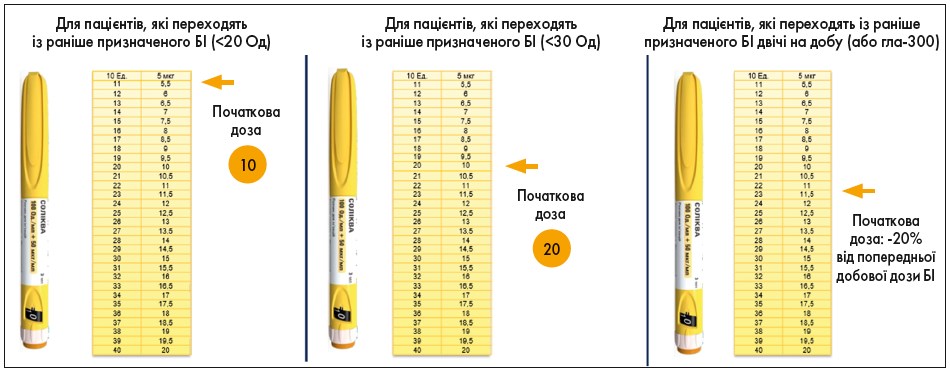
Якщо переводити пацієнта з раніше призначеного БІ в дозі 20 Од, то початкова доза Солікви буде дорівнювати 10 Од. У тих, хто приймав БІ у дозі <30 Од, стартова доза Солікви складе 20 Од. Для пацієнтів, які переходять із раніше призначеного БІ двічі на добу або гларгіну‑300 (гла‑300), початкова доза препарату складатиме 20% від попередньої добової дози БІ. Найбільш поширений темп титрації: 1 раз на тиждень за рівнем глюкози крові натще (рис. 6).
Після детального розбору принципу дії та особливостей дозування препарату Соліква нашій пацієнтці перед початком лікування комбінованим препаратом було рекомендовано припинити інсулінотерапію та призначено початкову дозу 20 Од (хвора приймала інсулін НПХ: 18 Од/вранці, 9 Од/ввечері, метформін 2000 мг/добу) з подальшою титрацією 1 раз на тиждень до цільових рівнів глікемії. Якщо ГПН >7,2 ммоль/л, ми додаємо 2 Од Солікви; якщо ГПН 4,4-7,2 ммоль/л, дозу не змінюємо; якщо ГПН <4,4 ммоль/л, дозу зменшуємо на 2 Од. Загалом титрація дози препарату в пацієнтів відбувається протягом від 1 до 2 місяців. Через 3 міс пацієнтка отримувала 28 Од Солікви, препарат титрували впродовж 4 тижнів. За цей період порушень із боку ШКТ зазначено не було, ІМТ знизився до 26,5 кг/м². Досягнуто рівні: глікемії натще – до 6,9-7,0 ммоль/л, ППГ – 8-9 ммоль/л, HbA1c – 6,8%. Пацієнтці рекомендовані: дотримання дієти, регулярні фізичні навантаження, продовження терапії, самоконтроль ГПН 1 раз на добу, самоконтроль ППГ 2-3 рази на добу, контроль HbA1c через 3 місяці.
Рис. 6. Дозування препарату Соліква в пацієнтів, які переходять із раніше призначеного БІ
В Україні препарат Соліква було зареєстровано 21.06.2018 р.: розчин для ін’єкцій, 100 Од/мл + 50 мкг/мл (ТОВ «Санофі Авентіс Україна»). Інсулін гларгін + ліксисенатид 100/50 випускається у вигляді заздалегідь заповненої шприц-ручки одноразового використання по 3 мл для підшкірних ін’єкцій (рис. 7). 
ЦД 2 типу – прогресуюче захворювання, і для досягнення й підтримки глікемічного контролю часто потрібна інтенсифікація лікування. БІ і АР ГПП‑1 усувають деякі дефекти, які спостерігаються в фізіопатології діабету 2 типу. При порівнянні комбінацій інсулін / АР ГПП‑1 із фіксованим співвідношенням і БІ спостерігається перевага в зниженні рівня HbA1c, при цьому загальна перевага проявляється також у нейтральності ваги або її втраті, зниженні ризику гіпоглікемії та потреби в дозі інсуліну. До того ж комбінація з фіксованим співвідношенням має перевагу завдяки менш складній схемі лікування – з однією ін’єкцією в день. Результати надійних клінічних випробувань демонструють величезний потенціал цих продуктів. Отже, комбінація АР ГПП‑1 і БІ з фіксованим співвідношенням є потенційно корисним інструментом у терапії пацієнтів із ЦД 2 типу завдяки сприятливому профілю безпеки та ефективності.
Підготувала Юлія Золотухіна
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 2 (50), 2020 р.