25 липня, 2020
Що нового в лікуванні діабетичної нейропатії?
Діабетична нейропатія (ДН) – це ускладнення, яке найчастіше спостерігається у хворих на цукровий діабет (ЦД) та викликає неабияке занепокоєння в пацієнтів та лікарів, передусім через свою здатність значуще погіршувати якість життя хворого. Нейропатія являє собою широкий спектр порушень, які вражають проксимальні й дистальні рухові та чутливі нерви. Зазвичай ДН супроводжується пекучим болем, парестезіями та онімінням – так званий синдром «шкарпеток-рукавичок», названий так за місцем появи симптомів захворювання. Завчасна діагностика ДН, лікування й профілактика її наслідків є дуже важливим завданням будь-якої національної системи охорони здоров’я. Ті, хто буде старанно компенсувати прояви ЦД, слідкувати за станом своєї нервової системи, запобігати розвитку нейропатії або прогресуванню вже наявного ускладнення, матимуть шанс суттєво подовжити тривалість свого життя та покращити його якість. А завдання клініцистів – ураховувати функціональний стан пацієнта, а також потенційний несприятливий вплив медикаментозних засобів при виборі препаратів для лікування ДН.
ДН характеризується ознаками та симптомами дисфункції периферичного нерва у хворих на діабет, в яких були виключені інші причини нейропатії [1]. Залежно від класів залучених нервових волокон ДН включає низку різних синдромів [2]. У 1988 р. в м. Сан-Антоніо (США) на конференції з ДН було прийнято класифікацію (так звана Конвенція Сан-Антоніо), згідно з якою основними групами неврологічних розладів у хворих на ЦД є:
- субклінічна нейропатія – діагностується при виявленні порушень під час проведення електродіагностики та кількісному дослідженні порогу чутливості вібрації, тактильної чутливості, тепла й холоду;
- дифузна клінічна нейропатія з дистальним сенсомоторним та вегетативним синдромами;
- вогнищеві синдроми [3].
Щонайменше 25% пацієнтів із ЦД страждають на дистальну симетричну полінейропатію (ДСП), одну з проблем охорони здоров’я, оскільки ця патологія є причиною значної захворюваності та смертності [4-7]. ДСП – основний фактор, який призводить до виникнення діабетичної виразки стопи, остеоартопатії, остеомієліту та ампутації нижніх кінцівок. Невропатичний біль вражає приблизно 16% пацієнтів із ЦД [9]. Цей суб’єктивний симптом погіршує якість життя та сну, оскільки зазвичай він посилюється вночі [1, 8]. Часто це змушує пацієнтів звертатися за медичною допомогою [10]. Однак лікування діабетичної симетричної полінейропатії все ще є проблемою для лікаря [11].
Є декілька базових моментів у лікуванні ДН:
- Контроль глікемії до рівнів нормоглікемії.
- Патогенетично орієнтована терапія.
- Антиоксидантна терапія.
- Уникання факторів ризику [8].
Погано контрольований рівень глюкози в крові призводить до розвитку ДН і її прогресування до тяжкої форми. Кокранівський огляд двох рандомізованих контрольованих досліджень (n=1228) зазначив, що посилений контроль рівня глюкози в пацієнтів із ЦД 1 типу значуще знижує ризик розвитку ДН (різниця ризиків =1,84%; 95% ДІ від -1,11 до -2,56) [2]. Фактори ризику серцево-судинної системи: вік, куріння, наявність артеріальної гіпертензії, ожиріння, дисліпідемія та захворювання периферичних артерій, також асоційовані з підвищеним ризиком ДН [1].
Підтримання нормоглікемії сьогодні визнано першим кроком у профілактиці ДН [12, 13]. Оскільки досягти цього доволі важко, часто потрібне додаткове лікування симптомів нейропатії [14]. Патогенетично орієнтована терапія може затримати, зупинити або сповільнити прогресування нейропатії, а також полегшити біль. Хоча симптоматична терапія не впливає на перебіг захворювання, але вона може полегшити хворобливі симптоми і покращити якість життя пацієнтів [15].
Антидепресанти, опіоїди (наприклад, оксикодон із контрольованим вивільненням), а також такі відомі протисудомні засоби, як, карбамазепін, полегшують біль, але мають низку несприятливих побічних ефектів [16]. Більш нові протисудомні препарати – габапентин та прегабалін мають високу спорідненість до зв’язування з α2-δ-субодиницею каналів кальцію, активованих напругою. Вони впливають на ДН частково завдяки модуляції кальцієвих каналів у патогенезі захворювання [16, 17].
Патогенез ДН
Патогенез ДН доволі складний. Виділяють такі основні його механізми:
- посилений потік через поліольний шлях, опосередкований альдозоредуктазою та сорбітолдегідрогеназою, що призводить до накопичення сорбіту та виснаження міоінозитолу [8];
- порушується функція мікрокапілярів ендоневрію з виникненням їх гіпоксії внаслідок інактивації оксиду азоту [18];
- накопичуються кінцеві продукти посиленого глікозилювання (КПГ), які, зв’язуючися зі специфічними рецепторами нейронів, викликають оксидативний стрес і призводять до накопичення нуклеарного фактору каппа B (NF-κB) [8, 18-20];
- посилене перекисне окислення ліпідів in vivo. Найбільш надійним показником підвищеного оксидативного стресу є зниження рівня глутатіону [18];
- активація протеїнкінази С (ПКС) через посилене вивільнення внутрішньоклітинного діацилгліцерину (ДАГ) внаслідок гліколізу. Гіперглікемія активує ПКС, особливо її βII ізоформу. Підвищена активність ПKC-β може погіршити ендоневральний кровоток. Останнім часом гіперглікемія асоціюється з активацією ПКС та підвищенням ізоформ натрієвих каналів натрію; обидва відіграють вирішальну роль у сприйнятті болю [21-24];
- зміни білкових кіназ, активованих мітогеном, призводять до сигнального каскаду, який бере участь у патогенезі периферичної ДН [25];
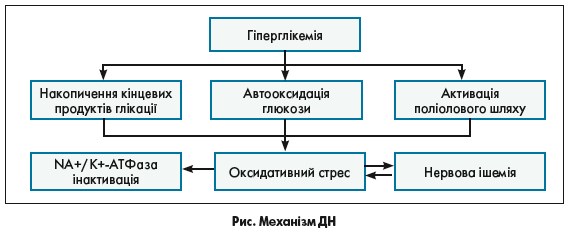
- порушений гомеостаз Ca2+ [26] (рис.).
Сьогодні продовжують вивчати ефективність та переносимість інгібіторів редуктази альдози та інгібіторів ПКС [40]. Крім того, при діабеті спостерігається дефіцит ацетил-L-карнітину. Заміщення ацетил-L-карнітину коригує порушення нейронної Na+/K+-ATФази, міоінозитолу й окису азоту. Це також покращує регенерацію нервових волокон та полегшує симптоми, особливо біль у пацієнтів із встановленою ДН [41-43]. Тіоктова кислота (ТК) нормалізує активність ендоневральної Na+/K+-ATФази в досліджуваних діабетичних нервах [44]. ТК впливає на поглинання глюкози, тим самим збільшуючи активність поліольних шляхів [44], а також циклу Кребса [45].
Лікування ДН
У підходах до лікування ускладнень ЦД, зокрема уражень нервової системи, залишається багато невирішених питань. При високій поширеності ДН і відсутності дієвих превентивних заходів постає завдання її своєчасного виявлення та лікування ускладнень.
Основним методом профілактики й терапії ДН є досягнення і тривале підтримання оптимального глікемічного контролю у хворих на ЦД. Останніми роками на фармацевтичному ринку з’явилися нові класи препаратів, які забезпечують ефективнішу й безпечнішу антигіперглікемічну терапію. На жаль, у реальній клінічній практиці лише в частини пацієнтів удається досягти тривалого забезпечення цільових значень вуглеводного обміну. При цьому навіть поліпшення його компенсації, доведення показників до цільових значень у хворих на ЦД не супроводжуються нормалізацією оксидативного статусу. Це пояснює доцільність застосування антиоксидантів у комплексному лікуванні ЦД. Застосування препаратів з антиоксидантним механізмом дії в лікуванні ДН патогенетично обґрунтовано.
Базова терапія ЦД 2 типу метформіном може змінювати вираженість оксидативного стресу [66]. З іншого боку, є повідомлення, що тривалий прийом метформіну здатен спричинити розвиток дефіциту вітаміну В12, але без переконливих доказів того, що цей дефіцит впливає на наявність або тяжкість периферичної нейропатії [67, 68]. Деякі автори рекомендують додатково призначати препарати вітаміну В12 пацієнтам, які тривалий час приймають метформін.
Патогенетична терапія є першою лінією лікування ДН, оскільки вона сприяє не тільки зниженню суб’єктивних невропатичних симптомів (біль, печіння, парестезії), але й зменшенню неврологічних порушень (чутливі та рухові розлади, такі як зниження чутливості в ногах, слабкість м’язів стоп). На тлі симптоматичної терапії спостерігається тільки зменшення больового синдрому, тоді як функціональний стан нерва продовжує погіршуватися.
Сьогодні роль оксидативного стресу в розвитку ДН вважається однією з провідних, тому логічним є застосування в якості патогенетичної терапії препаратів з антиоксидантною дією. Перше місце серед антиоксидантів і взагалі препаратів, які використовують для патогенетичного лікування ДН, посідає вже згадана тіоктова кислота (ТК) (або α-ліпоєва кислота, АЛК), природний ліпофільний антиоксидант, що діє як кофактор для основних комплексів у мітохондріальних ферментах. ТК містить 2 тіолові групи, здатні окислюватися або відновлюватися. Відновлена форма називається дігідроліпіновою кислотою (ДЛК), її окисленою формою і є ТК. Остання може проникати крізь гематоенцефалічний бар’єр і відновлювати інші антиоксиданти, такі як вітаміни С, Е і глутатіон [72]. Як експериментальні, так і клінічні дані свідчать на користь ефективності застосування ТК при ураженні нервової системи.
Хворі на діабет із невропатією, які отримували ТК в дозі 600 мг внутрішньовенно протягом 3 тиж, зазначають зменшення болю, парестезій та оніміння [14, 80, 81]. Згідно з результатами недавнього метааналізу (n=1258) таке лікування полегшувало невропатичні симптоми через 3 тиж [81]. Болюсна інфузія ТК покращувала опосередковану оксидом азоту вазодилатацію ендотелію в пацієнтів із ЦД та мікроциркуляцію у хворих на ДН [60-65, 81-89].
Пероральний прийом тіоктової кислоти протягом 5 тиж покращував нейропатичні симптоми та коригував її дефіцит у 187 пацієнтів із діабетичною симетричною полінейропатією. Такий результат можна вважати обнадійливим, оскільки дефіцит тіоктової кислоти – основний фактор ризику виникнення нейропатичної виразки стопи [10, 90-92].
Можливості ТК зменшувати оксидативний стрес при ЦД доведені в низці досліджень (ALADIN I, ALADIN II, SYDNEY I, SYDNEY II, NATAN II, ORPIL та ін.), в яких було продемонстровано, що важливою перевагою ТК є не лише її участь у зменшенні проявів оксидативного стресу, тобто у впливі на судинний компонент, але й її здатність збільшувати вміст в нерві нейротрофічних факторів, наприклад фактору росту нерва. Крім того, у дослідженні Deutsche Kardiale Autonome Neuropathie (DEKAN) у 73 хворих на ЦД 2 типу з порушенням варіабельності серцевого ритму протягом 4 міс використовували для лікування або ТК в таблетках (200 мг 4 рази на день, сумарна доза 800 мг), або плацебо. У ході аналізу динаміки на тлі лікування варіабельності серцевого ритму в спокої, під час дихання і при добовому моніторуванні ЕКГ (спектр потужності високих і низьких частот) виявлено достовірне збільшення варіабельності серцевого ритму в групі ТК проти групи плацебо. Ученими також було зазначено поліпшення стану симпатичної нервової системи та зменшення вегетативних нервових розладів.
Лікування за допомогою ТК підвищує кількість глутатіону in vivo та in vitro. Глутатіон є важливим ендогенним антиоксидантом, разом із ліпоєвою кислотою він, схоже, відіграє переважну роль в окислювально-відновних механізмах різних клітинних мішеней.
Отже, відповідно до останніх тенденцій, ТК в дозі 800 мг можна вважати важливим компонентом антиоксидантної терапії у хворих на ДН. Нещодавно на фармацевтичному ринку України з’явився новий продукт Тіокт Q10® від компанії Acino Group (Швейцарія). Це унікальний комбінований продукт, до складу якого входить тіоктова кислота (800 мг), ацетил L-карнітин (500 мг) та коензим Q10 (25 мг).
Амінокислота L-карнітин задіяна в процесі транспорту довголанцюгових жирних кислот (ЖК) усередину мітохондрій. Карнітин забезпечує нормальну функцію м’язів, допомагає підтримувати оптимальний фізіологічний стан. За нестачі карнітину невикористані ЖК накопичуються в цитоплазмі, і тоді виникає дефіцит енергії, найбільш відчутний для м’яза серця і скелетної мускулатури. Крім того, як уже було зазначено, ацетил-L-карнітин коригує порушення нейронної Na+/K+-ATФази, міоінозитолу та окису азоту, а ТК нормалізує активність ендоневральної Na+/K+-ATФази.
Кофермент Q10, коензим Q10 (також відомий як убіхінон, кофермент Q, СоQ10, СоQ, Q10 або Q) – група коферментів – бензохінонів, які містять хіноїдну групу і 10 ізопренових хімічних груп. Убіхінон належить до так званих вітаміноподібних сполук. Виявлений в багатьох рослинних і тваринних клітинах. Ця сполука також синтезується в організмі людини з амінокислоти тирозину, через що убіхінон не вважають вітаміном, хоча його роль у метаболічних процесах аналогічна вітамінам. Коензим Q10 є компонентом ланцюга переносу мітохондріальних електронів і сприяє синтезу аденозинтрифосфату (АТФ). Він відновлюється до убіхінолу і перерозподіляється в ліпопротеїни для захисту їх від окислення [70]. Ступінь зниження скорочувальної здатності серця прямо пропорційна ступеню дефіциту АТФ в клітинах серцевого м’яза. Це дає підстави зробити висновок: недостатність коензиму Q10 у серцевому м’язі може призвести до зниження толерантності до фізичного навантаження. Коензим Q10 сприяє поліпшенню мікроциркуляції в усіх тканинах і органах, нормалізації рівня артеріального тиску. АЛК, яка входить до складу продукту, грає роль універсального антиоксиданту, який контролює і нейтралізує вільні радикали в організмі. Ця речовина відновлює ендогенні антиоксиданти, як-от: глутатіон, вітаміни Е і С, коензим Q10. Також АЛК бере участь в обміні речовин, перетворюючи глюкозу в енергію для потреб організму, допомагає підтримувати нормоглікемію. За нормальних умов у клітині зберігається рівновага між вільнорадикальним окисленням та активністю антиоксидантних систем.
Усі вищезазначені позитивні ефекти характеризують продукт Тіокт Q10®, який випускається у вигляді саше. Рекомендована добова доза для дорослих 1 саше на добу. Уміст саше необхідно розчинити в склянці води та ретельно перемішати до утворення однорідної суспензії. Довготривала терапія продуктом Тіокт Q10® сприяє значному зменшенню симптомів ДН.
Унікальність Тіокту Q10 полягає не лише в унікальному складі продукту та посиленому дозуванні ТК, а й в запатентованій формі контрольованого вивільнення ТК протягом 8 год, тоді як для інших препаратів, що містять ТК, цей час дорівнює лише 20-30 хвилинам (Pasotti et al.; Patent №: US 9,333,170,B2; May 10, 2016)*.
Отже, досвід застосування та результати досліджень свідчать про те, що є багато причин вважати ТК основою патогенетичного лікування ДН:
- ТК – це ендогенний антиоксидант прямої (зв’язує вільні радикали) та непрямої (відновлює внутрішньоклітинний рівень глутатіону) дії. Будучи «пасткою вільних радикалів», ТК захищає всі органи і тканини від оксидативного стресу. Використання її в лікувані ЦД нормалізує рівень цукру в крові у хворих на діабет;
- довготривалий прийом 800 мг продукту Тіокт Q10® (1 саше на день) визначеним лікарем курсом;
- завдяки участі в метаболізмі жирів збільшує синтез фосфоліпідів – покращує структуру кліткових мембран;
- нормалізує енергетичний обмін;
- покращує проведення нервових імпульсів.
Час безпосереднього впливу ТК на нервові волокна впливає на ефективність у лікуванні ДН та на зменшення проявів оксидативного стресу. Ось чому фармацевтичні бренди ведуть боротьбу буквально за хвилини перебування ТК в крові! Продукт Тіокт Q10® містить унікальну запатентовану форму контрольованого звільнення, завдяки якій ТК в активній формі перебуває в крові протягом 8 годин (Pasotti et al.; Patent №: US 9,333,170,B2; May 10, 2016). Низка досліджень за участю пацієнтів із ДН, які отримували ТК в дозі 800 мг, продемонстрували значуще зменшення болю, парестезій та оніміння. А комбінація ТК з ацетил L-карнітином та коензимом Q10 посилювала ефективність кожного з компонентів.
ДН – складний і багатогранний клінічний феномен, і нерідко він є наслідком не завжди однозначних і успішних підходів до корекції комплексу метаболічних змін у хворих на ЦД. Успіхи, яких було досягнуто за останні десятиліття в фармакотерапії діабету, сьогодні дають можливість покращувати показники вуглеводного обміну. Важливо зазначити, що лікування ДН має проводитися індивідуалізовано і з використанням комплексного підходу, що включає, зокрема, патогенетичну корекцію і застосування антиоксидантних субстратів.
* Адаптовано з: Белоусов Ю.Б. и соавт. Применение тиоктовой кислоты в терапии диабетической полиневропатии. Качественная клиническая практика. 2011;(1):85-91.
Література
- Spallone V., Lacerenza M., Rossi A., Sicuteri R., Marchettini P. Painful diabetic polyneuropathy: approach to diagnosis and management. Clin J Pain. 2012;28(8):726-743. doi:10.1097/AJP.0b013e318243075c.
- Callaghan B.C., Little A.A., Feldman E.L., Hughes R.A. Enhanced glucose control for preventing and treating diabetic neuropathy. Cochrane Database Syst Rev. 2012;6(6):CD007543. Published 2012 Jun 13. doi:10.1002/14651858.CD007543.pub2.
- Bansal V., Kalita J., Misra U.K. Diabetic neuropathy. Postgrad Med J. 2006;82(964):95-100. doi:10.1136/pgmj.2005.036137.
- Vinik A.I., Park T.S., Stansberry K.B., Pittenger G.L. Diabetic neuropathies. Diabetologia. 2000;43(8):957-973. doi:10.1007/s001250051477.
- Shaw J.E., Zimmet P.Z., Gries F.A., Ziegler D. Epidemiology of Diabetic Neuropathy // Textbook of diabetic neuropathy / Ed. by F.A. Gries, N.E. Cameron, P.A. Low, D. Ziegler. — Stuttgart/New York: Thieme, 2003. — 64-82.
- Boulton A.J., Vinik A.I., Arezzo J.C. et al. Diabetic neuropathies: a statement by the American Diabetes Association. Diabetes Care. 2005;28(4):956-962. doi:10.2337/diacare.28.4.956.
- Coppini D.V., Bowtell P.A., Weng C., Young P.J., Sönksen P.H. Showing neuropathy is related to increased mortality in diabetic patients - a survival analysis using an accelerated failure time model. J Clin Epidemiol. 2000;53(5):519-523. doi:10.1016/s0895-4356(99)00170-5.
- Ziegler D. Treatment of diabetic polyneuropathy: Update 2006. Ann N Y Acad Sci. 2006;1084:250-266. doi:10.1196/annals.1372.008.
- Daousi C., MacFarlane I.A., Woodward A., Nurmikko T.J., Bundred P.E., Benbow S.J. Chronic painful peripheral neuropathy in an urban community: a controlled comparison of people with and without diabetes. Diabet Med. 2004;21(9):976-982. doi:10.1111/j.1464-5491.2004.01271.x.
…
99. Ziegler D. Thioctic acid for patients with symptomatic diabetic polyneuropathy: a critical review. Treat Endocrinol. 2004;3(3):173-189. doi:10.2165/00024677-200403030-00005.
Повний список літератури знаходиться в редакції.
Підготувала Юлія Золотухіна
UA-TIOK-PIM-072020-013
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 2 (50), 2020 р.


