1 вересня, 2020
Ранолазин у лікуванні стабільної стенокардії напруги і хронічної серцевої недостатності зі збереженою фракцією викиду лівого шлуночка
Сутність грудної жаби як клінічного синдрому зводиться до двох основних пунктів: болю і смерті
Д.Д. Плетньов
 Визначенню хронічної ішемічної хвороби серця (ІХС) класика російської терапії та кардіології Д.Д. Плетньова більше як 100 років. Однак уявлення про ІХС здебільшого не змінилися, як не змінилися її симптоми і прогноз. Сьогодні, на тлі дієвих інвазивних методів лікування ІХС, вдається подовжити життя пацієнту, але захворюваність продовжує зростати і «молодшати» в усьому світі.
Визначенню хронічної ішемічної хвороби серця (ІХС) класика російської терапії та кардіології Д.Д. Плетньова більше як 100 років. Однак уявлення про ІХС здебільшого не змінилися, як не змінилися її симптоми і прогноз. Сьогодні, на тлі дієвих інвазивних методів лікування ІХС, вдається подовжити життя пацієнту, але захворюваність продовжує зростати і «молодшати» в усьому світі.
Бачення сучасної кардіології можна представити кількома напрямами, чітко сформульованими в рекомендаціях Європейського товариства кардіологів (ESC, 2013) [1]:
- поліпшення прогнозу, попередження виникнення інфаркту міокарда й раптової смерті та, відповідно, продовження життя;
- зниження частоти, інтенсивності нападів стенокардії та, відповідно, поліпшення якості повсякденної активності пацієнтів.
Засоби, що впливають на прогноз пацієнтів з ІХС, вивчені у багатьох міжнародних рандомізованих дослідженнях і чітко регламентовані тими ж рекомендаціями:
- Щоденне приймання аспірину в малих дозах усіма пацієнтами (I, A).
- У разі непереносимості аспірину альтернативне застосування клопідогрелю (I, B);
- Призначення статинів усім пацієнтам з ІХС (I, A);
- Призначення інгібіторів ангіотензинперетворювального ферменту (іАПФ) або блокаторів рецепторів ангіотензину (БРА) за наявності супутніх захворювань, як-то артеріальна гіпертензія, хронічна серцева недостатність (СН), цукровий діабет (ЦД) (I, А).
Важливість контролю симптомів та поліпшення якості життя хворих
Питання взяття під контроль симптомів і тим самим поліпшення якості життя пацієнта залишається досить проблематичним і дискутабельним. Під якістю життя (health related quality of life – HRQL) розуміють інтегральну характеристику фізичного, психологічного, соціального і емоційного стану хворого, яку оцінюють з огляду на його суб’єктивне сприйняття. Тобто для поліпшення якості життя пацієнта недостатнім, хоча й вельми важливим, є зменшення больового синдрому.
Стенокардія – найбільш грізний і деструктивний для життя пацієнта прояв ІХС. Чим частіше виникають епізоди стенокардії та чим інтенсивніший їхній характер, тим гірша не тільки якість життя пацієнта, але також прогноз. Не слід забувати, що стенокардія – не лише відчуття хворого, а й маркер порушення коронарного кровообігу, гемодинамічної обструкції коронарної артерії(-й) або глибини мікроваскулярного ураження серця. Проте якість життя кардіального пацієнта – це ще й поліпшення толерантності до фізичного навантаження і контроль порушень ритму, що також визначає його психологічний статус і «соціальний комфорт».
Якість життя виходить на перший план в осіб із хронічними захворюваннями з поганим прогнозом. Цьому визначенню повною мірою відповідає хронічна ІХС. Особливо якщо вже чи ще не ставиться питання про планове хірургічне втручання, або ж якщо стенокардія виникає після стентування чи шунтування судин серця.
В європейських рекомендаціях 2013 р. регламентовані такі препарати для поліпшення симптоматики ІХС:
- короткодіючі нітрати для купірування нападів стенокардії (I, B);
- β-блокатори (ББ) та антагоністи кальцію (АК) як препарати першої лінії для контролю частоти серцевих скорочень (ЧСС) і симптоматики (I, A);
- препарати другої лінії: довготривалі нітрати, івабрадин, нікорандил, ранолазин (IIa, B), триметазидин (IIb, B).
Важливим доповненням у рекомендаціях слугує наступне твердження: у пацієнтів з коморбідними станами і непереносимістю лікарських засобів першої лінії можливе призначення відразу препаратів другої лінії (I, C).
Комплекс ефектів ранолазину
Ранолазин – новий оригінальний антиангінальний та антиішемічний препарат, що не впливає на артеріальний тиск, ЧСС і периферичний опір судин, тобто на центральну та периферичну гемодинаміку. Тому особливо корисним ранолазин є для пацієнтів зі схильністю до брадикардії та гіпотонії, за умов коли інші класичні антиангінальні ліки, особливо ББ та АК, значно обмежені [2‑4].
Ранолазин – препарат, який шляхом селективного пригнічення пізнього Na-току суттєво впливає на внутрішньосерцеву гемодинаміку, а саме діастолічне наповнення лівого шлуночка (ЛШ) [5‑8]. Найважливішою складовою відповіді міокарда на пригнічення пізнього натрієвого току є зниження концентрацій внутрішньоклітинного кальцію, що насамперед супроводжується покращенням діастолічного розслаблення. Зменшення діастолічного напруження сприяє більш якісному та легкому наповненню коронарних судин, що своєю чергою не тільки значно поліпшує кровопостачання міокарда, але й опосередковано попереджає розвиток аритмій та прогресування СН [5‑9]. На сьогодні саме цей механізм вважається основним у комплексі антиішемічних та антиангінальних ефектів ранолазину.
Слід зазначити, що покращення діастолічної функції ЛШ ранолазином відбувається без погіршення його систолічної функції, адже препарат не зменшує пікового вхідного натрієвого або кальцієвого потоку. Цей ефект дозволяє використовувати ранолазин у пацієнтів із будь-якою фракцією викиду (ФВ), що вигідно відрізняє його від інших антиангінальних засобів (ББ та АК) і робить препаратом вибору в осіб з ішемічною систолічною дисфункцією міокарда (переважної більшості післяінфарктних хворих). На даний час триває декілька досліджень щодо вивчення ефективності ранолазину в пацієнтів із різними формами ІХС.
На додачу, ранолазин є гарним метаболіком, із чим спочатку й пов’язували його ефективність у пацієнтів з ІХС. Він впливає на енергетичний обмін у кардіоміоциті шляхом пригнічення ліполізу та активації гліколізу, внаслідок чого в кардіоміоциті накопичується більша кількість АТФ [6, 9]. Даний ефект також опосередковано зменшує ішемію міокарда та піднімає больовий поріг в осіб з ІХС, що є особливо цінним саме в жінок зважаючи на їхню високу чутливість до болю як такого та, зокрема, ішемічного походження.
У результаті проведення низки вагомих досліджень (MARISA, CARISA, ERICA) було доведено антиішемічну та антиангінальну ефективність ранолазину як у монотерапії, так і в потенціюванні антиангінальної активності АК, ББ і нітратів тривалої дії [10‑12]. У пацієнтів достовірно зростала толерантність до фізичних навантажень, зменшувалася кількість нападів стенокардії та потреба у прийманні нітратів короткої дії.
Накопичені дані клінічних досліджень дозволяють констатувати той факт, що ранолазин покращує глюкометаболічний гомеостаз, тобто ефективний у пацієнтів із серцево-судинними захворюваннями та ЦД. Це підтвердили результати субаналізів декількох випробувань (MERLIN-TIMI, CARISA, ТERISA), в яких продемонстроване статистично достовірне зниження рівня глікованого гемоглобіну і повторних епізодів ішемії у хворих на ЦД, а також частоти випадків прогресування порушень вуглеводного обміну до ЦД [13‑15]. Крім того, у пацієнтів із ЦД на тлі застосування ранолазину було показане не тільки зменшення частоти і сили нападів стенокардії, але й дозування та частоти приймання нітратів.
Як інгібітор вихідного току натрію в фазі реполяризації, ранолазин збільшує на декілька мс тривалість потенціалу дії та QT-інтервалу. Проте препарат не впливає на механізми, що підвищують ризик розвитку шлуночкової тахікардії Torsades de pointes, тобто не має проаритмогенного ефекту [9]. Сучасні дані свідчать про те, що застосування ранолазину може навіть знижувати частоту випадків розвитку як шлуночкових аритмій, так і фібриляції передсердь (ФП) [16‑19].
На сьогодні ранолазин можна позиціонувати як препарат другого ряду або засіб комплексної антиаритмічної терапії ФП. Ранолазин навіть запропонований для самостійного зняття приступу ФП за принципом «таблетка у кишені» (рill in the pocket) у перші 10 хв після виникнення нападу [20]. Такі дані дозволяють віддавати перевагу призначенню ранолазину в пацієнтів зі стенокардією та ФП, особливо за неефективності або неможливості призначення ББ (гіпотонія, брадикардія), або в комплексі з ББ та аміодароном. Розглядаючи антиаритмічну активність ранолазину, слід зазначити, що його не можна поєднувати з антиаритміками класу Іа (хінідин та ін.) та класу ІІІ (соталол). Дане заперечення не стосується аміодарону.
Зважаючи на те що у розвитку стенокардії велику роль відведено ендотеліальній дисфункції, на сьогодні ранолазин є досить перспективним препаратом. Так, у нещодавно опублікованих роботах показано, що препарат володіє протизапальною та антиоксидантою дією, що може зумовити поліпшення ендотеліальної функції в різних клінічних умовах [4, 21]. Доведений суттєвий вплив на ендотеліальну дисфункцію може вивести ранолазин із групи антиангінальних у групу прогноз-модифікувальних препаратів, чого ще не сталося з жодним із відомих наразі антиангінальних засобів.
Таким чином, основною метою комплексного антиангінального лікування та монотерапії ранолазином слід, насамперед, вважати зниження виразності симптомів стенокардії, а також пов’язаних із нею порушень ритму та толерантності до фізичного навантаження.
Ранолазин з’явився на ринку фармакологічних препаратів України декілька років тому і зайняла своє гідне місце. Спочатку були опубліковані статті з описами клінічних випадків застосування ранолазину в пацієнтів із різними варіантами стенокардії [22, 23]. Далі, в міру накопичення досвіду його використання, виникла потреба в узагальненні отриманих результатів.
Було проведене дослідження, мета якого полягала у вивченні впливу ранолазину на клінічний стан, інструментальні показники структурно-функціонального стану та внутрішньо-серцевої гемодинаміки, а також холтерівського моніторування електрокардіограми (ХМЕКГ) в осіб зі стабільною стенокардією напруги.
Матеріали й методи дослідження
Характеристики пацієнтів та критерії включення
У дослідження були залучені пацієнти з ІХС від 42 до 62 років (медіана – 55,3±0,6 року). Чоловіків було 26, жінок – 6. В усіх хворих діагностовано стабільну стенокардію II‑III функціонального класу (ФК). Тривалість анамнезу стенокардії становила 2‑6 років. Основним критерієм включення був класичний стенокардитичний біль, який зберігався на тлі підібраної антиангінальної терапії першої лінії (нітрати, ББ, АК). Всі пацієнти мали синусовий ритм. У 18 учасників ІХС було підтверджено коронарографічно; 9 мали супутній ЦД 2-го типу, 20 – АГ І‑ІІ ст. Діастолічну дисфункцію лівого шлуночка (ДДЛШ) було зареєстровано у всіх пацієнтів, що було умовою відбору. У дослідження не були включені післяінфарктні хворі та особи після проведення стентування чи шунтування коронарних судин.
Усі хворі отримували прогноз-модифікувальну терапію ІХС (статини, аспірин, іАПФ/сартани). Лікування не змінювали протягом двох тижнів перед призначенням ранолазину.
Клінічна оцінка
Аналіз структурно-функціонального стану серця проводили за даними ехокардіографії (ЕхоКГ) в одно- та двомірному режимах із кольоровою, імпульсною та постійно-хвильовою доплерографією за допомогою ехокардіографа Мy Lab 25 (Італія). Для оцінки ЛШ і систолічної функції визначали та розраховували кінцево-систолічний (КСР, КСО) й кінцево-діастолічний розміри та об’єми (КДР, КДО), товщину міжшлуночкової перегородки (ТМШП) та задньої стінки ЛШ у діастолу (ТЗСЛШ), поперечний розмір лівого передсердя (ЛП), правого шлуночка (ПШ) та правого передсердя (ПП). Розраховували масу міокарда ЛШ (ММЛШ) й відносну товщину стінок (ВТС). Паралельно визначали індексовані показники: індекс маси міокарда ЛШ (ІММЛШ), кінцево-систолічний та кінцево-діастолічний індекси (КСІ, КДІ).
Діастолічну функцію ЛШ оцінювали за даними доплер-ЕхоКГ в імпульсному та тканинному режимах. Визначали наступні показники трансмітрального кровотоку: максимальну швидкість раннього (Е), пізнього діастолічного наповнення (А) та їхнє співвідношення (Е/А), час сповільнення раннього діастолічного наповнення (Тdec), ізоволюметричного розслаблення (IVRT) і децелерації (DТ), а також E’ і A’, з визначенням співвідношення E/E’.
ХМЕКГ проводили в амбулаторних та стаціонарних умовах за допомогою апарату моделі 3225 «ДІАКАРД» (АОЗТ «Сольвейг», Україна). Визначали наступні показники: середню добову ЧСС, загальну кількість шлуночкових (ШЕ) та надшлуночкових екстрасистол (НШЕ) за добу, співвідношення НШЕ/ШЕ у пасивний та активний періоди (НШЕпас/НШЕакт, ШЕпас/ШЕакт), середню кількість епізодів за добу та сумарну денну тривалість депресії сегмента ST.
Показники добової ВСР оцінювали шляхом ХМЕКГ. Обробку даних виконували за допомогою системи аналізу ВСР «HRV», яка входить до складу холтерівських систем моніторування ЕКГ «ДІАКАРД» виробництва фірми «Сольвейг» (Україна). Відповідно до рекомендацій вивчали часові й частотні показники ВРС: стандартне відхилення NN-інтервалу (SDNN) та % сусідніх, різниця між якими перевищує 50 мс (pNN50%), квадратний корінь суми квадратів різниць тривалості сусідніх інтервалів NN (RMSSD), потужність у діапазоні низьких частот (0,04‑0,15 Гц) (LF), а також спектра високочастотного компонента (0,15‑0,4 Гц) (HF), відношення LF/HF. Аналіз даних проводили тричі за дослідження: при включенні (базовий рівень), через один і три місяці. Пацієнти приймали ранолазин по 1 таблетці 500 мг двічі на добу, за потреби дозу збільшували до 2000 мг.
Статистичний аналіз
Статистичний аналіз отриманих даних проводили за допомогою методів варіаційної статистики з використанням програми Statistica v.12 (StatSoft). Результати дослідження представлені для кількісних величин як медіана й інтерквартильний розмах (25 і 75 перцентиль) і для відносних величин у вигляді %. Достовірність різниці % розраховано за критерієм χ2. Достовірність різниці величин показників при порівнянні двох незалежних вибірок визначено за допомогою непараметричного статистичного U-критерію Манна – Уїтні. Значення р<0,05 вважали як достовірну різницю між порівнюваними групами.
Результати дослідження та обговорення
Всі пацієнти мали певні ознаки серцево-судинного ремоделювання зважаючи на тривалий анамнез захворювання, стійкий характер кардіалгій та коморбідність (АГ, ЦД). У 12 учасників були зареєстровані концентричні ремоделювання та концентрична гіпертрофія ЛШ, у решти 20 – ексцентрична. Систолічна функція у всіх хворих була збережена: середня величина ФВ у групі становила 54,8% (табл. 1).
Через чотири тижні лікування намітилася чітка тенденція до зменшення порожнини ЛШ: на 2,9% знизився показник КДІ та майже на 7% – КСІ ЛШ, унаслідок чого ІММЛШ скоротився на 4,7%. Через три місяці тенденція до зменшення систолічного об’єму ЛШ досягла рівня достовірності (-9,9%, р<0,05), що зумовило зростання ФВ ЛШ (+3,1%). Отже, через три місяці постійного приймання ранолазину в дозі 1000‑2000 мг/добу мали місце певні невеликі зміни структури та систолічної функції ЛШ, які загалом не досягли рівня достовірності.
Слід зазначити, що для істотного впливу на структурне ремоделювання ЛШ тримісячної терапії будь-яким препаратом недостатньо, до того ж у дослідження були включені хворі зі збереженою глобальною скоротливою здатністю міокарда. Отримані дані збігаються з результатами інших авторів щодо впливу тримісячного курсу ранолазину на стан діастоли та відсутність значущого ефекту на систолу [24, 25]. Проте деякі науковці виявили достовірне зростання ФВ на тлі використання ранолазину в пацієнтів зі зниженою ФВ та суттєвими клінічними проявами хронічної СН [26].
Ключовою складовою відповіді міокарда на зменшення пізнього потоку натрію через натрієві канали, спричиненого ранолазином, є зниження концентрацій внутрішньоклітинних натрію і кальцію, що супроводжується покращенням діастолічного розслаблення. Розвантаження діастоли є вкрай важливим для оптимізації внутрішньосерцевої гемодинаміки, тож якість коронарного кровообігу насамперед залежить від вільного наповнення коронарних артерій у діастолу. Зменшення діастолічної напруги серцевого м’яза та якісніше його розслаблення дозволяє коронарним судинам збільшитися в об’ємі та прийняти в себе більшу кількість крові. Тому ранолазин, що забезпечує такий ефект, є потужним внутрішньоміокардіальним гемодинаміком.
Оцінку стану діастоли проводили у двох групах: із ДДЛШ 1-го та 2-го типів. Пацієнтів із ДДЛШ 3-го типу не було включено у дослідження. Медикаментозне «розвантаження» діастоли в такому разі навіть теоретично видається дуже сумнівним зважаючи на перевагу фіброзу міокарда та дуже високої його жорсткості. З огляду на відсутність достовірних змін інструментальних показників стану діастоли через один місяць лікування, далі наведені результати 3-місячного лікування ранолазином.
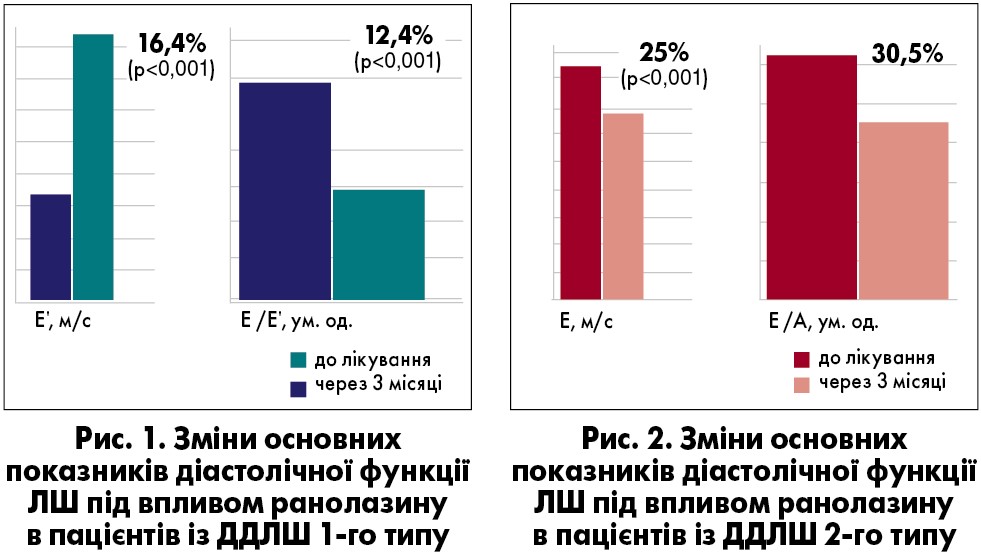
Позитивний вплив ранолазину на діастолічну функцію ЛШ у хворих із ДДЛШ 1-го типу вбачався у достовірному (р<0,05) зменшенні тривалості IVRT майже на 10% та збільшенні швидкості руху фіброзного кільця мітрального клапана Е’ на 16,4% (табл. 2, рис. 1). Середню величину швидкості ранньої діастолічної хвилі Е’ <0,09 м/с, виміряну в області фіброзного кільця мітрального клапана, вважають однією з найбільш значущих ознак уповільнення розслаблення міокарда ЛШ. Співвідношення Е/Е’ є обов’язковим для вимірювання інформативним показником погіршення діастолічного розслаблення [27]. Наслідком достовірного збільшення значення Е’ у хворих першої підгрупи стало істотне зниження співвідношення Е/Е’ на 12,5%. Це свідчило про поліпшення наповнення ЛШ у діастолу, переважно за рахунок процесів релаксації ЛШ.
У 3 із 18 пацієнтів цієї підгрупи після закінчення терапії основні діастолічні індекси (Е/А, IVRT, DT, Е/Е’, Е) досягли норми. Зазначені зміни супроводжувалися гемодинамічним розвантаженням ЛП, його лінійний розмір достовірно зменшився з 4,0±0,1 до 3,7±0,2 см (р<0,05).
При ДДЛШ 2-го типу зміни розслаблення поєднуються з певним ростом жорсткості міокарда ЛШ. Це супроводжується не зростанням, як при ДДЛШ 1-го типу, а навпаки, зменшенням тривалості всієї діастоли та її складових. Даний вид ДДЛШ відображає глибші порушення діастоли та ріст кінцево-діастолічного тиску.
За даними тканинного доплера, в цій підгрупі хворих достовірних змін швидкісних показників Е’ і A’, а також співвідношення Е’/A’, нажаль, не відбулося навіть через 12 місяців лікування ранолазином. Це свідчило про складні порушення у структурі міокарда ЛШ та суттєвіші зміни його діастолічного наповнення.
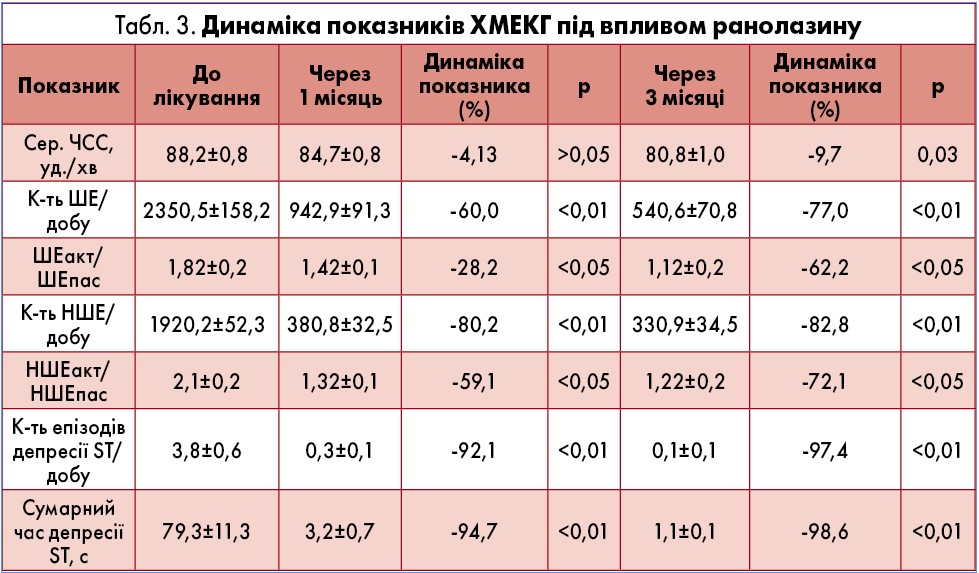
Проте в осіб із ДДЛШ 2-го типу через 12 тижнів терапії спостерігалися зміни часових та швидкісних показників трансмітрального кровотоку, що також було значущим компонентом розвантаження діастоли. Відбулося достовірне (р<0,05) збільшення тривалості інтервалів IVRT та DT, зниження швидкості раннього діастолічного наповнення Е на 25%, а також співвідношення Е/А на 30,5% (рис. 2). Це асоціювалося з достовірним зменшенням розміру ЛП із 4,4 ± 0,1 до 4,0 ± 0,1 см (р<0,05), що свідчило про зменшення кінцево-діастолічного тиску й тиску в ЛП. Перехід псевдонормального кровотоку (ДДЛШ 2-го типу) в спектр із порушеним розслабленням (ДДЛШ 1-го типу) після трьох місяців лікування ранолазином відбувся у 5 з 14 хворих.
Отже, 12-тижневе лікування ранолазином суттєво покращило стан ДДЛШ у пацієнтів із різними її типами та ІХС. Дані зміни спостерігалися на тлі тенденції до зменшення порожнин серця та зростання ФВ ЛШ.
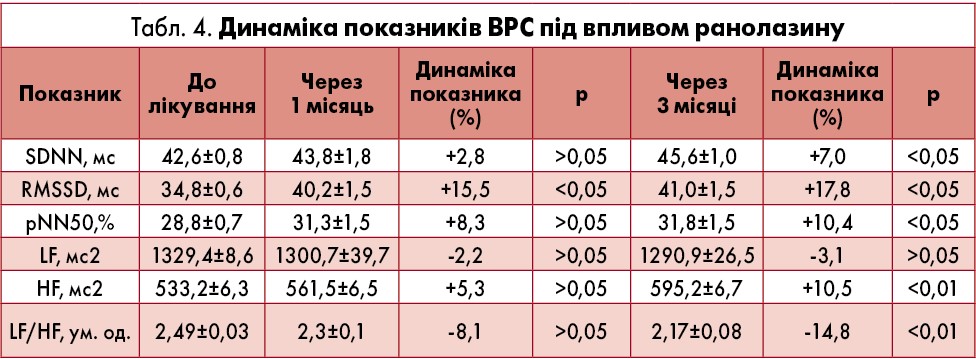
На додачу, слід підкреслити остаточну ключову перевагу ранолазину – антиангінальний та антиішемічний ефекти – клінічне зменшення кількості та тривалості нападів стенокардії, а також епізодів депресії сегмента ST. Аналіз даних ХМЕКГ чітко продемонстрував суттєву антиішемічну дію препарату вже через чотири тижні лікування: на 92% зменшилася частка епізодів депресії та на 94,7% – сумарний добовий час депресії сегмента ST (табл. 3). Через 12 тижнів терапії зниження цих показників сягнуло 97,4 та 98,6% відповідно. Дані інструментального дослідження супроводжували суттєве зменшення кількості й тривалості стенокардитичних епізодів у всіх 32 пацієнтів, причому в 22 із них стенокардію було взято під контроль вже на першому місяці лікування, а в решти 10 відбулося значуще зниження частоти приступів стенокардії. Варто зауважити, що у семи хворих дозу ранолазину було підвищено до 1500 мг, у трьох – до 2000 мг на добу в два приймання.
Як було зазначено вище, перевантаження кардіоміоцитів в умовах ішемії міокарда натрієм і, відповідно, кальцієм, призводить не тільки до механічної дисфункції ЛШ, але й до електричної нестабільності міокарда, тому ранолазин, блокуючи пізній потік іонів натрію, діє як антиаритмік.
Якщо антиішемічна та антиангінальна дія ранолазину була суттєвою вже на першому місяці лікування, а діастолічна функція достовірно покращилася через декілька місяців, то щодо антиаритмічного впливу спостерігався певний накопичувальний позитивний ефект. Через чотири тижні терапії кількість НШЕ, яких спостерігалося досить багато до початку приймання ранолазину, зменшилася відразу на 80% та через три місяці – на 82,8%. Зменшення числа ШЕ через один місяць становило 60%, через три – 77%. Крім загальної добової кількості ЕС, було проаналізовано їх добовий розподіл. На початку лікування співвідношення їхньої кількості в активний та пасивний періоди доби (НШЕпас/НШЕакт, ШЕпас/ШЕакт) було 2,2 та 1,82 відповідно. Даний розподіл свідчив про переважання денних екстрасистол. Вища денна аритмічна активність серця зумовлена більшою мірою денною фізіологічною, а також активованою ішемією гіперсимпатикотонією.
Антиаритмічний ефект ранолазину привів не тільки до суттєвого зменшення загальнодобової кількості ЕС, але й до їхнього добового перерозподілу. Зменшення співвідношення ЕСакт/ЕСпас свідчило про перевагу впливу саме на денні, симпатико-активовані аритмії. Подальший аналіз виявив також достовірне зниження ЧСС через 12 тижнів лікування майже на 10%. Хоча ранолазин прямо не впливає на ЧСС, можна припустити, що такий результат вдалося отримати за рахунок покращення якості життя хворих, зменшення частки та тривалості кардіалгій, а також схвильованості пацієнтів щодо прогнозу захворювання.
Упродовж останніх років дослідження варіабельності ритму серця (ВРС) стало одним із доступних неінвазивних методів стратифікації ризику в пацієнтів із серцево-судинною патологією, особливо ІХС. Його використовують для вивчення стану вегетативної регуляції серцевого ритму, прогнозу захворювання та оцінки ефективності лікування. Очевидно, реально говорити про прогностичне значення показників можна лише в осіб зі структурною хворобою серця, зокрема, після перенесеного інфаркту міокарда або із СН високого ФК [28, 29]. Проте оцінка впливу лікарський засобів на стан автономної нервової системи (АНС) у пацієнтів зі стабільними формами ІХС є актуальним і цікавим питанням, яке вивчають при аналізі ефективності всіх серцево-судинних препаратів.
Найбільш інформативними інтегральними часовими показниками ВРС є SDNN та RMSSD, визначені протягом 24 год. Вони залежать від активності обох відділів ВНС і характеризують стан вегетативної регуляції загалом. Їхнє збільшення або зменшення свідчить про зміщення вегетативного балансу в бік переважання одного з відділів АНС. Найчастіше на підвищений ступінь ризику вказує зниження часових значень ВРС, через що можна спостерігати послаблення активності парасимпатичного відділу АНС і зниження «захисту» серця від виникнення життєво небезпечних аритмій. У зазначених пацієнтів під впливом ранолазину було виявлено тенденцію до зростання (на 2,8%) SDNN через один місяць та достовірне зростання (на 7%) через три місяці лікування (табл. 4). RMSSD підвищився на 15 та 17% відповідно.
Корисним спектральним показником ВРС, який відображає баланс активності симпатичного і парасимпатичного відділів АНС, є симпато-парасимпатичний коефіцієнт LF/HF. LF – низькочастотний компонент спектра, який більшою мірою відображає активність симпатичної нервової системи. HF – високочастотний компонент спектра, пов’язаний із дихальною аритмією і переважно відображає активність парасимпатичного відділу АНС. У пацієнтів у розглянутому дослідженні симпато-парасимпатичний коефіцієнт вказував на високу активність симпатичної АНС та суттєво перевищував норму [30]. Через місяць лікування ранолазином з’явилася тенденція до його зменшення, яка через три місяці досягла рівня достовірності та становила 15%. Дані зміни коефіцієнта були визначені за рахунок зростання компоненту HF (+10,5%, р<0,01). Тобто покращення симпато-парасимпатичного балансу відбулося не завдяки прямому пригніченню симпатичної ланки, а опосередковано – за рахунок зростання парасимпаточної активності.
Зменшення переважно денних аритмій – як шлуночкових, так і надшлуночкових – на тлі тривалого лікування ранолазином, ймовірно, пов’язане не тільки із прямим механізмом дії на калій-натрієвий насос, але й компенсаторним підвищенням активності парасимпатичного відділу вегетативної АНС. Збалансування АНС, відносне зменшення симпатичного «допінгу» у пацієнтів з ІХС при тривалому застосуванні є перспективним також для основної причини аритмій – ішемії, що й було підтверджене значним антиангінальним і антиішемічним ефектом ранолазину. Факт впливу даного препарату на ВРС є цікавою та суттєвою знахідкою дослідження, тому потребує детальнішого підтвердження й обговорення.
L. Gary et al. також описали покращення симпато-парасимпатичного балансу в осіб з ІХС при довготривалому прийманні ранолазину [26]. У дослідженні в порівняльному аспекті оцінювали стан АНС у групі реваскуляризованих пацієнтів, що отримували стандартну антиангінальну терапію (група контролю) та у хворих на симптомну стенокардію, яким до стандартного лікування додавали 500‑1000 мг ранолазину двічі на добу. Тривалість дослідження була вельми переконливою – шість років, як і використовувані методи. Так, двічі на рік у пацієнтів оцінювали не лише коронарний кровоток, але й вегетативну АНС із розрахунком усіх відомих на сьогодні параметрів та коефіцієнтів ВРС. Результати перевершили всі можливі очікування: на тлі «вирівнювання» симпато-парасимпатичного балансу за рахунок переважно зростання активності парасимпатичної АНС кількість випадків гострого коронарного синдрому була в 4,5 разів меншою у групі ранолазину, ніж контролю.
Вплив на симпатовагальний баланс автори дослідження пов’язують з основним ефектом ранолазину – блокадою пізнього Na-току. За отриманими результатами, ранолазин можливо позиціонувати як препарат, який перешкоджає виникненню гострого коронарного синдрому, за рахунок чого покращує віддалений прогноз у пацієнтів зі стабільною стенокардією.
Висновки
Таким чином, ранолазин – препарат, запропонований у сучасних рекомендаціях для лікування стабільної стенокардії у вигляді монотерапії та в комбінації з іншими антиангінальними й антиішемічними засобами. На сьогодні визначені основні ефекти ранолазину – антиіангінальний, антиішемічний та антиаритмічний. Вони реалізуються шляхом селективного пригнічення пізнього Na-току, що суттєво впливає як на діастолічне наповнення ЛШ, так і на аритмогенну активність серця. В зазначеному дослідженні ще раз інструментально та клінічно підтверджено ключові ефекти ранолазину та виявлено його вплив на варіабельність серцевого ритму – достовірне збільшення активності парасимпатичної ланки АНС, що покращує природній «захист» серця від спровокованої гіперсимпатикотонією ішемії та аритмій.
Отримані на даний час переконливі дані дозволяють використовувати ранолазин у пацієнтів із коморбідними станами – при поєднанні ІХС з артеріальною гіпертензією, ЦД та будь-якими аритміями. Зважаючи на те що ранолазин є внутрішньосерцевим гемодинаміком без істотного впливу на тиск та ЧСС, продовжується вивчення його ефективності при різних формах ІХС.
Література
- 2012 ACCF/AHA/ACP/AATS/PCNA/SCAI/STS Guideline for the Diagnosis and Management of Patients with Stable Ischemic Heart Disease // Circulation. – 2012. – 126: e354-e471.
- Phelps C.E., Buysman E.K., Gomez Rey G. Costs and clinical outcomes associated with use of ranolazine for treatment of angina // Clin Ther. – 2012. – 34 (6). – Р. 1395‑1407; e1394.
- Kohn C.G., Parker M.W., Limone B.L., Coleman C.I. Cost-effectiveness of ranolazine added to standard-of-care treatment in patients with chronic stable angina pectoris // Am J Cardiol. – 2014. – 113 (8). – Р. 1306‑1311.
- Hidalgo-Vega A., Ramos-Goni J.M., Villoro R. Cost-utility of ranolazine for the symptomatic treatment of patients with chronic angina pectoris in Spain // Eur J Health Econ,2013.
- Lovelock J.D., Monasky M.M., Jeong E.M. et al. Ranolazine improves cardiac diastolic dysfunction through modulation of myofilament calcium sensitivity // Circ Res. – 2012. – 110. – Р. 841-850; PMID:22343711.
- Татарский Б.А. Антиаритмический потенциал ранолазина: от теории к практике // Consilium Medicum. – 2014. – 10. – С. 32‑39.
- Michels G., Kochanek M., Hoppe U.C. Ranolazine – an additional anti-anginal drug // Dtsch Med Wochenschr. – 2010. – 135 (41). – Р. 2037‑2040.
- Maier L.S. A novel mechanism for treatment of angina, arrhythmias, and diastolic dysfunction: inhibition of late INa using ranolazine // J Cardiovasc Pharmacol. – 2009. – 54 (4). – Р. 279‑286.
- Cattaneo M., Porretta A.P., Gallino A. Ranolazine: Drug overview and possible role in primary microvascular angina management // Int J Cardiol. – 2015. – 181. – Р. 376‑381.
- Chaitman B.R., Skettino S.L., Parker J.O. et al. for the MARISA Investigators. Anti-ischemic effects and long-term survival during ranolazine monotherapy in patients with chronic severe angina // J Am Coll Cardiol. – 2004. – 43. – Р. 1375‑1382.
Повний список літератури, що включає 30 пунктів, знаходиться в редакції
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 3 (70) 2020 р.