22 жовтня, 2020
Можливості імунотерапії при множинній мієломі: що нового?
За матеріалами 25-го щорічного конгресу EHA
 11-21 червня відбувся 25-й щорічний конгрес Європейської асоціації гематологів (EHA), який об’єднує усіх вчених і лікарів, котрі прагнуть бути в курсі останніх досягнень та інновацій у сучасній гематології. Цього року через спричинені пандемією COVID‑19 безпрецедентні обмеження конгрес вперше пройшов у віртуальному форматі. Проте це не позначилося на рівні інтересу до цього масштабного заходу – протягом 10 днів роботи його учасниками стали більш ніж 11 000 лікарів з Європи й інших регіонів світу. Вже традиційно однією з провідних тем форуму були проблемні питання онкогематології. Зокрема, цього року багато доповідей і наукових робіт було присвячено прогресу у веденні пацієнтів з множинною мієломою (ММ) – злоякісною пухлиною, морфологічним субстратом якої є плазматичні клітини, що накопичуються у кістковому мозку і продукують моноклональний імуноглобулін.
11-21 червня відбувся 25-й щорічний конгрес Європейської асоціації гематологів (EHA), який об’єднує усіх вчених і лікарів, котрі прагнуть бути в курсі останніх досягнень та інновацій у сучасній гематології. Цього року через спричинені пандемією COVID‑19 безпрецедентні обмеження конгрес вперше пройшов у віртуальному форматі. Проте це не позначилося на рівні інтересу до цього масштабного заходу – протягом 10 днів роботи його учасниками стали більш ніж 11 000 лікарів з Європи й інших регіонів світу. Вже традиційно однією з провідних тем форуму були проблемні питання онкогематології. Зокрема, цього року багато доповідей і наукових робіт було присвячено прогресу у веденні пацієнтів з множинною мієломою (ММ) – злоякісною пухлиною, морфологічним субстратом якої є плазматичні клітини, що накопичуються у кістковому мозку і продукують моноклональний імуноглобулін.
Хоча ММ і досі залишається невиліковною, останнім часом результати лікування хворих значно покращилися, передусім завдяки появі у розпорядженні лікарів принципово нових біологічних препаратів. Схвалені протягом останніх років для застосування у пацієнтів з рецидивуючою/рефрактерною множинною мієломою (РРММ) інноваційні біологічні протипухлинні засоби, включаючи інгібітори протеасом та імуномодулюючі препарати, зараз уже є стандартом лікування при цій онкогематологічній патології. Серед найсучасніших імуномодулюючих засобів, ефективних при ММ, істотну увагу вчених і практикуючих онкогематологів сьогодні привертає даратумумаб – людське моноклональне антитіло IgG, що безпосередньо зв’язується з білком CD38, який на високому рівні експресується на поверхні пухлинних клітин при ММ. Отже, даратумумаб характеризується таргетною протипухлинною активністю, асоційованою з імуномодуляторним механізмом дії. У комбінації зі стандартними режимами лікування, котрі включають бортезоміб і дексаметазон (режим VD, дослідження CASTOR) або леналідомід та дексаметазон (режим RD; дослідження POLLUX), даратумумаб достовірно збільшував виживаність без прогресування (ВБП) та покращував відповідь на лікування у пацієнтів з РРММ. Це стало підставою для схвалення препарату у Європі для застосування у пацієнтів з ММ, які потребують проведення ≥1 лінії терапії. Наразі активні дослідження даратумумабу тривають, і на цьогорічному конгресі ЕНА були оприлюднені дані одразу декількох із них.
Режими терапії з включенням даратумумабу у пацієнтів з РРММ: звіт GIMEMA Lazio Group
У рамках 25-го конгресу ЕНА вчені з італійської дослідницької групи з вивчення ММ GIMEMA Lazio Group представили власні дані щодо 118 пацієнтів з РРММ (56 чоловіків та 62 жінки; медіана віку – 66,9 року), які отримували лікування даратумумабом у комбінації з бортезомібом або леналідомідом, що застосовувалися разом з дексаметазоном. Згідно з оцінкою за Міжнародною системою стадіювання (International Staging System – ISS), 43 (39,45%) пацієнти мали I стадію захворювання, 40 (36,7%) – II стадію, 26 (23,85%) – III стадію; у 9 (7,63%) пацієнтів стадія захворювання не піддавалася точній оцінці. На момент включення у дослідження 24 (21,05%) пацієнти отримали 1 попередню лінію терапії, 53 (46,49%) – 2 лінії, 25 (21,93%) – 3 лінії; 9 (7,89%) – 4 лінії; 2 (1,75%) – 5 ліній і лише 1 (0,88%) пацієнт – вже 6 попередніх ліній терапії.
Як засвідчив аналіз отриманих результатів, 65 (55%) пацієнтів успішно завершили принаймні один цикл терапії, і у них можна було оцінити гематологічну відповідь. Загальна частота відповіді на лікування склала 81,97%; зокрема, у 4 (6,56%) пацієнтів було отримано строгу повну відповідь, у 20 (32,79%) – повну відповідь, у 5 (8,2%) – практично повну відповідь, у 13 (21,31%) – дуже добру часткову відповідь (ДДЧВ) та у 8 (13,11%) пацієнтів – часткову відповідь. Після періоду подальшого спостереження, медіана тривалості якого склала 8,8 міс (діапазон 0,23-22,3), 50 (42,37%) пацієнтів залишалися живими у стані досягнутої ремісії, у 8 (13,11%) відзначалося прогресування захворювання, а 1 (1,64%) пацієнт помер. Загальна виживаність (ЗВ) і ВБП становили 86,3 (95% довірчий інтервал – ДІ – 79,2-94,0) та 70,8% (95% ДІ 61,2-82,0) відповідно.
Найчастіші пов’язані з лікуванням гематологічні небажані явища 3 або 4 ступеня включали нейтропенію, анемію та тромбоцитопенію. Небажані інфузійні реакції 3 або 4 ступеня вираженості не спостерігалися. Загалом даратумумаб у комбінації з бортезомібом або леналідомідом (+ дексаметазон) добре переносився та характеризувався прийнятним профілем безпеки.
Таким чином, отримані дані свідчать про доцільність включення даратумумабу у стандартні режими лікування пацієнтів з РРММ. Попередні результати вказують на те, що застосування даратумумабу в комбінації з леналідомідом або бортезомібом (+ дексаметазон) є високоефективним режимом лікування, добре переноситься та може розглядатися як варіант терапії у пацієнтів з РРММ після першого рецидиву.
F. Fazio, G. Sfara, F. Vozella et al. EHA Library. Fazio F. 06/12/20; 297948; PB2032.
Порівняння режимів D-VD та VD у китайських пацієнтів з РМММ: дослідження III фази MMY3009 (LEPUS)
Нещодавно у дослідженні III фази CASTOR було показано, що у пацієнтів з РРММ використання режиму D-VD (даратумумаб/бортезоміб/дексаметазон) забезпечувало достовірне збільшення ВБП, індукувало більш глибоку та стійку відповідь на лікування та покращувало показники відсутності ознак мінімального резидуального захворювання порівняно з застосуванням режиму VD (бортезоміб/дексаметазон) (Weisel et al., ASH 2019, abstract 3192). Дослідники з Китаю цього року представили на конгресі ЕНА результати проміжного аналізу даних дослідження III фази LEPUS (MMY3009), який мав на меті порівняти ефективність і безпеку режимів D-VD та VD в популяції китайських пацієнтів з РРММ.
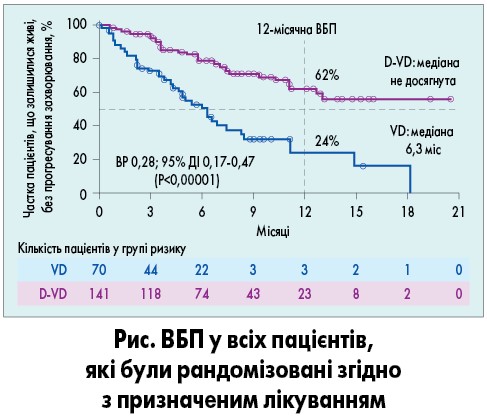 Загалом до дослідження було включено 211 пацієнтів, які отримали ≥1 попередньої лінії терапії та були рандомізовані для отримання одного з двох досліджуваних режимів (D-VD – 141 пацієнт; VD – 70 пацієнтів). Після періоду подальшого спостереження, медіана (діапазон) тривалості якого становила 8,2 (0-20,5) міс, застосування режиму D-VD сприяло достовірному зниженню ризику прогресування захворювання або смерті (на 72%) порівняно з режимом VD (медіана ВБП не досягнута порівняно з 6,3 міс; ВР 0,28; 95% ДІ 0,17-0,47; P<0,00001; рис.).
Загалом до дослідження було включено 211 пацієнтів, які отримали ≥1 попередньої лінії терапії та були рандомізовані для отримання одного з двох досліджуваних режимів (D-VD – 141 пацієнт; VD – 70 пацієнтів). Після періоду подальшого спостереження, медіана (діапазон) тривалості якого становила 8,2 (0-20,5) міс, застосування режиму D-VD сприяло достовірному зниженню ризику прогресування захворювання або смерті (на 72%) порівняно з режимом VD (медіана ВБП не досягнута порівняно з 6,3 міс; ВР 0,28; 95% ДІ 0,17-0,47; P<0,00001; рис.).
Перевага режиму D-VD над режимом VD у контексті ВБП зберігалася у попередньо визначених підгрупах, включаючи пацієнтів, які отримували попереднє лікування бортезомібом (ВР 0,31; 95% ДІ 0,19-0,51), та пацієнтів з цитогенетичними показниками високого ризику (ВР 0,36; 95% ДІ 0,18-0,75). Медіана часу до прогресування захворювання достовірно збільшувалася на тлі застосування режиму D-VD порівняно з режимом VD (не досягнута порівняно з 6,5 міс; ВР 0,26; 95% ДІ 0,15-0,46; P<0,00001).
У пацієнтів, які мали доступні для оцінювання дані (D-VD, n=137; VD, n=63), додавання даратумумабу до режиму VD достовірно збільшувало загальну частоту відповіді (83 порівняно з 65%; P=0,00527) та частоту досягнення ДДЧВ або навіть кращої відповіді (65 порівняно з 33%; P=0,00002), а також частоту повної або ще кращої відповіді (33 порівняно з 11%; P=0,00079). Медіана часу до першої відповіді була коротшою при застосуванні режиму D-VD порівняно з VD (0,79 порівняно з 1,05 міс), а медіана тривалості відповіді при застосуванні режиму D-VD взагалі не була досягнута, тоді як при використанні режиму VD вона становила 6,9 міс. Загалом було констатовано 31 випадок смерті: 13 (9%) у групі D-VD та 18 (26%) у групі VD (ВР ЗВ 0,34; 95% ДІ 0,16-0,68; P=0,00162); подальше спостереження за пацієнтами триває.
Таким чином, у дослідженні LEPUS застосування режиму D-VD покращувало ефективність лікування пацієнтів з РРММ, включаючи достовірне збільшення ВБП. Ці дані підтримують доцільність додавання даратумумабу до режиму стандартного лікування (VD) пацієнтів з РРММ.
X. Huang, J. Lu, W. Fu et al. EHA Library. Huang X. 06/12/20; 294905; EP988.
Ефект даратумумабу при лікуванні ММ залежно від цитогенетичного ризику
Включення даратумумабу до стандартного режиму терапії при ММ сприяє підвищенню частоти досягнення відповіді на лікування та збільшенню ВБП. Однак залишається незрозумілим, чи спостерігається це покращення й у підгрупі пацієнтів з цитогенетичними показниками високого ризику, особливо при вперше діагностованій ММ. Під час конгресу були представлені дані систематичного огляду результатів рандомізованих клінічних досліджень III фази, у яких порівнювали результати лікування пацієнтів з ММ при застосуванні стандартних режимів та аналогічних режимів у комбінації з даратумумабом при вперше діагностованій ММ чи РРММ залежно від цитогенетичного ризику (високий ризик порівняно зі стандартним ризиком). Цитогенетичні показники високого ризику визначалися як наявність мутацій t(4;14), t(14;16) або del(17p). Як первинна кінцева точка розглядалася ВБП.
Після проведення скринінгу до аналізу було включено 6 рандомізованих клінічних досліджень III фази: 3 дослідження за участю пацієнтів з вперше діагностованою ММ (Alcyone, Maia та Cassiopeia: 2528 пацієнтів, 358 – із цитогенетичними показниками високого ризику) та 3 дослідження за участю пацієнтів з РРММ (Castor, Pollux та Candor: 1533 пацієнтів, 222 – із цитогенетичними показниками високого ризику). Включення даратумумабу до стандартного режиму лікування пацієнтів з вперше діагностованою ММ у підгрупі хворих із цитогенетичними показниками високого ризику сприяло покращенню ВБП (об’єднаний відносний ризик – ВР – 0,666; 95% ДІ 0,468-0,949; p=0,025), аналогічного такому у пацієнтів з РРММ (об’єднаний ВР 0,451; 95% ДІ 0,303-0,670; p<0,001). Аналогічні результати спостерігалися при цитогенетичних показниках стандартного ризику при вперше діагностованій ММ (об’єднаний ВР 0,445; 95% ДІ 0,369-0,538; p<0,001) та при РРММ (об’єднаний ВР 0,378; 95% ДІ 0,253‑0,564; p<0,001).
Таким чином, режими терапії на основі даратумумабу є варіантами вибору для пацієнтів з вперше діагностованою ММ і РРММ як при цитогенетичних показниках стандартного ризику, так і високого ризику.
S. Giri, A. Grimshaw, M. Dimopoulos et al. EHA Library. Costa L. 06/12/20; 294869; EP952.
Ефективність і безпека даратумумабу у лікуванні РРММ: досвід Саудівської Аравії
Багато досліджень вже продемонстрували ефективність і прийнятний профіль безпеки у лікуванні РРММ даратумумабу – біологічного препарату на основі людських моноклональних антитіл IgG, які зв’язуються з CD38. Під час цьогорічного конгресу ЕНА дослідники з Саудівської Аравії представили аналіз перших даних щодо застосування даратумумабу в умовах клінічної практики у 3 великих онкологічних центрах країни. Первинним критерієм оцінки ефективності лікування у цьому аналізі була ВБП, а як вторинні кінцеві точки розглядалися ЗВ, загальна частота відповіді та частота серйозних небажаних явищ (НЯ). Для оцінки вказаних показників був виконаний ретроспективний аналіз медичних карт 32 пацієнтів (медіана віку – 57 років, чоловіки – 68,8%) з РРММ, яким було встановлено цей діагноз за визначенням Міжнародної робочої групи з вивчення ММ (IMWG) і які отримували даратумумаб з січня 2016 по грудень 2019 р. З усіх пацієнтів 87,5% осіб мали стандартний профіль ризику на момент встановлення діагнозу, а 65,6% хворих була проведена аутологічна трансплантація стовбурових клітин. Медіана кількості попередніх ліній терапії дорівнювала 2, при цьому у 68,8% випадків була констатована рефрактерність до останньої лінії. Даратумумаб застосовували у складі режимів DVD, DPD, DRD*, а також як монотерапію (50; 37,5; 9,4 та 3,1% відповідно). Медіана тривалості терапії даратумумабом складала 5 міс, при цьому найчастішою причиною припинення його застосування було прогресування захворювання (68,7% пацієнтів). Частота об’єктивної відповіді становила 59,4%. ДДЧВ або навіть краща відповідь були зафіксовані у 40,7% хворих, а часткова відповідь – у 18,8% пацієнтів. Після завершення періоду подальшого спостереження, медіана тривалості якого склала 7,5 міс, оцінений показник ВБП через 12 міс становив 50,2%, а ЗВ – 63% (з медіаною ВБП 12 міс). Про інфузійні реакції повідомлялося у 46,9% пацієнтів; у переважній більшості випадків вони мали 1 або 2 ступінь вираженості (3 ступінь – у 9,4% пацієнтів). Найчастішими НЯ 3 або 4 ступеня були анемія, тромбоцитопенія та нейтропенія. Про інші серйозні НЯ у цій когорті пацієнтів не повідомлялося.
Таким чином, представлені дані підтвердили, що в умовах клінічної практики призначення даратумумабу є дійсно ефективним варіантом лікування РРММ, який має прийнятний профіль безпеки.
M. Althomali, E. Mutahar, H. Al Hashmi et al. EHA Library. Althomali M. 06/12/20; 298002; PB2086.
CP-182668
Підготувала Інга Боброва
* DVD – даратумумаб/бортезоміб/дексаметазон; DPD – даратумумаб/помалідомід/дексаметазон; DRD – даратумумаб/леналідомід/дексаметазон.




