27 жовтня, 2020
Сучасні інфузійні препарати для лікування розсіяного склерозу в Україні: клінічна ефективність, безпека та економічні аспекти застосування
.jpg) Розсіяний склероз (РС) – хронічне автоімунне захворювання центральної нервової системи (ЦНС). Його патогенез базується на реакції, опосередкованій автореактивними Т- та В-лімфоцитами і макрофагами, що призводить до демієлінізації та раннього ураження аксонів. У 90% випадків дана патологія розпочинається з форми, для якої характерні періодичні яскраво виражені періоди загострень та ремісій – рецидивуючо-ремітуючого РС (РРРС). У більшості пацієнтів із часом він переходить у форму вторинно-прогресуючого РС (ВПРС), яка відрізняється наростанням неврологічних симптомів із короткими періодами ремісії.
Розсіяний склероз (РС) – хронічне автоімунне захворювання центральної нервової системи (ЦНС). Його патогенез базується на реакції, опосередкованій автореактивними Т- та В-лімфоцитами і макрофагами, що призводить до демієлінізації та раннього ураження аксонів. У 90% випадків дана патологія розпочинається з форми, для якої характерні періодичні яскраво виражені періоди загострень та ремісій – рецидивуючо-ремітуючого РС (РРРС). У більшості пацієнтів із часом він переходить у форму вторинно-прогресуючого РС (ВПРС), яка відрізняється наростанням неврологічних симптомів із короткими періодами ремісії.
Слід зауважити, що з-поміж осіб із РРРС окремо виділяють підгрупу, яка потребує особливої уваги. Це хворі на високоактивний РС, для якого характерні часті рецидиви з неповним одужанням та швидке прогресування інвалідизації [28]. У решти 10% РС починається з поступового неухильного прогресування захворювання без виразних загострень та ремісій і має назву первинно-прогресуючого РС (ППРС) [19].
Кількість хворих на РС в Україні стрімко зростає. Якщо у 2016 р. на обліку перебувало близько 20 тис. пацієнтів, то, за даними Центру медичної статистики МОЗ України, нині їх близько 22 тис. При цьому існує висока ймовірність недостатнього діагностування даного захворювання. Поширеність РС в Україні становить близько 60 осіб на 100 тис. населення, тоді як у Польщі – 120, Чехії – 160, Угорщині – 176 [2]. Результатом дослідження поширеності РС у США за оригінальною методологією M.T. Wallin et al. (2019) є показник, який перевищує 300 осіб на 100 тис. населення, що, проте, потребує додаткового підтвердження [32].
РС є найпоширенішим запальним захворюванням ЦНС, що уражає молодих працездатних людей та пов’язане зі значним економічним навантаженням на пацієнтів, членів їхніх родин і систему охорони здоров’я загалом. В 2019 р. у межах заходів із реалізації бюджетної програми «Забезпечення медичних заходів окремих державних програм та комплексних заходів державного характеру» за напрямом «Закупівля лікарських засобів, імунобіологічних препаратів (вакцин), медичних виробів, інших товарів та послуг» у частині «Закупівля медикаментів для лікування хворих на розсіяний склероз» наказом МОЗ України від 14.02.2019 р. № 334 внесені зміни до затверджених «Методичних рекомендацій планування та розрахунку потреби у лікарських засобах для лікування хворих на розсіяний склероз». Згідно з ними до Програми закупівель медикаментів для лікування хворих на розсіяний склероз станом на 01.01.2019 р. було включено (ампули, флакони, шприци):
- інтерферон β‑1b у дозі 960 000 МО (0,3 мг);
- інтерферон β‑1a у дозі 6 000 000 МО (30 мкг);
- глатирамеру ацетат по 20, 40 мг;
- метилпреднізолон у дозі 1000 мг;
- мітоксантрон у дозі 2 мг/мл по 5 мл;
- фінголімод у капсулах по 0,5 мг.
Також у Державному бюджеті України 2019 р. було передбачене збільшення коштів для забезпечення пацієнтів із РС до 120 млн грн (у 2018 р. виділено 71 млн грн).
Станом на початок 2020 р. наказом МОЗ України від 28.12.2019 р. № 2711 затверджено номенклатуру лікарських засобів та медичних виробів, що закуповуються за напрямами використання бюджетних коштів у 2020 р. за бюджетними програмами: кодів програмної класифікації видатків та кредитування 2301400 «Забезпечення медичних заходів окремих державних програм та комплексних заходів програмного характеру» і 2301040 «Громадське здоров’я та заходи боротьби з епідеміями». Слід зазначити, що номенклатура лікарських засобів за напрямом «Медикаменти для лікування хворих на розсіяний склероз» не змінилася відносно вказаної вище, а бюджетні ресурси та кількісні дані планованих закупівель будуть уточнені МОЗ України після збору регіональних заявок на закупівлю профільних медикаментів.
Незважаючи на зусилля держави щодо забезпечення фармакотерапії, результати кількісного дослідження міжнародного дослідницького агентства IFAK Institut GmbH & Co (2018) виявили, що 88% осіб із РС в Україні мають інвалідність, а у 68% відсутня можливість працювати або навчатися. Це свідчить про низький рівень охоплення належним лікуванням пацієнтів із РС у нашій країні, що спричиняє прямі втрати держави до 350 млн грн на рік.
Враховуючи виявлені економічні збитки, особливо пов’язані з періодами загострень та загальним прогресуванням тяжкості захворювання у пацієнта, отримання належної медикаментозної терапії РС є дуже важливим [21]. Від початку ери лікування РС – застосування 1993 р. першого препарату інтерферону, арсенал препаратів значно розширився, що надає клініцистам нових можливостей для ефективної індивідуалізованої фармакотерапії цього захворювання.
Нещодавно в Україні лікарі та пацієнти отримали доступ до нових хворобомодифікуючих препаратів (ХМП), які впливають на перебіг РС, сповільнюючи прогресування різних його форм, та мають доведену високу ефективність. Так, 2017 р. компанією «Ф. Хоффманн-Ля Рош Лтд.» зареєстровано препарат Окревус (окрелізумаб), 2019 р. – ТОВ «Санофі-Авентіс Україна» – препарат Лемтрада (алемтузумаб). Тому порівняльний аналіз економічних аспектів застосування даних ліків у вітчизняній системі охорони здоров’я є актуальним.
Порівняння ефективності й безпеки терапії окрелізумабом та алемтузумабом
Передусім розглянемо показники ефективності та безпеки окрелізумабу та алемтузумабу, що ґрунтуються на даних клінічних досліджень, зокрема тих, на основі результатів яких були зареєстровані ці препарати.
Окрелізумаб
Окрелізумаб – рекомбінантне гуманізоване моноклональне антитіло – глікований імуноглобулін G1, що селективно діє на CD20-позитивні В-лімфоцити через механізм комплемент- та антитілозалежної цитотоксичності. При цьому він не впливає на плазматичні чи стовбурові лімфоїдні клітини, в яких CD20 не експресується [4]. Препарат схвалений до використання при РРРС, ВПРС та ППРС: у березні 2017 р. у США, у вересні 2017 р. в Україні, у січні 2018 р. у країнах ЄС [23, 24].
Вивчення ефективності та безпеки окрелізумабу при PPPC та ВПРС проводили на основі OPERA I й OPERA II – рандомізованих подвійних засліплених клінічних досліджень III фази з однаковим дизайном, подвійною імітацією та використанням препарату порівняння інтерферону β‑1а – стандарного лікування першої лінії. Випробування тривали два роки та включали 827 пацієнтів, яким внутрішньовенно вводили окрелізумаб у дозі 600 мг кожні шість місяців і плацебо підшкірно тричі на тиждень, а також 829 хворих, яким вводили інтерферон β‑1а по 44 мкг підшкірно три рази на тиждень і внутрішньовенно плацебо кожні 24 тижні.
При цьому в дослідженнях рецидивну форму РС було визначено як РРРС та ВПРС із рецидивами [22]. Також слід акцентувати увагу на тому, що до обох випробувань були включені як хворі, що отримували попередню фармакотерапію препаратами специфічної дії (пацієнти з досвідом лікування), так і ті, хто такої терапії не застосовував («наївні» пацієнти) [13].
На 96-му тижні оцінювали первинну кінцеву точку – середньорічну частоту рецидивів та вторинні – швидкість наростання інвалідизації, визначену за розширеною шкалою оцінки ступеня інвалідизації (EDSS), та динаміку показників магнітно-резонансної томографії (МРТ). Зафіксовано:
- майже дворазове зниження середньорічного показника рецидивів у групі окрелізумабу: у дослідженні OPERA I – 0,155; OPERA II – 0,156 (група інтерферону β‑1а – 0,290 та 0,292 відповідно);
- суттєве зниження ризику прогресування інвалідизації за EDSS у пацієнтів, що лікувалися окрелізумабом (6,9%), порівняно з тими, яким вводили інтерферон β‑1а (10,5%);
- загальна кількість вогнищ на Т1-зображеннях, що накопичують контрастну речовину, була на 94% (OPERA I) і 95% (OPERA II) нижча у групі окрелізумабу.
Також проводили оцінку досягнення статусу «без ознак захворювання» (NEDA), при якому фактично немає клінічних і нейровізуалізаційних ознак активності та прогресування хвороби, як-то загострення, наростання інвалідизації, показники МРТ. В обох дослідженнях OPERA I та OPERA II у групі окрелізумабу статусу NEDA досягли 48% пацієнтів, інтерферону β‑1а –29 та 25% відповідно [13].
Алемтузумаб
Алемтузумаб – рекомбінантне гуманізоване IgG1-κ-моноклональне антитіло до поверхневого клітинного глікопротеїну кластера диференціації СD52. У людини СD52 експресується на T- і В-лімфоцитах, у нижчих концентраціях – на природних клітинах-кілерах, моноцитах і макрофагах. Зв’язування алемтузумабу з лімфоцитарним CD52 приводить до руйнування T- і B-лімфоцитів. Після курсу терапії починається процес репопуляції лімфоцитів, який для B-лімфоцитів триває шість, а для T-лімфоцитів – до 12 місяців. При цьому змінюються число, відсотковий вміст і властивості лімфоцитів зі зменшенням інтенсивності Т-клітинної відповіді та запальних реакцій.
Алемтузумаб схвалений для використання при РРРС у вересні 2013 р. у країнах ЄС, в листопаді 2014 р. – у США, у квітні 2019 р. – в Україні [3, 16, 17]. Передусім препарат було вивчено у невеликій когорті пацієнтів із РРРС, ВПРС, ППРС та отримано достовірні ознаки зменшення активності захворювання з одночасним виявленням прогресування неврологічного дефіциту в більшості осіб із ВПРС та ППРС, тому до наступних досліджень залучали лише хворих на РРРС.
Спосіб застосування алемтузумабу є унікальним для препаратів, що призначають для лікування РС:
- перший курс – внутрішньовенне введення 12 мг/добу впродовж п’ятьох послідовних днів;
- другий курс – 12 мг/добу протягом трьох послідовних днів, які вводять через 12 місяців після першого курсу терапії;
- за потреби може бути розглянуто доцільність використання двох додаткових курсів у вигляді введення препарату в дозуванні 12 мг/добу протягом трьох наступних днів.
Важливі результати трьох досліджень показників ефективності та безпеки алемтузумабу, в яких препарат порівнювали з інтерфероном β‑1а для підшкірного введення. У СAMMS223 (II фази) та СARE-MS I (III фази) брали участь пацієнти, що раніше не використовували профільні препарати для лікування РС, а в CARE-MS II (III фази) – ті, в кого попередня фармакотерапія такими ліками виявилася невдалою.
У випробуванні СAMMS223, яке тривало два роки, у групі алемтузумабу було показано зниження частоти рецидивів на 74%, зменшення прогресування неврологічного дефіциту на 71% та значуще зменшення активності захворювання порівняно із хворими на інтерфероні β‑1а. У продовженому до чотирьох років спостереженні за пацієнтами СAMMS223 встановлено, що 65% із них досягли статусу NEDA (у групі інтерферону β‑1а – лише 27%).
Перший етап СARE MS I та СARE MS IІ тривав два роки, з фіксацією результатів та подальшим продовженням спостережень до п’яти років із щорічною фіксацією даних.
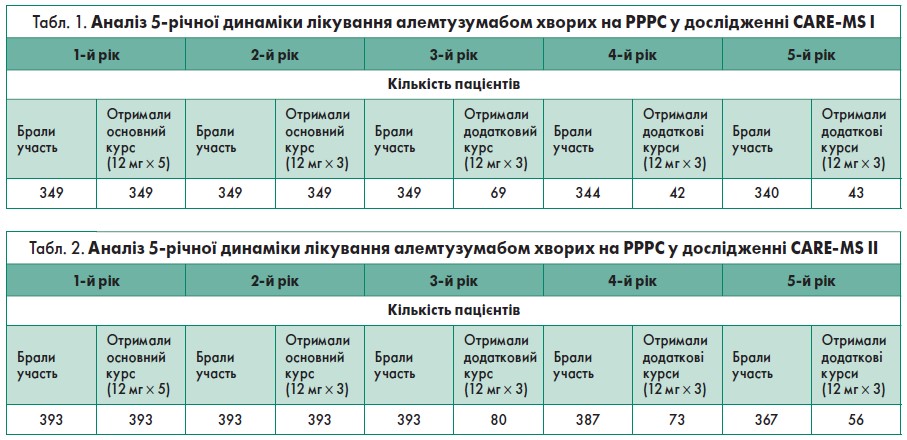
У таблиці 1 представлено когорту пацієнтів, що брали участь у СARE MS I та спостереженні до п’яти років із зазначенням кількості учасників, які отримали додаткові курси лікування алемтузумабом [14]. У таблиці 2 наведено аналогічні дані для популяції хворих СARE MS IІ [10].
У межах СARE MS I 95,1% пацієнтів, що лікувалися алемтузумабом, були включені до розширеного дослідження і 68,5% із них не отримували повторно алемтузумаб. За п’ятирічний період у хворих зафіксовано:
- зниження середньорічного показника рецидивів: 2-й рік – 0,16; 3-й рік – 0,19; 4-й рік – 0,14; 5-й рік – 0,15;
- відсутність у 79,7% пацієнтів показника шестимісячного підтвердження погіршення інвалідизації (підвищення показника згідно з EDSS ≥1, або ≥1,5, коли початковий показник за EDSS = 0);
- досягнення у 33,4% хворих показника шестимісячного підтвердження зменшення інвалідизації (зниження на ≥1 за початкового показника ≥2);
- високі показники досягнення статусу NEDA: 2-й рік – 68%; 3-й рік – 61,7%; 4-й рік – 60,2%; 5-й рік – 62,4% випадків;
- низькі показники зменшення об’єму мозку: 2-й рік – 0,25%; 3-й рік – 0,19%; 4-й рік – 0,15%; 5-й рік – 0,2%.
У дослідженні СARE MS II 92,9% пацієнтів, що отримували алемтузумаб, були включені до розширеного п’ятирічного спостереження. При цьому 59,8% із них не отримували повторної терапії алемтузумабом. За п’ятирічний період у групі хворих, що лікувалися алемтузумабом, встановлено:
- зниження середньорічного показника рецидивів: 2-й рік – 0,28; 3-й рік – 0,22; 4-й рік – 0,23; 5-й рік – 0,18;
- відсутність у 75,1% пацієнтів показника шестимісячного підтвердження погіршення інвалідизації;
- досягнення у 42,9% хворих показника шестимісячного підтвердження зменшення інвалідизації;
- високі показники досягнення статусу NEDA: 2-й рік – 58%; 3-й рік – 52,9%; 4-й рік – 54,2%; 5-й рік – 58,2% випадків;
- низькі показники зменшення об’єму мозку: 2-й рік – 0,22%; 3-й рік – 0,10%; 4-й рік – 0,19%; 5-й рік – 0,07%.
Слід додатково наголосити на встановленому в численних дослідженнях факті високої прихильності пацієнтів до терапії алемтузумабом. Також варто відзначити незначну кількість хворих, для ефективності лікування яких використовували хоча б один додатковий курс введення алемтузумабу.
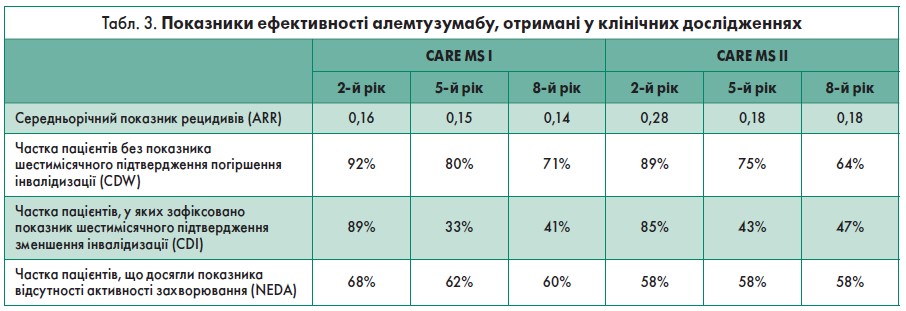
У таблиці 3 представлено виокремлені результати ефективності алемтузумабу, отримані у клінічних дослідженнях III та IV фази, які тривають нині (станом на 8-й рік). Вони свідчать про збереження позитивного впливу препарату на високому рівні протягом восьми років за відсутності безперервного лікування [25, 33].
Внаслідок інформаційного пошуку в Кокранівській базі даних систематичних оглядів виявлено два випробування. У вересні 2014 р. на основі отриманих даних дослідники дійшли висновку, що алемтузумаб – препарат із найвищою ефективністю для профілактики рецидивів РС [29]. Станом на квітень 2016 р., на основі результатів констатоване зменшення рецидивів під час лікування алемтузумабом, кількості нових та наявних вогнищ РС, що виявляються за допомогою МРТ, порівняно з терапією інтерфероном β‑1а. Також було озвучене припущення щодо відсутності зростання загального ризику побічних явищ. Одночасно автори систематичного огляду вказали на недостатність інформації про вплив алемтузумабу на якість життя хворих, ризик виникнення кожної небажаної реакції та частоту розвитку довготривалих та значних побічних ефектів [27]. Окрім того, 2019 р. був затверджений протокол проведення дослідження для формування систематичного огляду з оцінки ефективності та безпеки застосування окрелізумабу в пацієнтів із PPPC та ППРС [18].
У 2017 р. опубліковано звіт Інституту клінічних та економічних досліджень (ICER) про проведення мережевого метааналізу ефективності та безпеки 16 сучасних ХМП, що впливають на перебіг РС. За шкалою найефективнішої фармакотерапії, де основними були показники запобігання прогресуванню інвалідизації та скорочення рецидивів, алемтузумаб отримав рейтинг «А» (найвищий), тоді як окрелізумаб – рейтинг «В+» [11].
Аналогічну найвищу позицію за ознаками ефективності алемтузумаб посів у ранжованому переліку препаратів, сформованому висококваліфікованими експертами [6]. Було виконано багатогранну оцінку п’ятьох ХМП для лікування РС: наталізумабу, фінголімоду, кладрибіну, окрелізумабу та алемтузумабу [6].
Щодо показників безпеки, станом на кінець 2018 р. у клінічних та постмаркетингових дослідженнях лікування окрелізумабом отримали близько 80 тис. пацієнтів. Серед виявлених побічних ефектів фармакотерапії найчастіше траплялися: інфузійні реакції – 34,3%, нетяжкі інфекції верхніх дихальних шляхів – 15,2%, герпетична інфекція (оперізувальний лишай – 2,1%, простий герпес – 0,7%). Кількість тяжких інфекційних захворювань у групі окрелізумабу порівняно із такою інтерфероном β‑1а не збільшилася.
До травня 2019 р. у клінічних та постмаркетингових дослідженнях алемтузумабу взяли участь близько 34 тис. пацієнтів [15]. У спостереженнях, що тривають, частота виявлених побічних реакцій була нижчою, ніж в основних клінічних випробуваннях. Пік захворювань щитоподібної залози спостерігався до третього року, а далі зменшувався. Найчастіше фіксували інфузійні реакції (91,6%) та вторинні автоімунні захворювання.
Слід зазначити, що Kомітет із фармаконагляду й оцінки ризиків (PRAC) Європейського агентства з лікарських засобів (ЕМА) наприкінці квітня 2019 р. видав звіт про можливість виникнення імуноопосередкованих розладів із констатацією потреби у проведенні оцінки алемтузумабу та рекомендацією щодо інформування про ризик виникнення деяких ускладнень [31]. Вказані у листопаді 2019 р. тимчасові заходи через імовірність виникнення рідкісних, але значних побічних ефектів, були змінені на рекомендації, схвалені Комітетом із лікарських засобів для людини (CHMP) ЕМА:
- Використання алемтузумабу для лікування високоактивних форм РРРС у пацієнтів, які мають невдалий досвід фармакотерапії хоча б одним ХМП, або якщо хвороба швидко прогресує.
- Заборона застосування препарату в пацієнтів із певними порушеннями роботи серцево-судинної системи та кровообігу в анамнезі чи в осіб з іншими (відмінними від РС) автоімунними порушеннями.
- Уведення алемтузумабу хворому лише у стаціонарі під контролем спеціалістів та з доступом до інтенсивної терапії;
- Оновлення інформації та рекомендацій для лікаря і пацієнта щодо мінімізації ризиків серцево-судинних порушень, які можуть виникнути одразу ж після виконання ін’єкції, а також ризиків, пов’язаних із порушеннями роботи імунної системи, що інколи проявляються через певний час після лікування [20].
Дані рекомендації діятимуть до опублікування заключного висновку Європейської комісії ЄС.
Аналіз результатів фармакоекономічних досліджень
На наступному етапі було проведено пошук опублікованих фармакоекономічних досліджень окрелізумабу та алемтузумабу в доступних інформаційних джерелах.
У США 2017 р. на основі побудованої моделі для часового горизонту 20 років був виконаний аналіз методом «вартість/ефективність» окрелізумабу порівняно з інтерфероном β‑1а для лікування РРРС. Результати показали, що для фармакотерапії окрелізумабом при загальних витратах 614 519 $ пацієнт отримує 8,89 збережених років якісного життя (QALY), для інтерферону β‑1а – показники становили 678 341 $ та 6,27 відповідно [34]. Інше дослідження з вивчення економічної ефективності окрелізумабу порівняно з інтерфероном β‑1а для терапії PPPC, також проведене 2017 р. у США на основі моделі з урахуванням ступенів інвалідизації для часового горизонту 30 років, продемонструвало, що при загальних витратах для окрелізумабу 1 586 553 $ QALY становить 11,29, для інтерферону – показники 1874 266 $ та 10,46 відповідно [12].
У 2017 р. на щорічному форумі Європейського комітету з лікування та вивчення розсіяного склерозу (ECTRIMS) було представлено результати клініко-економічної оцінки алемтузумабу порівняно з окрелізумабом при лікуванні РРРС у США. На основі побудованої моделі (найважливіші компоненти – висока частота скасування окрелізумабу та довготривала ефективність алемтузумабу) для часового горизонту 20 років виявлено, що при загальних витратах на алемтузумаб 426 169 $ пацієнт отримує 8,89 QALY, окрелізумаб – показники 908 742 $ та 8,46 відповідно. Таким чином, результати показали фармакоекономічні переваги використання алемтузумабу в системі охорони здоров’я США [8].
У 2018 р. в США проведений фармакоекономічний аналіз методом «вартість/користь» ХМП для лікування PPРС. Як препарати першої лінії вивчали: диметилфумарат, глатирамеру ацетат, інтерферон β‑1a/β‑1b, пегінтерферон β‑1a, терифлуномід, наталізумаб, фінголімод та окрелізумаб; другої лінії: алемтузумаб, наталізумаб, фінголімод, окрелізумаб. Результати аналізу показали перевагу окрелізумабу як терапії першої лінії, алемтузумабу – другої лінії [35].
У 2019 р. опубліковано дані дослідження з фармакоекономічної оцінки методом «вартість/ефективність» алемтузумабу порівняно з іншими препаратами при РPPC у США. Автори побудували модель (часовий горизонт – 20 років), яка містила об’єднані демографічні та клінічні характеристики пацієнтів, що брали участь у випробуваннях CARE-MS I та CARE-MS II, дані про ефективність та безпеку медикаментів із мережевого метааналізу, інформацію про безпеку з інструкцій для медичного застосування, частоту скасування ліків, побічні реакції, економічні та вартісні показники – з опублікованих досліджень та клінічних експертних оцінок. Результати показали, що у разі лікування алемтузумабом при загальних витратах 421 996 $ пацієнт отримує 8,977 збережених QALY, окрелізумабом – показники 908 365 $ та 8,478 відповідно. Таким чином, отримані дані, що можуть допомогти у прийнятті управлінських рішень, продемонстрували вищу економічну ефективність алемтузумабу порівняно з окрелізумабом, наталізумабом, фінголімодом та глатирамеру ацетатом [9].
У 2018 р. в Нідерландах був проведений порівняльний фармакоекономічний аналіз методом «мінімізація вартості» з урахуванням виключно витрат на лікування при застосуванні алемтузумабу, фінголімоду та наталізумабу. Встановлено, що сума заощаджених витрат за п’ятирічного лікування одного пацієнта алемтузумабом порівняно з фінголімодом становила 30 327, з наталізумабом – 42 522 [26].
Наступним завданням дослідження стало проведення порівняльного фармакоекономічного аналізу схем лікування алемтузумабом та окрелізумабом. З огляду на вищевказані дані про наближені показники ефективності препаратів, було обрано метод «мінімізація вартості» на основі моделювання, методика якого полягала у наступному:
- При обчисленнях враховували лише вартісні показники алемтузумабу та окрелізумабу. Це дозволило розрахувати витрати на лікування кожним препаратом за певний час, що особливо актуально для алемтузумабу, оскільки схема лікування відрізняється від такої окрелізумабу і передбачає суттєві витрати на початковому етапі терапії.
- Ціна окрелізумабу (препарату Окревус) – концентрату для приготування розчину для інфузій по 300 мг/10 мл по 10 мл у флаконі – 172 003,96 грн – отримана з Реєстру оптово-відпускних цін на лікарські засоби станом на 10.12.2019 р. [5]; ціна алемтузумабу (препарату Лемтрада) – концентрату для приготування розчину для інфузій по 12 мг/1,2 мл по 1,2 мл у флаконі – 219 450,00 грн – є оптово-відпускною, розрахованою для наступної реєстрації у відповідному Реєстрі.
- Обрано горизонт часу п’ять років для охоплення додаткового 48-місячного періоду моніторингу стану пацієнта згідно з рекомендаціями щодо лікування алемтузумабом.
- Розрахунки проведено на основі когорти пацієнтів, що були залучені до клінічного випробування СARE-MS II, як найближчої за фармакотерапевтичними характеристиками до учасників клінічних досліджень алемтузумабу та окрелізумабу (див. табл. 2). При цьому було враховано реальні дані щодо отримання хворими додаткових курсів алемтузумабу та динаміки припинення участі пацієнтів у дослідженнях, а схему лікування окрелізумабом – екстрапольовано на вищевказану популяцію.
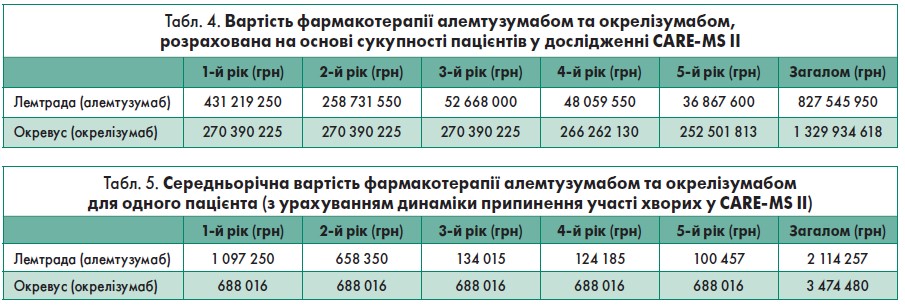
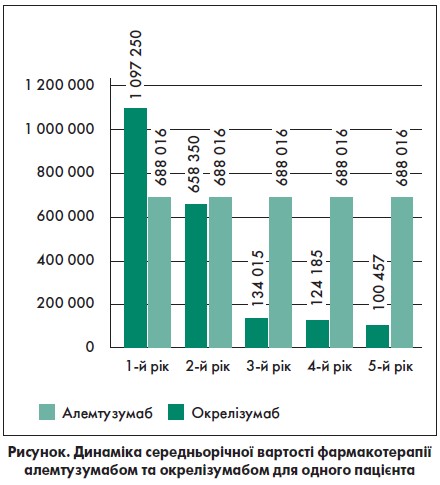
Отримані результати сумарної вартості лікування повної когорти пацієнтів представлено у таблиці 4. При цьому середні витрати за п’ятирічний період (табл. 5) на терапію алемтузумабом одного пацієнта становлять 2 114 257 грн, окрелізумабом – 3 474 480 грн (сума заощаджених витрат – 1 360 223 грн). Розраховані результати середньої вартості лікування одного пацієнта в динаміці за п’ять років представлено у таблиці 5 та на рисунку.
Лікування алемтузумабом, на відміну від окрелізумабу, потребує значно більших витрат протягом першого року (1 097 250 та 688 016 грн відповідно). Але вже на другий рік ситуація змінюється: витрати на алемтузумаб є меншими за такі на окрелізумаб (658 350 та 688 016 грн відповідно). Упродовж наступних років витрати на терапію алемтузумабом різко мінімізуються, зменшуючись на п’ятому році до 100 457 грн, тоді як на окрелізумаб – лишаються стабільними – 688 016 грн на рік. Середні витрати на одного пацієнта за п’ятирічний період при лікуванні алемтузумабом у 1,6 раза нижчі від аналогічних при терапії окрелізумабом.
Висновки
 Для фармакотерапії РС в Україні доступні сучасні інфузійні ХМП, що мають високу доведену ефективність: Окревус (окрелізумаб), який застосовують при РРРС та ППРС, та Лемтрада (алемтузумаб) – при високоактивному РРРС. Схема фармакотерапії препаратом Окревус (окрелізумаб) традиційна – введення внутрішньовенно у дозі 600 мг кожні шість місяців пожиттєво чи до моменту іншого рішення клініциста. Схема застосування засобу Лемтрада (алемтузумаб) є унікальною для препаратів, що використовують для лікування РС. Вона складається із двох основних курсів: перший – внутрішньовенне введення у дозі 12 мг/добу протягом п’ятьох послідовних днів; другий – 12 мг/добу впродовж трьох послідовних днів, які вводять через 12 місяців після першого курсу терапії (доцільність використання додаткових двох курсів встановлює лікар).
Для фармакотерапії РС в Україні доступні сучасні інфузійні ХМП, що мають високу доведену ефективність: Окревус (окрелізумаб), який застосовують при РРРС та ППРС, та Лемтрада (алемтузумаб) – при високоактивному РРРС. Схема фармакотерапії препаратом Окревус (окрелізумаб) традиційна – введення внутрішньовенно у дозі 600 мг кожні шість місяців пожиттєво чи до моменту іншого рішення клініциста. Схема застосування засобу Лемтрада (алемтузумаб) є унікальною для препаратів, що використовують для лікування РС. Вона складається із двох основних курсів: перший – внутрішньовенне введення у дозі 12 мг/добу протягом п’ятьох послідовних днів; другий – 12 мг/добу впродовж трьох послідовних днів, які вводять через 12 місяців після першого курсу терапії (доцільність використання додаткових двох курсів встановлює лікар).
Для вказаних лікарських засобів опубліковано результати клінічних випробувань, що доводять їхню відносно паритетну ефективність та безпеку при застосуванні. Дослідження ефективності препарату Лемтрада (алемтузумаб) тривають вже сім років. Отримані дані достовірно підтверджують попередньо виявлені показники ефективності, високий комплаєнс із незначною кількістю хворих, які використовували ще хоча б один додатковий курс.
Результати тривалих фармакоекономічних досліджень ХМП для лікування РС, проведених із використанням препаратів Лемтрада і Окревус, незважаючи на високу вартість, переконливо доводять їхні значущі фармакоекономічні переваги перед іншими ліками, зокрема тими, що закуповувалися в Україні за бюджетними програмами 2019 р. чи закуповуватимуться 2020 р.
Проведене у США окреме дослідження з фармакоекономічної оцінки методом «вартість/ефективність», в якому одночасно вивчали алемтузумаб та окрелізумаб, показало, що впродовж 20-річного періоду лікування РРРС застосування препарату Лемтрада буде у 2,3 раза економічно вигіднішим, ніж препарату Окревус.
Вивчення економічних аспектів застосування препаратів Лемтрада та Окревус в Україні продемонструвало, що лікування алемтузумабом, на відміну від окрелізумабу, потребує значно більших витрат протягом першого року. Але вже на другий рік витрати на лікарський засіб Лемтрада є меншими за такі на препарат Окревус, а на п’ятому році терапії – майже у сім разів меншими.
Фармакоекономічний аналіз «мінімізація вартості», проведений методом моделювання на основі реальної когорти пацієнтів дослідження СARE-MS II, показав, що при лікуванні в Україні за п’ятирічний період середні витрати для одного пацієнта на профільний засіб Лемтрада (алемтузумаб) будуть у 1,6 раза нижчими, ніж аналогічні за використання препарату Окревус (окрелізумаб).
Література
- Алифарова В.М., Бисага Г.Н., Бойко А.Н., Брюхов В.В., Давыдовская М.В., Захарова М.Н., та ін. Клинические рекомендации по применению препарата алемтузумаб (лемтрада) // Журнал неврологии и психиатрии. – 2017. – 2 (2). – С. 115‑116; DOI:10.17116/jnevro201711722115‑126.
- Антонюк T. Розсіяний склероз: ситуаційний аналіз проблеми в Україні // НейроNEWS. – 2018. – 3. – С. 6‑9.
- Iнструкція для медичного застосування лікарського засобу Лемтрада. Режим доступу: http://www.drlz.com.ua/ibp/ddsite.nsf/all/shlz1?opendocument&stype=9067FB4EF651E286C22583EE00293394.
- Iнструкція для медичного застосування лікарського засобу Окревус. Режим доступу: http://www.drlz.com.ua/ibp/ddsite.nsf/all/shlz1?opendocument&stype=3CE8884FCF551096C225841F002F0900.
- Реєстp оптово-відпускних цін на лікарські засоби станом на 10.12.2019 р. Режим доступу: http://moz.gov.ua/reestr-optovo-vidpusknih-cin-na-likarski-zasobi.
- Alroughani R., Inshasi J.S., Deleu D. et al. An Overview of High-Efficacy Drugs for Multiple Sclerosis: Gulf Region Expert Opinion // Neurology and Therapy. – 2019. – 8 (1). – Р. 13‑23; DOI: 10.1007/s40120‑019‑0129‑0.
- Atlas of MS2013. Available from: https://www.msif.org/about-us/who-we-are-and-what-we-do/advocacy/atlas.
- Chirikov V. Clinical and Economic Evaluation of Alemtuzumab Compared to Ocrelizumab in the Treatment of Relapsing Forms of Multiple Sclerosis in the United States: A Payer Perspective ECTRIMS Online Library. – 2017; 199703: EP1683.
- Chirikov V., Ma I., Joshi N. et al. Cost-Effectiveness of Alemtuzumab in the Treatment of Relapsing Forms of Multiple Sclerosis in the United States // Value in Health. – 2019. – 22 (2). – Р. 168‑176; DOI: https://doi.org/10.1016/j.jval.2018.08.011.
- Coles A.J., Cohen J.A., Fox E.J. et al. Alemtuzumab CARE-MS II 5-year follow-up: Efficacy and safety findings // Neurology. – 2017. – 89 (11). – 1117‑1126; DOI:10.1212/WNL.0000000000004354.
- Disease-Modifying Therapies for Relapsing-Remitting and Primary-Progressive Multiple Sclerosis: Effectiveness and Value Final Evidence Report // Institute for Clinical and Economic Review. – 2017. – 217 p. Аvailable from: https://icer-review.org/wp-content/uploads/2016/08/CTAF_MS_Final_Report_030617.pdf.
- Frasco M.A., Shih T., Incerti D. et al. Incremental net monetary benefit of ocrelizumab relative to subcutaneous interferon β‑1a // Journal of Medical Economics. – 2017. – 20 (10). – Р. 1074‑1082; DOI: 10.1080/13696998.2017.1357564.
- Hauser S.L., Bar-Or A., Comi G. et al., for the OPERA I and OPERA II Clinical Investigators. Ocrelizumab versus Interferon Beta‑1a in Relapsing Multiple Sclerosis // N Engl J Med. – 2017.– 376 (3). – Р. 221‑236; DOI: 10.1056/NEJMoa1601277.
- Havrdova E., Arnold D.L., Cohen J.A. et al. Alemtuzumab CARE-MS I 5-year follow-up: Durable efficacy in the absence of continuous MS therapy // Neurology. – 2017. – 89 (11). – Р. 1107‑1116; DOI:10.1212/WNL.0000000000004313.
- Lemtrada (alemtuzumab) and serious cardiovascular and immune-mediated adverse reactions: new restrictions to use and strengthened monitoring requirements // Drug Safety Update. – 2019. – 12 (10). Available from: https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/802701/May‑2019-PDF-DSU.pdf.
- Lemtrada Approval History. Available from: https://www.drugs.com/history/lemtrada.html.
- Lemtrada; EMA. Available from: https://www.ema.europa.eu/en/medicines/human/EPAR/lemtrada (30).
- Lin M., Shi S., Zhang J. et al. Ocrelizumab for multiple sclerosis // Cochrane Database of Systematic Reviews. – 2019. – 1. – CD013247; DOI: 10.1002/14651858.CD013247.
- Lublin F.D., Reingold S.C. National Multiple Sclerosis Society (USA) Advisory Committee on Clinical Trials of New Agents in Multiple Sclerosis. Defining the clinical course of multiple sclerosis: results of an international survey // Neurology. – 1996. – 46 (4). – Р. 907‑911; DOI:10.1212/WNL.46.4.907.
- Measures to minimise risk of serious side effects of multiple sclerosis medicine Lemtrada. 15 November 2019 ЕМА/609015/2019. Аvailable from: https://www.ema.europa.eu/en/documents/referral/lemtrada-article‑20-procedure-measures-minimise-risk-serious-side-effects-multiple-sclerosis_en.pdf.
- Naci H. Economic burden of multiple sclerosis: a systematic review of the literature // Pharmacoeconomics. – 2010. – 28 (5). – Р. 363‑379.
- New OCREVUS (ocrelizumab) data at ECTRIMS advance clinical understanding of underlying progression in multiple sclerosis // Media Release, 2017. Аvailable from: https://www.roche.com/media/releases/med-cor‑2017‑10‑27.html.
- Ocrevus (ocrelizumab) injection. Available from: https://www.accessdata.fda.gov/drugsatfda_docs/nda/2017/761053Orig1s000TOC.cfm.
- Ocrevus (ocrelizumab). Available from: https://www.ema.europa.eu/en/medicines/human/EPAR/ocrevus.
- Oreja-Guevara C., Amato M.P., Barnett M. et al. On behalf of the CARE-MS II, CAMMS03409, and TOPAZ Investigators. Alemtuzumab outcomes over 6 Years in RRMS patients who switched from SC IFNB‑1a: follow-up of CARE-MS II patients (TOPAZ study) // ECTRIMS Online Library. – 2018. – 229079. – 1239. Аvailable from: https://onlinelibrary.ectrims-congress.eu/ectrims/2018/ectrims‑2018/229079/celia.oreja-guevara.alemtuzumab.outcomes.over.6.years.in.rrms.patients.who.html.
- Piena M.A., Heisen M., Wormhoudt L.W. et al. Cost-minimization analysis of alemtuzumab compared to fingolimod and natalizumab for the treatment of active relapsing-remitting multiple sclerosis in the Netherlands // Journal of Medical Economics. – 2018. – 21 (10). – Р. 968‑976; DOI: 10.1080/13696998.2018.1489255.
- Riera R., Porfirio G.J., Torloni M.R. Alemtuzumab for multiple sclerosis // Cochrane Database of Systematic Reviews. – 2016. – 4. – CD011203; DOI: 10.1002/14651858.CD011203.pub2.
- Rush C.A., MacLean H.J., Freedman M.S. Aggressive multiple sclerosis proposed definition and treatment algorithm // Nature Reviews Neurology. – 2015. – 11. – Р. 379‑389; https://doi.org/10.1038/nrneurol.2015.85.
- Tramacere I., Del Giovane C., Salanti G. et al. Immunomodulators and immunosuppressants for relapsing-remitting multiple sclerosis: a network meta-analysis // Cochrane Database of Systematic Reviews. – 2015. – 9. – CD011381; DOI: 10.1002/14651858.CD011381.pub2.
- Type of MS; National Multiple Sclerosis Society (USA). Available from: https://www.nationalmssociety.org/What-is-MS/Types-of-MS.
- Use of multiple sclerosis medicine Lemtrada restricted while EMA review is ongoing. Press release 12/04/2019. https://www.ema.europa.eu/en/news/use-multiple-sclerosis-medicine-lemtrada-restricted-while-ema-review-ongoing.
- Wallin M.T., Culpepper W.J., Campbell J.D. et al. The prevalence of MS in the United States // Neurology. – 2019. – 92 (10). – Р. 1029‑1040; DOI:10.1212/WNL.0000000000007035.
- Wijmeersch B., Barone D., Broadley S. et al. On behalf of the CARE-MS I, CAMMS03409, and TOPAZ Investigators. Alemtuzumab outcomes over 6 years in RRMS patients who switched from SC IFNB‑1a: follow-up of CARE-MS I patients (TOPAZ study) // ECTRIMS Online Library. – 2018. – 228750. – 907. Аvailable from: https://onlinelibrary.ectrims-congress.eu/ectrims/2018/ectrims‑2018/228750/bart.van.wijmeersch.alemtuzumab.outcomes.over.6.years.in.rrms.patients.who.html.
- Yang H., Duchesneau E., Foster R. et al. Cost-effectiveness analysis of ocrelizumab versus subcutaneous interferon beta‑1a for the treatment of relapsing multiple sclerosis // Journal of Medical Economics. – 2017. – 20 (10). – Р. 1056‑1065; DOI: 10.1080/13696998.2017.1355310.
- Zimmermann M., Brouwer E., Tice J.A. et al. Carlson Disease-Modifying Therapies for Relapsing–Remitting and Primary Progressive Multiple Sclerosis: A Cost-Utility Analysis // CNS Drugs. – 2018. – 32 (12). – 1145‑1157; DOI:10.1007/s40263‑018‑0566‑9.
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 3 (54) 2020 р.