28 жовтня, 2020
Електрокардіографічна діагностика інфаркту міокарда: звертаємося до підручника
 Редакція медичної газети «Здоров’я України», тематичного номера «Кардіологія. Ревматологія. Кардіохірургія» продовжує знайомити наших читачів із ґрунтовним і детальним підручником «Функціональна діагностика» за редакцією д. мед. н., професора О.Й. Жарінова, д. мед. н., професора Ю.А. Іваніва та к. мед. н., доцента В.О. Куця. Пропонуємо до вашої уваги розділ «Електрокардіографічна діагностика інфаркту міокарда».
Редакція медичної газети «Здоров’я України», тематичного номера «Кардіологія. Ревматологія. Кардіохірургія» продовжує знайомити наших читачів із ґрунтовним і детальним підручником «Функціональна діагностика» за редакцією д. мед. н., професора О.Й. Жарінова, д. мед. н., професора Ю.А. Іваніва та к. мед. н., доцента В.О. Куця. Пропонуємо до вашої уваги розділ «Електрокардіографічна діагностика інфаркту міокарда».
Інфаркт міокарда (ІМ) – гостра хвороба, за якої внаслідок абсолютної або відносної недостатності коронарного кровообігу в серцевому м’язі виникають одне або кілька вогнищ некрозу. Згідно з патоморфологічним визначенням, ІМ – це смерть клітин міокарда, зумовлена тривалою ішемією.
ІМ є однією із провідних причин інвалідності та летальності в сучасному світі. Кожний шостий випадок смерті в Європі у чоловіків і кожний сьомий у жінок спричинені ІМ (ACCF/AHA, 2013; Roffi et al., 2016). Відповідно до рекомендацій Асоціації кардіологів України (2013), в Україні щорічно реєструють близько 50 тис. випадків гострого ІМ. Своєчасне встановлення діагнозу гострого ІМ є необхідною передумовою успішного лікування хвороби, а реєстрація та правильна інтерпретація даних електрокардіограми (ЕКГ) – одним із ключових елементів діагностики ІМ.
Критерії діагностики ІМ
Поява більш чутливих і специфічних маркерів ушкодження міокарда, нових методів візуалізації серця зумовлює еволюцію критеріїв діагностики гострого ІМ. Згідно із третім універсальним визначенням ІМ, термін «інфаркт міокарда» слід використовувати у випадках доведеного некрозу міокарда внаслідок тривалої гострої ішемії.
Критерії встановлення діагнозу ІМ (ESC/AHA/ACC/WHF, 2012; Thygesen et al., 2012):
- підвищення рівня та/або закономірна динаміка зниження рівня маркера(-ів) ушкодження міокарда (кардіоспецифічних ферментів, бажано серцевого тропоніну) в крові, що супроводжується хоча б однією з таких ознак:
- симптоми ішемії міокарда;
- діагностично значущі зміни сегмента ST і зубця Т, що вказують на нове вогнище ішемії, або виникнення повної блокади лівої ніжки пучка Гіса (ЛНПГ);
- поява на ЕКГ патологічних зубців Q;
- поява ознак некрозу міокарда або нових зон гіпо-/акінезії за даними методів візуалізації серця;
- виявлення внутрішньокоронарного тромбу при ангіографічному або патологоанатомічному дослідженні;
- раптова серцева смерть на тлі симптомів, що свідчать про ішемію міокарда та супроводжуються, ймовірно, новими ішемічними змінами на ЕКГ або появою нової блокади ЛНПГ, коли смерть настає до підвищення рівня серцевих біомаркерів у крові;
- тромбоз стента або ускладнення під час/після черезшкірного коронарного втручання, що асоціюються з виникненням ІМ, виявляються під час коронарної ангіографії або автопсії, коли є ознаки активної ішемії міокарда й підвищення та/або зниження рівня маркера(-ів) ушкодження міокарда.
Реєстрація ЕКГ та інтерпретація виявлених змін мають ключове значення для ранньої діагностики ІМ. На початковому етапі обстеження для оцінки стану пацієнта з болем у грудній клітці переважно застосовують термін «гострий коронарний синдром».
При першому контакті з пацієнтом протягом 10 хв необхідно зареєструвати та інтерпретувати ЕКГ. Саме залежно від даних ЕКГ розрізняють гострі коронарні синдроми з/без підйому сегмента ST. Своєю чергою вказаний поділ визначає потребу та терміни виконання реваскуляризації міокарда (Асоціація кардіологів України, 2013; ACCF/AHA, 2013; Roffi et al., 2016).
Раннім виявом ішемії міокарда є поява позитивного «коронарного» зубця Т у двох послідовних відведеннях. Дещо пізніше з’являється елевація сегмента ST у точці J на ≥1 мм принаймні у двох суміжних відведеннях, яка є надійним критерієм гострої ішемії міокарда. Наголосимо, що у відведеннях V2-V3 ознакою гострої ішемії є підйом сегмента ST на ≥2 мм у чоловіків віком понад 40 років, на ≥2,5 мм у чоловіків віком до 40 років і на 1,5 мм у жінок. Депресія сегмента ST у відведеннях V1-V3, особливо у поєднанні з позитивними зубцями Т у вказаних відведеннях, дає підстави припускати ішемію протилежної (задньобазальної) ділянки лівого шлуночка (ЛШ). У такому разі доцільно зареєструвати ЕКГ у відведеннях V7-V9 та за Слопаком і Партіллою (S1-S4), де виявляються «прямі» ознаки пошкодження міокарда.
Ознаками некрозу міокарда є комплекс QS або патологічний зубець Q у двох і більше суміжних відведеннях (I, aVL, V4-V6 або ІІ, ІІІ, aVF, V7-V9). Зубець Q вважають патологічним, якщо його тривалість ≥0,02 с у відведеннях V2-V3 або ≥0,03 с в інших відведеннях, амплітуда становить ≥1 мм. Ознаками некрозу задньої стінки ЛШ є зубець R тривалістю ≥0,04 с у відведеннях V1-V2 і співвідношення R/S ≥1 у поєднанні з позитивним зубцем Т у цих же відведеннях за відсутності порушення внутрішньо-шлуночкової провідності (Асоціація кардіологів України, 2013; ACCF/AHA, 2013).
У деяких випадках інтерпретація ЕКГ утруднена, але існує потреба у невідкладному здійсненні діагностичних та лікувальних заходів. Прикладом можуть бути ситуації, коли є клінічні симптоми ішемії міокарда, але при цьому зміни ЕКГ діагностично незначущі, або ЕКГ-діагностика ускладнюється через деформацію комплексу QRS при штучній кардіостимуляції, блокаді ЛНПГ, синдромі преекзитації тощо.
Можливі причини відсутності елевації сегмента ST у 12 загальноприйнятих відведеннях в осіб із гострою коронарною оклюзією: занадто ранні терміни обстеження пацієнта після появи симптомів, ізольований задньобазальний ІМ, обструкція стовбура лівої вінцевої артерії (ЛВА).
Формування змін ЕКГ при ІМ
Вже через 15‑20 хв від початку епізоду ішемії міокарда формується пошкодження, і цей процес ще може бути зворотним. Наслідком тривалішого пошкодження є некроз кардіоміоцитів. На периферії ділянки некрозу виявляються ознаки пошкодження, а поза нею – зона ішемії. Таким чином, при гострому ІМ виділяють три зони:
- некрозу;
- пошкодження;
- ішемії.
Ішемія відображається на ЕКГ змінами зубця Т, пошкодження – зміщенням сегмента ST, а некроз – патологічними змінами комплексу QRS (Сиркін, 1991; Орлов, 2003).
Ішемія міокарда призводить до сповільнення процесів реполяризації в ураженій ділянці та змінює її напрямок. У нормі реполяризація міокарда поширюється в напрямку від епікарда до ендокарда, а за наявності ішемії – сповільнюється в зоні недостатнього коронарного кровопостачання. Субендокардіальні відділи міокарда гірше постачаються кров’ю і найбільше схильні до ішемії. У відведеннях, розміщених над ділянкою субендокардіальної ішемії, внаслідок уповільнення реполяризації реєструється високий поширений «коронарний» зубець Т. При субепікардіальній, як і при трансмуральній ішемії реполяризація змінює свій напрямок на протилежний, а саме починається в ендокарді та поширюється до епікарда. Таким чином, у відведеннях над зоною ішемії формується негативний поширений рівнобічний («коронарний») зубець Т.
При виникненні субендокардіальної ішемії на протилежній активному електроду стінці ЛШ у прямих відведеннях реєструється низькоамплітудний позитивний зубець Т. У разі трансмуральної ішемії (або субепікардіальних відділів) протилежної стінки під активним електродом реєструється позитивний, високоамплітудний, із гострою вершиною зубець Т (реципрокні зміни).
При пошкодженні міокарда формуються глибокі порушення структури та функції клітини, які не змінюють напрямок деполяризації. З огляду на це, у разі своєчасного відновлення кровопостачання процес може бути зворотним. Сегмент ST відображає період повного охоплення деполяризацією всього міокарда шлуночків і в нормі розташований на ізолінії. При формуванні ділянки пошкодження з’являється різниця потенціалів між нею і здоровою тканиною.
Пошкоджена ділянка має позитивний заряд, а збуджені ділянки здорової тканини – негативний, і вектор електрорушійної сили спрямований від здорових до пошкоджених ділянок міокарда. При субендокардіальному пошкодженні вектор електрорушійної сили спрямований до ендокарда. Отже, під активним електродом, розміщеним над місцем субендокардіального пошкодження, реєструється депресія сегмента ST.
Водночас при субепікардіальному або трансмуральному пошкодженні у відведеннях над цією зоною реєструється підйом сегмента ST (пряма ознака пошкодження), а в протилежних відведеннях – депресія сегмента ST (реципрокні зміни). Крім того, пошкоджений міокард шлуночків збуджується повільніше, що може призвести до деякого зменшення амплітуди зубця R над місцем пошкодження та її збільшення у відведеннях, розміщених над протилежною стінкою.
Ділянка некрозу не здатна проводити імпульси. Під електродом, розташованим над зоною трансмурального некрозу, реєструється комплекс QS, що відображає деполяризацію протилежної стінки ЛШ. Якщо частину міокарда у зоні некрозу збережено, під електродом над зоною ІМ реєструється комплекс QR. Чим більший розмір ІМ, тим більшим за тривалістю та амплітудою є зубець Q, і меншим – зубець R. На протилежній стінці виявляються реципрокні зміни: збільшення амплітуди та тривалості зубця R зі зменшенням амплітуди зубця S.
При інтрамуральному некрозі ділянка міокарда, не здатна до деполяризації, розташована у товщі міокарда, а субендокардіальні та субепікардіальні відділи зберігають здатність проводити імпульси. На ЕКГ не реєструється патологічний зубець Q, але може зменшуватися амплітуда зубця R, або ж він розщеплений на висхідній частині. Зону інтрамурального некрозу оточують зони пошкодження та ішемії, що відображається змінами процесів реполяризації (депресія/елевація сегмента ST і негативний зубець Т). При субендокардіальному ІМ формується некроз тонкого шару міокарда, розташованого під ендокардом. Відсутність його деполяризації не призводить до змін сумарного вектора збудження ЛШ, але субендокардіальне пошкодження та ішемія супроводжуються глибокою тривалою депресією сегмента ST із переходом у (-/+) зубець Т у відведеннях над зоною ураження (Де Луна, 1993; Асоціація кардіологів України, 2013).
Стадії гострого ІМ
За характером змін ЕКГ виділяють чотири стадії великовогнищевого Q-ІМ: найгострішу, гостру, підгостру та рубцеву (Де Луна, 1993; Асоціація кардіологів України, 2013). Ці стадії не повністю узгоджуються із клінічними стадіями ІМ.
Найгостріша стадія («стадія пошкодження») триває від кількох хвилин до доби, рідко – до 2‑3 діб. У перші хвилини хвороби на ЕКГ реєструються високі симетричні «коронарні» зубці Т без змін сегмента ST і комплексу QRS. Вони відображають субендокардіальну ішемію. Ці зміни рідко вдається зареєструвати на ЕКГ внаслідок їхньої швидкоплинності. Далі з’являється елевація сегмента ST, що зливається з позитивним зубцем Т у «монофазну криву» внаслідок появи трансмурального пошкодження під електродом. Елевацію сегмента ST часто характеризують як дугоподібну, з випуклістю догори, інколи – у вигляді плато або з випуклістю донизу.
Існує прямопропорційна залежність між ступенем елевації сегмента ST і глибиною подальшого інфаркту. Втім зміни ЕКГ, які відображають пошкодження та ішемію міокарда, можуть бути зворотними у разі швидкого відновлення прохідності інфарктзалежної вінцевої артерії.
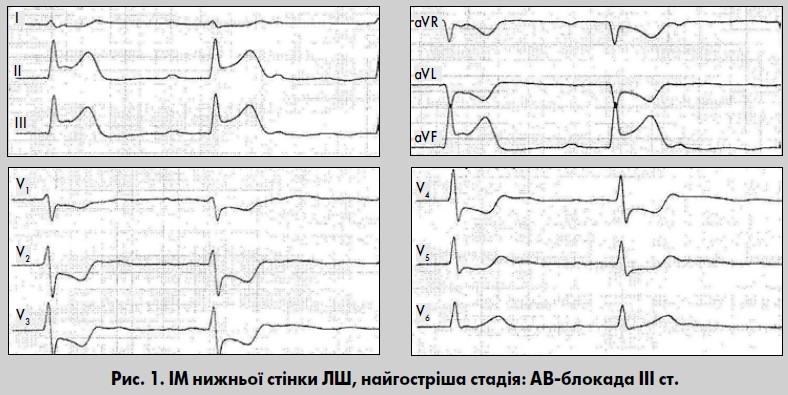
Вже через кілька годин у центрі зони пошкодження може сформуватися вогнище некрозу, що веде до появи патологічних зубців Q у відповідних відведеннях. Проте глибину ІМ у цій стадії визначити ще неможливо. У відведеннях над стінкою, протилежною до зони інфаркту, реєструються реципрокні зміни у вигляді депресії сегмента ST та високого коронарного зубця Т (рис. 1).
Гостра стадія позначається як стадія диференціації зони пошкодження. Вона триває від трьох діб до трьох тижнів, характеризується появою та продовженням формування зони некрозу, розширенням зони ішемії за рахунок зменшення зони пошкодження. На ЕКГ у відведеннях над зоною інфаркту з’являється або поглиблюється патологічний зубець Q, сегмент ST поступово наближається до ізолінії, починає формуватися негативний зубець Т.
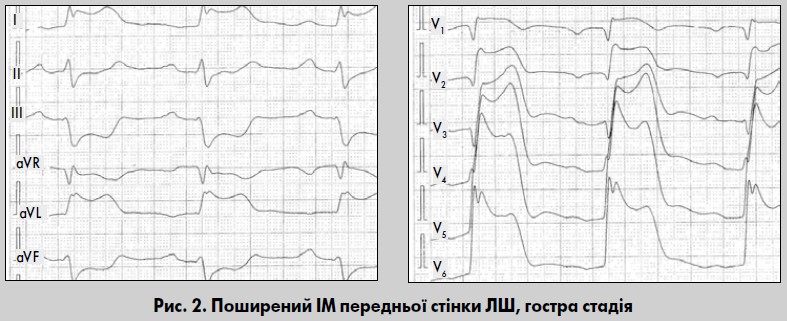
Тривале збереження підйому сегмента ST (понад трьох тижнів від початку хвороби, інколи – невизначено довго) спостерігають при поширених або трансмуральних ІМ передньої локалізації, які асоціюються з формуванням аневризми ЛШ. У відведеннях, розташованих над зоною некрозу, формуються шлуночкові комплекси QR, Qr або QS, і може збільшуватися кількість відведень, де вони реєструються. Одночасно виявляються реципрокні зміни у протилежних відведеннях у вигляді збільшення амплітуди та тривалості зубця R, зміщення сегмента ST нижче від ізолінії, а також високого «коронарного» зубця Т (рис. 2).
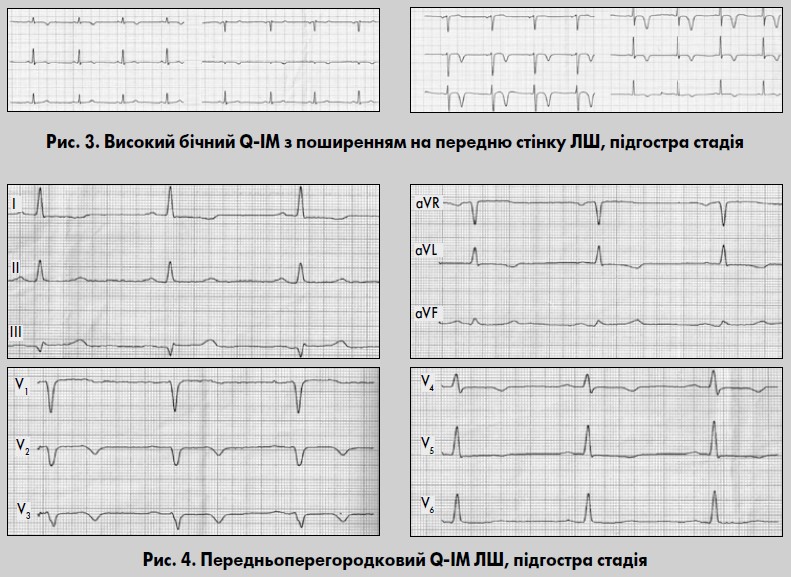
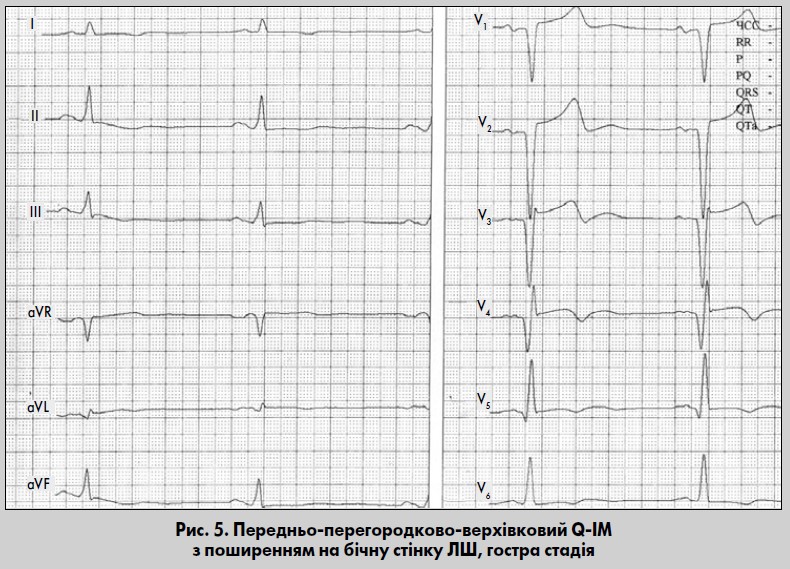
Підгостра стадія характеризується повним зникненням ознак пошкодження (рис. 3, 4). На ЕКГ сегмент ST повертається до ізолінії. Зубець Q у цій стадії вже повністю сформований, і чітко визначаються відведення, за якими можна судити про локалізацію ІМ. Остаточно формується глибокий, симетричний, загострений зубець Т. Можуть спостерігатися також динамічні зміни зубця Т, зменшення його амплітуди під кінець цієї стадії. Тривалість підгострої стадії становить від трьох тижнів до трьох місяців.
Рубцева стадія характеризується утворенням рубця на місці інфаркту. Її ознаки можуть зберігатися невизначено довго. На ЕКГ реєструється патологічний зубець Q, а сегмент ST залишається на ізолінії (рис. 5). Зубець Т спочатку негативний. Через деякий час після перенесеного ІМ амплітуда негативного зубця Т інколи зменшується, він може стати ізоелектричним або навіть позитивним. Пізніше за рахунок зменшення зони ІМ можливе скорочення кількості відведень, в яких реєструється патологічний зубець Q. Іноді графіка шлуночкового комплексу QS трансформується в QR або навіть qR, або патологічний зубець Q зникає, що пояснюють компенсаторною гіпертрофією прилеглих ділянок міокарда та «стягненням» зони рубця. Якщо в рубцевій стадії зберігається негативний зубець Т, за амплітудою він не повинен перевищувати 5 мм або ½ амплітуди зубця Q у цьому ж відведенні. Поглиблення зубця Т у рубцевій стадії може свідчити про ішемію міокарда в зоні рубця.
Топічна діагностика ІМ
Локалізація ІМ визначається за ЕКГ-відведеннями, в яких спостерігають характерні вогнищеві зміни. Окрім того, зміни ЕКГ дають змогу орієнтовно визначити вінцеву артерію, тромбоз якої міг стати причиною ІМ. Така оцінка важлива для прогнозування перебігу та ускладнень ІМ (Орлов, 2003; Мурашко, Струтинський, 2014). Водночас потрібно враховувати можливість переважного постачання окремих ділянок міокарда різними вінцевими артеріями.
Виділяють три типи кровопостачання міокарда. Найчастіше реєструють правий тип, коли права вінцева артерія (ПВА) формує задню низхідну артерію, постачає кров’ю значну частину правого шлуночка (ПШ), задню стінку ЛШ, задню частину міжшлуночкової перегородки, верхівку серця, праве передсердя, міжпередсердну перегородку, синусовий і атріовентрикулярний (АВ) вузол, стовбур пучка Гіса, правої ніжки ПГ (ПНПГ) і задню гілку ЛНПГ. ЛВА зазвичай ділиться на передню міжшлуночкову (ПМШГ) і обвідну гілки (ОГ).
ПМШГ постачає кров’ю передню стінку, верхівку, інколи задньодіафрагмальну поверхню ЛШ, більшу частину перегородки і частину розгалужень внутрішньошлуночкової провідної системи. ОГ забезпечує кров’ю бічну стінку ЛШ та ліве передсердя. При лівому типі кровопостачання ОГ утворює задню низхідну гілку, яка постачає кров’ю задню стінку ЛШ, задню частину міжшлуночкової перегородки, нерідко – синусовий вузол, інколи – АВ-вузол і частину задньої гілки ЛНПГ. При змішаному типі задня стінка ЛШ постачається через ПВА та ОГ ЛВА. При тромбозі тієї або іншої вінцевої артерії виникають зони ішемії, пошкодження і некрозу певної анатомічної локалізації, що відображається змінами у відповідних відведеннях ЕКГ (Доценко та співавт., 2008; Мурашко, Струтинський, 2014). На цьому базується виділення груп суміжних відведень, в яких спостерігаються зміни при ураженні певної вінцевої артерії (Мурашко, Струтинський, 2014) (таблиця).
ЕКГ при передньо- перегородковому ІМ
Інфаркт передньоперегородкової ділянки зумовлений тромбозом ПМШГ ЛВА із залученням її першої перегородкової гілки. Прямі ознаки ІМ реєструються у відведеннях V1-V2 (V3), реципрокні – у протилежних грудних відведеннях (V7-V9) (Сиркін, 1991; Орлов, 2003). У стандартних відведеннях і від кінцівок змін може не бути (див. рис. 4). У нормі зубець r у відведеннях V1-V2, що формується внаслідок деполяризації міжшлуночкової перегородки, невеликий за амплітудою, а інколи у відведенні V1 може взагалі не реєструватися. Тому комплекс QS у відведенні V1 не є доказом вогнищевих змін. Водночас поява навіть невеликого зубця q з формуванням комплексу qrS у V1-V2 із реципроним зникненням зубця q у V5-V6 може свідчити про вогнищеві зміни в міжшлуночковій перегородці.
Крім формування комплексу QS, qrs або qrS у відведеннях V1-V2, у них же спостерігається підйом сегмента ST над ізолінією з випуклістю догори. У перші дні гострої стадії сегмент ST зливається з зубцем Т, із подальшою характерною динамікою кінцевої частини шлуночкового комплексу. У правих грудних відведеннях формується негативний зубець Т, сегмент ST поступово наближається до ізолінії. Надалі амплітуда негативного зубця Т зменшується, інколи він стає навіть слабкопозитивним. Про раніше перенесений ІМ у цій ділянці може свідчити також відсутність приросту зубця R у відведеннях від V1 до V4 або співвідношення зубців RV1>RV2>RV3.
Нерідко виникають складності інтерпретації ЕКГ із графікою QS у відведеннях V1-V2, а також коли немає приросту амплітуди зубця R у V1-V5, або він є недостатнім. Подібна графіка може траплятися в осіб із поворотом серця навколо поздовжньої осі за годинниковою стрілкою, емфіземою легень, плевроперикардіальними зрощеннями, а також інколи при гіпертрофії та дилатації ЛШ, блокаді передньої гілки або повній блокаді ЛНПГ, за наявності правобічного пучка Кента, який функціонує (Гришкін, Журавльова, 2008). Шлуночковий комплекс типу qR у відведеннях V1-V2 може реєструватися при виразній гіпертрофії ПШ, блокаді ПНПГ та серединного розгалуження ЛНПГ. Інфаркт передньоперегородкової ділянки може призводити до виникнення постійної або транзиторної внутрішньошлуночкової блокади.
ІМ передньої стінки ЛШ, або передньо-перегородково-верхівковий ІМ
Зазвичай ІМ зазначеної локалізації зумовлений ураженням ПМШГ ЛВА у проксимальному сегменті (Байєс де Луна та співавт., 2009). Прямі ознаки ІМ реєструються у відведеннях V1-V4, Anterior за Небом (див.рис. 5) (Орлов, 2003). В них формується комплекс QS (при трансмуральному некрозі) або QR. Наголосимо, що патологічний зубець Q формується у гострій стадії хвороби; співвідношення амплітуд зубців Q і R, а також кількість відведень із патологічним зубцем Q остаточно визначають після повернення сегмента ST на ізолінію. У перші дні хвороби у відведеннях V3-V4 може реєструватися комплекс QR із подальшою трансформацією в QS. Часто реєструється підйом сегмента ST до 7‑8 мм. У підгострій стадії сегмент ST розташований на ізолінії, формуються глибокі негативні «коронарні» зубці Т.
Реципрокні зміни реєструються у відведеннях V7-V9, інколи у ІІ, III, aVF, Dorsalis за Небом, де спостерігають збільшення амплітуди зубця R, горизонтальну або з випуклістю донизу депресію сегмента ST із формуванням високого симетричного зубця Т. Реципрокні зміни більш швидкоплинні, але інколи реєструються раніше, ніж прямі ознаки, що дає підставу запідозрити ІМ передньої стінки. У рубцеву стадію амплітуда негативного зубця Т у відведеннях V1-V4 зменшується, він інколи стає ізоелектричним або слабкопозитивним, можуть з’явитися зубці r невеликої амплітуди із трансформацією графіки QS на Qr.
ІМ передньобічної стінки ЛШ
ІМ бічної стінки ЛШ виникає при оклюзії ОГ ЛВА, її крайової гілки або діагональної гілки ПМШГ ЛВА (Орлов, 2003; Байєс де Луна та співавт., 2009). Прямі ознаки інфаркту реєструються у відведеннях V5, V6, I, aVL, інколи у II та Inferior. Зубець Q вважається патологічним у лівих грудних відведеннях, якщо його амплітуда перевищує 2 мм або 15% наступного за ним зубця R. При верхньобічній локалізації ІМ прямі ознаки можуть бути більш виражені у відведенні aVL, ніж у V5, V6. Для уточнення діагнозу в цьому разі необхідно зареєструвати ЕКГ у відведеннях V5, V6 на 2 ребра вище.
Потрібно зважати на те, що амплітуда зубця Q у відведенні aVL при вертикальній позиції серця інколи становить до 50% від амплітуди зубця R, і може навіть реєструватися комплекс QS. У цьому випадку зубці P і T у відведенні aVL також будуть негативними. Якщо прямі ознаки ІМ реєструються не лише у V5, V6, але й у V7-V9, це свідчить про поширення інфаркту на базальні відділи задньої стінки ЛШ. Ознаками бічного ІМ, особливо в рубцеву стадію, можуть бути суттєве зниження амплітуди зубця R, глибокий зубець S у відведеннях V5, V6, виразна зазубреність комплексу QRS у відведеннях V5, V6, aVL, I, II. Утім ці ознаки неспецифічні й реєструються при багатьох інших станах, а їхня інтерпретація можлива лише з урахуванням інших ознак ІМ. Реципрокні зміни, такі як збільшення амплітуди зубця R, депресія сегмента ST і високий зубець T, можуть реєструватися у відведеннях III, aVF, V1, V2, V3R-V4R.
Високий бічний ІМ
ІМ високих відділів бічної стінки (див. рис. 3) зазвичай зумовлений ураженням крайової гілки, яка відходить від ОГ ЛВА, або діагональної гілки ПМШГ ЛВА (Орлов, 2003; Байєс де Луна та співавт., 2009). Ізольований ІМ високих бічних відділів ЛШ нерідко складно діагностувати при використанні лише 12 загальноприйнятих відведень ЕКГ. Прямі ознаки реєструються ізольовано у відведеннях aVL або I і aVL. Зубець Q у відведенні aVL вважається патологічним, якщо його амплітуда у ньому ≥1/2 R, при цьому зубці P і T в aVL позитивні.
У разі підозри на високий ІМ передньої стінки ЛШ необхідно зареєструвати ЕКГ у грудних відведеннях на 1‑2 міжребер’я вище від звичайних позицій. Нерідко у відведеннях V4-V6 також визначають прямі ознаки ІМ, як-от патологічний зубець Q, відповідна динаміка сегмента ST і зубця Т. Реципрокні зміни можуть реєструватися у відведеннях III і aVF.
Передньо-верхівково-бічний ІМ
ІМ зазначеної локалізації частіше зумовлений ураженням діагональної артерії, що відходить від ПМШГ ЛВА (Орлов, 2003; Байєс де Луна та співавт., 2009). Прямі ознаки ІМ реєструються у відведеннях V3-V6, I, aVL, Anterior, Inferior за Небом, реципрокні – у III, aVF, іноді у II відведенні.
Поширений ІМ передньої стінки ЛШ
Такий ІМ зумовлений частіше оклюзією стовбура ЛВА або її ПМШГ у проксимальному сегменті (Орлов, 2003; Байєс де Луна та співавт., 2009). Прямі ознаки ІМ реєструються у відведеннях V1-V6, а також I, aVL, Anterior, Inferior, інколи – у II відведенні (див. рис. 2). У цих відведеннях реєструються патологічний зубець Q, значний підйом сегмента ST, часто у вигляді монофазної кривої. Поява зубця Q призводить до формування шлуночкового комплексу із графікою QR або QS. Реєстрація комплексу QS у відведеннях V1-V4 вказує на трансмуральний ІМ передньої стінки ЛШ, а наявність графіки QS у відведеннях з V1 до V5-V6 – високу ймовірність формування гострої або, надалі, хронічної аневризми ЛШ зазначеної локалізації.
При поширеному трансмуральному некрозі формування патологічного зубця Q (QS) може відбуватися дуже швидко та інколи навіть випереджає динаміку сегмента ST і зубця Т (Сиркін, 1998). На це необхідно зважати при повторному ІМ вказаної локалізації, який виникає у зоні рубця, про що свідчить зникнення зубця R або поглиблення зубця Q. Реципрокні зміни з’являються у відведеннях III, aVF (інколи також у II), Dorsalis. Якщо при Q-ІМ передньої стінки ЛШ реципрокні зміни не реєструються, це може бути зумовлено лише великовогнищевим рубцевим кардіосклерозом задньої стінки ЛШ.
Поширений ІМ передньої стінки ЛШ прогностично несприятливий, часто ускладнюється серцевою недостатністю, життєво небезпечними шлуночковими аритміями, фібриляцією передсердь. Нерідко виникають стійкі порушення внутрішньошлуночкової провідності. АВ-блокади виникають рідко, але їхня поява при цій локалізації ІМ асоціюється з погіршенням прогнозу виживання хворих у чотири рази.
Задньодіафрагмальний ІМ
ІМ цієї локалізації зазвичай пов’язаний з оклюзією задньої низхідної артерії. Прямі ознаки реєструють у відведеннях III, aVF, II, Dorsalis за Небом (див. рис. 1) (Орлов, 2003). Діагностика нижнього ІМ ускладнюється тим, що в нормі у III відведенні часто реєструється непатологічний зубець q. Водночас при ІМ зубець q у III відведенні за своїми характеристиками не завжди відповідає патологічному. Зубець Q у відведенні III вважається патологічним, якщо за амплітудою він становить >25% зубця R, тривалістю ≥0,03 с або є розщепленим. Інколи в рубцевій стадії вогнищеві зміни задньої стінки ЛШ виявляються розщепленням, зазубреністю зубця R або шлуночковим комплексом rSr´ у III відведенні.
 Втім наявність вказаних змін лише в III відведенні не є значущою ознакою гострого ІМ. Водночас характерним є поєднання ознак: зниження амплітуди зубця R після патологічного зубця QIII, характерні зміни сегмента ST і зубця Т у цьому ж відведенні. Зміни ЕКГ у III відведенні обов’язково поєднуються з патологічним зубцем Q у відведеннях aVF і II. Велике значення має аналіз ЕКГ у динаміці спостереження разом з оцінкою клінічної симптоматики. Реципрокні зміни реєструються у відведеннях I, aVL, V1-V3, Anterior у вигляді зниження сегмента ST і високого позитивного («коронарного») зубця Т. Еволюція реципрокних змін відбувається швидше, ніж прямих ознак ІМ. Задньодіафрагмальний (нижній) ІМ нерідко ускладнюється АВ-блокадами проксимального типу.
Втім наявність вказаних змін лише в III відведенні не є значущою ознакою гострого ІМ. Водночас характерним є поєднання ознак: зниження амплітуди зубця R після патологічного зубця QIII, характерні зміни сегмента ST і зубця Т у цьому ж відведенні. Зміни ЕКГ у III відведенні обов’язково поєднуються з патологічним зубцем Q у відведеннях aVF і II. Велике значення має аналіз ЕКГ у динаміці спостереження разом з оцінкою клінічної симптоматики. Реципрокні зміни реєструються у відведеннях I, aVL, V1-V3, Anterior у вигляді зниження сегмента ST і високого позитивного («коронарного») зубця Т. Еволюція реципрокних змін відбувається швидше, ніж прямих ознак ІМ. Задньодіафрагмальний (нижній) ІМ нерідко ускладнюється АВ-блокадами проксимального типу.
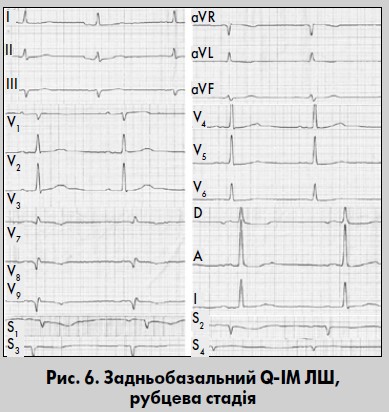
Задньобазальний ІМ
Це один із найскладніших для діагностики ІМ, оскільки прямих ознак ІМ у 12 загальноприйнятих відведеннях немає (рис. 6). Характерні для ІМ зміни ЕКГ можуть бути виявлені у відведеннях V7-V9, Dorsalis та S1-S4 (Орлов, 2003). У цих відведеннях реєструються патологічні зубці Q, спостерігається характерна динаміка кінцевої частини шлуночкового комплексу. Важливо зважати на реципрокні зміни у відведеннях V1-V3, V3R, Anterior. Це, зокрема, збільшення амплітуди та розширення зубців R, горизонтальна або дугою вниз депресія сегмента ST, високі гостровершинні зубці T. Комплекс QRS у відведеннях V1, V2, V3R може мати графіку R, RS, Rs, а тривалість зубця R становить ≥0,04 с. Реципрокні зміни можуть передувати появі прямих ознак ІМ. У відведеннях II, III, aVF прямих ознак гострого ІМ може не бути.
 У разі ІМ задньої стінки ЛШ нерідко з’являються порушення автоматизму синусового вузла, передсердні тахіаритмії та АВ-блокади різного ступеня. Загалом при задніх інфарктах АВ-блокади з’являються дещо частіше, ніж при передніх. Їхній перебіг є відносно більш сприятливим, але в деяких випадках виникає потреба в імплантації електрокардіостимулятора. Задньобазальний (задній) ІМ переважно зумовлений оклюзією правої задньої низхідної артерії (Байєс де Луна та співавт., 2009).
У разі ІМ задньої стінки ЛШ нерідко з’являються порушення автоматизму синусового вузла, передсердні тахіаритмії та АВ-блокади різного ступеня. Загалом при задніх інфарктах АВ-блокади з’являються дещо частіше, ніж при передніх. Їхній перебіг є відносно більш сприятливим, але в деяких випадках виникає потреба в імплантації електрокардіостимулятора. Задньобазальний (задній) ІМ переважно зумовлений оклюзією правої задньої низхідної артерії (Байєс де Луна та співавт., 2009).
Поширений ІМ задньої стінки ЛШ
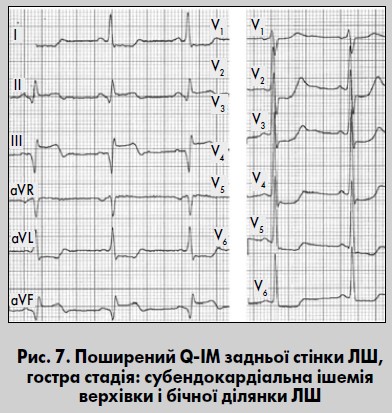
Цей тип поєднує ознаки ІМ нижньої та задньобазальної стінок ЛШ. Прямі ознаки гострого ІМ реєструються у відведеннях III, aVF, II, V7-V9, Dorsalis, S1-S4, реципрокні – у відведеннях I, aVL, V1-V3, V3R, Anterior (рис. 7). ІМ задньої стінки може поширюватися на задню частину міжшлуночкової перегородки. У цьому разі нерідко з’являються постійні чи минущі блокади ніжок пучка Гіса або порушення АВ-провідності. Поширений ІМ задньої стінки ЛШ переважно виникає внаслідок оклюзії проксимального сегмента ПВА або ОГ ЛВА при лівому типі кровопостачання серця.
Задньобічний ІМ
 Задньобічний ІМ зумовлений одночасним ураженням задньої та бічної стінок ЛШ. Такий ІМ зазвичай виникає при оклюзії ОГ ЛВА (Байєс де Луна та співавт., 2009). Прямі ознаки ІМ реєструються у відведеннях I, II, III, aVL, aVF, Dorsalis, Inferior, V5, V6, можливо V7-V9, реципрокні – у відведеннях V1-V3.
Задньобічний ІМ зумовлений одночасним ураженням задньої та бічної стінок ЛШ. Такий ІМ зазвичай виникає при оклюзії ОГ ЛВА (Байєс де Луна та співавт., 2009). Прямі ознаки ІМ реєструються у відведеннях I, II, III, aVL, aVF, Dorsalis, Inferior, V5, V6, можливо V7-V9, реципрокні – у відведеннях V1-V3.
Циркулярний ІМ
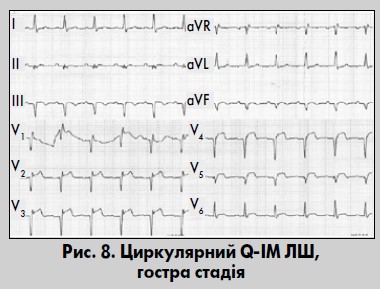
Циркулярний (верхівковий) ІМ переважно виникає при ураженні ОГ ЛВА або ПВА при правому типі коронарного кровообігу, коли ці судини постачають кров’ю бічну стінку ЛШ і верхівку (Байєс де Луна та співавт., 2009; Орлов, 2003). Некроз охоплює верхівку серця та прилеглі відділи передньої, бічної і задньої ділянок ЛШ. Прямі ознаки ІМ реєструються майже в усіх відведеннях, крім V1-V2 (рис. 8). Якщо циркулярний ІМ охоплює задньобазальні відділи ЛШ, то у відведеннях V1-V2 реєструються характерні реципрокні ознаки некрозу: високі зубці R і Т з одночасною депресією сегмента ST. Інший варіант ЕКГ-виявів циркулярного ІМ – поява прямих ознак ІМ у відведеннях V2-V4 (V5, V6), I, aVL, II, III, aVF, Anterior, Dorsalis, Inferior.
Передньозадній ІМ
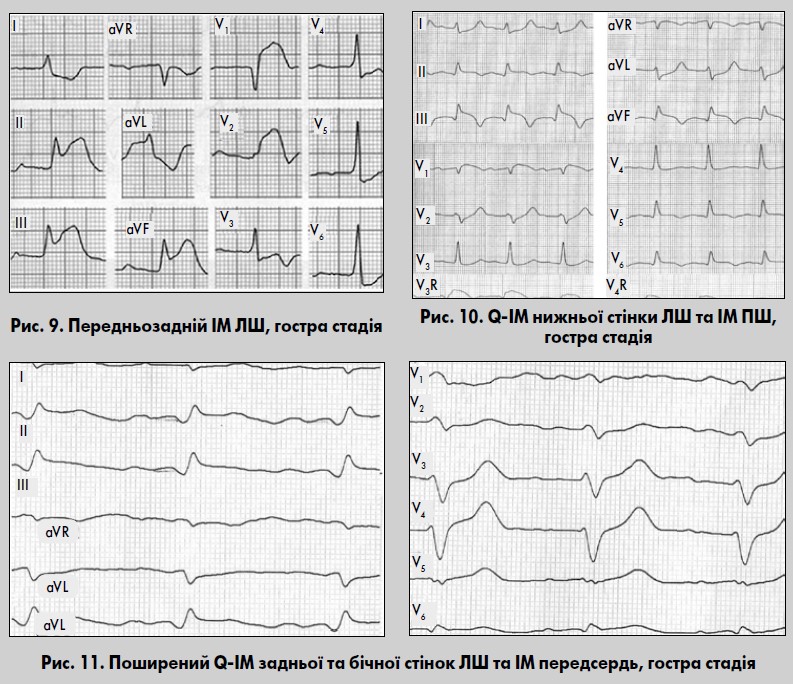
Передньозадній ІМ виникає при одночасному ураженні передньої та задньої частин міжшлуночкової перегородки і прилеглих до неї ділянок передньої та задньої стінок. Характерні прямі ознаки ІМ реєструються одночасно у відведеннях II, III, aVF, Dorsalis, іноді V7-V9 та у відведеннях V1-V4, Anterior або в деяких із них (рис. 9) (Сиркін, 1991; Орлов, 2003).
В осіб із хронічною ішемічною хворобою серця часто спостерігається багатосудинне стенозувальне ураження вінцевих артерій з розвитком колатерального кровообігу. В цьому разі при субтотальному стенозі однієї з вінцевих артерій постачання її зони частково забезпечується за рахунок колатералей з іншої артерії, оклюзія якої може призвести до розвитку циркулярного ІМ або навіть ІМ двох протилежних ділянок. Наприклад, якщо у хворого сформувався субтотальний стеноз ПВА, і кровопостачання відповідних ділянок міокарда забезпечувалося за рахунок колатералей з ПМШГ ЛВА, гострий її тромбоз може призвести до передньозаднього ІМ або поширеного циркулярного ІМ.
ІМ правого шлуночка
ІМ ПШ зазвичай поєднується з ІМ задньої стінки ЛШ. Переважно ураження міокарда поширюється на задню стінку ПШ, значно рідше – на бічну або навіть передню стінку. Клінічно ІМ ПШ виявляється ознаками виразної правошлуночкової серцевої недостатності (Сиркін, 1991; Орлов, 2003; Асоціація кардіологів України, 2013).
Поширення ІМ із ЛШ на ПШ погіршує прогноз виживання хворих. Ознаки ІМ ПШ у загальноприйнятих відведеннях ЕКГ практично не виявляються. Запідозрити його можливо, якщо на тлі ознак задньодіафрагмального або поширеного заднього ІМ у відведенні V1, рідше у V1-V2 реєструється елевація сегмента ST із випуклістю догори в поєднанні з негативними зубцями Т. Прямі ознаки ІМ ПШ (зникнення зубця R, поява зубців Q і підйом сегмента ST дугою догори) виявляють у відведеннях V3R-V6R (рис. 10).
Діагностичне значення має типова для інфаркту динаміка сегмента ST і зубця Т у цих відведеннях. Реципрокні зміни ІМ ПШ інколи реєструються у відведеннях V7-V9, якщо немає ушкодження задньобазальної стінки ЛШ. ІМ задньої стінки ЛШ із поширенням на ПШ переважно виникає внаслідок оклюзії проксимального сегмента ПВА. Ізольований ІМ ПШ трапляється рідко – у випадку оклюзії крайової гілки ПВА, або коли після перенесеного раніше нижнього ІМ виникла нова проксимальна оклюзія ПВА.
Інфаркт передсердь
Інфаркт передсердь ізольовано практично не трапляється. Ураження передсердь частіше діагностують при задньобазальному ІМ. Клінічно інфаркт передсердь виявляється появою різноманітних суправентрикулярних порушень ритму: фібриляції та тріпотіння передсердь, пароксизмальних тахікардій, суправентрикулярної екстрасистолії, синоаурикулярних блокад (Орлов, 2003). Значущою ознакою інфаркту передсердь є підйом сегмента PQ на ≥1,5 мм тривалістю 0,04‑0,08 с (рис. 11).
Інфаркт міокарда без зубця Q
Терміном «ІМ без зубця Q» (не-Q-ІМ, або дрібновогнищевий ІМ) об’єднують поняття інтрамурального і субендокардіального ІМ. Втім інколи обсяг ураження при дрібновогнищевому ІМ може бути не меншим, ніж при великовогнищевому.
Інтрамуральний ІМ
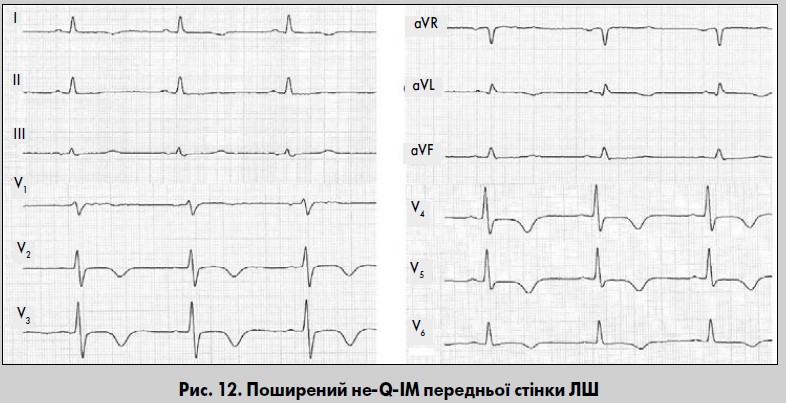
При інтрамуральному ІМ вогнище некрозу розташоване у товщі міокарда, не досягає ні ендокарда, ні епікарда. При такій локалізації ІМ не формується патологічний зубець Q, а над зоною некрозу реєструється зниженої амплітуди зубець R, який нерідко розщеплений. Сегмент ST інколи залишається на ізолінії з випуклістю дугою вверх, але частіше реєструється його типова для ІМ елевація, рідше – депресія. Крім того, з’являються глибокі, негативні, рівнобічні зубці Т. Зміни кінцевої частини шлуночкового комплексу реєструються у трьох і більше послідовних грудних відведеннях (рис. 12). «Коронарні» зубці Т в осіб з інтрамуральним ІМ зберігаються протягом кількох тижнів (Орлов, 2003).
Субендокардіальний ІМ
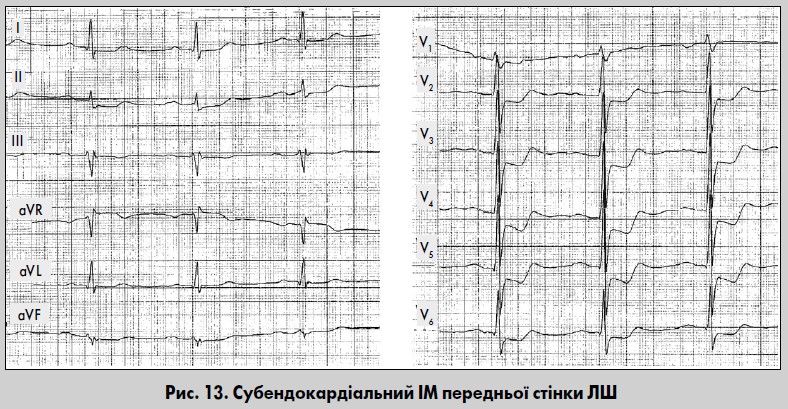
При субендокардіальному ІМ формується інфаркт тонкого шару міокарда, розташованого під ендокардом. Некроз може бути поширеним, але зубця Q зазвичай немає. В нормі збудження субендокардіальних відділів міокарда не впливає на формування комплексу QRS. Тому при локалізації некрозу в цій ділянці зубця Q немає, а зміни ЕКГ зумовлені появою субендокардіального пошкодження та ішемії навколо інфаркту. Найхарактерніша ознака субендокардіального ІМ – стійка горизонтальна або косонизхідна депресія сегмента ST у кількох суміжних відведеннях тривалістю не менш ніж 0,08 с (рис. 13). Зубець Т може бути негативним, зливатися зі зниженим сегментом ST, двофазним або позитивним. У відведеннях над зоною ІМ ймовірне зниження амплітуди зубця R.
Загалом ЕКГ-ознаки ІМ без зубця Q неспецифічні, й діагностика такого ІМ завжди здійснюється на підставі аналізу клінічних даних та результатів лабораторних тестів. За наявності больового синдрому без супутнього підйому сегмента ST на ЕКГ або у разі невизначеності ЕКГ-даних спочатку встановлюють діагноз гострого коронарного синдрому без підйому сегмента ST. Далі необхідно визначити біомаркери некрозу міокарда – тропонін Т або I. Якщо результат тропонінового тесту позитивний, діагностують ІМ без зубця Q (ESC/AHA/ACC/WHF, 2012; Асоціація кардіологів України, 2013). ІМ без зубця Q особливо часто спостерігається при повторних ІМ.
Інфаркт папілярних м’язів
Інфаркт папілярних м’язів не трапляється ізольовано, а може супроводжувати ІМ передньої або задньої стінки ЛШ. Ознаки інфаркту папілярних м’язів неспецифічні. До них належать стійка депресія сегмента ST, поява негативного зубця U у III, aVF і грудних відведеннях (Орлов, 2003). Більше діагностичне значення мають клінічні ознаки та дані ехокардіографії.
Повторний ІМ
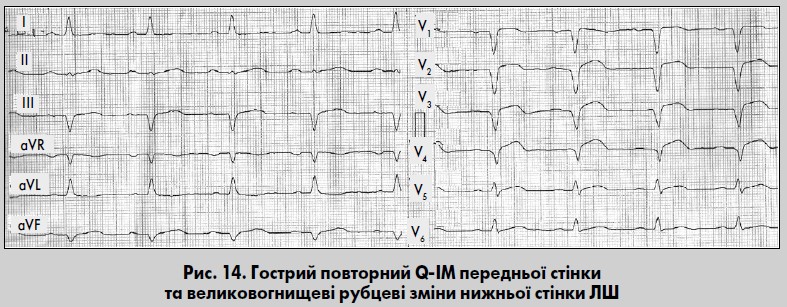
Діагностика повторних ІМ досить складна. Ознак повторного ІМ на ЕКГ може взагалі не бути. Корисним є порівняння ЕКГ, зареєстрованої після больового нападу, з попередніми. Повторний ІМ може виникати у різних відділах міокарда: поруч чи на відстані від рубця, на протилежній до нього стінці, в зоні рубця. Якщо свіжий ІМ формується поруч або на відстані від ділянки рубця (наприклад ІМ бічної стінки за наявності рубця у передньоперегородковій або передньо-перегородково-верхівковій ділянці), раніше перенесений ІМ не ускладнює діагностики повторного ІМ (рис. 14).
У ситуації, коли повторний ІМ виникає на протилежній до рубця стінці, ознаки рубцевих змін можуть нівелюватися внаслідок появи реципрокних змін у протилежних до зони ІМ відведеннях. Залежно від співвідношення розмірів старого рубця та гострого ІМ, нівелювання ознак може виявлятися у зменшенні або зникненні зубця Q, збільшенні амплітуди зубця R, трансформації негативного зубця Т у позитивний. Що більшими є розміри гострого ІМ, то більше нівелюються ознаки рубцевих змін. Реципрокні зміни у разі повторного ІМ можуть з’являтися раніше від прямих.
Отже, раптова позитивна динаміка у ділянці старого рубця може бути першою ознакою повторного ІМ. Незважаючи на виразність ЕКГ-ознак гострого повторного ІМ, вони можуть бути меншими за дійсні розміри за поширеністю і глибиною, виявлятися лише змінами кінцевої частини шлуночкового комплексу і спостерігатися в меншій кількості відведень. При невеликих розмірах гострий повторний ІМ може взагалі не відображатися на ЕКГ (Сиркін, 1991; Орлов, 2003).
Діагностика повторного ІМ у ділянці старого рубця ще важча. Гострий ІМ у зоні рубця призводить до збільшення ознак рубцевих змін у вигляді поглиблення зубця Q, зменшення амплітуди зубця R. Одночасно може спостерігатися підйом сегмента ST із характерною для гострого ІМ графікою та позитивізацією раніше негативного зубця Т. Повторний ІМ без зубця Q у ділянці рубця інколи виявляється лише надто швидкою позитивною динамікою зубця Т. «Позитивні» зміни сегмента ST і зубця Т можуть спостерігатися також при повторному ІМ із зубцем Q у зоні рубця в перші години хвороби.
Наголосимо, що за наявності рубцевих змін будь-яка динаміка ЕКГ після нападу болю може бути зумовлена погіршенням коронарного кровоплину. В усіх таких випадках встановленню діагнозу допомагає залучення клінічних та лабораторних даних (Асоціація кардіологів України, 2013).
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (71) 2020 р.