15 грудня, 2015
Атипичные проявления саркоидоза органов дыхания: клинические наблюдения
Атипичные изменения внутригрудных лимфатических узлов и паренхимы легких при компьютерной томографии (КТ) больных саркоидозом органов дыхания в большинстве случаев сочетаются с классическими высокоспецифичными симптомами, в связи с чем не создают особых трудностей для диагностики. Однако примерно в 2% случаев атипичные КТ-симптомы являются единственными проявлениями заболевания, что обусловливает необходимость применения дополнительных методов диагностики.
Частота бессимптомного течения саркоидоза органов дыхания составляет в среднем от 30% (II-III стадии) до 80% (I стадия) случаев. При этом клинические проявления саркоидоза (сухой кашель, одышка, общая слабость, повышение температуры тела) являются неспецифичными, в связи с чем их присутствие не позволяет не только диагностировать, но даже заподозрить наличие саркоидоза.
По этой причине международное положение Statement on Sarcoidosis, опубликованное в 1999 году [1], предусматривало обязательную верификацию диагноза с помощью патогистологических методов исследования. Однако за 16 лет, прошедших от момента опубликования Положения, диагностические возможности КТ органов грудной полости возросли настолько, что, по результату морфологической диагностики интерстициальных заболеваний легких, КТ в настоящее время успешно конкурирует с методами патогистологического исследования. В связи с этим в Унифицированном клиническом протоколе «Саркоидоз» (приказ МЗ Украины от 08.09.2014 № 634) [2] показания к проведению биопсии легкого с целью верификации диагноза значительно сужены – биопсия показана только при наличии весомых оснований для исключения лимфаденопатии или легочной диссеминации другого происхождения.
Необходимо отметить, что даже качественно выполненная рентгенография органов грудной полости позволяет уверенно диагностировать саркоидоз примерно в 80% случаев – именно с такой частотой у больных саркоидозом органов дыхания встречается двусторонняя прикорневая лимфаденопатия (ДПЛ) [1, 3]. Если учесть, что симметричная ДПЛ у больных с лимфомами наблюдается только в 3,8% случаев, при бронхогенной карциноме – в 0,8%, при злокачественных опухолях экстраторакальной локализации – в 0,2% [4], а дифференциальная диагностика с бронхоаденитом туберкулезной этиологии не представляет особых трудностей, то можно заключить, что рентгенологический симптомокомплекс ДПЛ является в высшей степени специфичным для саркоидоза.
Вместе с тем возможности рентгенографии в диагностике саркоидозного поражения паренхимы легких весьма ограниченны, в связи с чем все больные с подозрением на саркоидоз органов дыхания должны быть обследованы методом КТ высокого разрешения.
В таблице представлены современные критерии КТ-диагностики саркоидоза органов дыхания [5], которые подразделяются на классические и атипичные.
К классическим относятся симптомы, характерные для саркоидоза и редко наблюдаемые при других заболеваниях. Например, симптомокомплекс ДПЛ наблюдается у 80% больных саркоидозом и только у 4% пациентов с лимфомами. И наоборот, атипичные изменения чаще характерны для других заболеваний органов грудной полости и редко встречаются при саркоидозе.
Например, лимфаденопатия передних медиастинальных узлов характерна для лимфогранулематоза и редко встречается при саркоидозе.
Атипичные КТ-признаки в большинстве случаев сочетаются с классическими высокоспецифичными симптомами. Однако в редких случаях атипичные КТ-симптомы являются единственными проявлениями заболевания, что обусловливает значительные трудности в диагностике саркоидоза.
Клинический случай 1
Пациентка М., 1963 года рождения, направлена в Национальный институт фтизиатрии и пульмонологии (НИФП) им. Ф.Г. Яновского для уточнения диагноза.
Жалобы на умеренно выраженный сухой кашель, субфебрильную температуру тела, умеренную общую слабость и повышенную утомляемость.
Считает себя больной на протяжении трех месяцев. Начало заболевания малозаметное – появился незначительный сухой кашель, затем стала беспокоить общая слабость, повышенная утомляемость, через некоторое время появилась субфебрильная температура. Безуспешно самостоятельно лечилась антибиотиками и муколитическими средствами.
При рентгенографии была выявлена правосторонняя прикорневая лимфаденопатия, для уточнения диагноза больная была направлена в НИФП.
Хронических заболеваний органов дыхания в анамнезе нет. Не курит, работа с неблагоприятными производственными факторами не связана.
Кожа и периферические лимфатические узлы без изменений. Аускультативно: дыхание везикулярное, хрипов нет. Тоны сердца ритмичные, звучные. ЧСС – 84 уд/мин. АД – 130/80 мм рт. ст. Тоны сердца ритмичные, звучные. Живот мягкий, при пальпации безболезненный. Периферические отеки не определяются. Другие органы и системы – без видимой патологии.
Клинический анализ крови: Hb – 122 г/л, эритроциты – 4,1×1012/л, лейкоциты – 11,4×109/л, СОЭ – 61 мм/ч.
Уровень ионизированного кальция в крови: 1,37 ммоль/л – гиперкальциемия (норма до 1,32 ммоль/л).
Многосрезовая КТ (МСКТ) органов грудной полости: правосторонняя прикорневая лимфаденопатия (рис. 1 слева) в сочетании с увеличением бифуркационных и нижних паратрахеальных узлов справа; мелкоузелковая диссеминация преимущественно в средних и верхних легочных полях.
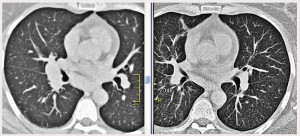 Рис. 1. МСКТ больной М., слева – до лечения: правосторонняя прикорневая лимфаденопатия, мелкоузелковая диссеминация легких; справа – после трехмесячной терапии метилпреднизолоном: регрессия лимфаденопатии, сохраняется необильная мелкоузелковая диссеминация.
Рис. 1. МСКТ больной М., слева – до лечения: правосторонняя прикорневая лимфаденопатия, мелкоузелковая диссеминация легких; справа – после трехмесячной терапии метилпреднизолоном: регрессия лимфаденопатии, сохраняется необильная мелкоузелковая диссеминация.Показатели легочной вентиляции в норме, снижение диффузионной способности легких (DLCO) – 66,6% от должного.
Учитывая то, что атипичное проявление саркоидоза (односторонняя прикорневая лимфаденопатия) сочеталось с гиперкальциемией и классическими КТ-изменениями (увеличение бифуркационных и нижних паратрахеальных узлов справа, микроузелковый паттерн легочной диссеминации), больной без применения дополнительных методов исследования был установлен диагноз: саркоидоз органов дыхания, впервые выявленный, II стадия. Назначена терапия метилпреднизолоном в дозе 0,4 мг/кг массы тела в течение 8 недель с последующим снижением дозы до 0,2 мг/кг к концу третьего месяца.
На втором визите через 3 мес лечения: субъективные проявления заболевания исчезли; СОЭ – 18 мм/ч; уровень кальция в крови – 1,28 ммоль/л; DLCO – 74,5% от должного.
МСКТ: отмечается регрессия прикорневой лимфаденопатии (рис. 1 справа), уменьшение бифуркационных и нижних паратрахеальных узлов справа, сохраняется необильная мелкоузелковая диссеминация.
Диагноз: саркоидоз органов дыхания, II стадия, фаза регрессии.
Пациентке рекомендовано продолжение лечения метилпреднизолоном в режиме постепенного снижения дозы до 0,1 мг/кг к третьему визиту (конец 6-го месяца).
Клинический случай 2
Пациент П., 1993 года рождения, направлен в НИФП для уточнения диагноза после проведения профилактического рентгенологического исследования, на котором были выявлены патологические изменения легких и внутригрудных лимфатических узлов.
Жалоб нет. В анамнезе острые респираторные вирусные инфекции, хронических заболеваний внутренних органов не отмечает. Не курит, в контакте с неблагоприятными производственными факторами не работал.
При объективном обследовании: кожа обычной окраски, без высыпаний, периферические лимфатические узлы не увеличены. Аускультативно: дыхание везикулярное, хрипов нет. ЧСС – 64 уд/мин, АД – 110/70 мм рт. ст. Тоны сердца ритмичные, звучные. Другие органы и системы без видимой патологии.
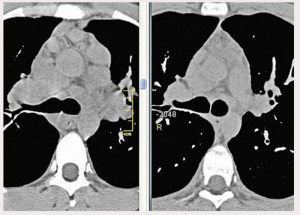 Рис. 2. МСКТ больного П. (мягкотканный режим), слева – первичное обследование: значительное увеличение передних медиастинальных лимфатических узлов, расположенных преимущественно вокруг восходящего отдела аорты; справа – после трехмесячного периода наблюдения: регрессия лимфаденопатии.
Рис. 2. МСКТ больного П. (мягкотканный режим), слева – первичное обследование: значительное увеличение передних медиастинальных лимфатических узлов, расположенных преимущественно вокруг восходящего отдела аорты; справа – после трехмесячного периода наблюдения: регрессия лимфаденопатии.МСКТ: значительное увеличение передних медиастинальных (рис. 2, слева) и бронхопульмональных (рис. 3, слева) лимфатических узлов. Билатерально в легких определяется мелкоузелковая диссеминация преимущественно в верхних и средних отделах с распределением узелков вдоль бронхо-сосудистых пучков.
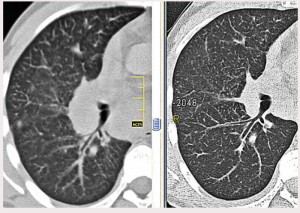 Рис. 3. МСКТ больного П., слева – первичное обследование: мелкоузелковая диссеминация паренхимы легких, увеличение прикорневых лимфатических узлов; справа – после трехмесячного периода наблюдения: регрессия лимфаденопатии, сохраняется мелкоузелковая диссеминация.
Рис. 3. МСКТ больного П., слева – первичное обследование: мелкоузелковая диссеминация паренхимы легких, увеличение прикорневых лимфатических узлов; справа – после трехмесячного периода наблюдения: регрессия лимфаденопатии, сохраняется мелкоузелковая диссеминация.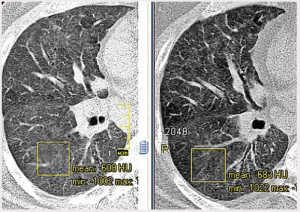 Рис. 4. МСКТ больного К., слева – первичное обследование: диффузное снижение прозрачности паренхимы легких по типу «матового стекла», плотность паренхимы: –609 HU; увеличение прикорневых лимфатических узлов; справа – через 12 мес лечения: повышение прозрачности паренхимы, плотность паренхимы: –683 HU; регрессия лимфаденопатии.
Рис. 4. МСКТ больного К., слева – первичное обследование: диффузное снижение прозрачности паренхимы легких по типу «матового стекла», плотность паренхимы: –609 HU; увеличение прикорневых лимфатических узлов; справа – через 12 мес лечения: повышение прозрачности паренхимы, плотность паренхимы: –683 HU; регрессия лимфаденопатии.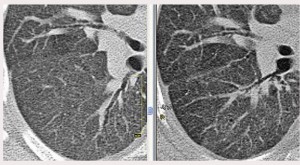 Рис. 5. МСКТ больного К. (фрагмент среза правого легкого в режиме увеличения), слева – первичное обследование: интенсивное диффузное снижение прозрачности паренхимы легких по типу «матового стекла»; справа – через 12 мес лечения: повышение прозрачности паренхимы, на срезе более отчетливо дифференцируется легочный рисунок.
Рис. 5. МСКТ больного К. (фрагмент среза правого легкого в режиме увеличения), слева – первичное обследование: интенсивное диффузное снижение прозрачности паренхимы легких по типу «матового стекла»; справа – через 12 мес лечения: повышение прозрачности паренхимы, на срезе более отчетливо дифференцируется легочный рисунок.При бодиплетизмографии отмечено незначительное уменьшение общей емкости и остаточного объема легких, показатели кривой форсированного выдоха в пределах нормы. DLCO – 72,7%.
Содержание кальция в крови – 1,31 ммоль/л.
В данном случае атипичное проявление (увеличение передних медиастинальных лимфатических узлов) также сочеталось с высокоспецифичными КТ-признаками саркоидоза (ДПЛ, микроузелковый паттерн диссеминации с распределением узелков вдоль бронхо-сосудистых пучков). Кроме того, отсутствовали клинические проявления лимфопролиферативного заболевания. В связи с этим больному без проведения дополнительных методов исследования был установлен диагноз: саркоидоз органов дыхания, впервые выявленный, II стадия.
Учитывая отсутствие клинических проявлений, изменений функции дыхания, нормальный уровень кальция в крови, лечение не назначалось, больному было рекомендовано контрольное обследование через 3 месяца.
При повторном обследовании на МСКТ органов грудной полости констатирована регрессия медиастинальной (рис. 2 справа) и прикорневой (рис. 3 справа) лимфаденопатии, при этом сохранялась мелкоузелковая диссеминация паренхимы. В соответствии с клиническим протоколом противовоспалительная терапия не назначалась, больному было рекомендовано очередное обследование через 3 месяца.
Клинический случай 3
Пациент К., 1977 года рождения, поступил в отделение интерстициальных заболеваний легких НИФП с жалобами на одышку при незначительной физической нагрузке (ходьбе по ровной местности), сухой кашель, выраженную общую слабость, повышенную утомляемость.
Заболевание началось три года назад без очевидных причин с малозаметной одышки, которая медленно прогрессировала. Периодически отмечался сухой кашель. На протяжении последних двух месяцев одышка значительно усилилась, появилась выраженная общая слабость, в связи с чем впервые обратился к врачу.
В анамнезе частые ОРВИ, трижды болел пневмонией. Не курит. Работал водителем дальних рейсов, строителем.
Объективно: одышки в покое и при разговоре нет. Частота дыхания – 22 в 1 мин. При аускультации дыхание с жестким оттенком, над базальными отделами билатерально – крепитирующие хрипы. ЧСС – 104 уд/мин, АД – 130/90 мм рт. ст. Тоны сердца ритмичны, приглушены. Другие органы и системы при физикальном обследовании без изменений.
СОЭ – 15 мм/ч, содержание кальция в крови в пределах нормы (1,29 ммоль/л).
МСКТ (рис. 4 слева): диффузное снижение прозрачности паренхимы легких по типу «матового стекла», небольшое увеличение бронхопульмональных лимфатических узлов с обеих сторон.
Функция внешнего дыхания: значительное уменьшение общей (44,7%) и жизненной (31,6%) емкости легких, резкое снижение диффузионной способности легких (DLCO – 22,6%).
Газовый состав крови: выраженная гипоксемия (РаО2 – 44 мм рт. ст., SaO2 – 82%).
Анализ результатов обследования не позволил уверенно предположить характер заболевания, при этом диагноз саркоидоза представлялся маловероятным по следующим причинам.
Симптом «матового стекла» без наличия мелкоузелковой диссеминации относится к перечню атипичных КТ-признаков саркоидоза и является не следствием альвеолита, а результатом атипичного диффузного распределения гранулем в интерстиции. Однако при саркоидозе феномен «матового стекла» обычно представлен отдельными изолированными участками, а в нашем случае наблюдалось диффузное снижение прозрачности паренхимы, что при саркоидозе встречается крайне редко.
Двустороннее небольшое увеличение бронхопульмональных лимфатических узлов также имело сомнительную диагностическую ценность, поскольку при саркоидозе прикорневая лимфаденопатия обычно выражена в значительно большей степени.
Кроме того, клинические и функциональные симптомы тяжелой респираторной недостаточности несовместимы с диагнозом саркоидоза II стадии, они характерны для IV стадии заболевания – распространенного пневмосклероза.
Наиболее вероятным был диагноз: гиперсенситивный пневмонит неустановленной природы, хроническая форма. При этом заболевании КТ-признаки диффузного снижения прозрачности паренхимы в виде «матового стекла» в сочетании с умеренной и тяжелой респираторной недостаточностью наблюдаются достаточно часто.
Вместе с тем диагноз требовал верификации. С этой целью пациенту была проведена видеоторакоскопия с биопсией паренхимы легких и внутригрудного лимфатического узла. При патогистологическом исследовании выявлены эпителиоидноклеточные гранулемы, характерные для саркоидоза.
Таким образом, больному был установлен диагноз: саркоидоз органов дыхания, впервые выявленный, II стадия, легочная недостаточность II степени.
Больному был назначен метилпреднизолон по 24 мг/сут на протяжении 4 нед с последующим снижением дозы по схеме до 12 мг к концу 3-го месяца. Однако пациент самостоятельно снизил дозу до 2 мг/сут. При обследовании на визите 2 через 3 мес клиническая картина заболевания и КТ-семиотика сохранялись на прежнем уровне, в связи с чем доза метилпреднизолона была увеличена до 16 мг/сут на протяжении 4 нед с постепенным ее снижением до 8 мг/сут к концу 6-го месяца. Однако и на третьем визите (6 мес) улучшения клинического состояния больного и признаков регрессии изменений в легких при КТ-исследовании не наблюдалось. Дополнительно к лечению метилпреднизолоном (8 мг/сут) назначен гидроксихинолин по 200 мг 2 раза в сутки.
На визите 4 (12 мес) выявлены признаки регрессии саркоидоза – уменьшение бронхопульмональных лимфатических узлов и повышение прозрачности паренхимы (рис. 4 справа), при этом на фоне «матового стекла» стали отчетливо дифференцироваться бронхо-сосудистые структуры (рис. 5 справа). При исследовании функции внешнего дыхания отмечено увеличение жизненной емкости легких (35,6%), вместе с тем диффузионная способность сохранялась на крайне низком уровне (21,8%).
Результаты газового состава крови свидетельствовали о существенном уменьшении степени артериальной гипоксемии (РаО2 – 57 мм рт. ст., SaO2 – 89%).
Вместе с тем темпы регрессии патологического процесса были явно недостаточны – сохранялось значительное снижение прозрачности паренхимы легких, были крайне низкими показатели легочной вентиляции и диффузии. В связи с этим больному была назначена иммуносупрессивная терапия метотрексатом по 10 мг/нед в комбинации с фолиевой кислотой на фоне лечения метилпреднизолоном, рекомендовано наблюдение пульмонологом по месту жительства с целью мониторинга возможных побочных эффектов терапии и контрольное обследование в НИФП через 3 месяца.
Заключение
По нашим данным, атипичные проявления саркоидоза при КТ органов грудной полости в группе больных с поражением паренхимы наблюдаются с частотой от 0,7% (односторонняя прикорневая лимфаденопатия) до 36,5% (сluster-симптом – скопление микроузелков в виде куста или грозди). При этом классические высокоспецифичные симптомы регистрируются значительно чаще – от 67,1% (перилимфатическое распределение узелков) до 91,1% (ДПЛ). В связи с этим атипичные признаки, как правило, сочетаются с классическими (случаи 1 и 2) и не создают особых трудностей для диагностики. Однако примерно в 2% случаев атипичные КТ-симптомы являются единственными проявлениями заболевания, что иллюстрирует случай 3. Это обусловливает необходимость применения методов трансбронхиальной или хирургической биопсии.
Литература
1. American Thoracic Society (ATS), European Respiratory Society (ERS), World Association of Sarcoidosis and Other Granulomatous Disoders (WASOG). Statement on Sarcoidosis // Am. J. Respir. Crit. Care Med. – 1999. – Vol. 160. – P. 736-755.
2. Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) та третинної (високоспеціалізованої) медичної допомоги «Саркоїдоз» // Наказ МОЗ України № 634 від 08.09.2014.
3. Nunes H. Imaging of sarcoidosis of the airways and lung parenchyma and correlation with lung function / H. Nunes, Yu. Uzunhan, T. Gille et al. // Eur. Respir. J. – 2012. – Vol. 40. – P. 750-765.
4. Winterbauer R.H. Clinical interpretation of bilateral hilar adenopathy / R.H. Winterbauer, N. Belik, K.D. Moores // Ann. Intern. Med. – 1973. – Vol. 78. – P. 65-71.
5. Veltkamp M. The pulmonary manifestations of sarcoidosis / M. Veltkamp, J.C. Grutters // Pulmonary sarcoidosis. M.A. Judson Editor. – Humana Press – brand of Springer, 2014. – P. 19-40.



