8 липня, 2015
Ультразвуковая бронхоскопия в пульмонологии. Первый опыт применения эндобронхиальной ультразвуковой трансбронхиальной аспирационной биопсии внутригрудных лимфоузлов (EBUS-TBNA)
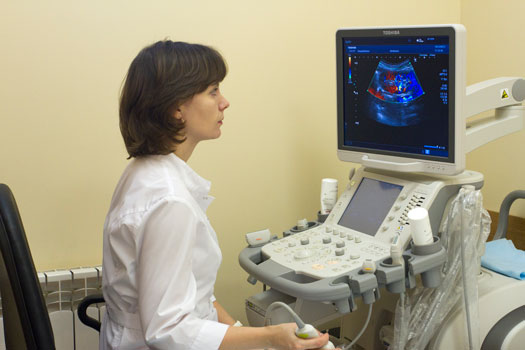
Бронхология является важной и неотъемлемой частью пульмонологии, в которой прогрессивные технологии произвели революцию наиболее очевидно и ярко.
Начало бронхологии связывают с именем австрийского врача Gustav Killian, который в 1897 г. впервые через жесткий бронхоскоп под местной анестезией кокаином произвел удаление инородного тела. После того прошло около 100 лет, прежде чем бронхология получила следующий импульс к развитию, и связано это было с совершенствованием анестезиологии и изобретением первого жесткого дыхательного бронхоскопа (Friedel, 1956), который позволял осуществлять бронхоскопию под внутривенным наркозом. Уже через 10 лет был изобретен первый гибкий бронхоскоп с фиброволоконной оптикой (Shigeto Ikeda, 1966), и бронхофиброскопии начали проводить под местной анестезией, что дало возможность широкого применения бронхоскопии.
С этого времени началось активное развитие бронхологии: в 1980 г. (Ijean F. Dumon) впервые применен Nd:YAG лазер через бронхофиброскоп; в 1987 г. (Asahi Pentax Corp.) разработан первый видеобронхоскоп.
Однако, учитывая то, что во время бронхоскопии обзор бронхолога ограничен просветом и внутренней поверхностью трахеи и бронхов, возникла необходимость в разработке новых диагностических методов. В 2000 г. в связи с развитием и широким применением новых технологий было сформулировано понятие «интервенционная бронхоскопия» – диагностическая и терапевтическая бронхоскопия, которая осуществляется с помощью жесткого бронхоскопа, фибробронхоскопа или в комбинации и включает все виды диагностики и лечения бронхов и легких с применением специализированной современной аппаратуры, которая позволяет вмешиваться в ранее недоступные зоны и области бронхов, легких и средостения и находится в стороне от простой бронхоскопии [1].
Фирма Olympus (Япония) с 1980 г. начала разрабатывать ультразвуковую эндоскопическую аппаратуру. В 1990 г. впервые был применен трансбронхиальный миниатюрный ультразвуковой зонд диаметром 2,5 мм и с частотой 12/20 МГц (UN-2R/3R) для диагностики периферических образований в легких [2-4].
Первый ультразвуковой бронхоскоп был выпущен в 2004 г. Система для проведения EBUS-TBNA включала ультразвуковой бронхоскоп с ультразвуковым датчиком на дистальном конце, специальную иглу для проведения аспирационной биопсии и ультразвуковой процессор [5].
EBUS позволяет определить состояние бронхиальной стенки и структур средостения на глубину до 4 см. В отличие от Ro-лучей, где изображение зависит от разности поглощения рентгеновских лучей водой и воздухом, ультразвуковое изображение зависит от различного поглощения, рассеивания и отражения ультразвуковых волн тканями различной плотности.
EBUS-TBNA позволяет получать материал для цитологического и гистологического исследований из лимфоузлов средостения при лимфаденопатии средостения.
По данным литературы, чувствительность EBUS-TBNA при лимфаденопатии средостения составляет 94,6-100%, специфичность – 100%, диагностическая ценность метода – 96,3-99,1%. Современные мировые клиники широко используют эту методику для диагностики лимфаденопатии средостения.
Цель исследования: изучить возможности EBUS-TBNA при лимфаденопатии средостения.
Материалы и методы
На протяжении 2012-2014 гг. на базе эндоскопического отделения было выполнено 75 EBUS-TBNA внутригрудных лимфатических узлов (ВГЛУ): мужчин – 43 (57,3%), женщин – 32 (42,7%) (табл. 1).
Все EBUS-TBNA проводились под седацией 1% раствором пропофола с применением местной анестезии 2-4% раствора лидокаина.
Для проведения исследований использовались видеобронхоскоп EVIS EXERA BF-UC-160F OL8 (Olympus, Япония), ультразвуковой центр EUS EXERA EU-C60, иглы аспирационные NA-201SX-4022. На первом этапе всем больным осуществлялась бронхофиброскопия с помощью видеобронхоскопов EVIS EXERA BF-1T180, BF-Q180, BF-P180, BF-XT160 для определения состояния слизистой оболочки бронхов, наличия патологического секрета, санации бронхов для подготовки к биопсии. Затем трансорально через загубник вводился ультразвуковой бронхоскоп.
Для определения топографии групп пораженных лимфоузлов нами использовалась классификация лимфатических коллекторов грудной клетки, которая была предложена T. Naruke [6].
Как правило, при EBUS-TBNA осуществлялась биопсия 2, 4, 7, 10 и 11-го коллекторов лимфатических узлов. Наиболее безопасными являются лимфатические узлы 7-го коллектора из-за отсутствия магистральных сосудов. Хотя для проведения EBUS-TBNA это не так важно, так как аспирационная биопсия всегда выполняется под контролем ультрасонографии.
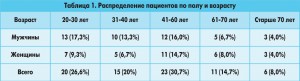
Схема выполнения EBUS-TBNA изображена на рисунке 1.
Ультразвуковой датчик устанавливается напротив лимфоузла. Устанавливается ход иголки для забора материала 1,5-2,0 см. Выводится максимальный размер лимфоузла, вводится аспирационно-биопсийная игла и осуществляется прокол стенки трахебронхиального дерева с введением иглы в лимфоузел, производится до 25-30 движений для нарезания столбика ткани лимфатического узла. Аспирация материала осуществляется за счет вакуума, который искусственно создается на конце иглы специальным шприцем. Материал направляется на цитологическое и гистологическое исследование.
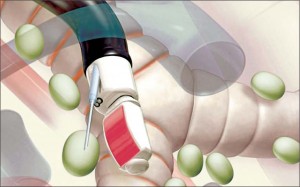
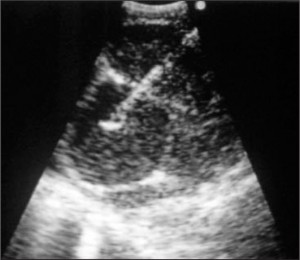
На рисунке 2 показан момент нахождения иглы в лимфатическом узле при заборе биопсийного материала. Игла проходит через 2 лимфатических узла, на ультрасонографии четко видны границы оболочки.
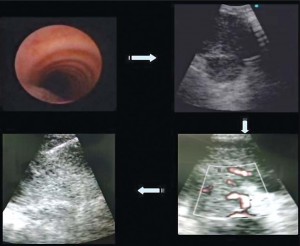
На рисунке 3 показан алгоритм исследования:
• выполнение бронхофиброскопии для определения состояния слизистой оболочки бронхов, наличия патологического секрета, санации бронхов для подготовки к биопсии;
• определение номера коллектора, из которого будет выполнена биопсия, и выведение лимфатического узла в наибольшем его размере;
• определение непосредственного места пункции с учетом расположения сосудов в паралимфатическом пространстве и лимфатическом узле.
Результаты
Из 75 больных, которым была проведена EBUS-TBNA, диагноз верифицирован у 66 (88%) человек. У 9 (12%) пациентов полученный биопсийный материал был неинформативен. Во всех 75 (100%) случаях материал пункционной биопсии был отправлен на цитологическое исследование. На гистологическое исследование был отправлен материал только 35 (46,7%) больных. Это было связано с необходимостью отработки во времени гистологического метода исследования материала пункционной биопсии.
Результаты представлены в таблицах 2 и 3.
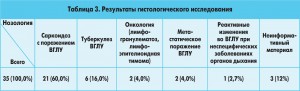
Таким образом, цитологическое исследование позволило верифицировать диагноз у 66 (88%) больных. Из них гранулематозный процесс был установлен у 57 (76%) пациентов, онкологические заболевания – у 3 (4%), метастазы лимфоузлов – у 2 (2,7%), реактивные изменения в лимфоузлах – у 4 (5,3%) больных.
По данным гистологического исследования, удалось дифференцировать гранулематозный процесс, установленный цитологическим исследованием. Из 27 пациентов с установленным цитологически гранулематозным процессом с помощью гистологического исследования был поставлен диагноз саркоидоза в 21 (60%) случае, туберкулеза – в 6 (16%) случаях.
Выводы
1. EBUS-TBNA ВГЛУ является методом выбора у больных с лимфаденопатией средостения.
2. EBUS-TBNA является малоинвазивным, наименее травматичным и наиболее безопасным методом диагностики лимфаденопатии средостения, так как биопсия проводится под контролем ультразвукового датчика, что позволяет четко определить место взятия материала, контролировать глубину прохождения биопсийной иглы и избежать повреждения магистральных сосудов, которые расположены в непосредственной близости к исследуемым лимфатическим узлам.
3. Биопсийный материал, полученный при EBUS-TBNA, можно исследовать как цитологическим, так и гистологическим методами.
4. Гистологическое исследование EBUS-TBNA является предпочтительным по отношению к цитологическому методу, так как позволяет дифференцировать гранулематозные процессы.
5. Наибольшее количество пациентов приходится на трудоспособный возраст (от 20 до 60 лет, 77,3%), что свидетельствует об актуальности своевременной диагностики патологии ВГЛУ.
Литература
1. Bolliger C.T., Mathur P.N. Interventional Bronchoscopy. – Vol. 30. – 2000.
2. Hurther T.H., Hanrath P. Endobronchiale. Songraphie zur Diagnostik pulmonaler und mediastinaler Tumoren. Dtsch Med Wochenschr. – 1990. – 115: 1899-1905.
3. Becker H.D. Endobronchialer Ultraschall – Eineneue Perspektive in der Bronchologie. – Ultraschall Med. – 1996. – 17: 106-112.
4. Kurimoto N., Murayama M., Yoshioka S., Nishisaka T., Inai K., Dohi K. Assessment of usefulness of endobronchial ultrasonography in determination of depth of tracheobronchial tumor invasion. – Chest. – 1999. – 115: 1500-1506.
5. Bolliger C.T., Herth F.J.F., Mayo P.H., Miyazawa T., Beamis J.F. Clinical Chest Ultrasound. From the ICU to the Bronchoscopy Suit. – Vol. 37. – 2009.
6. Lymph Node Map. T. Naruke. Картирование лимфоузлов при раке легкого. Вестник РОНЦ им. Н.Н. Блохина РАМН. – 2004. – Вып. № 4. – Т. 15.