25 лютого, 2021
Пацієнт молодого віку з COVID-19: у фокусі – серцево-судинні ускладнення та реабілітація
 Коронавірусна хвороба (COVID‑19) і постковідний синдром (Long COVID) – проблема, з якою сьогодні прямо чи опосередковано вже стикався практично кожен представник медичної спільноти. Крім варіабельності клінічної картини патології, обмеженого арсеналу лікарських засобів і нормативних документів, роботу лікарів ускладнює низька доступність діагностичних тестів, особливо для осіб, які мешкають у сільській місцевості. Тому в рамках цієї публікації пропоную проаналізувати сучасні можливості в лікуванні та відновленні після COVID‑19 на прикладі типової клінічної ситуації, а також акцентувати увагу колег на важливих практичних нюансах.
Коронавірусна хвороба (COVID‑19) і постковідний синдром (Long COVID) – проблема, з якою сьогодні прямо чи опосередковано вже стикався практично кожен представник медичної спільноти. Крім варіабельності клінічної картини патології, обмеженого арсеналу лікарських засобів і нормативних документів, роботу лікарів ускладнює низька доступність діагностичних тестів, особливо для осіб, які мешкають у сільській місцевості. Тому в рамках цієї публікації пропоную проаналізувати сучасні можливості в лікуванні та відновленні після COVID‑19 на прикладі типової клінічної ситуації, а також акцентувати увагу колег на важливих практичних нюансах.
Слід зазначити, що сьогодні в медичній пресі дискутується питання щодо терміна «постковідний синдром». У Великій Британії група лікарів, які об’єдналися в спільноту Long COVID Group, виступає категорично проти цього терміна, пропонуючи Всесвітній організації охорони здоров’я (ВООЗ) замість нього запровадити поняття Long COVID. Вони піддають серйозній критиці «Настанови щодо стійкого впливу COVID‑19 (тривалий COVID) на пацієнтів», розроблені Національним інститутом охорони здоров’я та підвищення кваліфікації (NICE), Шотландською міжвишівською мережею рекомендацій (SIGN) і Королівським коледжем лікарів загальної практики (RCGP), котрі було опубліковано 18 грудня 2020 р. Ця група лікарів наполягає на тому, що точна оцінка, діагностика, лікування та реабілітація особливо важливі з урахуванням зростання кількості свідоцтв патології й ураження органів у постковідних хворих. Тому питання, як називатиметься цей клінічний стан, залишається відкритим, але це не зменшує негативні прояви останнього.
Крім того, досить складно визначити саме типову клінічну картину COVID‑19. Зазвичай спостерігаються численні порушення з боку різних органів і систем:
- лихоманка, кашель, які призводять до задишки, втоми, біль у горлі;
- втрата смаку та нюху, головний і м’язовий біль;
- висипання на шкірі, припухлість і гіперемія, подібні до вірусної екзантеми;
- сплутаність/втрата свідомості, судоми, синдром Гійєна-Барре;
- гастроінтестинальні симптоми (діарея, біль у животі, нудота, блювання);
- кон’юнктивіт;
- нежить;
- менінгіт;
- тромбози, «ковідні пальці», інсульти.
Коморбідні стани, котрі погіршують перебіг COVID‑19 (ESC/ACC/AHA/CDC, 2020):
- хронічне захворювання легень;
- серцева недостатність – СН (III-IV функціонального класу за NYHA);
- потреба в проведенні кардіохірургічного втручання;
- імунодефіцит і необхідність трансплантації;
- артеріальна гіпертензія (АГ);
- ішемічна хвороба серця;
- цереброваскулярна патологія;
- цукровий діабет (ЦД);
- виражене ожиріння (індекс маси тіла >40 кг/м2).
Коморбідність не тільки пов’язана з тяжчим перебігом COVID‑19, а й істотно погіршує прогноз. Рівень смертності серед пацієнтів із COVID‑19, які мають онкопатологію, – 5,6%, АГ – 6%, хронічне захворювання легень – 6,3%, ЦД – 7,3%, серцево-судинні захворювання (ССЗ) – 10,5%.
COVID‑19 і серцево-судинні ускладнення в пацієнтів молодого віку: основні механізми та клінічні перспективи
У рекомендаціях Європейського товариства кардіологів (ESC, 2020) схематично представлено (рис.) механізм дії вірусу SARS-CoV‑2, що спричиняє COVID‑19, на різні органи та системи: легені (внаслідок чого виникає коронавірусна пневмонія), ураження ендотелію (зокрема, судин мікроциркуляторного русла, що призводить до мікроваскулярної дисфункції, зростання ймовірності гострого коронарного синдрому – ГКС).
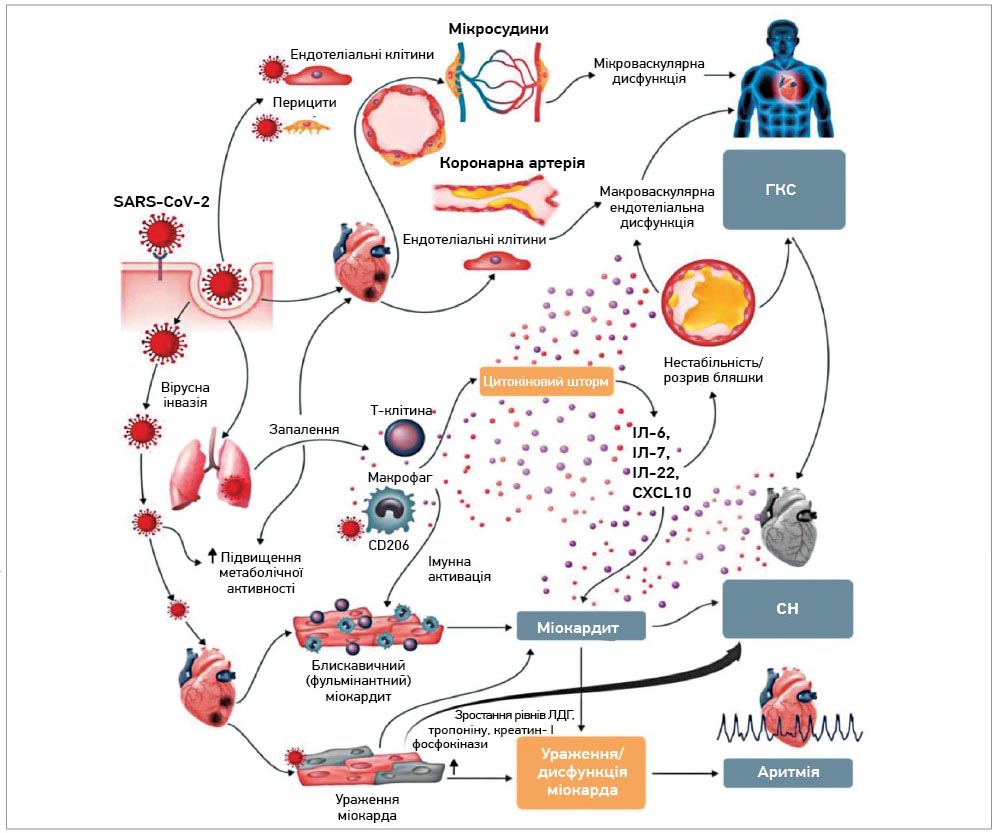 Рис. Кардіоваскулярні порушення при COVID-19: потенційні механізми розвитку (ЕSC, 2020)
Рис. Кардіоваскулярні порушення при COVID-19: потенційні механізми розвитку (ЕSC, 2020)
Примітки: ІЛ – інтерлейкін; ЛДГ – лактатдегідрогеназа.
При ураженні міокарда вірусом SARS-CoV‑2 підвищуються рівні кардіомаркерів – тропоніну I, ЛДГ, розвиваються аритмії, міокардит, СН, асоційовані з COVID‑19. Цитокіновий шторм, який виникає через дисбаланс активації Т‑клітин із порушенням регуляції вивільнення ІЛ‑6, ІЛ‑7 та інших цитокінів, може спричиняти ССЗ під час COVID‑19. Активація імунної системи в поєднанні з імунометаболічними порушеннями здатні спровокувати нестабільність бляшок і ГКС (насамперед в осіб молодого віку).
Доведено, що для потрапляння в клітину шипоподібний S‑білок вірусу SARS-CoV‑2 зв’язується з рецепторами ангіотензинперетворювального ферменту‑2 (АПФ‑2) на поверхні клітини хазяїна. Високим рівнем експресії AПФ‑2, що є основним компонентом ренін-ангіотензин-альдостеронової системи (РААС), задіяної в патофізіології кардіоваскулярних захворювань, відрізняються легені, серце, судини, нирки, шлунково-кишковий тракт.
ССЗ, асоційовані з COVID‑19, імовірно, спричинені порушенням регуляції РААС/AПФ‑2 через інфікування SARS-CoV‑2 й супутню патологію, наприклад АГ. ССЗ у разі COVID‑19 можуть бути як первинними, так і вторинними відносно гострого ураження легень, що призводить до збільшення навантаження на серце та є потенційно небезпечним для хворих із наявною СН.
! Усіх пацієнтів із проявами гострої респіраторної вірусної інфекції (ГРВІ) варто сприймати як потенційних хворих на COVID‑19.
COVID‑19: щоденник молодого пацієнта
На щастя, в більшості пацієнтів молодого віку COVID‑19 має легкий або середньотяжкий перебіг. Пропоную розглянути типовий клінічний випадок і тактику ведення такої категорії хворих.
Клінічний випадок
Пацієнт Р. 41 року звернувся до сімейного лікаря зі скаргами на головний біль, підвищення температури тіла до 37,6 °C, слабкість, пирхоту в горлі, нежить, неприємні відчуття в ділянці серця та перебої в його роботі.
Об’єктивно: шкірні покриви вологі, температура тіла – 37,2 °C, збільшення мигдаликів, гіперемія дужок зіва, артеріальний тиск (АТ) – 160 мм рт. ст., тони серця звучні, аритмічні (поодинока екстрасистолія), частота серцевих скорочень (ЧСС) – 84/хв. У легенях – везикулярне дихання, хрипи відсутні. Живіт без особливостей, симптом поколочування негативний, набряків немає.
Анамнез: погіршення самопочуття відчув уранці; виникла слабкість, яка поступово посилювалася, під час робочого дня з’явилася пирхота в горлі, підвищилася температура. Покинувши робоче місце, прибув на консультацію до лікаря. Підтверджених контактів із хворими на COVID‑19 не було, проте ймовірність інфікування висока, оскільки пацієнт щоденно користується громадським транспортом.
Сімейний анамнез: обтяжений щодо АГ із боку матері. Стосовно підвищення АТ раніше не обстежувався.
Попередній діагноз: ГРВІ.
Тактика: відкрито лікарняний лист, призначені ПЛР‑тест на COVID‑19, електрокардіографія (ЕКГ), моніторинг АТ у домашніх умовах.
Результати додаткових обстежень. На ЕКГ: ритм синусовий, нерегулярний, ЧСС – 86/хв, нормальне положення електричної осі серця, проте реєструвалися поодинокі шлуночкові екстрасистоли.
Рекомендації: напівліжковий режим; повноцінне харчування, збагачене мікроелементами та вітамінами, з обмеженим до 3-6 г умістом солі; споживання рідини, в т. ч. лужної, до 2-3 л/добу, полоскання горла.
Тактика в разі аритмій (ESC, 2020):
- у госпіталізованих пацієнтів із фібриляцією/тріпотінням передсердь без гемодинамічної нестабільності припинення використання протиаритмічних засобів і початок терапії контролю ЧСС із метою створення умов для безпечного використання гідроксихлорохіну та/або азитроміцину як противірусного препарату є розумним терапевтичним рішенням;
- варто брати до уваги взаємодію противірусних, протиаритмічних засобів і антикоагулянтів (https://reference.medscape.com/drug-interactionchecker).
- у тяжкохворих осіб із гемодинамічною нестабільністю внаслідок рецидивних гемодинамічно нестабільних фібриляції/тріпотіння шлуночків або фібриляції/тріпотіння передсердь препарат вибору – аміодарон внутрішньовенно.
! Слід зауважити, що на сьогодні ВООЗ відмовилася від використання гідроксихлорохіну та/або азитроміцину (Mehra M. R., Desai S.S, Ruschitzka F., 2020).
Питання про госпіталізацію хворого не розглядалося, він перебував на самоізоляції й підтримував телефонний зв’язок із сімейним лікарем.
Коли ж пацієнтів із COVID‑19 обов’язково треба госпіталізувати? Якщо вони належать до групи ризику, тобто за наявності таких станів:
- тяжкі хронічні захворювання легень / ССЗ;
- ниркова недостатність;
- імуносупресивні стани;
- тяжкі алергічні порушення;
- автоімунні захворювання;
- тяжкий перебіг коронавірусної інфекції;
- порушення психічного стану.
Динаміка. На 2-й день з’явилося часткове порушення нюху (різкі інтенсивні запахи розрізнялися, помірні – ні). Зафіксовано підвищення АТ (135/90-140/100 мм рт. ст., що відповідає критеріям для встановлення діагнозу АГ за показником домашнього АТ ≥135/85 мм рт. ст.).
На 3-й день хворого продовжували турбувати слабкість, лихоманка, інтенсивний головний біль. Надійшов позитивний результат ПЛР‑тесту на COVID‑19. Хворому призначили вітамін С (1000 мг/добу), вітамін D (2000 мг/добу), полівітаміни з цинком (усі призначення – поза показаннями), периндоприл 4 мг 1 р/добу (вранці).
Вибір антигіпертензивної терапії (АГТ) базується на показниках АТ і наявності у хворого ураження органів-мішеней. Пацієнт з АГ 1 ступеня без ураження органів-мішеней – кандидат на монотерапію. Якщо у хворого на АГ і COVID‑19 наявні епізоди гіпотензії, гостре ураження нирок, то відповідно до рекомендацій ESC передбачені госпіталізація, моніторинг аритмій, гіпокаліємії, адже в цій популяції рівень смертності сягає 6%.
У клінічній ситуації, що розглядається, для АГТ вибрали інгібітор АПФ з огляду на його здатність впливати на органи-мішені: серце, судини, нирки, а також надниркові залози, синапси нейронів. Призначили периндоприл, який забезпечує ефективний 24-годинний контроль АТ і зменшення ризику інфарктів, інсультів, рівня кардіоваскулярної смертності, має зручний режим прийому.
Як було наголошено, використання вітамінів С, D та цинку є призначенням поза показаннями в протоколі МОЗ України. Проте певне наукове обґрунтування ця тактика має: вітаміни С та D, препарати цинку й ацетилсаліцилова кислота (АСК) унесені до протоколів лікування FLCCC Alliance (MATH+ and I-MASK+ Protocols, 2020) й оцінюються як перспективні в профілактиці та лікуванні COVID‑19.
Наразі рекомендації щодо лікування COVID‑19 поповнюються й удосконалюються, проте вони базуються на чітких лабораторних показниках, що не завжди можливо в українських реаліях. Вибір лікувальної тактики «всліпу», без підкріплення даними лабораторних тестів, нині не рідкість, особливо в сільській місцевості через відсутність доступу до сучасної діагностики. Тому рекомендовано зважувати користь/ризики та, коли це виправдано, виходити за рамки протоколів.
Динаміка. На 4-5-й день стан пацієнта Р. оцінювали як стабільний, турбували виражена слабкість і підвищення температури тіла до 37,4 °C, АТ – 120/80-130/80 мм рт. ст.
На 6-й день спостерігалося погіршення самопочуття: з’явилися сухий кашель і задишка, посилилася слабкість, температура тіла підвищилася до 38,5 °C, АТ – 120/80-130/85 мм рт. ст., сатурація – 95-96%.
Рекомендовано: КТ органів грудної порожнини, ЗАК, визначення рівнів D‑димеру, прокальцитоніну та СРБ.
На 7-й день зберігалися сухий кашель і задишка, посилилася слабкість, виникла пітливість, температура тіла – 37,8 °C, АТ і сатурація – без змін. Проведено лабораторні дослідження.
На 8-й день отримано результати лабораторних тестів: за даними ЗАК, швидкість осідання еритроцитів становила 12 мм/г, D‑димер – 780 нг/мл, СРБ – 10 мг/л. На КТ – ознаки двобічної полісегментарної пневмонії (CO-RADS5), уражено 10-15% паренхіми легень.
На 9-й день пацієнту додатково призначили АСК.
В українських рекомендаціях із лікування COVID‑19 АСК відсутня: рекомендується відразу призначати НМГ. Проте препарат має додаткові переваги: є дані, що АСК завдяки впливу на циклооксигеназу‑2, NF-κB, НО‑1 забезпечує опосередковану противірусну дію щодо SARS-CoV‑2. Переконливо доведена здатність АСК запобігати тромбоутворенню. У пацієнтів із COVID‑19, які отримували АСК, ризик потрапити до відділень реанімації / інтенсивної терапії зменшувався на 43%, на штучну вентиляцію легень – на 44%. Рівень внутрішньолікарняної смертності знижувався на 47%.
У разі використання АСК у кишковорозчинній формі антитромбоцитарний ефект низьких доз препарату може зменшуватися, тому слід застосовувати не 75 мг, а 100 мг. Бажано моніторувати рівень тромбоцитів, щоб уникнути тромбоцитопенії.
Динаміка. На 10-12-й день від появи симптомів стан хворого оцінювали як задовільний. Продовжували турбувати сухий кашель (поступово зменшувався), задишка, слабкість, пітливість, температура тіла – 37,5 °C, АТ – 120/80-130/80 мм рт. ст.
На 13-й день пацієнт здійснив візит до лікаря.
Спостерігалася позитивна динаміка: зменшилися сухий кашель, задишка, пітливість, температура тіла підвищувалася лише у вечірній час (до 37,2 °C), але зберігалася слабкість.
Об’єктивно: стан задовільний, температура тіла – 36,7 °C, шкірні покриви вологі, лімфатичні вузли не збільшені. У легенях – жорстке дихання, хрипи відсутні. Тони серця звучні, ритмічні. ЧСС – 72/хв. АТ – 120/80 мм рт. ст. Живіт без особливостей, симптом поколочування негативний. Рекомендовано продовжити лікування.
Повторний ПЛР‑тест на COVID‑19 негативний.
З огляду на наявність у пацієнта АГ й аритмії йому рекомендовані ехокардіографія, добове моніторування АТ, холтер-ЕКГ, біохімічний аналіз крові, консультація кардіолога.
Реабілітація після COVID‑19: далі буде
Сьогодні перед лікарями постало питання, як відновлювати працездатність хворих, як проводити реабілітацію постковідного синдрому. Однією з найпоширеніших скарг у хворих після перенесеної COVID‑19 є астенія. Так, у нещодавньому великому 6-місячному дослідженні взяли участь 1733 хворі, котрі перенесли COVID‑19. Середній вік пацієнтів становив 57,0 року. Втома чи м’язова слабкість (63%) і труднощі зі сном (26%) були найпоширенішими симптомами. Тривога чи депресія були зареєстровані у 23% пацієнтів. (Chaolin Huang, Lixue Huang, Yeming Wang et al., 2021). Проблема м’язової слабкості, астенії, відчуття втоми є вагомою причиною зниження працездатності.
Варто зазначити, що в усуненні цієї проблеми ефективно допомагає призначення мельдонію (Мілдронат®, «Гріндекс»).
За даними відкритого постреєстраційного дослідження препарату Мілдронат® у пацієнтів із хронічною СН і COVID‑19, ускладненою пневмонією, його застосування сприяло статистично достовірному зменшенню тривалості госпіталізації: 16,2 vs 11,2 дня (Верткін А.Л. і співавт., 2020). Крім того, на тлі терапії препаратом Мілдронат® зменшувалися рівні маркерів запалення: СРБ (-55,8%) і D‑димеру (-15,7%). Якість життя в пацієнтів, які додатково до базисної терапії отримували Мілдронат®, згідно з показниками опитувальника EQ‑5D покращувалася, як і задоволеність станом власного здоров’я. Зафіксовано кращу клінічну динаміку в осіб із хронічною СН, які вживали Мілдронат®. Через 3 міс ці відмінності досягали рівня статистичної достовірності.
У дослідженні А. Л. Верткіна та співавт. Мілдронат® призначався за такою схемою: 1 г/добу внутрішньовенно струменево протягом періоду госпіталізації з подальшим переходом на пероральний прийом під час амбулаторного лікування в дозі 500 мг 2 р/добу курсом 2 тиж.
У пацієнтів із хронічною СН і COVID‑19, ускладненою пневмонією, Мілдронат® сприяв:
- скороченню періоду госпіталізації;
- зниженню рівнів маркерів запалення та тромботичних ускладнень;
- покращенню якості життя за опитувальником EQ‑5D;
- збільшенню задоволеності станом власного здоров’я;
- покращенню клінічного стану;
- зменшенню вираженості астенії за шкалою MFI‑20.
Важливий нюанс, який слід ураховувати при веденні пацієнтів із ССЗ, – мельдоній може підсилювати дію препаратів, які містять гліцерилтринітрат, ніфедипін, β-адреноблокатори й інші гіпотензивні засоби та периферичні вазодилататори.
Мілдронат® – препарат, який свого часу розроблявся для впливу на енергетичний обмін у спортсменів, нині дуже успішно застосовується не тільки в лікуванні ССЗ, а й у відновленні після COVID‑19 у пацієнтів з астенією, в осіб, які перенесли грип та ін. Досить ефективним і безпечним є пероральне застосування мельдонію в дозі 500 мг двічі на день (уранці й увечері), тривалість курсу становить 4-6 тиж.
Медична газета «Здоров’я України 21 сторіччя» № 2 (495), 2021 р.



