26 червня, 2021
Порівняльна ефективність препаратів хворобомодифікуючої терапії при лікуванні пацієнтів із розсіяним склерозом
Із появою хворобомодифікуючої терапії (ХМТ) прогноз для пацієнтів із розсіяним склерозом (РС) суттєво поліпшився. Нині найдієвішою стратегією лікування рецидивно-ремітивного РС (РРРС) є ранній початок ХМТ для уповільнення чи запобігання розвитку хвороби, усунення загострень або зниження їх частоти. Засіб ХМТ першої лінії диметилфумарат (ДМФ) чинить імуномодулюючу та цитопротективну дію, впливаючи на ключові етапи патогенезу РС. Пропонуємо до вашої уваги огляд результатів дослідження S. Braune et al., проведеного у реальних клінічних умовах і присвяченого порівняльній ефективності терапії ДМФ із модифікованим вивільненням та інтерфероном (ІФН), глатирамеру ацетатом (ГА) і терифлуномідом (ТЕР). Матеріал опубліковано у виданні Journal of Neurology (2018; 265 (12): 2980‑2992).
Ефективність ДМФ із модифікованим вивільненням, тобто кишковорозчинної форми ДМФ, у терапії РРРС доведено в рандомізованих клінічних дослідженнях (РКД), ретроспективних аналізах, дослідженнях у реальних клінічних умовах (Chan et al., 2017; Fox et al., 2015). Але для медичного застосування цього лікарського засобу та прийняття рішень щодо політики в галузі охорони здоров’я таких даних може бути недостатньо. Натомість дослідження порівняльної ефективності (ДПЕ) препаратів у терапії тієї чи іншої патології дозволяють отримати докази у реальній клінічній практиці. Вони можуть включати багато препаратів порівняння, а також охоплювати когорти пацієнтів, яких зазвичай виключають із РКД через жорсткі вимоги.
Ефективність ДМФ та альтернативних засобів ХМТ шляхом аналізів даних реєстрів методом псевдорандомізації порівнювали й раніше. Було показано ліпшу позитивну дію ДМФ щодо зниження частоти загострень на рік та збільшення часу до першого загострення порівняно з ІФН, ГА і ТЕР (Sattarnezhad et al., 2017; Spelman et al., 2017). S. Braune et al. (2018) на основі даних реєстру NeuroTransData (NTD; Німеччина) виконали порівняння ефективності ДМФ з ІФН, ГА і ТЕР в умовах реальної клінічної практики у пацієнтів із РРРС, відібраних методом псевдорандомізації.
Матеріали й методи дослідження
Пацієнтів розподілили на дві групи: лікування ДМФ та ІФН, ГА, ТЕР. Критерії включення у дослідження були такі: РРРС, вік ≥18 років, наявність даних за шкалою оцінки ступеня інвалідизації (EDSS) та/або рецидив після початку терапії. Медіана періодичності візитів хворих для огляду – близько трьох місяців. Для порівняння з ефективністю терапії ІФН, ГА чи ТЕР пацієнти відповідних груп повинні були не отримувати ХМТ до початку дослідження або ж перебувати на попередньому лікуванні іншим препаратом першої лінії (наприклад, ГА або ТЕР у разі оцінки ефективності ІФН).
Первинною кінцевою точкою ДПЕ був час до першого загострення, вторинними – частота загострень на рік, частка пацієнтів без загострень за період 12 та 24 місяці, причини та час до переривання терапії. Також фіксували час підтвердженого прогресування ступеня інвалідизації (ППСІ) за шкалою EDSS упродовж 3- та 6-місячного періоду (тобто збільшення показника за шкалою EDSS на 0,5 та 1 бал для пацієнтів із початковими показниками ≥5,5 та 0‑5,5 бали відповідно).
Коефіцієнти схильності розраховували методом множинної логістичної регресії. Група відповідного лікування являла собою залежну змінну, а такі фактори-конфаундери, як вік, стать, тривалість захворювання до початку досліджуваного лікування, попередня терапія (кількість призначень – 0, 1, 2, 3, 4+), бали за шкалою EDSS на початку спостереження, загальна частота загострень за останні 12 і 24 місяці – незалежні змінні (метод псевдорандомізації враховує лише такі конфаундери, які можуть бути виміряні, та не може враховувати, наприклад, дані магнітно-резонансної томографії). Непарне цензурування використовували як метод первинного аналізу всіх отриманих результатів, а попарне – як аналіз чутливості до зміщень для врахування потенційної різниці у часі приймання препарату та оцінки стійкості даних.
Результати дослідження
Порівняння ДМФ та ІФН
Показник щодо часу до першого загострення (первинна кінцева точка) був значуще нижчим у хворих, які отримували ДМФ, порівняно з такими на ІФН, що свідчило про вищу ефективність ДМФ (рис. 1). Щодо вторинної кінцевої точки, у більшості пацієнтів (83,5 і 77%) групи ДМФ порівняно з ІФН (76,5 і 61%) не спостерігалося загострень упродовж 12 і 24 місяців відповідно. Річна частота загострень у хворих на лікуванні ДМФ була значуще нижчою, ніж серед тих, хто отримував ІФН (рис. 2). Час до переривання терапії у групах ДМФ і ІФН суттєво не відрізнявся. В обох групах відмова від лікування у деяких випадках була пов’язана переважно з побічними явищами та немедичними причинами, при цьому брак терапевтичного ефекту частіше мав місце на тлі застосування ІФН. Час до ППСІ упродовж 3 і 6 місяців та частка пацієнтів без прогресування РС протягом 12 місяців були дещо більшими у групі ДМФ порівняно з ІФН.
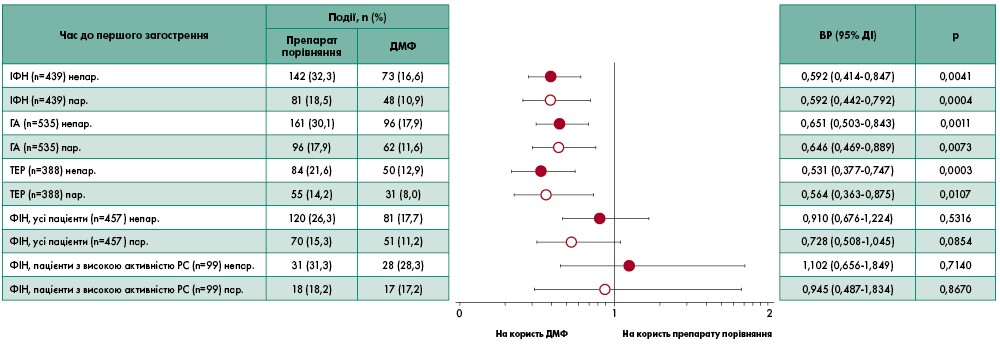 Рис. 1. Відносний ризик щодо часу до першого загострення у групах, які отримували ДМФ та препарати порівняння
Рис. 1. Відносний ризик щодо часу до першого загострення у групах, які отримували ДМФ та препарати порівняння
Примітки: ВР – відносний ризик, ДІ – довірчий інтервал, ФІН – фінголімод, непар. – непарне цензурування (первинний аналіз), пар. – попарне цензурування (аналіз чутливості).
Адаптовано за S. Braune et al., 2018
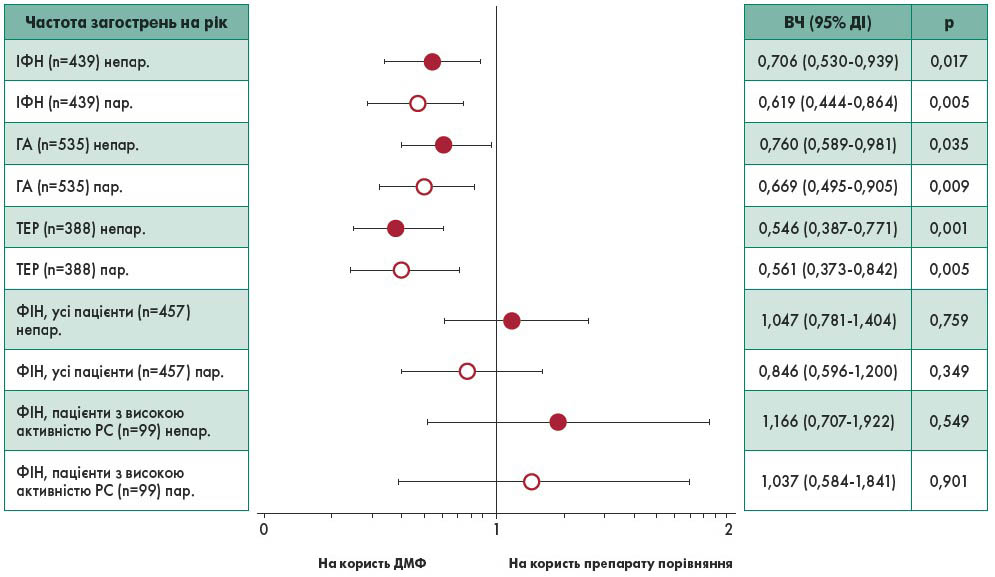 Рис. 2. Відношення частот загострень РС у річному обчисленні в групах, які отримували ДМФ та препарат порівняння
Рис. 2. Відношення частот загострень РС у річному обчисленні в групах, які отримували ДМФ та препарат порівняння
Примітки: ВЧ – відношення частот, ФІН – фінголімод, непар. – непарне цензурування (первинний аналіз), пар. – попарне цензурування (аналіз чутливості).
Адаптовано за S. Braune et al., 2018
Порівняння ДМФ і ГА
Показник щодо часу до першого загострення (первинна кінцева точка) був значуще нижчим у пацієнтів на лікуванні ДМФ порівняно з тими, хто отримував ГА, що свідчило про вищу ефективність ДМФ (рис. 1). У групі ДМФ більшість хворих (82,7 і 76,3%) порівняно з ГА (75,3 і 64,3%) не мали загострень упродовж 12 і 24 місяців відповідно. Річна частота загострень серед пацієнтів, які застосовували ДМФ, була суттєво нижчою, ніж на тлі лікування ГА (рис. 2). Час до переривання терапії у групах ДМФ і ГА суттєво не відрізнявся. В обох групах відмова від лікування у деяких випадках корелювала переважно з побічними ефектами та немедичними причинами. Час до ППСІ упродовж 3 і 6 місяців та частка осіб без прогресування РС протягом 12 місяців були подібними у групах ДМФ і ГА.
Порівняння ДМФ і ТЕР
Показник щодо часу до першого загострення (первинна кінцева точка) був значуще нижчим у пацієнтів, які отримували ДМФ, порівняно з групою ТЕР, що свідчило про вищу ефективність ДМФ (рис. 1). Стосовно вторинної кінцевої точки, у групі ДМФ у більшості пацієнтів (86,8 і 81,4%) порівняно з ТЕР (79 і 69,1%) були відсутні загострення упродовж 12 і 24 місяців відповідно. Річна частота загострень у хворих, які отримували ДМФ, була суттєво нижчою, ніж серед тих, хто перебував на лікуванні ТЕР (рис. 2). Час до переривання терапії у групах ДМФ і ТЕР суттєво не відрізнявся. В обох групах відмова лікування у певних випадках асоціювалася здебільшого з побічними явищами та немедичними причинами, при цьому відсутність терапевтичного ефекту частіше мала місце у групі ТЕР. Час до ППСІ упродовж 3 і 6 місяців та частка осіб без прогресування РС протягом 12 місяців були подібними у групах ДМФ і ТЕР.
Обговорення
Незважаючи на переваги РКД у визначенні ефективності та безпеки нових методів або засобів терапії, вони мають певні недоліки. Так, РКД не можуть надати порівняльну інформацію про всі можливі варіанти застосування, до того ж відбір учасників РКД відбувається згідно з суворими критеріями, тому не відображає широкого різноманіття характеристик пацієнтів, їхніх коморбідностей, попередньої терапії тощо у реальній клінічній практиці. Тож для ухвалення як медичних, так і управлінських рішень необхідна більш надійна та прозора інформація. Національні та міжнародні реєстри пацієнтів із РС містять високоякісні дані, які завдяки статистичній обробці дають змогу порівняти різні методи лікування та допомогти клініцистам і пацієнтам у спільному прийнятті рішень щодо вибору терапії.
Під час аналізу даних рееєстру NTD:
- застосування методу псевдорандомізації мінімізувало ризик систематичної помилки вибірки при зіставленні даних пацієнтів, які отримували ДМФ або препарат порівняння;
- чітке визначення загострення РС та залучення сертифікованих спеціалістів для оцінки стану пацієнтів за шкалою EDSS мінімізували ризик систематичної помилки, пов’язаної з виявленням клінічних подій;
- регулярні візити пацієнтів усіх груп до лікаря (приблизно один раз на три місяці) знижували ризик систематичної помилки, пов’язаної з процесом дослідження;
- аналіз чутливості, оснований на парному цензуруванні, мінімізував ризик систематичної помилки, пов’язаної з різним часом спостереження за пацієнтами різних груп.
Аналіз даних реєстру NTD показав, що терапія ДМФ, призначена пацієнтам з високою активністю РС, тобто після загострення, яке відбулося на тлі застосування іншого препарату або за відсутності терапії, виявилася ефективнішою щодо зниження активності РС, ніж ІФН, ГА і ТЕР. Автори зазначають, що дослідження включало досить велику вибірку, а спостереження було тривалим, із частими візитами, зокрема для оцінки стану за шкалою EDSS. Обох цих характеристик одночасно не мало жодне попереднє випробування.
Загалом результати вивчення даних реєстру NTD добре узгоджуються з даними попередніх ДПЕ, де порівнювали ефективність ДМФ та інших препаратів ХМТ (Chan et al., 2017; Hutchinson et al., 2014). Результати клінічних випробувань, дані реальної клінічної практики та пацієнтів із дослідних медичних центрів також підтверджують, що ефективність ДМФ вища за таку ІФН, ГА або ТЕР, незалежно від того, чи проводили пряме порівняння чи застосовували псевдорандомізацію (Boster et al., 2017; Nicholas et al., 2017). Так, ретроспективний аналіз даних щодо звернень за страховими виплатами у США показав, що річна частота загострень РС була нижчою серед пацієнтів, які приймали ДМФ, ніж на тлі лікування ІФН, ГА або ТЕР (Boster et al., 2017).
Аналіз даних реєстру NTD включав також порівняння ефективності ДМФ і фінголімоду – засобу ХМТ, що застосовують у пацієнтів із високоактивним РРРС. Аналіз не показав суттєвої різниці між ДМФ і фінголімодом щодо часу до першого загострення та річної частоти загострень (рис. 1, 2). Автори звертають увагу на результати аналізу в підгрупах, що демонструє високу ефективність ДМФ, близьку до такої фінголімоду, серед пацієнтів із високою активністю захворювання – осіб, в яких повний курс лікування принаймні одним препаратом ХМТ не дозволив досягти терапевтичного ефекту (Braune et al., 2018).
Висновки
У підсумку автори зазначають, що ДМФ має переваги перед ІФН, ГА та ТЕР щодо часу до першого рецидиву та частоти рецидивів на рік. Ці висновки узгоджуються з результатами попередніх ДПЕ та підтверджені додатковими доказами на основі аналізу методом псевдорандомізації, ретельного підбору груп та визначення кінцевих точок, тривалішого періоду спостереження тощо. Отримані результати є корисними для прийняття клінічних рішень щодо призначення засобів ХМТ в умовах реальної клінічної практики.
Підготувала Тетяна Ткаченко
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 2 (57) 2021 р.



