24 липня, 2021
Рак грудної залози у молодих фертильних жінок
Рак у пацієнтів молодого віку відрізняється від такого в осіб літнього віку за клінічними симптомами, гістологічними особливостями, молекулярною біологією, прогнозом і виживаністю, а проведення протипухлинного лікування є складним завданням і також має відмінності.
20-29 травня відбувся мультидисциплінарний конгрес з міжнародною участю «Рак у молодих пацієнтів – проблеми профілактики, скринінгу, лікування, реабілітації», в рамках якого обговорювалися найактуальніші медичні та біологічні проблеми, а також соціальне значення злоякісних пухлин у молодого населення України. Конгрес проходив у форматі онлайн-лекцій, презентацій, фільмів і дискусій. Учасниками заходу стали понад 2000 лікарів різних спеціальностей, а запрошеними експертами – провідні фахівці, відомі як в Україні, так і за кордоном.
 Експерт МОЗ України за спеціальністю «Онкологія», завідувач кафедри онкології ДЗ «Запорізька медична академія післядипломної освіти МОЗ України», доктор медичних наук, професор Олексій Олексійович Ковальов представив доповідь «Ескалаційна терапія раку грудної залози – нова парадигма лікування та оптимальні комбінації».
Експерт МОЗ України за спеціальністю «Онкологія», завідувач кафедри онкології ДЗ «Запорізька медична академія післядипломної освіти МОЗ України», доктор медичних наук, професор Олексій Олексійович Ковальов представив доповідь «Ескалаційна терапія раку грудної залози – нова парадигма лікування та оптимальні комбінації».
– Рак грудної залози (РГЗ) – найпоширеніше онкологічне захворювання у жінок у всьому світі. За даними GLOBOCAN за 2019 р., естроген-рецепторпозитивний (ER+) люмінальний підтип РГЗ є другою за частотою причиною смерті пацієнток молодого віку від онкологічних захворювань. При цьому у жінок віком до 40 років поширеність РГЗ сягає 6,5%, тоді як у хворих молодших 30 років – 0,6%. Низький ризик розвитку РГЗ у жінок молодого віку та, як наслідок, відсутність скринінгових програм у цій віковій групі сприяють тому, що РГЗ часто виявляють вже на пізніх стадіях (W. Han et al., 2010). Особливостями РГЗ у пацієнток молодого віку є високий ризик та швидкий розвиток місцевого рецидиву, високий ризик смерті після локального рецидиву чи розвитку раку другої молочної залози та складний взаємозв’язок між ендокринною й імунною системами. Крім цього, молоді жінки більшою мірою страждають не лише фізично, а й емоційно, рідше дотримуються режиму ендокринної терапії. Під час лікування РГЗ у пацієнток молодого віку необхідно враховувати спосіб їх життя та потенційні проблеми із фертильністю. Як відомо, на виживаність молодих жінок із РГЗ впливають стадія захворювання, вік пацієнтки, наявність чи відсутність аменореї та біологічні властивості пухлини.
З молекулярно-генетичного погляду, РГЗ є гетерогенною пухлиною, що продемонстровано Charles M. Perou та співавт., які у 2000 р. запропонували першу молекулярно-генетичну класифікацію РГЗ. Найчастіше, а саме у 80% випадків, виявляють ER+ РГЗ.
ER+ РГЗ є хронічним рецидивуючим захворюванням із найвищим ризиком розвитку рецидиву у перші 5 років, який, втім, в окремих пацієнток зберігається і впродовж 20 років. Імовірність рецидиву та в подальшому смерті складає приблизно 5-10% у хворих із І стадією, 15-20% – із ІІ стадією та 50% – ІІІ стадією раку. У 5-10% пацієнток із діагностованим метастатичним РГЗ через тривалий час після лікування розвинеться не рецидив захворювання, а рак de novo.
Історично для лікування пацієнток із метастатичним естроген-рецепторпозитивним без рецепторів 2 типу людського епідермального фактора росту (HER2-) РГЗ використовували антиестрогени й інгібітори ароматази, медіана виживаності таких пацієнтів у ХХ столітті становила від 16 до 20 міс. Поворотним моментом у лікуванні метастатичного РГЗ стало впровадження інгібіторів циклінзалежних кіназ 4/6 (CDK 4/6) та інгібіторів мішені рапаміцину у ссавців (mTOR), що сприяло різкому збільшенню виживаності хворих та зумовило необхідність перегляду алгоритмів лікування ER+ РГЗ.
Сьогодні добре відомо, що механізмом виникнення істинної ендокринорезистентності при ER+ РГЗ є порушення регуляції клітинного циклу. Порушення ліміту поділу (ліміту Хейфліка) є однією із 10 ознак ракової клітини (D. Hanahan, R.A. Weinberg, 2011). У нормі клітина має обмежене число клітинних циклів. Ключову роль в управлінні поділом клітини відіграє особливий клас білків – цикліни, концентрація яких змінюється залежно від фази клітинного циклу. Висока експресія генів циклінів характерна для багатьох видів раку (L. Hartwell, T. Hunt, P. Nurse, 2001). Механізм дії інгібіторів CDK 4/6 полягає у зупинці клітини у фазі G1, інгібуванні гена-супресора Rb, епітеліально-мезенхімального переходу та проліферації, модуляції імунної системи (за рахунок продукції інтерферону ІІІ, зниження проліферації Treg та стимуляції проліферації NK), а також у синергічній протипухлинній активності з інгібіторами фосфоінозитид 3-кінази (РІ3К; D. Fry, P. Toogood, 2014).
Управління з контролю якості харчових продуктів і лікарських препаратів США схвалило три інгібітори CDK 4/6 – палбоцикліб, рибоцикліб та абемацикліб, ефективність яких була доведена у дослідженнях PALOMA, MONALEESA та MONARCH відповідно. Їх прямого порівняння у клінічних дослідженнях не проводилось.
Цікавим є дослідження MONALEESA‑2, що включало 668 раніше не лікованих пацієнток у постменопаузі із ER+/HER2- РГЗ, у якому порівнювали ефективність застосування комбінації рибоциклібу у дозі 600 мг/добу та летрозолу у дозі 2,5 мг/добу із монотерапією летрозолом 2,5 мг/добу (летрозол + плацебо). Згідно з отриманими результатами, додавання рибоциклібу дозволило збільшити виживаність без прогресування (ВБП) до 25,3 міс, тоді як у контрольній групі медіана ВБП дорівнювала 16 міс (рис. 1; G.N. Hortobagyi et al., 2018). Медіана загальної виживаності (ЗВ) сягала 33 міс у групі плацебо + летрозол, а у групі рибоциклібу досягнута не була. Варто зауважити, що ефективність рибоциклібу не залежала від локалізації метастазів та віку хворих (рис. 2А, Б; G.S. Sonke et al., 2018).
 Рис. 1. Розрахунок ВБП за оцінкою дослідника методом Каплана – Маєра у дослідженні MONALEESA‑2
Рис. 1. Розрахунок ВБП за оцінкою дослідника методом Каплана – Маєра у дослідженні MONALEESA‑2
 Рис. 2. Розрахунок ВБП за методом Каплана – Маєра у групі хворих віком ≥65 років (А) та ≤65 років (Б) у дослідженні MONALEESA‑2
Рис. 2. Розрахунок ВБП за методом Каплана – Маєра у групі хворих віком ≥65 років (А) та ≤65 років (Б) у дослідженні MONALEESA‑2
Зіставні результати були отримані у дослідженні ІІІ фази MONALEESA‑3, у якому оцінювали ефективність рибоциклібу у дозі 600 мг/добу у поєднанні із фулвестрантом 500 мг у жінок у пре- та постменопаузі (вік хворих варіював від 31 до 89 років) та у чоловіків із ER+/HER2- РГЗ, які раніше не отримували або пройшли не більше одного курсу ендокринної терапії (ЕТ). Аналіз даних показав, що ВБП значно покращилась у пацієнтів, які приймали рибоцикліб із фулвестрантом, порівняно з групою контролю: медіана ВБП склала 20,5 та 12,8 міс відповідно (рис. 3; відносний ризик – ВР – 0,593; 95% довірчий інтервал – ДІ – 0,480-0,732; p<0,001; D.J. Slamon et al., 2019).
 Рис. 3. Розрахунок ВБП за оцінкою дослідника методом Каплана – Маєра у дослідженні MONALEESA‑3
Рис. 3. Розрахунок ВБП за оцінкою дослідника методом Каплана – Маєра у дослідженні MONALEESA‑3
Отже, інгібітори CDK 4/6 у поєднанні з ЕТ сьогодні є стандартом лікування пацієнтів з ER+/HER2- РГЗ. Інгібітори CDK 4/6 у комбінації з інгібіторами ароматази/фулвестрантом застосовують при метастатичному РГЗ de novo, при первинній чи вторинній резистентності, у жінок у постменопаузі, а також у жінок у пременопаузі та чоловіків у поєднанні з агоністами лютеїнізуючого гормону. Більшість експертів надає перевагу призначенню інгібіторів CDK 4/6 у 1-й лінії терапії, проте існує невелика група пацієнтів із обмеженим метастатичним навантаженням та менш агресивною біологією пухлини, у яких можна застосовувати лише ЕТ (F. Cardoso et al., 2020). Згідно з рекомендаціями Національної онкологічної мережі США (NCCN) 2020 р., комбінації рибоциклібу з інгібіторами ароматази та рибоциклібу з фулвестрантом є пріоритетними режимами 1-ї лінії лікування метастатичного ER+/HER2- РГЗ.
Проте наразі залишається низка невирішених питань, зокрема не зрозуміло, коли краще використовувати інгібітори CDK 4/6 – в 1-й чи 2-й лінії лікування, а також якою є оптимальна комбінація препаратів цієї групи. На сьогодні не визначено біомаркерів, що дозволили б ідентифікувати пацієнтів, які отримали б найбільш виражений ефект від лікування, адже валідність наявних предиктивних маркерів не доведена. Крім цього, актуальною залишається проблема резистентності до інгібіторів CDK 4/6. Щодо застосування інгібіторів CDK 4/6 у поєднанні із ЕТ як підтримуючої терапії після хіміотерапії, то даних на підтвердження ефективності такої комбінації немає, тому підтримуючу терапію рекомендовано проводити лише з використанням ЕТ. Можливість використання інгібіторів CDK 4/6 в (нео)ад’ювантному режимі вивчається.
Кіскалі (рибоцикліб) – єдиний інгібітор CDK 4/6, що забезпечує доведене збільшення тривалості життя пацієнток із метастатичним ER+/HER2- РГЗ. Доведеною є клінічна ефективність рибоциклібу в пацієнток у пре- та менопаузі, в комбінації із різними ендокринними препаратами, при гормоночутливому та гормонорезистентному РГЗ. Застосування препарату Кіскалі (рибоцикліб) дозволяло відтермінувати початок хіміотерапії, а також покращити або зберегти якість життя пацієнтів (D.J. Slamon et al., 2019; S.A. Im et al., 2019).
 Профіль безпеки інгібіторів CDK 4/6 у терапії ER+/HER2- РГЗ у жінок в пременопаузі висвітлила завідувачка відділення хiмiотерапiї Центру мiжнародних клiнiчних дослiджень (м. Днiпро), кандидат медичних наук Наталія Григорівна Уржумова.
Профіль безпеки інгібіторів CDK 4/6 у терапії ER+/HER2- РГЗ у жінок в пременопаузі висвітлила завідувачка відділення хiмiотерапiї Центру мiжнародних клiнiчних дослiджень (м. Днiпро), кандидат медичних наук Наталія Григорівна Уржумова.
– РГЗ є найчастіше діагностованою онкологічною патологією у жінок віком 25‑39 років у всьому світі. Близько 5-7% всіх випадків РГЗ припадає на вік менше 40 років. Смертність у цій віковій групі у 1,5 разу переважає таку при виявленні РГЗ у жінок старшого віку (C. Reyna et al., 2014). Факторами ризику розвитку РГЗ у молодих жінок є генетична схильність і щільна тканина грудної залози, відсутність вагітності, вагітність у зрілому віці, використання пероральних контрацептивів, надмірне вживання алкоголю, ожиріння тощо (A. Surakasula et al., 2014).
Ефективність і безпеку інгібіторів CDK 4/6 у лікуванні РГЗ вивчали у дослідженні MONALEESA‑2. Так, найчастішим побічним ефектом у разі терапії рибоциклібом була нейтропенія (про неї свідчило зниження рівня нейтрофілів і гранулоцитів), яка розвивалась у 74,3% випадків у групі рибоциклібу + летрозолу порівняно з 5,2% у групі летрозолу + плацебо. При цьому частота нейтропенії 3-4 ступеня склала 59,3 та 0,9% відповідно; фебрильна нейтропенія розвивалась лише в 1,5% пацієнтів. Серед інших небажаних явищ відмічали нудоту (у 51,5 порівняно з 28,5%), приєднання інфекційних захворювань (у 50,3 порівняно з 42,4%), втомлюваність (у 36,5 порівняно з 30,0%) та діарею (у 35,0 порівняно з 22,1%), в основному, вони були 1-2 ступеня тяжкості та не потребували корекції дози чи відміни терапії. Серед небажаних явищ 3-4 ступеня переважали лейкопенія (у 21 та 0,6% осіб), підвищення рівня аланінамінотрансферази (у 9,3 та 1,2%) та аспартатамінотрансферази (у 5,7 та 1,2%). Деякі небажані явища мали характерні ознаки щодо часу їх виникнення та розрішення. Так, медіана часу до розвитку нейтропенії склала близько 16 днів, а до її розрішення – 15 днів, інтервал Q-T найчастіше подовжувався на 15‑ту добу прийому рибоциклібу, медіана часу до розвитку гепатотоксичності сягала 57 днів, а розрішення або зменшення ступеня гепатотоксичності можна було очікувати приблизно через 24 дні.
За необхідності редукції дози рибоциклібу її знижували спочатку із 600 (200 мг 3 рази на день) до 400 мг (200 мг 2 рази на день), а при потребі – до 200 мг 1 раз на день. Загалом редукція дози була необхідна для 169 (50,6%) пацієнтів. Аналіз даних показав, що у дослідженні MONALEESA‑2 при редукції дози рибоциклібу його ефективність не знижувалася. Зокрема, медіана ВБП у пацієнтів, яким проводили редукцію дози, склала 25,3 міс, тоді як у групі пацієнтів, яким дозу не коригували, – 27,7 міс (J.T. Beck et al., 2019). У групі пацієнтів, які отримували терапію комбінацією рибоцикліб + летрозол, частота нейтропенії склала 65% серед всіх побічних проявів, які потребували редукції дози рибоциклібу. Одну редукцію дози проводили 33,2% пацієнтів групи рибоциклібу + летрозолу та 5,2% осіб у групі летрозолу + плацебо. Дві редукції дози були необхідні у 19,2 та 1,2% пацієнтів групи рибоциклібу та плацебо відповідно (G.N. Hortobagyi et al., 2018).
У дослідженні ІІІ фази MONALEESA‑7, що включало 672 пацієнтки у пре- або перименопаузі із дисемінованим ER+/HER2- РГЗ, які раніше не отримували ЕТ та пройшли не більше 1 курсу хіміотерапії з приводу РГЗ, порівнювали ЕТ у комбінації з рибоциклібом із ЕТ без додавання рибоциклібу. Пацієнток у співвідношенні 1:1 було рандомізовано у групи рибоцикліб + тамоксифен/нестероїдні інгібітори ароматази (НСІА) та плацебо + тамоксифен/НСІА. Всім хворим проводили терапію гонадотропін-рилізинг-гормоном з метою пригнічення функції яєчників. Згідно з отриманими результатами, додавання рибоциклібу дозволило збільшити ВБП до 23,8 міс, тоді як у контрольній групі ВБП дорівнювала 13 міс (рис. 4; D. Tripathy et al., 2018).
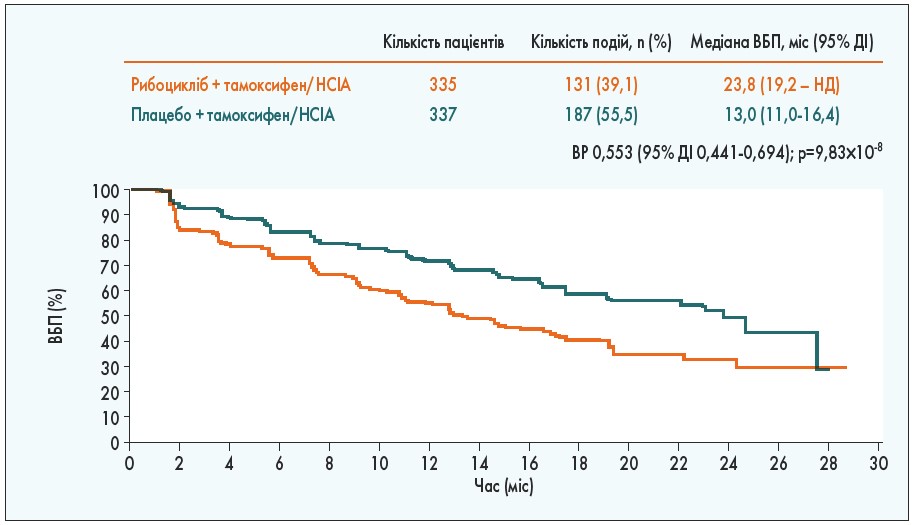 Рис. 4. Розрахунок ВБП за оцінкою дослідника методом Каплана – Маєра у дослідженні MONALEESA‑7
Рис. 4. Розрахунок ВБП за оцінкою дослідника методом Каплана – Маєра у дослідженні MONALEESA‑7
При аналізі за підгрупами було продемонстровано перевагу комбінації рибоцикліб + НСІА порівняно з комбінацією рибоцикліб + тамоксифен, про що, зокрема, свідчила вища ВБП (27,5 проти 22,1 міс відповідно). Крім цього, вищу ВБП виявлено у пацієнтів, які не отримували попередньої хіміотерапії з приводу дисемінованого РГЗ (медіана ВБП склала 24,7 міс).
Застосування рибоциклібу дозволило збільшити не лише ВБП, а й статистично значущо подовжити ЗВ. Так, 42-місячна ЗВ становила 70,2% у групі рибоцикліб + ЕТ проти 46% у групі плацебо + ЕТ (ВР 0,712; 95% ДІ 0,535-0,948; р=0,00973). При цьому в групі рибоциклібу медіана ЗВ досягнута не була, тоді як у групі плацебо дорівнювала 40,9 міс (рис. 5; S.A. Im et al., 2019).
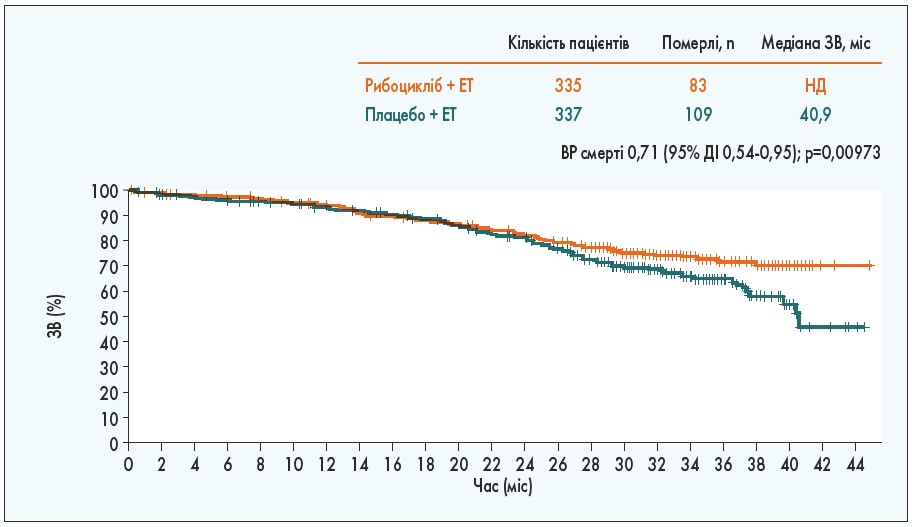 Рис. 5. Розрахунок ЗВ за методом Каплана – Маєра у дослідженні MONALEESA‑7
Рис. 5. Розрахунок ЗВ за методом Каплана – Маєра у дослідженні MONALEESA‑7
Після дострокового припинення лікування з тих чи інших причин подальшу терапію інгібіторами CDK 4/6 у групі рибоциклібу застосовували рідше, ніж у групі плацебо (10 проти 18,6%; S.A. Im et al., 2019).
Окремо оцінювали час із моменту рандомізації до прогресування захворювання на фоні 2-ї лінії лікування або смерті – ВБП2. Медіана ВБП2 для рибоциклібу досягнута не була, а для плацебо склала 32,3 міс. При аналізі даних через 42 міс спостереження 54,6% (95% ДІ 46,8-61,8) пацієнтів у групі рибоциклібу були живими та не мали прогресування захворювання на фоні 2-ї лінії терапії. Для групи плацебо цей показник склав 37,8% (95% ДІ 28,4-47,2).
Серед побічних проявів діагностували припливи, біль у суглобах, втомлюваність, головний біль і діарею, частота яких майже не відрізнялась у групах рибоциклібу та плацебо. Нудота дещо частіше виникала у групі рибоциклібу (31,6 проти 19,6%). Подовження інтервалу Q-T понад 480 мс відмічалось у 6,9% пацієнтів, які отримували рибоцикліб, та 1,2% – плацебо, а понад 500 мс – у 1,5 та 0,3% відповідно. Варто зауважити, що подовження інтервалу Q-T не супроводжувалося клінічними проявами, а випадки тахікардії типу пірует не виявляли.
Медіана тривалості лікування сягала близько 2 років у групі рибоциклібу та близько 1 року в групі плацебо. Терапія рибоциклібом дозволяла відтермінувати початок хіміотерапії, а також сприяла покращенню або збереженню якості життя пацієнтів (D.J. Slamon et al., 2019; S.A. Im et al., 2019).
Профіль безпеки рибоциклібу був зіставний із таким в інших дослідженнях. Нейтропенія 3-4 ступеня тяжкості була зафіксована у 63,5% пацієнтів, гепатотоксичність – в 11%, а подовження інтервалу Q-T – у 1,8% (D. Tripathy et al., 2018).
Враховуючи можливу кардіологічну токсичність препарату, під час терапії рибоциклібом рекомендовано проводити моніторинг електрокардіографічних показників, зокрема до лікування, через 2 тижні від ініціювання першого циклу та перед початком наступного циклу. Слід контролювати рівні калію, кальцію, фосфору та магнію перед кожним циклом лікування впродовж 6 міс. Перед початком лікування рекомендовано провести ехокардіографію, при цьому рибоцикліб можна призначати за умови, що фракція викиду лівого шлуночка становить не менше 55%.
Інгібітори CDK 4/6 не застосовують для лікування пацієнтів, які впродовж останніх 3 міс перенесли гострий інфаркт міокарда, при серцевій недостатності ІІБ та вище (клас 2-3 за NYHA), інтервалі Q-T понад 450 мс, при неконтрольованих аритміях та нестабільній стенокардії.
Також потрібно пам’ятати про токсичність інгібіторів CDK 4/6 для легень, яка може проявлятися розвитком інтерстиціальної хвороби легень або пневмоніту. Комп’ютерну томографію органів грудної клітки слід проводити перед лікуванням та надалі з інтервалом 8 тижнів. Тимчасової відміни інгібіторів CDK 4/6 та редукції дози на 1 рівень (до 400 мг на добу) потребує пневмоніт 2 ступеня, а при пневмоніті 3 ступеня препарати цієї групи відміняють назавжди.
Стосовно побічних проявів з боку шкіри, то при реакціях 2 ступеня, коли ділянка ураження займає 10-30% площі тіла, застосування препарату переривають та відновлюють терапію після зменшення вираженості реакції до 1 ступеня, знижуючи при цьому дозу до 400 мг на добу. Про 3 ступінь тяжкості свідчить ураження понад 30% площі тіла, що супроводжується системними проявами, такими як лихоманка, гіпотензія, біль у суглобах і м’язах, зміни у загальному аналізі крові. У такому разі інгібітори CDK 4/6 відміняють назавжди.
Нейтропенія 1-2 ступеня корекції дози не потребує, проте щотижня рекомендовано оцінювати показники загального аналізу крові. При нейтропенії 3 ступеня прийом інгібіторів CDK 4/6 переривають, а при досягненні 2 ступеня – відновлюють у попередній дозі 600 мг на добу із щотижневою оцінкою показників загального аналізу крові. Проте при повторному виникненні епізоду нейтропенії 3 ступеня та при нейтропенії 4 ступеня дозу знижують до 400 мг на добу. Фебрильна нейтропенія 3 ступеня потребує переривання прийому препарату до підвищення рівня нейтрофілів до 1,0×109, після чого його застосування відновлюють у дозі 400 мг на добу.
Вживання їжі на всмоктування інгібіторів CDK 4/6 не впливає. Застосування сильних інгібіторів CYP3A4 (кларитроміцин, кетоконазол, ітраконазол, грейпфрутовий сік тощо) посилює ефект інгібіторів CDK 4/6. Прийом рибоциклібу посилює ефект фентанілу, еверолімусу, циклоспорину й ерготаміну, а його комбінація з аміодароном, кларитроміцином, галоперидолом, метадоном, моксифлоксацином та ондансетроном посилює вплив на інтервал Q-T. Прийом інгібіторів протонної помпи зменшує всмоктування інгібіторів CDK 4/6, а індукторів CYP3A4 (карбамазепін, фенітоїн, рифампіцин і звіробій) знижує рівень інгібіторів CDK 4/6 у плазмі крові.
Таким чином, Кіскалі (рибоцикліб) показаний у комбінації з інгібітором ароматази або фулвестрантом для лікування жінок із місцево-поширеним або метастатичним РГЗ з позитивним статусом ER та негативним статусом HER2 як початкова ЕТ або для лікування пацієнток, які попередньо отримували ЕТ. У жінок в пре- або перименопаузі ЕТ слід проводити у комбінації з агоністом лютеїнізуючого гормону рилізинг-гормону.
Підготувала Ольга Нестеровська
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 3 (70) 2021 р



