25 вересня, 2021
Функціональні проби: звертаємося до підручника
Продовження. Початок у № 3, 2021 р.
Редакція медичної газети «Здоров’я України», тематичного номера «Кардіологія. Ревматологія. Кардіохірургія» продовжує знайомити наших читачів із ґрунтовним і детальним підручником «Функціональна діагностика» за редакцією д. мед. н., професора О.Й. Жарінова, д. мед. н., професора Ю.А. Іваніва та к. мед. н., доцента В.О. Куця. Пропонуємо до вашої уваги розділ «Функціональні проби» ІІ частини «Функціональні проби. Амбулаторне моніторування ЕКГ і артеріального тиску».
Зміни ЕКГ під час НП
Фізіологічні зміни ЕКГ
Нормальна відповідь на фізичне навантаження виявляється у підвищенні ЧСС без суттєвих відхилень сегмента ST, порушень ритму або провідності серця (рис. 1). Під час навантаження амплітуда зубця Р може збільшуватися в нижніх відведеннях (II, III, aVF) без зміни тривалості. Тривалість сегмента PR зменшується, а його конфігурація в нижніх відведеннях низхідна. Цей феномен пов’язаний із реполяризацією передсердь (зубець Та), що може також спричинити косовисхідну депресію сегмента ST у нижніх відведеннях.
Під час НП амплітуда та тривалість зубця Q у тих відведеннях, в яких він наявний, істотно не змінюються. На максимумі навантаження амплітуда зубця Q може дещо зростати в нижніх відведеннях. Незначне зниження зубця R спостерігають у лівих грудних відведеннях (V5, V6) при максимальному навантаженні та в першу хвилину відновлювального періоду. Зменшення амплітуди зубця R супроводжується збільшенням глибини зубця S, що пов’язано з фізіологічними змінами електричної осі серця при навантаженні.
Під час навантаження у лівих грудних відведеннях спостерігають депресію точки J, яка досягає найбільшої величини на максимумі навантаження. Точка J поступово повертається до вихідного положення у відновлювальному періоді. Депресія точки J поширеніша в обстежуваних похилого віку, але при цьому в нормі відсутня депресія сегмента ST через 60‑80 мс після точки J. В осіб з елевацією точки J у спокої (феномен ранньої реполяризації) на тлі навантаження точка J може зміститися до ізоелектричної лінії; це розглядається як варіант норми.
На ранніх стадіях навантаження у всіх відведеннях спостерігають поступове зменшення амплітуди зубця Т. На максимумі навантаження зубець Т починає збільшуватися, а на 1-й хвилині відновлювального періоду його амплітуда повертається до вихідного рівня.
При навантаженні не спостерігають істотних змін зубця U. Утім, цей зубець інколи тяжко виявити при частоті ритму шлуночків понад 130 за хвилину, з огляду на наближення зубців Т і Р при підвищенні ЧСС.
Патологічні зміни ЕКГ
Рівень сегмента ST переважно вимірюють щодо сегмента PQ, оскільки під час навантаження інколи важко оцінити сегмент ТP. Оптимально слід орієнтуватися на три послідовні комплекси PQRST в одному і тому ж відведенні зі стабільною ізолінією і визначити середнє зміщення сегмента ST.
Етапи аналізу сегмента ST:
- оцінка ізолінії за положенням сегмента PQ або TP;
- оцінка положення точки J;
- оцінка положення сегмента ST через 60‑80 мс після точки J.
При ЧСС понад 130 за хвилину зміщення сегмента ST слід оцінювати через 60 мс після точки J. Коли на вихідній ЕКГ спостерігається депресія точки J порівняно з сегментом PQ, індуковані навантаженням зміни оцінюють у точці J і через 60‑80 мс після неї. При вихідній елевації точки J у стані спокою (рання реполяризація) і появі депресії точки J під час навантаження виразність зміщення сегмента ST оцінюють порівняно з сегментом PQ, а не вихідним положенням точки J.
Індукована навантаженням ішемія міокарда може виявлятися депресією або елевацією сегмента ST (рис. 2). Депресія сегмента ST – найпоширеніший вияв індукованої навантаженням ішемії міокарда (рис. 3, 4). Депресія сегмента ST відображає субендокардіальну ішемію у відповідних ділянках міокарда і залежить від поширеності зони ішемії, наявності рубцевих змін та місць накладання електродів.
Стандартний критерій патологічної відповіді – горизонтальна або косонизхідна депресія сегмента ST ≥0,1 мВ (1 мм) протягом 60‑80 мс після точки J, яка зберігається у трьох послідовних комплексах зі стабільною ізолінією. При косовисхідній депресії сегмента ST його зміщення на 1 мм і більше через 60‑80 мс після точки J розглядається як критерій ішемії міокарда. При «коритоподібному» зміщенні сегмента ST оцінюють амплітуду депресії в найнижчій точці сегмента ST. Подібне зміщення сегмента ST при НП спостерігають рідко, а як діагностично значущу розцінюють депресію сегмента ST на 0,1 мВ (1 мм) і більше.
Горизонтальна і косонизхідна депресії сегмента ST є специфічнішими для ішемії міокарда, ніж косовисхідна. За наявності виразних вихідних порушень ЕКГ специфічність депресії сегмента ST під час навантаження для діагностики ішемії міокарда знижується. Імовірність і тяжкість ІХС можна оцінити також за ступенем виразності, часом виникнення, тривалістю та кількістю відведень із депресією сегмента ST.
Для оцінки ступеня виразності стенозувального атеросклерозу вінцевих артерій слід враховувати також час виникнення ішемічних відхилень сегмента ST. Про ймовірне ураження стовбура лівої вінцевої артерії або багатосудинне ураження і несприятливий прогноз виживання хворих свідчить виникнення ішемічних змін сегмента ST при низькому рівні навантаження (25‑50 Вт) і низьких величинах подвійного добутку. Тривале збереження депресії сегмента ST у фазі відновлення також є суттєвим маркером тяжкості ІХС.
Індукована навантаженням елевація сегмента ST зазвичай може спостерігатися в зоні раніше перенесеного інфаркту, де наявні зубці Q, рідко – в неінфарктованій зоні у пацієнтів без ІМ в анамнезі при незміненому комплексі QRS. Патологічною відповіддю вважають розвиток елевації точки J >0,1 мВ, яка зберігається протягом 60‑80 мс після точки J у трьох послідовних комплексах зі стабільною ізолінією. Елевація сегмента ST (рис. 5) у відведеннях без зубця Q (крім V1 і aVR) відображає трансмуральну ішемію відповідних ділянок міокарда.
Раніше перенесений ІМ – найчастіша причина елевації сегмента ST під час навантаження. Такі зміни ЕКГ, очевидно, пов’язані з наявністю у ЛШ зон гіпокінезу або акінезу. Приблизно у 30% пацієнтів з ІМ передньої локалізації та 15% осіб з ІМ нижньої локалізації, обстежених у ранні терміни після ІМ, мають місце індуковані навантаженням елевації сегмента ST у відведеннях із зубцями Q. Зміни сегмента ST можуть супроводжуватися позитивізацією зубця Т у цих же відведеннях, формуючи графіку «омолодження» інфарктної ЕКГ-кривої.
Крім того, інколи спостерігають також реципрокну депресію сегмента ST, яка нагадує ішемію, у відведеннях, протилежних до зони елевації сегмента ST. Водночас наявність елевації та депресії сегмента ST у різних відведеннях протягом одного дослідження може вказувати на багатосудинне ураження вінцевих артерій. Із метою диференціації нової зони ішемії міокарда від реципрокних змін унаслідок елевації сегмента ST у відведеннях із зубцями Q можуть бути застосовані методи візуалізації міокарда. Описані зміни сегмента ST у післяінфарктних хворих є підставою для припинення НП.
В осіб без перенесеного раніше ІМ (без зубців Q на ЕКГ у спокої) оцінка елевації сегмента ST під час навантаження часто дозволяє встановити локалізацію транзиторної ішемії міокарда внаслідок тяжкого стенозувального ураження або спазму проксимального відділу вінцевої артерії. У пацієнтів з активною варіантною стенокардією (більш ніж 2 спонтанні епізоди на тиждень) індуковану навантаженням елевацію сегмента ST за механізмом коронарного вазоспазму виявляли приблизно у 30% обстежених. Зазвичай локалізація індукованої навантаженням елевації сегмента ST відповідає зворотному дефекту перфузії при проведенні сцинтиграфії міокарда з талієм‑201. У пацієнтів із таким варіантом відповіді на навантаження частіше з’являються шлуночкові аритмії під час проведення дослідження.
У здорових осіб повідомляли про різноманітні коливання амплітуди зубця R під час НП. Характерною відповіддю у них є збільшення амплітуди зубця R при виконанні субмаксимального навантаження, з його зниженням на максимальному навантаженні. Загалом урахування індукованих навантаженням змін амплітуди зубця R не дозволяє підвищити діагностичну точність обстеження.
Ізольовані зміни зубця Т (без ішемічних змін сегмента ST) при НП характеризуються низькою специфічністю і можуть бути зумовлені різними причинами, такими як зміни положення тіла, фази дихання, гіпервентиляція, приймання їжі, куріння, фонова медикаментозна терапія, а також наявність ішемії/некрозу міокарда. У популяціях пацієнтів із низькою поширеністю ІХС позитивізація інвертованих зубців Т під час навантаження не є діагностичною ознакою ІХС. Проте поява динаміки зубця Т потребує припинення НП у хворих із вогнищевими змінами на вихідній ЕКГ.
Інверсія зубця U може асоціюватися з гіпертрофією ЛШ, ІХС, аортальною або мітральною регургітацією. Ці стани супроводжуються порушеннями діастолічної функції ЛШ. Індукована навантаженням інверсія зубця U у лівих грудних відведеннях в осіб із нормальною ЕКГ у спокої є маркером ішемії міокарда і дозволяє припускати ураження лівої передньої низхідної артерії. Але зубці U тяжко розпізнати при ЧСС понад 130 за хвилину. Аналіз цього критерію не збільшує інформативності НП у конкретного обстежуваного.
Відсутність адекватного підвищення САТ або виразні порушення серцевого ритму і провідності, які не супроводжуються появою об’єктивних критеріїв ішемії, зумовлюють потребу в припиненні НП, але не дають достатніх підстав оцінювати її як позитивну.
Порушення внутрішньошлуночкової провідності
Порушення внутрішньошлуночкової провідності можуть бути наявні до початку НП, з’являтися або зникати під час дослідження. Залежна від ЧСС внутрішньошлуночкова блокада, яка виникає під час навантаження, часто передує виникненню хронічної блокади, яка зберігається у спокої. За наявності блокади ЛНПГ надійно діагностувати ішемію міокарда на підставі даних ЕКГ зазвичай неможливо. У здорових осіб із вихідною блокадою ЛНПГ може спостерігатися виразніша депресія сегмента ST порівняно з такою у спокої.
Відмінності у відхиленнях сегмента ST під час навантаження в осіб із вихідною блокадою ЛНПГ з/без ішемії міокарда відсутні. Виникнення блокади ЛНПГ при ЧСС <125 за хвилину в осіб із типовою стенокардією часто асоційоване з ІХС, тоді як поява блокади ЛНПГ при ЧСС ≥125 за хвилину частіше спостерігається за інтактних вінцевих артерій (рис. 6).
Вихідна блокада правої ніжки пучка Гіса (ПНПГ) не впливає на інтерпретацію змін сегмента ST, за винятком правих грудних відведень (V1-V3), в яких депресія сегмента ST зазвичай наявна у спокої.
Крім блокад лівої або правої ніжки пучка Гіса, під час НП можуть індукуватися блокади передньої або задньої гілки ЛНПГ, а також двопучкова блокада з поєднанням блокади ПНПГ і блокади лівої передньої або лівої задньої гілки. Наявність таких блокад зазвичай залежить від ЧСС. Інколи при ЧСС понад 150 за хвилину внутрішньошлуночкові блокади тяжко відрізнити від шлуночкової тахікардії. Рідкісним феноменом є зникнення під час навантаження внутрішньошлуночкових блокад, наявних у спокої.
Порушення атріовентрикулярної провідності
У нормі під час навантаження тривалість інтервалу PR зменшується до 0,11‑0,12 с, що зумовлено посиленням симпатичного тонусу і зменшенням парасимпатичної активності, особливо в молодих здорових осіб. У пацієнтів із вихідною затримкою АВ-провідності на вузловому рівні на тлі фізичного навантаження швидкість проходження імпульсу через АВ-вузол збільшується, що веде до зменшення тривалості інтервалу PQ (рис. 7).
Інколи АВ-блокада І ступеня виникає наприкінці навантаження або під час відновлювального періоду. Подовження інтервалу PR часто спостерігається в пацієнтів із міокардитами, а також при застосуванні препаратів, які погіршують АВ-проведення (дигоксин, ББ, верапаміл). Зазвичай поява під час навантаження АВ-блокади І ступеня є рідкісним феноменом. Клінічне значення індукованої навантаженням АВ-блокади ІІ ступеня І типу невідоме. Слід зважати на те, що така блокада може з’являтися при перевищенні «критичного» рівня частоти синусового ритму. Водночас АВ-блокада ІІ ступеня також буває виявом тяжкого фонового ураження провідної системи серця. За її появи НП слід припинити.
Набута повна АВ-блокада у спокої є відносним протипоказанням для виконання НП. В осіб із вродженою проксимальною повною АВ-блокадою НП можна виконувати, якщо немає інших тяжких вроджених аномалій.
У рідкісних випадках безпосередньо після припинення навантаження спостерігаються тривалі періоди зупинки синусового вузла. Зазвичай такі зміни виникають у пацієнтів із тяжкою ІХС.
Навантаження може провокувати, усувати або не мати впливу на аномальне АВ-проведення хворих із діагностованим синдромом Вольфа – Паркінсона – Уайта. Коли навантаження не впливає на вихідне аномальне АВ-проведення імпульсів, під час НП можна спостерігати виразну депресію сегмента ST. За наявності синдрому Вольфа – Паркінсона – Уайта депресія сегмента ST може бути не виявом ішемії, а хибнопозитивною, або невизначеною знахідкою (рис. 8). Хоча навантаження вважають чинником, який може спричиняти виникнення тахіаритмій у пацієнтів із даним синдромом, поширеність тахіаритмій під час або після навантаження у них низька.
Аритмії серця
Навантаження може індукувати серцеві аритмії за певних умов, зокрема на тлі терапії діуретиками або дигоксином. Виникнення аритмій зумовлює нещодавнє споживання алкоголю або кофеїну. Оскільки навантаження супроводжується збільшенням потреби міокарда в кисні, індукована навантаженням ішемія міокарда спричиняє появу ектопічної активності.
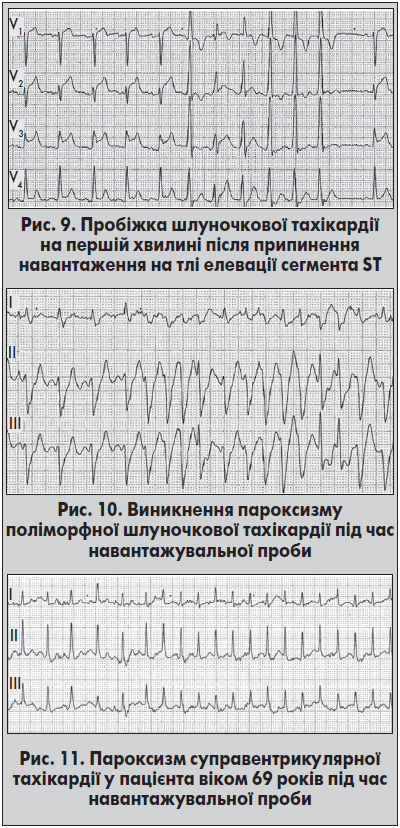
Припускають, що ішемія з депресією сегмента ST менш аритмогенна, ніж з елевацією сегмента ST. Механізми формування індукованих навантаженням аритмій – підвищення симпатичного тонусу та/або збільшення потреби міокарда в кисні. Особливо небезпечним є період безпосередньо після припинення навантаження, з огляду на поєднання високих рівнів катехоламінів та генералізованої вазодилатації (рис. 9).
Індукована навантаженням і зниженням серцевого викиду дилатація периферичних артерій, яка є наслідком зменшення венозного повернення крові до серця при раптовому припиненні активності м’язів, може призвести до зниження коронарної перфузії на початку відновлювального періоду, коли ЧСС ще підвищена. Активація симпатичного тонусу здатна стимулювати активність ектопічних водіїв ритму у волокнах Пуркіньє шляхом прискорення фази 4 потенціалу дії та підвищення патологічного автоматизму, а індукована навантаженням ішемія міокарда зумовлює виникнення кіл ріентрі.
Навантаження може також супроводжуватися зникненням аритмій, наявних у спокої. Цей феномен пояснюють частотним пригніченням формування ектопічних імпульсів на тлі синусової тахікардії, з підвищенням симпатичної та зменшенням парасимпатичної активності. Індукована навантаженням синусова тахікардія може пригнічувати автоматизм ектопічних вогнищ.
Шлуночкові порушення ритму під час навантаження є частішими, суправентрикулярні тахіаритмії спостерігаються дещо рідше. Поширеність аритмій прямо залежить від віку та наявності серцевої патології. Загалом шлуночкова екстрасистолія високих градацій є тривожним виявом у пацієнтів із кардіоміопатіями, ураженнями клапанів серця, тяжкою ішемією міокарда, а також випадками раптової смерті в сімейному анамнезі (рис. 10).
Як у здорових осіб, так і на тлі серцевої патології під час НП можуть виникати передсердні ектопічні скорочення, зокрема групові екстрасистоли. Індуковані навантаженням транзиторні фібриляція та тріпотіння передсердь виявляють менш ніж в 1% обстежуваних, яким виконують НП. Ці аритмії можуть бути індуковані як у здорових осіб, так і в пацієнтів із ревматичним ураженням серця, гіпертиреозом, синдромом Вольфа – Паркінсона – Уайта, кардіоміопатіями. Дуже рідко під час навантаження спостерігають пароксизмальну АВ-вузлову тахікардію. Індуковані навантаженням суправентрикулярні аритмії більшою мірою пов’язані не з ІХС, а наявністю хвороби легенів, нещодавнім прийманням алкоголю або кофеїну (рис. 11).
Вплив деяких препаратів на інтерпретацію результатів НП
Пацієнти зі стенокардією, які отримують ББ, можуть досягати більшої ТН із меншою депресією сегмента ST і меншими виявами стенокардії. Слід зважати на те, що на тлі застосування ББ обмежується приріст ЧСС і подвійного добутку, а це своєю чергою зменшує діагностичну точність методу. У разі постійної терапії ББ слід зазначати на ЕКГ час приймання та дозування препаратів.
Використання вазодилататорів короткої дії перед проведенням НП може призводити до підвищення ТН в осіб зі стабільною стенокардією напруження. Водночас здатність нітратів тривалої дії підвищувати ТН у хворих на стенокардію не доведено. У пацієнтів з артеріальною гіпертензією гіпотензивні засоби можуть чинити ефект на толерантність до навантаження через вплив на стан гемодинаміки і рівень АТ.
Дигоксин може індукувати або посилювати депресію сегмента ST під час виконання навантаження як у здорових осіб, так і в пацієнтів з ІХС. Зміни сегмента ST поєднуються з нормальною тривалістю інтервалу QT або його деяким зменшенням. Депресія сегмента ST може зберігатися протягом двох тижнів після припинення терапії дигоксином. Водночас на тлі ішемії, застосування антиаритмічних засобів 1-го класу, електролітного дисбалансу, деяких інших станів імовірне збільшення тривалості інтервалу QT.
Більшість діуретичних засобів мало впливають на ЧСС та показники функціонального стану міокарда, але зменшують об’єм крові, що циркулює, периферичний опір судин (при тривалому застосуванні) та рівень АТ. Діуретики можуть викликати гіпокаліємію, яка спричиняє м’язову втому, шлуночкову ектопію та інколи – депресію сегмента ST.
Діагностичний висновок при НП
Обов’язковим підсумком НП є діагностичний висновок. У ньому повинні бути відображені:
1. Демографічні дані: прізвище та ім’я пацієнта, дата народження, стать, зріст, маса тіла, а також дата дослідження.
2. Мета проведення НП.
3. Клінічні особливості пацієнта: чинники ризику ІХС, застосування препаратів, зміни ЕКГ у спокої.
4. Результати дослідження:
- використаний протокол, розрахункова субмаксимальна і максимальна ЧСС, розрахункова субмаксимальна потужність навантаження;
- причина припинення навантаження;
- гемодинамічні параметри у спокої, на піку навантаження, а також проміжні значення під час навантаження та у відновлювальному періоді, досягнутий відсоток від максимальної ЧСС;
- пікова потужність навантаження, піковий показник МЕТ (для навантажувальної проби на тредмілі), загальна тривалість навантаження у хвилинах;
- наявність і характер больового синдрому, час початку стенокардії та виникнення стенокардії, яка лімітує виконання навантаження;
- ознаки ішемії міокарда: відведення з патологічними змінами ЕКГ, максимальна депресія або елевація сегмента ST, період часу до появи та зникнення ішемічних відхилень сегмента ST.
5. Загальні коментарі.
Варіанти висновків при НП, здійснених із метою діагностики ІХС:
- проба позитивна: поєднання типового ангінозного болю та ЕКГ-ознак ішемії міокарда, або значущі ознаки ішемії міокарда на ЕКГ без ангінозного болю, або типовий ангінозний напад;
- проба негативна: досягнення розрахункової субмаксимальної або максимальної ЧСС без змін ЕКГ та без ангінозного болю;
- проба неповна або неінформативна: пацієнт не досяг субмаксимальної ЧСС через причини, не пов’язані з ангінозним болем або характерним для ішемії міокарда зміщенням сегмента ST;
- проба сумнівна: припинення навантаження внаслідок атипового болю без ішемічних змін сегмента ST; припинення проби через появу порушень ритму і провідності; зниження САТ при збільшенні потужності навантаження; горизонтальна депресія сегмента ST до 1 мм або косовисхідна – до 1 мм протягом 60‑80 мс після точки J.
НП в особливих категоріях пацієнтів
При виконанні НП на особливу увагу заслуговують пацієнти із синдромами передчасного збудження шлуночків та ранньої реполяризації. У них частіше фіксують хибнопозитивний результат НП. В осіб із повною блокадою ЛНПГ можна оцінювати лише толерантність до фізичного навантаження, тоді як діагностувати ішемію за змінами ЕКГ у них зазвичай неможливо.
Інша ситуація – у хворих із повною блокадою ПНПГ, а також неповними внутрішньошлуночковими блокадами. У таких пацієнтів оцінка сегмента ST можлива, але має певні особливості, на які потрібно зважати при проведенні НП. В осіб із постійною формою ФП, в яких частіше знижується толерантність до фізичного навантаження, а зміни ЧСС залежать від впливу застосованих антиаритмічних засобів на АВ-вузол, також спостерігаються певні особливості реакції на фізичне навантаження, а ЧСС може досить швидко перевищити розрахований субмаксимальний показник.
Отже, інтерпретація змін ЕКГ на тлі фізичного навантаження в пацієнтів із синдромами преекзитації, ранньої реполяризації, блокадами ніжок пучка Гіса, а також фібриляцією передсердь має суттєві особливості.
Загалом, незважаючи на істотну еволюцію підходів до ведення хворих на ІХС, широке застосування методів візуалізації серця й вінцевих артерій, НП залишаються фізіологічним, доступним і високоінформативним засобом неінвазивної діагностики, важливим компонентом стратифікації ризику, оцінки доцільності коронарографії та ефективності лікування ІХС. За діагностичною цінністю цей метод переважає інші неінвазивні тести. НП має принципово важливе значення у визначенні функціонального стану пацієнтів із діагностованою раніше ІХС, при виборі медикаментозного лікування та визначенні ефективності реваскуляризації вінцевих артерій. Використання НП дозволяє суттєво підвищити якість обстеження хворих на стабільну ІХС.
Функціональні проби з використанням медикаментозних засобів
Виділяють провокаційні та корегувальні функціональні проби з використанням фармакологічних засобів (Аронов, Лупанов, 2002). Провокаційні призначені для виявлення прихованої недостатності вінцевого кровообігу або реакції синусового вузла і провідної системи серця на дію фармакологічного препарату. До них відносять проби з дипіридамолом, аденозином, ізопротеренолом, добутаміном, епінефрином, ефедрином, ергометрином. Корегувальні функціональні проби спрямовані на усунення дисбалансу між системами регулювання й ураженим органом із тимчасовим усуненням патологічних виявів (як-то проби із хлористим калієм, пропранололом, нітрогліцерином, гілуритмалом, атропінова проба тощо).
Наголосимо, що дедалі ширше застосування сучасних методів візуалізації серця і судин зумовлює перехід від класичних медикаментозних функціональних проб із контролем ЕКГ до їх переважного поєднання з ЕхоКГ або сцинтиграфією міокарда (Montalescot et al., 2013).
Проба з дипіридамолом
Цю пробу проводять для діагностики ІХС, особливо в тих випадках, коли НП неможливо виконати з якої-небудь причини, або ж її результат сумнівний чи неінформативний. Протипоказання для проведення проби такі самі, як і для проби з дозованим фізичним навантаженням. Механізм дії дипіридамолу пов’язаний із блокуванням аденозиндезамінази, що призводить до різкого підвищення концентрації аденозину (потужного природного вазодилататора) з наступним виразним збільшенням міокардіального кровоплину в ділянках із незміненими вінцевими артеріями і зменшення його в басейні стенозованих судин. Виникає «міжвінцеве обкрадання», що супроводжується виникненням нападу стенокардії і появою ЕКГ-ознак ішемії міокарда.
Розрахункову дозу дипіридамолу (0,75 мг/кг маси тіла) набирають у 20-мілілітровий шприц і розбавляють розчином хлориду натрію до об’єму 20 мл. Приготовлений розчин вводять в/в протягом 5 хв зі швидкістю 4 мл/хв. Під час проведення проби виконують запис ЕКГ у 12 відведеннях і постійно оцінюють клінічні вияви. Введення препарату припиняють при появі ЕКГ-ознак ішемії міокарда, нападу стенокардії, порушень серцевого ритму, провідності або побічних реакцій (головний біль, нудота, виразна слабкість).
Порогова доза препарату, яка призводить до появи ішемії міокарда, різна і залежить від ступеня ураження вінцевих артерій серця. При стенозуванні 2‑3 вінцевих артерій порогова доза дипіридамолу може бути менш ніж 0,30 мг/кг маси тіла, а в осіб із нормальним вінцевим кровопостачанням після введення розрахункової дози ознаки ішемії міокарда не з’являються. При негативному чи сумнівному результаті може бути проведено пробу з розрахунковою дозою дипіридамолу 0,84 мг/кг маси тіла, яка вводиться протягом 10 хв. За такої дози препарату хибнонегативних результатів практично не буває (Picano et al., 1988).
Для припинення нападу стенокардії та усунення ЕКГ-ознак ішемії міокарда довенно повільно вводять до 10 мл 2,4% розчину еуфіліну (антагоніста аденозину). Оцінюють пробу за тими ж критеріями, що і проби із фізичним навантаженням. Проба з дипіридамолом малоінформативна для діагностики ІХС на початкових стадіях, коли атеросклеротичне ураження вінцевих артерій ще не є гемодинамічно значущим (Аронов, Лупанов, 2002).
Проба з аденозином
Як і проба з дипіридамолом, проба з аденозином проводиться для підтвердження або заперечення ІХС. Вона протипоказана при хронічному обструктивному захворюванні легень, бронхіальній астмі, артеріальній гіпер- і гіпотензії, АВ-блокадах ІІ‑ІІІ ступеня, застійній серцевій недостатності, гострому інфаркті міокарда. При введенні аденозину також виникає неоднорідна дилатація вінцевого русла серця, що зумовлює «міжвінцеве обкрадання» і виникнення ішемії міокарда. Аденозин вводять довенно інфузоматом зі швидкістю 140 мкг/кг/хв протягом 6 хв. Під час проби оцінюють клінічні вияви, кожну хвилину вимірюють АТ і проводять моніторування ЕКГ.
Пробу припиняють при появі ЕКГ-ознак ішемії міокарда або побічних реакцій (як-то головний біль, задишка, артеріальна гіпотензія, погіршення АВ-провідності). Для припинення нападу стенокардії та побічних реакцій можна застосовувати еуфілін. Проба вважається позитивною при появі достовірних ознак ішемії міокарда (горизонтальна або косонизхідна депресія сегмента на 1 мм і більше).
Аденозин також має властивості пригнічувати автоматичну активність синусового вузла і погіршувати АВ-провідність, тому пробу з аденозином можна використовувати для оцінки функціонального стану СВ і латентних порушень АВ-провідності, особливо в осіб із синкопальними станами в анамнезі. Для обстеження цих хворих 20 мг розчину аденозину вводять в/в болюсно (Вrignole et al., 1997). Зупинка СВ більше ніж на 6 с або АВ-блокада з паузою тривалістю понад 10 с можуть спричинити синкопе, а подовження корегованого часу відновлення функції СВ більш як 550 мс свідчить про його дисфункцію. Болюсне введення аденозину 6‑12 мг також використовують для диференціальної діагностики шлуночкових і надшлуночкових тахікардій із широкими комплексами QRS, передсердних тахіаритмій і АВ-тахікардій, а також для припинення реципрокних суправентрикулярних тахікардій.
Проба з ізопротеренолом
Ізопротеренол (ізадрин, ізупрел, новодрин) має виразну симпатоміметичну активність, що виявляється підвищенням ЧСС, АТ та посиленням інотропної функції серця. Все це збільшує потребу міокарда в кисні, тому в осіб зі стенозованими вінцевими артеріями можуть бути спровоковані ішемія міокарда і напад стенокардії.
Для проведення проби 0,5 мг ізопротеренолу розчиняють у 200 мл ізотонічного розчину хлориду натрію і починають вводити в/в крапельно зі швидкістю 10‑20 крапель/хв. Потім протягом 2‑3 хв швидкість введення збільшують, доводять ЧСС до розрахункової субмаксимальної величини й утримують її на цьому рівні упродовж 3 хв. Введення припиняють при появі «ішемічних» змін ЕКГ, нападу стенокардії, порушень серцевого ритму або виразних побічних реакцій. Для припинення нападу стенокардії використовують нітрогліцерин сублінгвально або пропранолол (обзидан) у дозі 5 мг в/в зі швидкістю 1 мг/хв.
Оцінку проби проводять за загальноприйнятими критеріями. Поява горизонтальної або косонизхідної депресії сегмента ST на 1 мм і більше на тлі нападу стенокардії свідчить про ймовірне гемодинамічно значуще атеросклеротичне ураження вінцевих артерій. Зі збільшенням кількості стенозованих вінцевих артерій і зменшенням функціонального класу стенокардії зростає частота позитивних проб. Проба з ізопротеренолом за чутливістю і специфічністю не поступається пробі з фізичним навантаженням (Хафізов, Сидоренко, 1985). Цю пробу інколи використовують для оцінки реакції синусового вузла та провідної системи серця на стимуляцію β-адренорецепторів.
Проба з добутаміном
Механізм індукції ішемії міокарда при проведенні проби з добутаміном аналогічний такому при пробі з ізопротеренолом. Добутамін вводять в/в за допомогою автоматичного інфузомату в дозах, що наростають (5, 10, 15, 20, 30 мг/кг/хв), з інтервалом 3 хв під постійним контролем ЕКГ, ЧСС і АТ. Якщо при введенні початкових доз добутаміну (0,15 мг/кг/хв) ЧСС зростає повільно, додатково вводять 0,5 мл розчину атропіну.
Критерії припинення проби: досягнення субмаксимальної (85%) ЧСС, «ішемічні» зміни ЕКГ, напад стенокардії, порушення серцевого ритму (суправентрикулярні та/або вентрикулярні аритмії) та поява побічних реакцій (як-от артеріальна гіпертензія або гіпотензія, головний біль, нудота, тремор). Антагоністом добутаміну є ББ пропранолол, який застосовують в/в у дозі 5 мг за 5 хв. Критерії припинення проби такі самі, як для проб із дозованим фізичним навантаженням.
Проби з дипіридамолом, аденозином, ізопротеренолом і добутаміном можна поєднувати з ЕхоКГ-дослідженням (стрес-ЕхоКГ), сцинтиграфією міокарда з Tl201 або радіонуклідною вентрикулографією. Порушення локальної скоротливості ЛШ, які виявляються під час стрес-ЕхоКГ, є чутливішим маркером ішемії міокарда, ніж зміни сегмента ST і виникнення нападу стенокардії (Аронов, Лупанов, 2002). Cтрес-ЕхоКГ разом із добутаміном використовують найчастіше.
Проба з ергометрином
Для діагностики вазоспастичної стенокардії запропоновано цілу низку функціональних проб (холодова, хлоретилова, гіпервентиляційна, содово-гіпервентиляційна та ін.), але найбільш інформативною для діагностики вазоспазму вінцевих артерій є проба з ергометрином. Ергометрин малеат є α-стимулятором, який збільшує тонус судинної стінки і може спровокувати спазм вінцевих артерій. Проба протипоказана в осіб із гострим ІМ, при виразному атеросклеротичному ураженні вінцевих і сонних артерій, значних порушеннях серцевого ритму, серцевій недостатності та аортальному стенозі.
Пробу з ергометрином проводять у ранкові години в положенні хворого лежачи. Перед дослідженням за 24‑48 год відміняються нітрати й антагоністи кальцію. Ергометрин вводять в/в струминно в дозах, що наростають (0,05; 0,1; 0,2; 0,3 мг), із 5-хвилинними інтервалами між ними. Введення припиняють за появи елевації або депресії сегмента ST на 1 мм і більше, нападу стенокардії, порушень серцевого ритму або виразних побічних реакцій. ЕКГ реєструють перед дослідженням, під час проби і протягом 15‑20 хв після її закінчення. Для припинення нападу стенокардії використовують нітрогліцерин сублінгвально або його довенне введення. Пробу вважають позитивною при появі ЕКГ-ознак ішемії міокарда. Для вазоспастичної стенокардії характерна елевація сегмента ST на 1 мм і більше з нападом стенокардії.
Калієва проба та проба із пропранололом
Ці проби призначені для оцінки змін кінцевої частини шлуночкового комплексу і диференціальної діагностики коронарогенних та некоронарогенних змін міокарда. Розрахункова доза хлориду калію становить 100 мг/кг маси тіла пацієнта, пропранололу – 1 мг/кг. Реєстрацію ЕКГ у 12 відведеннях здійснюють до дослідження, через 60, 90 і 120 хв після застосування розрахункової дози одного із препаратів. Корекція змін реполяризації (наприклад, поява позитивних зубців Т замість негативних або ізоелектричних на вихідній ЕКГ) може вказувати на важливість метаболічних факторів у виникненні цих змін. Позитивна калієва проба або проба із пропранололом може спостерігатися при дистрофіях міокарда різного походження (спортивна, дисгормональна, в осіб із вегетативною дисфункцією тощо), але не виключає атеросклеротичного ураження вінцевих артерій, що потребує подальшого обстеження хворого.
Атропінова проба
Атропінову пробу використовують для з’ясування ролі парасимпатичного впливу на автоматичну функцію синусового вузла, синоатріальну і АВ-провідність та функціональний стан структур, залучених у циркуляцію збудження. Розрахункова доза атропіну (в формі 0,1% розчину) зазвичай становить 0,02‑0,04 мг/кг маси тіла хворого і вводиться в/в на 4 мл ізотонічного розчину. Максимальна дія препарату настає через 2‑3 хв. Реєстрацію ЕКГ здійснюють до дослідження, щохвилини протягом перших 5 хв, потім на 7, 10 і 15-й хв.
Зростання ЧСС до 90 і більше за хвилину в пацієнтів із виразною вихідною синусовою брадикардією свідчить про вагусну дисфункцію синусового вузла. Водночас для синдрому слабкості синусового вузла характерним є недостатнє підвищення частоти синусового ритму (до 30% від вихідного рівня) або навіть її зниження, поява пасивних ектопічних ритмів та пауз ритму за рахунок синоатріальної блокади або зупинки синусового вузла. Зникнення під час атропінової проби АВ-блокади І ступеня свідчить про її функціональне походження, а покращення АВ-провідності у пацієнтів з АВ-блокадою ІІ ступеня І типу вказує на сприятливий прогноз.
При вузловій (проксимальний варіант) АВ-блокаді 2:1 атропін покращує АВ-провідність, тоді як при стовбуровій (дистальний варіант) вона погіршується, оскільки АВ-блокада 2:1 може трансформуватися у блокаду 3:1 або 4:1. У частки хворих із феноменом Вольфа – Паркінсона – Уайта введення атропіну може зумовити зникнення графіки преекзитації, що дозволяє оцінити зміни комплексу QRS, сегмента ST і зубця Т. Усунення екстрасистолії або суттєве зниження її частоти на тлі атропінової проби свідчить про вагозалежний тип аритмії.
Проба з гілуритмалом
Пробу з гілуритмалом (аймаліном) використовують для оцінки змін ЕКГ у пацієнтів із синдромом Вольфа – Паркінсона – Уайта. Гілуритмал подовжує ефективний рефрактерний період пучка Кента і майже не змінює АВ-провідність, що в деяких хворих (40‑80%) зумовлює блокування проведення імпульсу в додатковому шляху та відновлення звичайної графіки ЕКГ (Аронов, Лупанов, 2002). Розрахункову дозу гілуритмалу (1 мг/кг маси тіла пацієнта, але не більш як 50 мг) в 10 мл ізотонічного розчину хлориду натрію вводять довенно повільно (10 мг/хв) під постійним ЕКГ-контролем і подальшою щохвилинною реєстрацією ЕКГ протягом 5‑10 хв.
Відновлення звичайної графіки ЕКГ дозволяє оцінити зміни комплексу QRS і фази реполяризації, а блокада додаткових шляхів проведення свідчить про ефективність гілуритмалу для припинення пароксизмів АВРТ. Водночас збереження графіки преекзитації на ЕКГ дозволяє виявити пацієнтів із коротким рефрактерним періодом додаткових шляхів проведення і високим ризиком виникнення небезпечних аритмій та раптової серцевої смерті.
Інші функціональні проби
Холодову пробу застосовують для діагностики вазоспастичної стенокардії. Пробу проводять у ранкові години в положенні хворого лежачи. Передпліччя правої руки занурюють у воду, охолоджену до +1‑3 °C, на 3‑5 хв. Реєстрацію ЕКГ і контроль АТ здійснюють перед дослідженням, під час проби і протягом 10‑15 хв після її закінчення. Пробу припиняють за появи ішемічних змін ЕКГ, нападу стенокардії, порушень серцевого ритму або виразних побічних реакцій. Пробу вважають позитивною у разі появи депресії або елевації сегмента ST на 1 мм і більше. Для вазоспастичної стенокардії характерна елевація сегмента ST із нападом стенокардії. Інколи як холодову пробу використовують зрошення лівої половини грудної клітки та хребтового краю лівої лопатки хлоретилом до отримання ефекту охолодження (Лутай, Симорот, 1993).
Пробу з гіпервентиляцією використовують також для діагностики вазоспастичної стенокардії. Її проводять у ранкові години в положенні хворого лежачи. Пацієнт глибоко дихає з частотою 30‑40 дихальних рухів за хвилину протягом 3‑5 хв. ЕКГ реєструють перед дослідженням, постійно при проведенні проби і протягом 15‑20 хв після її закінчення. Критерії позитивної проби: елевація або депресія сегмента ST на 1 мм і більше та напад стенокардії.
За діагностичним значенням холодова проба та проба з гіпервентиляцією поступаються пробі з ергометрином. Їх можна використовувати за наявності клінічних виявів вазоспастичної стенокардії та в ситуаціях, коли проба з ергометрином протипоказана або недоступна.
Ортостатична проба слугує для оцінки реакції серцево-судинної системи на швидку зміну положення тіла. При переході з горизонтального у вертикальне зменшується поступлення крові до правих відділів серця, при цьому підвищуються тонус симпатичного відділу вегетативної нервової системи, ЧСС та загальний периферичний опір. Після 15-хвилинного перебування в горизонтальному положенні пацієнт швидко переходить у вертикальне і стоїть 10 хв без напруження м’язів. У горизонтальному положенні, а потім у вертикальному кожну хвилину, а після закінчення проби на 1, 3, 5 і 10-й хв вимірюють АТ, ЧСС та реєструють ЕКГ.
При пасивній ортостатичній пробі (тилт-тест) пацієнт після 20‑30-хвилинної адаптації в горизонтальному положенні за допомогою спеціального столу пасивно переміщується у напіввертикальне положення (60‑80°). Потім протягом 45 хв контролюють АТ, ЧСС і ЕКГ.
У здорових людей під час ортостатичної проби ЧСС зростає в середньому на 17%, а систолічний АТ знижується на 5‑10 мм рт. ст. (Аронов, Лупанов, 2002). Патологічна реакція при проведенні проби виявляється виразним зниженням АТ та неадекватною реакцією ЧСС (надмірне підвищення або поява тривалих пауз ритму).
Таким чином, лікар функціональної діагностики може використовувати в щоденній практичній роботі різноманітні функціональні тести з метою діагностики, зокрема диференціальної. Потрібно зважати на те, що кожен функціональний тест має певні обмеження. Результати бувають не лише позитивними чи негативними, але й хибнопозитивними або хибнонегативними, що може спричинити неправильні висновки та дії. З огляду на це, результати функціонального тесту потрібно зіставляти із клінічними даними та іншими діагностичними дослідженнями.