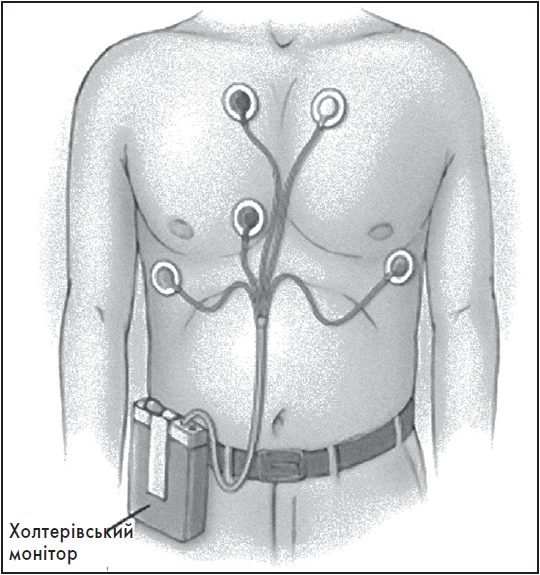
1 грудня, 2021
Амбулаторне моніторування електрокардіограми
Редакція медичної газети «Здоров’я України», тематичного номера «Кардіологія. Ревматологія. Кардіохірургія» продовжує знайомити наших читачів із ґрунтовним і детальним підручником «Функціональна діагностика» за редакцією д. мед. н., професора О.Й. Жарінова, д. мед. н., професора Ю.А. Іваніва та к. мед. н., доцента В.О. Куця. Пропонуємо до вашої уваги розділ «Амбулаторне моніторування електрокардіограми» ІІ частини «Функціональні проби. Амбулаторне моніторування ЕКГ і артеріального тиску».
 Одним із найпоширеніших і доступних сучасних методів функціональної діагностики є холтерівське (амбулаторне, добове) моніторування електрокардіограми (ХМ ЕКГ) – тривала реєстрація ЕКГ в умовах повсякденної активності пацієнта з подальшим аналізом отриманих даних. Метод названо на честь американського дослідника Нормана Холтера, який запровадив радіоелектрокардіографію і вперше здійснив тривалу реєстрацію ЕКГ.
Одним із найпоширеніших і доступних сучасних методів функціональної діагностики є холтерівське (амбулаторне, добове) моніторування електрокардіограми (ХМ ЕКГ) – тривала реєстрація ЕКГ в умовах повсякденної активності пацієнта з подальшим аналізом отриманих даних. Метод названо на честь американського дослідника Нормана Холтера, який запровадив радіоелектрокардіографію і вперше здійснив тривалу реєстрацію ЕКГ.
Основна ідея амбулаторної ЕКГ – збільшити тривалість та забезпечити можливість реєстрації ЕКГ в умовах звичайної добової активності пацієнта. Це дає змогу кардинально підвищити чутливість ЕКГ-методу в діагностиці порушень серцевого ритму і провідності. З огляду на поєднання неінвазивності та високої інформативності, можливостей використання у стаціонарних і амбулаторних умовах, ХМ ЕКГ широко застосовують для:
- діагностики порушень ритму та провідності серця, ішемічної хвороби серця (ІХС);
- оцінки ефективності лікування серцево-судинних захворювань.
У багатьох клінічних ситуаціях діагностичні можливості безперервного 24- або 48-годинного моніторування ЕКГ обмежені через фіксовану тривалість дослідження і нечасте виникнення клінічних симптомів. З огляду на це, значну увагу привертають також нові технології амбулаторного фрагментарного моніторування ЕКГ, які забезпечують:
- можливість необмеженого збільшення тривалості реєстрації сигналу ЕКГ;
- точнішу оцінку змін ЕКГ у момент виникнення клінічних симптомів;
- зворотний зв’язок лікаря і пацієнта.
Розглянемо можливості й обмеження амбулаторного моніторування ЕКГ порівняно з іншими методами діагностики аритмій серця та ІХС, методологічні аспекти дослідження й інтерпретації отриманих даних.
Еволюція холтерівського моніторування ЕКГ
Звичайна ЕКГ, знята на одноканальному електрокардіографі (не менш ніж чотири серцеві цикли у кожному відведенні), містить приблизно 50 комплексів PQRST, а тривалість реєстрації ЕКГ рідко перевищує одну хвилину. При ХМ ЕКГ запис здійснюється безперервно протягом 1440 хв, і для аналізу отримують близько 100 тис. комплексів QRS. Отже, тривалість спостереження за серцевою діяльністю при ХМ ЕКГ майже у 1500 разів більша, ніж при реєстрації звичайної ЕКГ.
На відміну від короткострокової реєстрації ЕКГ, тривале моніторування ЕКГ дозволяє (Crawford et al., 1999):
- Проаналізувати зв’язок аритмій та клінічної симптоматики, зокрема синкопальних станів.
- Виявити минущі порушення серцевого ритму в пацієнтів із відповідними клінічними симптомами.
- Зареєструвати моменти початку та припинення пароксизмів, що дозволяє визначати механізми виникнення аритмій і здійснювати диференціальну діагностику.
- Кількісно та якісно оцінити аритмії, що важливо для стратифікації ризику.
- Встановити залежність виникнення аритмій від недостатності коронарного кровопостачання.
- Кількісно оцінювати ефективність та безпеку медикаментозного лікування аритмій.
- Оцінити функціонування імплантованих пристроїв: електрокардіостимуляторів та кардіовертерів-дефібриляторів.
Однак не у всіх випадках ХМ ЕКГ – єдиний можливий метод розв’язання вказаних завдань. У багатьох клінічних ситуаціях для діагностики та оцінки порушень серцевого ритму достатньо здійснити запис ЕКГ у 12 відведеннях або нетривале моніторне спостереження. І навпаки, у певних категорій пацієнтів тривалість обстеження при ХМ ЕКГ недостатня через нечасте виникнення клінічних симптомів. Це зумовлює потребу в застосуванні тривалішого фрагментарного моніторування ЕКГ або «агресивніших» методів дослідження (як-то навантажувальні проби, черезстравохідне або внутрішньосерцеве електрофізіологічне дослідження, оцінка барорефлекторної чутливості, коронарографія тощо).
Удосконалення методу ХМ ЕКГ протягом уже понад 55 років переважно спрямоване на забезпечення зручності обстеження, покращання якості запису, збільшення кількості відведень та тривалості дослідження, доповнення алгоритмів автоматичного аналізу додаткових параметрів, забезпечення можливості передачі сигналу ЕКГ телефоном або через мережу інтернет тощо. Замість радіореєстратора масою 40 кг, який закріплювався на спині хворого, наразі використовують сучасні реєстратори з цифровими носіями інформації, масу яких уже зменшено до 80‑100 грамів. Об’єм інформації на дискових реєстраторах вимірюється вже десятками гігабайтів.
На додачу, зменшилася кількість артефактів, викликаних фізичною активністю хворого та впливом різноманітних електромагнітних полів. З’явилася можливість одночасної реєстрації кількох (за потреби – 12) відведень, що підвищує інформативність ХМ ЕКГ у діагностиці ІХС та деяких порушень серцевого ритму. Тривалість реєстрації сигналу в сучасних системах моніторування ЕКГ збільшилася від 24 год до кількох років (із використанням імплантованих пристроїв). Збільшення тривалості дослідження дозволяє оцінити умови виникнення багатьох порушень ритму, їх особливості, а також ЕКГ-феномени, які з’являються при відновленні ритму, що важливо для визначення лікувальної тактики.
Окремими напрямами тривалого моніторування ЕКГ є кількісна характеристика циркадних коливань частоти серцевих скорочень (ЧСС) і аритмій серця, показників варіабельності серцевого ритму (ВСР), відхилень сегмента ST, оцінка функції електрокардіостимулятора, тривалості та коливань корегованого інтервалу QT. Важливим кроком на шляху еволюції методу стало поліфункціональне моніторування, при якому, крім ЕКГ, реєструють рівень артеріального тиску (АТ) та інші фізіологічні параметри.
Методика холтерівського моніторування ЕКГ
Пристрій для ХМ ЕКГ повинен забезпечити:
- тривалий запис ЕКГ в умовах звичайної добової активності хворого;
- відтворення зареєстрованих сигналів;
- обробку та інтерпретацію отриманих даних.
Більшість сучасних систем ХМ ЕКГ складаються з реєстратора, відтворювального та аналізувального пристроїв. Реєстратор прикріплюється до тіла обстежуваного на весь період моніторування і живиться енергією акумуляторних батарей. Найчастіше в реєстраторі міститься знімний носій інформації, на який здійснюється запис ЕКГ. У сучасних системах ХМ ЕКГ носієм інформації переважно є флеш-карта (цифровий режим реєстрації сигналу). На більшості реєстраторів є кнопка для пацієнта, так званий маркер події, на яку обстежуваний натискає у разі появи певних симптомів. Реєстратори містять вмонтований калібратор мілівольта та кварцовий годинник. Після закінчення реєстрації дані переносяться на комп’ютер зі спеціальними програмами для обробки та інтерпретації сигналу ЕКГ.
Безпосередній контакт реєстратора з тілом пацієнта здійснюється за допомогою електродів. У електродах для середнього і тривалого спостереження використовується основа зі спіненого поліетилену, що забезпечує непроникність поля контакту для інших рідин. Основними компонентами гелю є вода і хлорид калію. Для добового спостереження можна застосовувати гель із більшим ступенем плинності, яким просочується мікропориста губка з поролону. Для тривалого спостереження краще застосувати желеподібний гель. Якщо на шкірі обстежуваного в місцях планованого накладання електродів є волосяний покрив, його потрібно ретельно зголити. Далі шкіру пацієнта слід обробити 70% спиртом або ацетоном і протерти спеціальною губкою чи абразивною пастою з метою знежирення. Це забезпечить зменшення опору шкіри, що покращить якість запису та запобігатиме відставанню електрода під час рухової активності обстежуваного.
Для оптимальної реєстрації ЕКГ опір між електродами і шкірою обов’язково має бути однаковий у всіх відведеннях під час моніторування, тому потрібно використовувати електроди лише одного типу. Електроди з’єднуються з реєстратором за допомогою спеціальних екранованих проводів, довжина яких повинна становити не менш ніж 85‑95 см. При встановленні реєстратора проводи потрібно прикріпити пластирем до тіла пацієнта у вигляді петлі. Це забезпечить кращу амортизацію натягу електродів при рухах. Якщо обстежуваний під час своєї звичайної добової активності перебуває у спекотних приміщеннях, усі електроди потрібно додатково закріпити широкою смужкою пластиру. Пацієнта варто попросити перед сном надягнути тісну натільну білизну.
Для ХМ ЕКГ застосовують двополюсні відведення. Із двох електродів один є активним (+), інший – пасивним (–). Накладати електроди на тіло пацієнта потрібно в місцях, де не розташовані великі групи м’язів, щоб уникнути деформації сигналу під час звичайної активності, тремтіння м’язів та дихальних рухів. Окрім кількох пар реєструвальних електродів, при моніторуванні завжди використовують ще один, «нульовий» електрод, який прикріплюють у правій епігастральній ділянці; він дозволяє зрівноважити потенціали між реєстратором та тілом пацієнта.
Кількість відведень, яку застосовують при моніторуванні ЕКГ, залежить від технічних можливостей пристрою та мети обстеження. До 1990-х рр. запис був можливим лише в одному відведенні. Сьогодні найчастіше здійснюють запис ЕКГ у двох або трьох відведеннях, хоча вже розроблені пристрої для реєстрації ЕКГ у 12 і навіть більше відведеннях. При ХМ ЕКГ найчастіше використовують модифіковані грудні відведення CS‑1 i CM‑5 (рис. 1).
Рис. 1. Позиції електродів при реєстрації грудних відведень CS‑1 i CM‑5
Запис, зареєстрований у відведенні СМ‑5 (негативний електрод у правій підключичній ділянці, позитивний – у позиції V5), приблизно відповідає ЕКГ у V5, іноді також – у ІІ стандартному відведенні. У цьому відведенні найкраще видно зубець R, який у нормі вищий, ніж Т. У відведенні СМ‑5 також добре видно зміни сегмента ST, які відображають порушення процесів реполяризації в передньобічній ділянці лівого шлуночка (ЛШ).
Відведення СS‑1 (негативний електрод у лівій підключичній ділянці, позитивний – у позиції V1) відповідає відведенню V1. У цьому відведенні добре візуалізується зубець Р, що має значення у виявленні надшлуночкових аритмій (Дабровскі та співавт., 2000). Це відведення важливе також для аналізу порушень внутрішньошлуночкової провідності.
Для ХМ ЕКГ використовують й інші відведення:
СМ‑2: (–) ліва підключична ділянка, (+) позиція V2;
СМ‑3: (–) ліва підключична ділянка, ближче до груднини, (+) позиція V3;
IS: (–) ліва підключична ділянка, (+) лівий кульшовий суглоб;
відведення, які відтворюють триосьову систему Франка:
– X: (–) позиція V6R, (+) позиція V6;
– Y: (–) верхня частина груднини, (+) мечоподібний відросток;
– Z: (–) позиція V8R, (+) позиція V1 або V2;
відведення за Небом:
D: (–) друге міжребер’я справа, (+) позиція V7;
A: (–) друге міжребер’я справа, (+) позиція V4;
I: (–) позиція V7, (+) позиція V4.
Загалом із метою діагностики порушень ритму достатньо двох відведень, осі яких перетинаються під прямим кутом або є близькими до цього. Водночас для діагностики ішемії міокарда потрібно використовувати не менш ніж три відведення, які могли б якомога повніше відображати хід процесів реполяризації у стінках міокарда ЛШ.
Після встановлення електродів здійснюють функціональну пробу, яка дозволяє перевірити якість контакту електродів із тілом пацієнта. На монітор комп’ютера виводять ЕКГ, яка послідовно записується в різних положеннях тіла пацієнта: стоячи, сидячи, лежачи на спині, на боці та під час глибокого дихання. Ця процедура дозволить при подальшому аналізі відрізнити позиційні відхилення сегмента ST від ішемічних.
У сучасній клінічній практиці ХМ ЕКГ є одним із ключових методів діагностики порушень ритму і провідності серця. Для виявлення більшості аритмій достатньо 24-годинного періоду моніторування. Для діагностики порушень ритму, які трапляються з періодичністю 1‑2 рази на місяць і частіше, але не щодня, слугують реєстратори із фрагментарним режимом запису. Вони активуються обстежуваним у момент виникнення певних симптомів. Існують також пристрої, які ведуть запис постійно, але зберігають у пам’яті лише ділянки ЕКГ, пов’язані з активацією кнопки – маркера події. Вибіркове моніторування ЕКГ може тривати протягом 30‑40 діб.
Зазначимо, що за умов широкого застосування коронарографії та методів оцінки перфузії міокарда користь ХМ ЕКГ для діагностики ІХС обмежується лише окремими клінічними ситуаціями.
Під час процедури ХМ ЕКГ хворі обов’язково ведуть запис усіх подій та відчуттів, які у них з’являються. Важливо вказати:
- Види занять (як-то сон, лікувальні процедури, прогулянка, водіння автомобіля, фізичне навантаження, стрес).
- Суб’єктивні відчуття (біль, задишка, серцебиття, запаморочення, слабкість, неприємні відчуття у грудній клітці); при виникненні болю потрібно вказати його характер (стискаючий, колючий, пекучий, ниючий, тупий), локалізацію, іррадіацію та тривалість, а також обставини, за яких біль виник і припинився.
- Застосування ліків (назва, доза препарату і час приймання).
- Точний час початку і закінчення суб’єктивних відчуттів та видів діяльності.
Після завершення обстеження вся інформація переноситься на комп’ютер, де відтворюється за допомогою спеціальних програм. Здійснюються аналіз серцевого ритму та ідентифікація подій, зокрема екстрасистол, епізодів тахі- та брадіаритмій, ішемічних змін сегмента ST. Основа аналізу ЕКГ – ідентифікація нормального комплексу QRS та інтервалів RR. Диференціацію комплексів QRS шлуночкового походження і артефактів від комплексів надшлуночкового походження виконують за «коефіцієнтом ширини», який являє собою співвідношення площі комплексу до довжини його контура. Коефіцієнт ширини найбільший у комплексах QRS шлуночкового походження, проміжний – у надшлуночкових комплексах, найменший – у випадку артефактів (рис. 2).
Для виявлення екстрасистол при автоматичній обробці сигналу ЕКГ використовують також коефі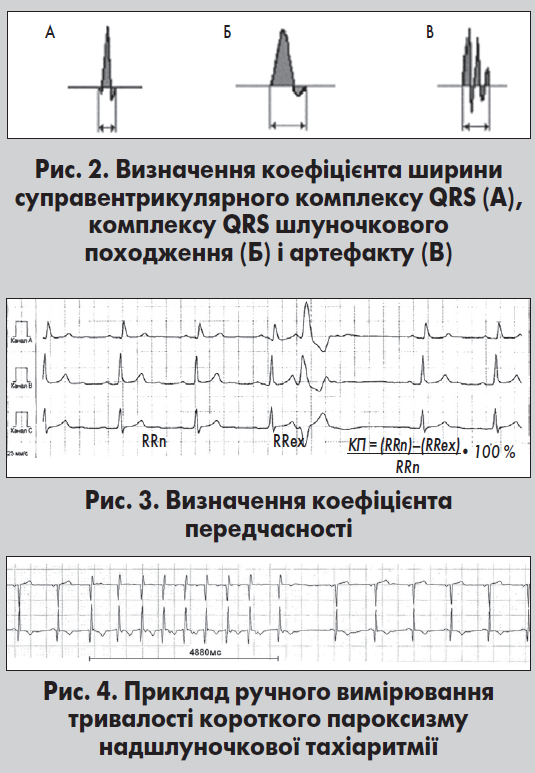 цієнт передчасності (КП) – відношення різниці між базовим (RRn) і передекстрасистолічним інтервалом RR (RRex) до базового інтервалу RR (рис. 3). Скорочення вважають передчасним, якщо цей показник перевищує 20%.
цієнт передчасності (КП) – відношення різниці між базовим (RRn) і передекстрасистолічним інтервалом RR (RRex) до базового інтервалу RR (рис. 3). Скорочення вважають передчасним, якщо цей показник перевищує 20%.
Будь-яке виявлене відхилення ритму або процесів реполяризації обов’язково виноситься комп’ютером для розгляду дослідником. Критерії, які використовують для інтерпретації даних ХМ ЕКГ, істотно відрізняються від таких оцінки звичайної ЕКГ у спокої. Зокрема, у стандартному протоколі аналізу даних ХМ ЕКГ застосовують такі визначення: брадикардія – ЧСС <60/хв, тахікардія – ЧСС >120/хв, пауза – інтервал RR >2000 мс, тривалість розширеного комплексу QRS >120 мс, коефіцієнт передчасності екстрасистоли – понад 20%, поріг зміщення сегмента ST >0,1 мВ, відстань від точки J для оцінки глибини депресії сегмента ST – 60 мс після комплексу QRS, мінімальна тривалість окремого епізоду відхилення сегмента ST – 60 c.
При аналізі можуть використовуватися також додаткові протоколи обробки, наприклад, для ЕКГ із постійно розширеним комплексом QRS при повній блокаді ЛНПГ. Сучасні програми обробки даних ХМ ЕКГ забезпечують можливість мануального (ручного) вимірювання тривалості інтервалів і сегментів комплексу PQRST, а також оцінки тривалості пауз та коротких пароксизмів тахікардії (рис. 4).
Лікар ознайомлюється з результатами автоматичного аналізу і здійснює контрольний перегляд виділених комп’ютером подій. У разі потреби він виконує корекцію результатів автоматичного аналізу, оскільки при ідентифікації подій комп’ютерною програмою можливі помилки. За наявності великої кількості артефактів дослідник має приділити увагу відокремленню їх від істинних порушень ритму. Тільки після видалення всіх артефактів можлива правильна якісна і кількісна оцінка порушень ритму. Пізніше дані моніторування порівнюються із суб’єктивними відчуттями хворого, тривалістю та інтенсивністю фізичних навантажень й іншими видами життєдіяльності, занесеними у щоденник.
Основні показники серцевого ритму в нормі
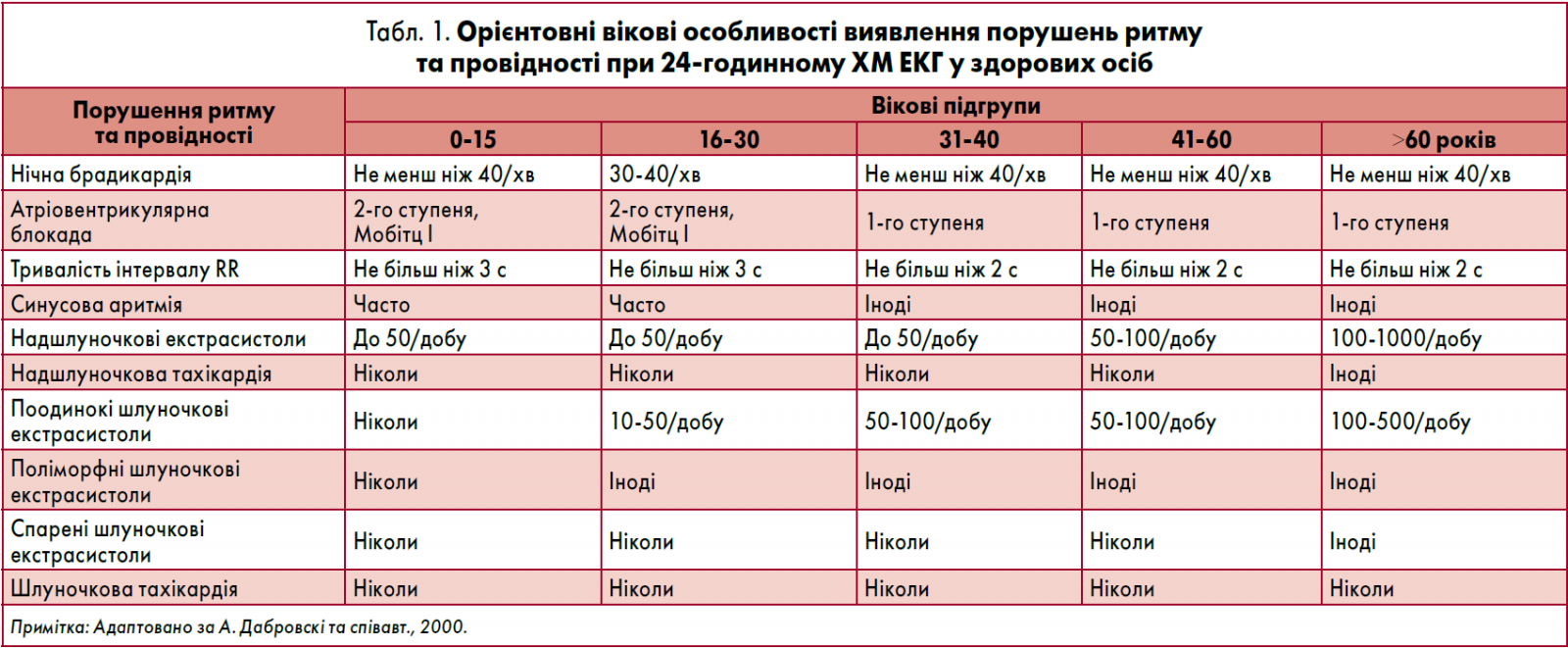
Єдиних нормативів для оцінки показників серцевого ритму у здорових людей на цей час не існує. Протягом доби майже у всіх обстежуваних спостерігаються відхилення від тих величин, які вважаються нормою при аналізі звичайної ЕКГ (табл. 1). Під час фізичних навантажень ЧСС може значно перевищувати показник 90‑100/хв і навіть досягати 150‑200/хв, а під час глибокого сну, особливо у тренованих молодих людей і спортсменів, – знижуватися до ≤40/хв (Макаров, 2003).
Частою знахідкою при аналізі добової ЕКГ є поодинокі надшлуночкові та шлуночкові екстрасистоли. Вночі, при підвищеній активності блукаючого нерва, можуть спостерігатися міграція водія ритму в передсердях та паузи між сусідніми серцевими скороченнями тривалістю до 2 с (Макаров, 2003). У здорових дітей і підлітків частими знахідками при ХМ ЕКГ є атріовентрикулярна (АВ) блокада І ступеня та епізоди АВ-блокади ІІ ступеня 1-го типу, особливо під час сну. Інколи у здорових осіб уночі спостерігаються епізоди синоатріальної (СА) блокади ІІ ступеня 1-го типу.
Загалом частота синусового ритму у здорових осіб може коливатися протягом доби в діапазоні від 40 до 180 за хвилину. Для диференціації фізіологічних і патологічних змін ЧСС враховують показники середньої, мінімальної та максимальної ЧСС за 24 год і в різні періоди доби (вдень – в активний та вночі – у пасивний період), а також під час виконання фізичних навантажень.
Середня ЧСС у нормі становить:
- в активний період доби – 70‑100/хв;
- під час сну – 55‑70/ хв.
У здорових молодих людей, спортсменів, а також інших осіб, які регулярно виконують значні фізичні навантаження, показники ЧСС у різні періоди доби можуть бути меншими. Крім того, в чоловіків ЧСС у різний час доби в нормі дещо нижча, ніж у жінок.
Рівень фізичного навантаження під час ХМ ЕКГ істотно нижчий, ніж при здійсненні навантажувальних проб. Якщо до протоколу ХМ ЕКГ спеціально вводять інтенсивні навантаження (ходьбу сходами), три чверті здорових осіб досягають 70% від максимальної ЧСС. Таким чином, нездатність до підвищення ЧСС до бажаного рівня набуває діагностичного значення. Нерідко максимальної, а також субмаксимальної ЧСС тяжко досягти у пацієнтів старших вікових груп. У цих випадках оцінюють ЧСС, досягнуту на тлі повсякденної фізичної активності. В нормі вона повинна становити не менш як 90‑100/хв.
За наявності брадикардії підрахунок ЧСС потрібно здійснювати за 10 с, інколи – навіть за 1 хв. Наголосимо, що паузи тривалістю до 1,5 с спостерігаються у 31‑68% здорових осіб, 1,5‑2 с – у 25%, понад 2 с – у 1‑4% здорових молодих чоловіків.
Співвідношення величин середньої ЧСС в активні та пасивні години називається циркадним індексом. У нормі цей показник становить від 1,22 до 1,45 (Malik, Camm, 1995; Дабровскі та співавт., 2000; Макаров, 2013). Зменшення циркадного індексу характерне для багатьох хвороб, які асоціюйовані з порушеннями вегетативної іннервації серця, наприклад інфаркту міокарда (ІМ), хронічної серцевої недостатності (СН), цукрового діабету. Показник циркадного індексу може також знижуватися при стійкій синусовій брадикардії, яка зберігається протягом усієї доби, зокрема на тлі синдрому слабкості синусового вузла, або стійкій синусовій тахікардії, зумовленій підвищенням тонусу симпатичної нервової системи. При цьому підвищення циркадного індексу відображає збільшення чутливості Р-клітин синусового вузла до симпатоадреналових впливів.
Така ситуація може спостерігатися як унаслідок підвищення симпатичного тонусу в активний період доби, так і виразної ваготонії у пасивний (ваготонічної дисфункції синусового вузла). Диференціація вказаних феноменів, яку здійснюють за показниками середньої ЧСС у різні періоди доби, важлива для вибору оптимального лікування.
У багатьох здорових осіб під час ХМ ЕКГ спостерігається синусова аритмія – синусовий ритм із коливаннями тривалості послідовних інтервалів RR більш ніж на 15%. Синусова аритмія характерніша для молодих людей, ніж осіб похилого віку. При коливаннях тривалості послідовних інтервалів RR >50% потрібно проводити диференціальну діагностику із СА-блокадою ІІ ступеня 1-го типу, а 100% і більше – із СА-блокадою ІІ ступеня 2-го типу або зупинкою синусового вузла. При цьому зважають на інші ЕКГ-ознаки порушень СА-провідності. Більш ніж у половини здорових осіб уночі спостерігається міграція водія ритму в передсердях. Водночас міграцію водія ритму до АВ-вузла розглядають як патологічну.
Незважаючи на можливість реєстрації порушень ритму в здорових осіб, факт виявлення деяких аритмій під час ХМ ЕКГ не дозволяє вважати пацієнта здоровим, навіть за повної відсутності скарг. Такими аритміями є шлуночкова тахікардія, надшлуночкові тахікардії, фібриляція/тріпотіння передсердь, паузи тривалістю більш як 2,5‑3 с, епізоди АВ-блокади ІІ ступеня 2-го типу або ІІІ ступеня, епізоди зупинки синусового вузла, активного або пасивного передсердного, вузлового та ідіовентрикулярного ритмів. При виявленні цих аритмій пацієнти потребують подальшого обстеження та відповідного лікування.
Дослідження варіабельності серцевого ритму
Чутливим відображенням впливів вегетативної нервової системи (ВНС) на роботу серця є оцінка варіабельності серцевого ритму (ВСР) – вираження коливань частоти серцевого ритму навколо її середнього рівня. Усі методи аналізу ВСР поділяються на три групи (Бобров та співавт., 1999):
- дослідження загальної ВСР (часовий аналіз);
- дослідження періодичних складових ВСР (спектральний аналіз);
- геометричні методи аналізу ВСР.
Основа часового аналізу ВСР – статистична оцінка змін тривалості послідовних інтервалів RR (або NN – normal-to-normal), які відбуваються протягом певних проміжків часу. Зокрема, ступінь коливань ЧСС протягом невеликих проміжків часу найкраще оцінювати за показниками rMSSD (корінь квадратний із суми квадратів різниць величин послідовних пар інтервалів RR, мс) та pNN50 (відсоток сусідніх синусових інтервалів RR, які відрізняються більш ніж на 50 мс, %). Вважають, що ці показники переважно визначаються активністю парасимпатичного відділу ВНС та відображають ступінь виразності синусової аритмії.
Для оцінки повільніших коливань ЧСС найпоширенішим є показник SDNN (стандартне відхилення середньої тривалості всіх інтервалів RR, мс), який залежить від активності парасимпатичного і симпатичного відділів ВНС та характеризує вегетативний баланс загалом. Оцінка SDNN не дозволяє диференціювати вплив окремих компонентів ВНС. Значення SDNN залежить від тривалості моніторування ЕКГ. Згідно з узгодженими міжнародними рекомендаціями, найкраще відтворюваним та найбільш цінним є показник SDNN протягом 24 год.
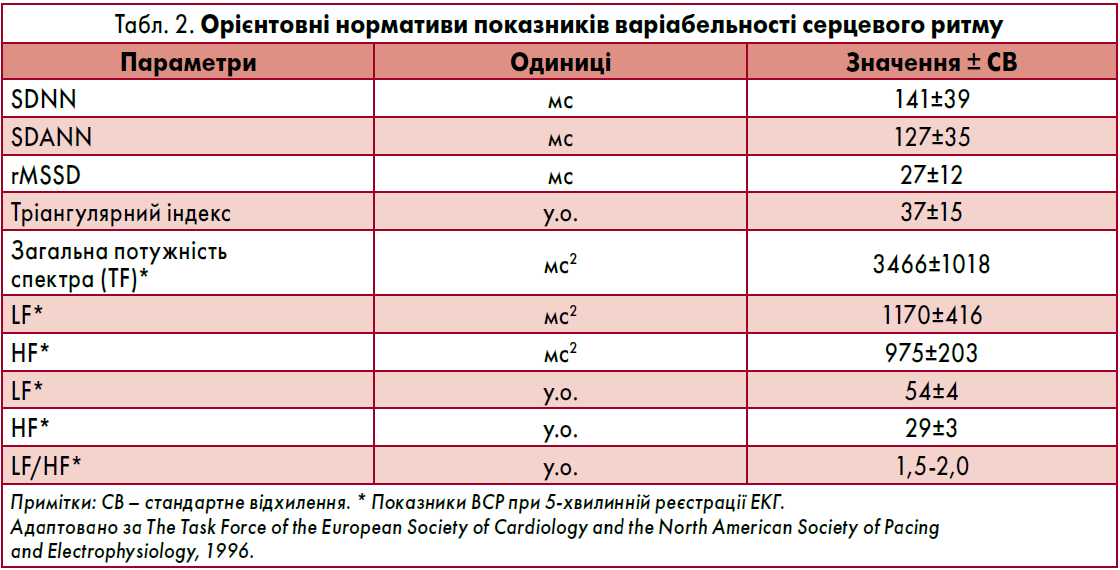
Використовують також інші стандартизовані показники ВСР: SDANN (стандартне відхилення середньої тривалості інтервалів RR протягом 5-хвилинних інтервалів, мс) (рис. 5) та SDNNindex (середнє зі стандартних відхилень середніх значень тривалості інтервалів RR протягом 5-хвилинних інтервалів, мс) (табл. 2).
Фізіологічна суть зазначених показників подібна, але має окремі відмінності. Їх переважне застосування залежить від тривалості оцінки ВСР. Зокрема, ступінь коливань ЧСС за короткі проміжки часу найкраще оцінювати за допомогою показників rMSSD та pNN50. Вони відображають вплив парасимпатичного відділу ВНС і ступінь виразності синусової аритмії. Втім відтворюваність цих показників низька.
Очевидно, для оцінки ризику краще підходять показники SDNN, SDNN-індекс і SDАNN протягом 24 год. Це інтегральні значення ВСР, які залежать від активності обох відділів ВНС і характеризують стан вегетативної регуляції загалом. Збільшення або зменшення даних показників свідчить про зміщення вегетативного балансу в бік переважання одного з відділів ВНС. Найчастіше про підвищений ступінь ризику свідчить зниження часових показників ВСР, що вказує на послаблення активності парасимпатичного відділу ВНС і зменшення «захисту» серця від виникнення життєво небезпечних аритмій.
Спектральний аналіз ВСР дає змогу диференціювати активність відділів ВНС. Високочастотний компонент спектра (HF) пов’язаний із фазами дихання і переважно відображає активність парасимпатичного відділу ВНС. Про це свідчить різке зниження потужності HF на тлі введення атропіну. Зміни частоти серцевого ритму у зв’язку з фазами дихання тісно пов’язані з функціонуванням барорефлекторної системи стабілізації АТ. Екскурсія грудної клітки та діафрагми при диханні зумовлює коливання тиску в грудній порожнині, що веде до зменшення серцевого викиду на вдиху і збільшення – на видиху, з відповідними коливаннями АТ. Зміни ЧСС є одним із механізмів забезпечення стабільності рівня АТ. У хворих після ІМ спостерігали тісний зв’язок амплітуди HF із показниками rMSSD і pNN50.
Значно складніше здійснювати інтерпретацію низькочастотного компонента ВСР (LF). Відомо, що повільні коливання мають змішане походження і відображають активність обох відділів ВНС. І хоча при підвищенні тонусу симпатичного відділу ВНС зростає потужність LF, у пацієнтів із тяжкою СН на тлі виразної симпатичної активації потужність LF істотно знижується. Вказані зміни можуть свідчити про втрату чутливості синусового вузла до впливів ВНС – «вегетативну денервацію серця», яка формується разом із посиленням СН. Потужність LF залежить від активності механізму підтримання барорефлексу.
Втім найціннішим показником вважають співвідношення LF і HF, яке відображає баланс активності симпатичного і парасимпатичного відділів ВНС. У хворих на СН вказаний показник значно залежить від чутливості адренорецепторів. Отже, збільшення в динаміці відношення LF/HF на тлі лікування може розглядатися як ознака покращення функціонального стану серцевого м’яза, причому нерідко в тих випадках, коли він виходить за межі рекомендованої «норми».
Припускають, що коливання ЧСС, які відбуваються з дуже низькою та ультранизькою частотою (VLF i ULF), пов’язані з процесами терморегуляції та насамперед відображають активність симпатичного відділу ВНС. Їх потужність може визначатися гуморальними впливами на синусовий вузол, тонусом вищих симпатичних центрів та ренін-ангіотензинової системи.
Зокрема, VLF – потужність хвиль дуже низької частоти (0,0033‑0,04 Гц). Фізіологічний зміст цього показника невідомий. Очевидно, він відображає активність «повільно діючих» гуморальних механізмів регуляції серцевого ритму, які зумовлюють закономірні зміни ЧСС протягом тривалих проміжків часу (дні, тижні).
ULF – потужність хвиль ультранизької частоти (до 0,0033 Гц). Цей показник може бути пов’язаний із коливаннями ЧСС протягом дуже тривалих періодів (місяці, пори року). Його відтворюваність оцінити проблематично, а чітких критеріїв норми і патології до цього часу не розроблено.
TF – загальна потужність спектра. Оскільки ТF є сумою всіх компонентів спектра, його фізіологічна суть не відрізняється від такої показника SDNN. Утім, відтворюваність ТF більше залежить від якості сигналу ЕКГ та наявності порушень серцевого ритму (рис. 6).
Серед графічних методів аналізу ВСР найпоширенішим у сучасних холтерівських системах є тріангулярний індекс. Його визначають як відношення загальної кількості інтервалів RR між синусовими комплексами до кількості інтервалів, які потрапили в діапазон моди. Гістограму розподілу інтервалів RR будують на шкалі з кроком 1/128 с. Тріангулярний індекс відображає ВСР загалом упродовж 24 год і нагадує за фізіологічним змістом SDNN. У нормі значення тріангулярного індексу становить 37±15 одиниць.
Останнім часом у холтерівських системах застосовують також метод скатерограми (scatter – розсіювання). Його суть полягає в побудові графічного зображення точок, кожна з яких відповідає тривалості двох сусідніх інтервалів RR. При цьому ордината точки відповідає поточному, а абсциса – наступному інтервалу RR (рис. 7). Цей метод дозволяє уникнути впливу аритмій серця, коли часовий та спектральний аналізи ВСР малоінформативні.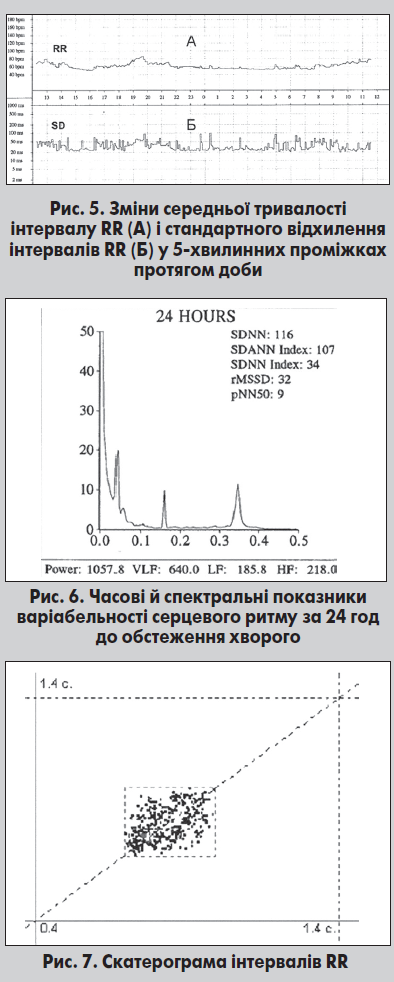
Загалом перевагою геометричних методів аналізу ВСР є можливість візуалізації усього масиву інтервалів RR, що дозволяє відокремити порушення ритму, провідності та артефакти сигналу ЕКГ. Але, по суті, вказані методики є лише новим способом графічного відображення коливань ЧСС і не дозволяють отримати принципово нової діагностичної інформації.
В узгоджених рекомендаціях наведено орієнтовні нормативи часових і спектральних показників ВСР, визначені на підставі обстеження здорових осіб (див. табл. 2). Оскільки ці значення істотно відрізняються від характерних для осіб із високим ступенем ризику, виникає питання щодо інтерпретації «межових» рівнів ВСР.
Інше обмеження стосується спектральних параметрів ВСР, норми яких визначені лише для 5-хвилинних проміжків часу в положенні лежачи. Добре відомо, що амплітуда компонентів спектра та їх співвідношення при зміні положення тіла є іншими. Отже, «за визначенням», спектри 5-хвилинної ЕКГ не можуть адекватно відобразити повільні коливання ЧСС і бути добре відтворюваними. У чинних стандартах нормативів спектральних показників ВСР за добу не вказано.
Оскільки великих досліджень із вивчення ВСР у популяції не здійснювали, наведені нормативи показників ВСР можна розглядати лише як орієнтовні. Слід враховувати, що на значення ВСР впливають:
- вік;
- стать;
- маса тіла;
- конституційний тип;
- психічний статус;
- циркадні коливання фізіологічних параметрів.
Найімовірніше, показники ВСР найбільш інформативні для оцінки стану вегетативної регуляції серцевого ритму в ситуаціях, коли їх значення нижчі від порогових рівнів, встановлених у здорових осіб. У цьому разі зниження часових показників ВСР дозволяє припускати наявність вегетативного дисбалансу з послабленням активності парасимпатичного відділу ВНС. Водночас аналіз спектральних показників ВСР має перспективу при оцінюванні в динаміці у конкретного пацієнта, наприклад, на тлі лікування СН.
Основний лейтмотив дослідження ВСР полягає у підвищенні точності оцінки прогнозу хвороби серця та ефективності терапії. З цих позицій дослідження ВСР найбільш інформативне в пацієнтів зі структурною хворобою серця, зокрема після перенесеного ІМ або із СН. В інших категорій хворих на кардіологічну та екстракардіальну патологію переконливих доказів прогностичної цінності показників ВСР дотепер не отримано. Крім того, лише окремі показники ВСР використовували для стратифікації ризику, що дозволяє припустити недоцільність збільшення обсягу дослідження ВСР із цією метою.
Зниження часових показників ВСР зазвичай розглядають як маркер послаблення парасимпатичного «захисту» серця. В осіб із гострим ІМ самостійним критерієм підвищеного ризику смерті вважають зменшення SDNN ˂50 мс (Umetani et al., 1997). У дослідженні ATRAMI встановили незалежне прогностичне значення показника SDNN менш ніж 70 мс для передбачення раптової серцевої смерті, а поєднана оцінка SDNN та фракції викиду ЛШ і барорефлекторної чутливості дозволила точніше ідентифікувати групи пацієнтів із високим ризиком у післяінфарктному періоді. Поєднання низької фракції викиду ЛШ (˂35%) із SDNN менш ніж 70 мс достовірно (у 6,7 раза) збільшувало ймовірність серцевої смерті.
На додачу до прагматичних міркувань, пов’язаних із користю отриманої інформації для вибору певного виду лікування, варто зважати також на обмежену специфічність показників ВСР. Адже крім ступеня тяжкості хвороби серця, вони суттєво залежать від віку, конституційних особливостей, психічного статусу, тривалості реєстрації ЕКГ, наявності аритмій та багатьох супутніх захворювань. Не дивно, що в рекомендаціях щодо ведення пацієнтів зі шлуночковими порушеннями ритму і профілактики раптової серцевої смерті американські та європейські експерти обмежили характеристику доцільності дослідження ВСР класом ІІа та рівнем доказовості В (Zipes et al., 2006).
Зміни показників ВСР залишаються одним із «сурогатних» критеріїв ефективності медикаментозної терапії серцево-судинних та інших хвороб. Зокрема доведено, що при успішному тромболізисі та відновленні прохідності інфарктзалежної вінцевої артерії збільшуються показники SDNN і HF. Сприятливі зміни значень ВСР показані також на тлі застосування β-адреноблокаторів та інгібіторів ангіотензинперетворювального ферменту в осіб із СН. В окремих випадках оцінка цих показників у динаміці корисна, оскільки дозволяє об’єктивізувати підсумки проведеної терапії.
Таким чином, на цей час оцінка ВСР залишається реальним компонентом стратифікації ризику в пацієнтів із післяінфарктною дисфункцією ЛШ і СН зі збереженим синусовим ритмом, інструментом оцінки ефективності медикаментозної терапії цих захворювань. Зміни показників ВСР також відображають ступінь виразності вегетативного дисбалансу та є додатковим критерієм визначення тяжкості СН. Утім клінічну інтерпретацію значень ВСР потрібно здійснювати з урахуванням даних інших інструментів обстеження, передусім щодо структурно-функціонального стану міокарда. При використанні цього методу з метою стратифікації ризику обсяг дослідження може бути обмежений найбільш інформативними показниками ВСР за 24 год, такими як SDNN і SDАNN, а також співвідношення LF/HF.
Продовження читайте у наступному номері