18 грудня, 2021
Енісамію йодид: результати 15 років закордонних і вітчизняних досліджень
Респіраторні віруси роблять серйозний внесок у показники захворюваності та смертності в усьому світі. Додаткову занепокоєність зумовлює одночасна циркуляція серед населення декількох респіраторних вірусів, включаючи вірус грипу групи В, різні підтипи вірусу групи А (наприклад, H3N2 і H1N1), аденовіруси, віруси парагрипу, респіраторно-синцитіальні віруси (RSV), а в останні роки і новий коронавірус – SARS-CoV‑2. Всі зазначені віруси здатні швидко поширюватися серед людей, спричиняти тяжкі захворювання та зумовлювати вторинні ускладнення. Крім того, нові штами респіраторних вірусів можуть передаватися до людини від тварин-носіїв (переважно дикі птахи та кажани), зумовлюючи серйозні епідемічні спалахи. Традиційні противірусні препарати в таких випадках є малоефективними, а розробка відповідних вакцин потребує досить тривалого часу. Як людство може протидіяти цим викликам?
Спробуємо надати відповіді на ці запитання в цьому огляді.
Віруси грипу
Традиційними противірусними препаратами, здатними протидіяти інфекції, спричиненій вірусами грипу, є два представники класу інгібіторів вірусної нейрамінідази – озельтамівір і занамівір, які вважаються ефективними за умови застосування в перші дні захворювання. Втім, резистентність вірусів грипу до інгібіторів нейрамінідази невпинно зростає. Наразі існує гостра потреба в розробці нових противірусних засобів, які могли б ефективно боротися з грипом. Сьогодні пошук науковців спрямований на створення та вивчення противірусної ефективності сполук, здатних впливати на вірусні білки.
! У поле зору науковців потрапив енісамію йодид, що використовується в клінічній практиці з 1997 року та продемонстрував ефективність у лікуванні гострих респіраторних вірусних інфекцій (рис. 1).
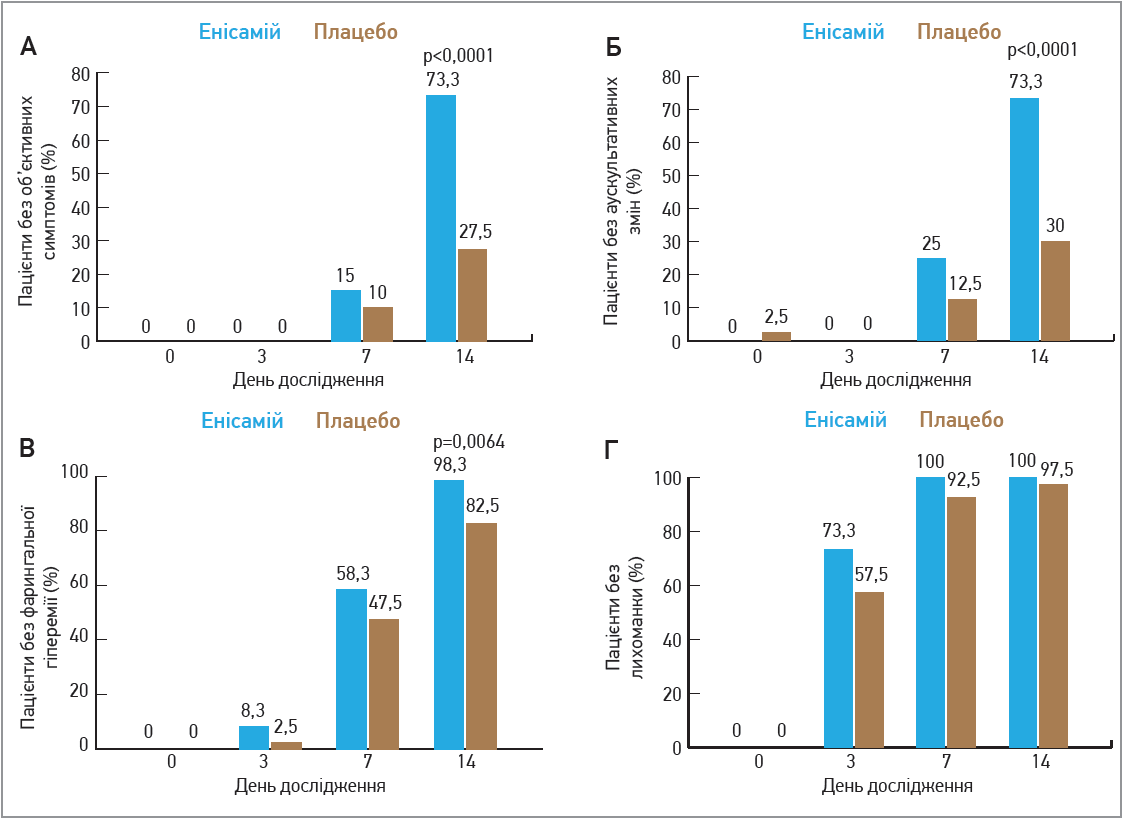
Рис. 1. Лікування енісамієм зменшує об’єктивні симптоми в пацієнтів із вірусним респіраторним захворюванням
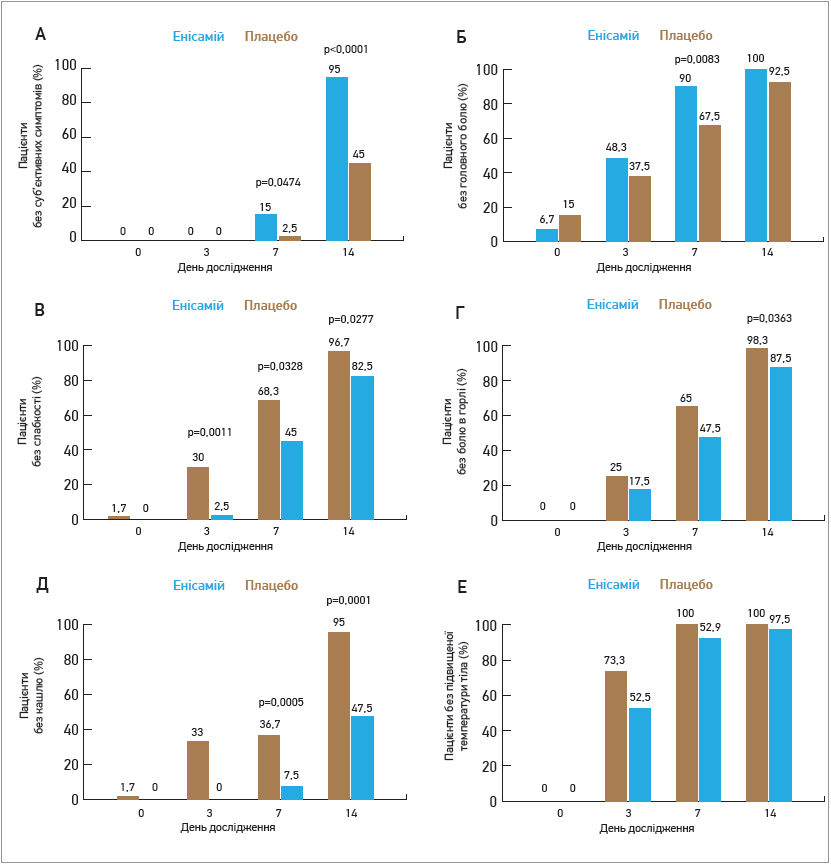
Рис. 2. Лікування енісамієм зменшує суб’єктивні симптоми в пацієнтів із вірусним респіраторним захворюванням
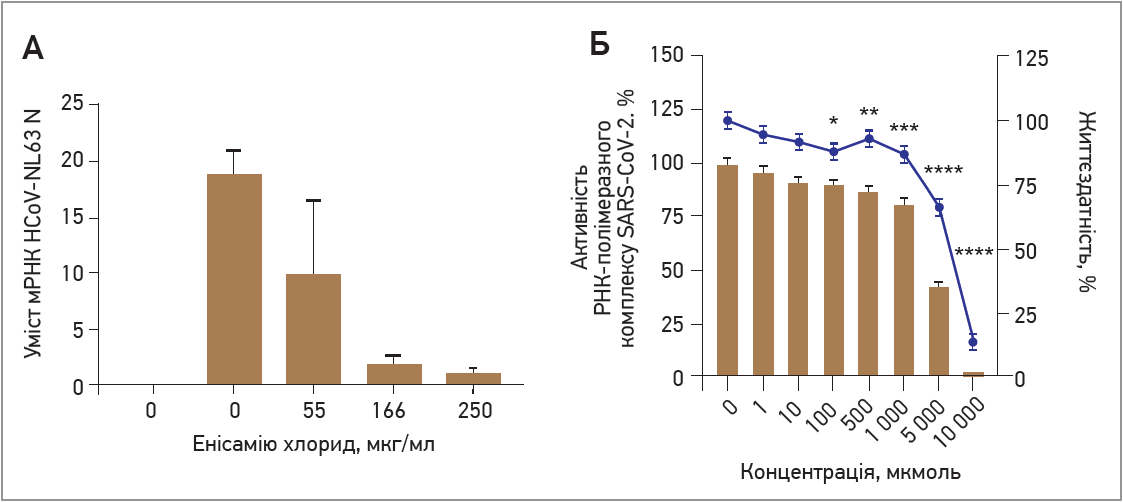
Рис. 3. Енісамій пригнічує вірусну інфекцію HCoV-NL63 в нормальних бронхоепітеліальних клітинах людини й активність SARS-CoV‑2 nsp12/7/8 in vitro
Однак донедавна ці результати не були підкріплені експериментальними даними. Дослідити це питання взялися D. Boltz і співавт. (2018) на експериментальній моделі нормальних бронхоепітеліальних клітин людини.
Енісамій додавали до диференційованих нормальних бронхоепітеліальних клітин людини за 24 год до інокуляції підтипів вірусів грипу А та В. Виявилося, що у випадку зараження оброблених клітин вірусами грипу не спостерігалося характерного вірусного цитопатичного ефекту. Загалом енісамій пригнічував реплікацію вірусів грипу з 90% ефективністю при застосуванні в діапазоні концентрацій 157-439 ммоль (дози, в 23-64 рази нижчі за цитотоксичні концентрації). Віруси грипу B трохи сильніше пригнічувалися енісамієм, ніж віруси грипу А.
Крім того, вивчали результати додавання енісамію через 4 год після інокуляції вірусу A (H1N1). Дослідники відзначили зниження титру вірусу в ≥100 разів, що дозволяє припустити таке: енісамій впливає на ранню стадію життєвого циклу вірусу. Отже, енісамій проявляв противірусну активність проти вірусів грипу in vitro, що свідчить про його імовірну клінічну ефективність проти інфекцій, зумовлених вірусом грипу.
В умовах нинішньої пандемії COVID‑19 інтерес науковців до противірусного потенціалу енісамію помітно зріс. У квітні цього року A.J.W. Te Velthuis і співавт. у журналі «Антимікробні агенти та хіміотерапія» Американської асоціації мікробіології опублікували результати дослідження з вивчення ефективності енісамію в пацієнтів віком від 18 до 60 років із підтвердженим діагнозом респіраторної інфекції вірусної етіології. Загалом для участі у випробуванні було відібрано 137 пацієнтів, які повідомили про нещодавній початок респіраторної інфекції, – 1,6±0,5 дня з моменту розвитку симптомів. Із них 100 пацієнтів відповідали критеріям включення. Результати тестування виявили, що 43% із них були позитивними на вірус грипу групи А; 16% – аденовірус; 14% – поєднання вірусу грипу А й аденовірусу; 12% – вірус грипу В; 8% – вірус парагрипу чи респіраторно-синцитіальний вірус. Загалом 69% хворих інфікувалися вірусами грипу В чи А. Згодом хворих розподілили на прийом енісамію (n=60) або плацебо (n=40). Пацієнти обох груп були зіставні за віком та статтю. Протягом усього дослідження не спостерігалося відхилень від запланованого прийому ліків; середня тривалість лікування склала 6,8±0,8 дня. Пацієнти обох груп мали змогу використовувати деконгестанти та відхаркувальні засоби (за необхідності). В групі енісамію деконгестанти застосовували протягом коротшого періоду лікування й значно рідше, ніж у групі плацебо (23,3 (n=14) проти 75% (n=30) відповідно). Відхаркувальні засоби використовували хворі обох груп, але більшість пацієнтів групи енісамію припинили їхнє застосування через 7 днів, тоді як більшість учасників групи контролю продовжували їх приймати протягом 14 днів.
Вплив на припинення виділення вірусу
На 3-й день лікування (перший візит) у 71,2% (n=42) пацієнтів, котрі отримували енісамій, та в 25% (n=10) хворих із групи плацебо спостерігали негативні результати на антигени вищезазначених респіраторних вірусів, визначені методом імунофлуоресцентного фарбування назальних мазків (р<0,0001). На 7-й день лікування (другий візит) у всіх пацієнтів групи енісамію та у 82,5% (n=33) хворих із групи плацебо тест на антиген респіраторних вірусів виявився негативним (рис. 2А).
Аналіз у підгрупах продемонстрував аналогічний позитивний ефект лікування енісамієм порівняно із плацебо для пацієнтів, інфікованих вірусами грипу групи А чи В (75,0 (n=24) і 22,7% (n=5) відповідно) або аденовірусом (71,4 (n=5) та 12,5% (n=1) відповідно).
Отже, лікування енісамієм сприяло швидшому припиненню вірусовиділення інфікованими пацієнтами.
Рівень повсякденної активності
В групі хворих, які отримували енісамій, спостерігався вищий рівень повсякденної активності (не було жодного дня або лише 1 день без повсякденної активності), ніж у групі плацебо, де більшість хворих не мали змоги здійснювати повсякденну активність протягом ≥2 днів (рис. 2Б). Ці відмінності між групами були статистично значимими (р<0,0001).
Вплив на об’єктивні симптоми
Дослідники проаналізували динаміку таких об’єктивних симптомів, як лихоманка, гіперемія глотки й аускультативні зміни. На початку дослідження не було різниці в показниках об’єктивних симптомів між двома групами (9,6±0,7 бала для групи енісамію та 9,7±1,1 бала для групи плацебо). Зниження показників об’єктивних симптомів з 0-го по 14-й день було статистично значимим (р<0,0001) у групі енісамію (із 9,6±0,7 до 4,6±0,9 бала) порівняно із групою плацебо (із 9,7±1,1 до 5,6±1,1 бала). Відсутність усіх об’єктивних симптомів спостерігалася в обох групах пацієнтів із 7-го дня, втім, у групі енісамію відсутність усіх трьох симптомів відзначалася в значно більшої частки пацієнтів на 14-й день лікування (рис. 3А).
Такі прояви захворювання, як гіперемія глотки та патологічні зміни при аускультації повернулися до норми значно швидше в групі енісамію, ніж у групі плацебо (рис. 3Б, 3В). Аналогічні результати були отримані й у підгрупі пацієнтів із грипом.
! Наведені результати переконливо свідчать, що лікування енісамієм спричиняло швидше та значиміше зменшення об’єктивних клінічних симптомів, пов’язаних з респіраторними вірусними інфекціями.
Вплив на суб’єктивні симптоми
На момент залучення до випробування в усіх пацієнтів спостерігалися такі суб’єктивні симптоми: слабкість, головний біль, відчуття підвищення температури тіла, біль у горлі та кашель. Менше половини хворих повідомили про міалгію (46,0%, n=46) і лише в декількох учасників спостерігався озноб (7,0%, n=7).
Аналіз динаміки суб’єктивних симптомів виявив стрімкіше їхнє зниження в групі енісамію (порівняно із прийомом плацебо) на 3-й, 7-й і 14-й дні від початку лікування (рис. 2). Зокрема, на 14-й день загальний показник симптомів знизився із 15,7±2,2 до 7,1±0,5 бала в групі енісамію порівняно із 15,4±1,8 до 8,0±1,3 в групі плацебо. Також було продемонстровано, що суб’єктивні скарги з найбільшим внеском до сумарного показника симптомів (слабкість, головний біль, підвищення температури тіла, біль у горлі та кашель) знижувалися швидше в групі енісамію. Схожі результати було отримано в підгрупах пацієнтів за різними типами вірусів. Отже, лікування енісамієм сприяє швидшому зниженню таких клінічно значимих суб’єктивних симптомів, як-от відчуття слабкості, головний біль, біль у горлі і кашель.
! Отже, лікування енісамієм зумовило більш раннє припинення виділення вірусу хворими, швидше одужання пацієнтів (на 14-й день лікування в групі енісамію одужали 93,9% пацієнтів порівняно із 32,5% у групі плацебо; р<0,0001), а також зменшення об’єктивних (із 9,6±0,7 до 4,6±0,9 бала в групі енісамію проти 9,7±1,1 до 5,6±1,1 бала в групі плацебо; р<0,0001) та суб’єктивних (із 15,7±2,2 до 7,1±0,5 бала в групі енісамію порівняно із 15,4±1,8 до 8,0±1,3 в групі плацебо; р<0,0001) симптомів захворювання.
Перспективи енісамію в лікуванні COVID‑19
Коронавірусна хвороба, спричинена коронавірусом SARS-CoV‑2, потребує пошуку нових стратегій лікування. Розробка та впровадження вакцин проти коронавірусу, на які покладали великі надії, не дозволила вирішити проблему подальшого поширення пандемії. Управління з контролю за якістю продуктів харчування та лікарських засобів США (FDA) схвалило декілька противірусних стратегій – лікування ремдесивіром або реконвалесцентною плазмою. Однак розробка ефективніших стратегій наразі все ще залишається вкрай необхідною. Ключовою мішенню для нових препаратів є РНК-полімераза SARS-CoV‑2.
Одним із препаратів, виокремлених Всесвітньою організацією охорони здоров’я як потенційно ефективний засіб проти SARS-CoV‑2, є енісамію йодид. Цей препарат ліцензований як засіб проти грипу в 11 країнах. Нещодавнє дослідження продемонструвало, що енісамій піддається гідроксилюванню в організмі та клітинах легень людини до сполуки VR17-04, здатної пригнічувати активність РНК-полімерази вірусу грипу А (Te Velthuis A. J.W. et al., 2021).
В цьому експериментальному дослідженні науковці вивчали вплив енісамію на розвиток вірусу SARS-CoV‑2 на моделях клітини епітеліальної аденокарциноми людини (Caco‑2) і на нормальних бронхоепітеліальних клітинах людини (NHBE).
Культури клітин обробляли серійними розведеннями енісамію йодиду (лабораторний код FAV00A, торгова назва Амізон®) або енісамію хлориду (лабораторний код FAV00B) за 6 год до зараження. Клітини інфікували SARS-CoV‑2, а після інокуляції вірусу повторно наносили сполуку. Через 48 год після зараження реєстрували цитопатичний ефект шляхом дослідження інфікованих культур за допомогою світлової мікроскопії, а також відбирали оточуючу рідину для визначення РНК вірусу за допомогою кількісної полімеразно-ланцюгової реакції у режимі реального часу.
Науковці спостерігали значне зниження експресії вірусного нуклеопротеїну, цитопатичного ефекту інфекції SARS-CoV‑2 на клітини Caco‑2 і зменшення числа копій вірусного геному в інфікованих клітинах залежно від концентрацій енісамію. Концентрація напівмаксимального інгібування для енісамію хлориду в клітинах Caco‑2 склала 1,2 ммоль (≈300 мкг/мл). Отримані результати виявилися зіставними з інгібувальною дією енісамію на реплікацію вірусу грипу А в клітинах Caco‑2, вивчену в попередніх дослідженнях (Te Velthuis A. J.W. et al., 2021).
Для перевірки здатності енісамію пригнічувати реплікацію коронавірусу в нормальних бронхоепітеліальних клітинах людини культуру цих клітин інкубували з енісамію йодидом протягом 6 год, після чого інфікували альфа-коронавірусом (HCoV-NL63). Аналіз рівнів умісту N гена РНК в інфікованих нормальних бронхоепітеліальних клітинах людини продемонстрував значний вплив енісамію на синтез вірусної РНК (рис. 3А) з концентрацією напівмаксимального інгібування ≈60 мкг/мл.
З метою перевірки здатності енісамію пригнічувати синтез РНК SARS-CoV‑2 in vitro дослідники застосували метод мінігеномного аналізу, що дозволяє визначити ступінь пригнічення активності РНК-полімеразного комплексу SARS-CoV‑2 nsp12/7/8. Додавання енісамію в середовище інкубації культури клітин значно пригнічувало сигнал мінігеному залежно від концентрації (рис. 3Б). Дослідження продемонструвало, що енісамій пригнічує реплікацію коронавірусу на моделі клітин епітеліальної аденокарциноми людини (Caco‑2) і нормальних бронхоепітеліальних клітин людини. Науковці пов’язують отриманий ефект із пригніченням елонгації РНК SARS-CoV‑2, що підтверджують результати моделювання молекулярної динаміки.
! Багатоцентрове подвійне сліпе рандомізоване плацебо-контрольоване дослідження III фази з вивчення ефективності енісамію (використовували Амізон® МАКС) у пацієнтів із COVID‑19 середнього ступеня тяжкості свідчить про досить високу клінічну ефективність цього препарату. Випробування здійснювалося в 14 клінічних центрах різних регіонів України із залученням 592 хворих з підтвердженою коронавірусною інфекцією.
На 15-й день дослідження в групі плацебо було виписано 85,7% пацієнтів, а в групі препарату Амізон® МАКС – 94,4%. Різниця у 8,7% свідчить про більшу ефективність лікування в групі Амізону МАКС порівняно із групою плацебо (р=0,0018). У групі препарату Амізон® МАКС ризик розвитку дихальної недостатності й інших ускладнень виявився майже вчетверо нижчим порівняно із групою плацебо – відношення ризику склало 4,244 (95% довірчий інтервал від 1,171 до 15,38; р=0,014) (Бабіч М. П. і співавт., 2021).
Отже, Амізон® МАКС допомагає пришвидшити одужання, запобігати розвитку дихальної недостатності та інших ускладнень COVID‑19.
Підготував В’ячеслав Килимчук