20 червня, 2022
Фолікулярна лімфома – від теорії до практики
 Фолікулярна лімфома (ФЛ) досі залишається невиліковним захворюванням із середньою виживаністю з моменту встановлення діагнозу 9,2 року й тенденцією до зменшення цієї цифри з кожним наступним рецидивом (P.W. Jonhson et al., 1995). Проте поступово з’являються нові терапевтичні можливості, які сприяють збільшенню тривалості життя пацієнтів із ФЛ. У рамках майстер-класу «Фолікулярна лімфома – від теорії до практики. Нові дані та нові виклики» провідні українські фахівці розповіли про ключові моменти у веденні хворих на ФЛ, нові терапевтичні можливості та перспективи їх впровадження у клінічну практику в нашій країні.
Фолікулярна лімфома (ФЛ) досі залишається невиліковним захворюванням із середньою виживаністю з моменту встановлення діагнозу 9,2 року й тенденцією до зменшення цієї цифри з кожним наступним рецидивом (P.W. Jonhson et al., 1995). Проте поступово з’являються нові терапевтичні можливості, які сприяють збільшенню тривалості життя пацієнтів із ФЛ. У рамках майстер-класу «Фолікулярна лімфома – від теорії до практики. Нові дані та нові виклики» провідні українські фахівці розповіли про ключові моменти у веденні хворих на ФЛ, нові терапевтичні можливості та перспективи їх впровадження у клінічну практику в нашій країні.
.jpg) Керівник Центру гематології, хіміотерапії гемобластозів та трансплантації кісткового мозку Клінічної лікарні «Феофанія» Державного управління справами, завідувач кафедри клінічної лабораторної діагностики Національного університету охорони здоров’я України імені П.Л. Шупика (м. Київ), доктор медичних наук, професор Сергій Вікторович Клименко представив доповідь «Оцінка факторів ризику при фолікулярній лімфомі».
Керівник Центру гематології, хіміотерапії гемобластозів та трансплантації кісткового мозку Клінічної лікарні «Феофанія» Державного управління справами, завідувач кафедри клінічної лабораторної діагностики Національного університету охорони здоров’я України імені П.Л. Шупика (м. Київ), доктор медичних наук, професор Сергій Вікторович Клименко представив доповідь «Оцінка факторів ризику при фолікулярній лімфомі».
– За даними різних досліджень, приблизно в кожного п’ятого пацієнта, який отримував імунохіміотерапію у 1-й лінії, спостерігають прогресування захворювання впродовж 2 років (O.W. Press et al., 2013; M.J. Rummel et al., 2013; F. Morschhauser et al., 2011). Прогресування захворювання протягом перших 2 років сильно корелює з менш тривалою загальною виживаністю (ЗВ) і вищим ризиком смерті. Для покращення результатів лікування необхідна стратифікація пацієнтів на групи ризику та вибір відповідної терапевтичної тактики.
Для виявлення пацієнтів із ФЛ та високим ризиком раннього прогресування захворювання застосовують конкретні інструменти. Насамперед потрібно підкреслити, що пацієнти з ФЛ та дифузною B-великоклітинною лімфомою мають різні фактори ризику. Зручною для застосування у клінічній практиці є прогностична система, заснована на комбінації діагностичних маркерів, виражених у балах. Для ФЛ існує велика кількість бальних систем.
Одним із найпоширеніших і найбільш перевірених прогностичних інструментів є система FLIPI, що включає 5 базових характеристик: стадія за Ann Arbor (ІІІ-IV проти І-ІІ), вік пацієнтів (>60 років проти ≤60 років), рівень гемоглобіну (<120 г/л проти ≥120 г/л), кількість залучених лімфатичних зон (>4 проти ≤4), рівень лактатдегідрогенази (ЛДГ) сироватки (більший за норму проти менший або рівний нормі; P.P Solal-Celigny et al., 2004).
За системою FLIPI пацієнтів з ФЛ розподіляють на 3 групи ризику: низького, проміжного та високого. На сучасному етапі терапевтичних можливостей при ФЛ система FLIPI уже застаріла, оскільки вона розроблена ще до впровадження ритуксимабу у схеми лікування, хоча і була пізніше валідована для схем терапії на основі ритуксимабу. Це стало приводом для створення схеми FLIPI-2, яка, окрім базових характеристик FLIPI, також включила 3 додаткові параметри: залучення кісткового мозку, діаметр ураженого лімфатичного вузла (ЛВ) >6 см, підвищення рівня β2-мікроглобуліну (M. Frederico et al., 2009). Спостерігається істотна відмінність у діапазоні тривалості 5-річної ЗВ залежно від групи ризику, встановленої за допомогою прогностичних інструментів FLIPI та FLIPI-2: при оцінюванні ризику за FLIPI ЗВ коливається в межах 53-91%, при FLIPI-2 – 19-80%. Ширший діапазон 5-річної ЗВ може вказувати на більшу точність прогностичного інструменту.
Досвід застосування FLIPI та FLIPI-2 для оцінювання ризику продемонстрував їх надійність, однак із появою терапевтичних опцій з’являється потреба в оновленні існуючих прогностичних інструментів. Так, у 2018 р. був розроблений новий прогностичний індекс PRIMA-PI для пацієнтів із ФЛ, які отримують імунотерапію
Створення нових терапевтичних опцій (окрім ритуксимабу) зумовило розроблення нових прогностичних інструментів, наприклад FLEX. Сьогодні існує ще низка потенційних прогностичних маркерів у пацієнтів з ФЛ, котрі можуть бути інтегровані у нові інструменти уже найближчим часом. Зокрема, стали доступні потужні платформи для генетичних аналізів і біоінформатики. Так, оцінювання профілю експресованих 23 генів, які відображають кілька аспектів біології пухлини, дозволяє розподіляти пацієнтів на групи високого та низького ризику. Однак ця технологія є дорогою та потребує проведення біопсії для взяття біологічного матеріалу і застосовується в основному у дослідницьких центрах. Тому у клінічній практиці значну увагу приділяють оцінюванню окремих генетичних параметрів. Із раннім прогресуванням ФЛ асоціюються мутація гена ТР53 та експресія білка р53, тому ці параметри в перспективі можуть бути розглянуті з метою стратифікації пацієнтів з ФЛ на групи ризику.
У клінічній практиці важливо оцінювати не лише факт наявності ризику прогресування ФЛ, а й те, наскільки швидко це відбудеться. У дослідженні GALLIUM, в якому оцінювали прогресування хвороби (progression of disease, POD) протягом 24 міс (POD24), було виявлено, що раннє прогресування ФЛ асоційоване з поганим прогнозом. Орієнтовний аналіз ЗВ показав у 12 разів вищий ризик смерті у пацієнтів з POD24 порівняно з тими, у кого не було прогресування протягом 2 років. Ці дані мають практичне значення, оскільки є підставою для модифікації терапевтичної тактики. У цьому ж дослідженні було показано, що застосування обінутузумабу з хіміотерапією зменшує ризик POD24 на 46% порівняно зі схемою ритуксимаб + хіміотерапія (рис. 1; A. Launonen et al., 2017).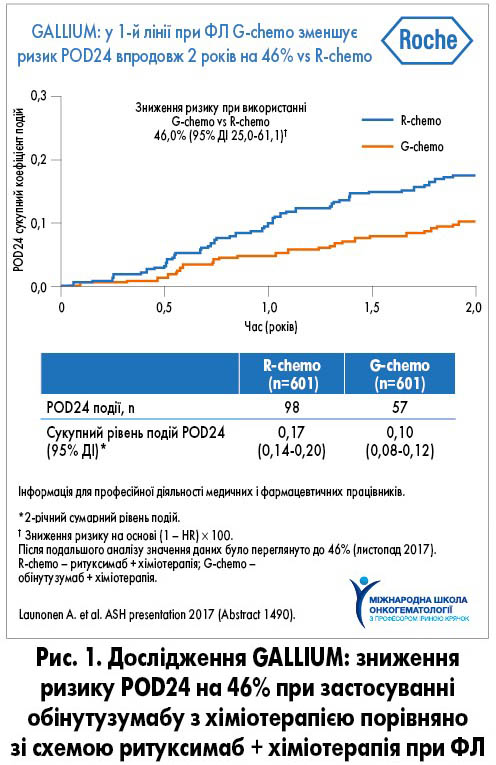
Для прогнозування POD24 сьогодні часто використовують клініко-генетичну модель ризику POD24-РІ, що включає 4 параметри: високий ризик за FLIPI, експресія генів ЕР300, FOX01 та EZHH2. Індекс POD24-РІ дозволяє прогнозувати POD24 з 71% точністю. Також до високоточних методів прогнозування POD24 належить m7-FLIPI, який інтегрує FLIPI за статусом мутації 7 генів і статусом за ECOG (точність 76%; V. Jurinovic et al., 2016). Метод m7-FLIPI зменшує пропорцію пацієнтів із високим ризиком порівняно з FLIPI (A. Pastore et al., 2015).
Таким чином, оптимального використання прогностичних факторів при ФЛ ще не досягнуто. Метод m7-FLIPI поки є дослідницьким інструментом і сьогодні проходить перспективну перевірку в кількох клінічних дослідженнях. Раннє прогресування хвороби (POD24) є надійним предиктором зменшення ЗВ і може застосовуватися для оцінювання ефективності нових препаратів.
 Завідувачка відділення онкогематології Національного інституту раку (м. Київ) Тетяна Вікторівна Каднікова розповіла про нові можливості 1-ї лінії терапії при ФЛ.
Завідувачка відділення онкогематології Національного інституту раку (м. Київ) Тетяна Вікторівна Каднікова розповіла про нові можливості 1-ї лінії терапії при ФЛ.
– Однією з опцій стандартної терапії у пацієнтів із ФЛ та високим пухлинним навантаженням є комбінація обінутузумабу та бендамустину. Перспективним препаратом для лікування ФЛ є венетоклакс – пероральний інгібітор BCL-2, експресія якого характерна для ФЛ. У рамках щорічної зустрічі Американського товариства гематології (American Society of Hematology, ASH) були представлені результати дослідження ІІ фази, у якому оцінювали застосування у 1-й лінії венетоклаксу у комбінації з обінутузумабом і бендамустином у хворих на ФЛ і високим пухлинним навантаженням. У дослідження було включено 56 пацієнтів з ФЛ, підтвердженою біопсією, які мали І, ІІ, IІІ стадію хвороби за класифікацією Всесвітньої організації охорони здоров’я без ознак гістологічної трансформації у великоклітинну лімфому. Відповідність показникам високого пухлинного навантаження визначали за такими ознаками: наявність одного з критеріїв французької групи з вивчення ФЛ (GELF) або ≥3 бали за FLIPI. У ході дослідження пацієнти отримали індукційну терапію венетоклаксом у комбінації з обінутузумабом і бендамустином (6 циклів). Після цього хворі з повною відповіддю (ПВ) продовжували підтримувальну терапію обінутузумабом (12 циклів), а пацієнти з частковою відповіддю або стабілізацією захворювання як підтримувальну терапію отримували обінутузумаб (12 циклів) і венетоклакс (24 цикли). На індукційну терапію загалом досягнуто відповідь у 92,9% пацієнтів, з них 72,3% мали ПВ. У ході подальшого спостереження була встановлена 2-річна ЗВ на рівні 94,4% (95% довірчий інтервал – ДІ – 82,4-98,3), а 2-річна виживаність без прогресування (ВБП) – 85,8% (95% ДІ 68,8-93,9). Основними побічними реакціями (ПР; >10%) на етапі індукційної терапії були нудота, втома, блювання, діарея, тромбоцитопенія, нейтропенія, головний біль, зниження апетиту, анемія, інфузійні реакції, гіперурикемія, підвищення рівня аланін- та аспартатамінотрансферази, запор, інфекції верхніх дихальних шляхів. Загалом у 83,9% хворих мали місце ПР ≥3 ступеня. Через ПР особливого значення, які виникли після початку лікування (цитомегаловірусний енцефаліт, пневмоцистна пневмонія, вірусна нефропатія), у терапію були внесені деякі зміни. На момент виникнення 4-ї ПР особливого значення (міокардиту) усі пацієнти завершили індукційну терапію, 7 пацієнтів залишалися на підтримувальній терапії, яка після обговорення з лікарями-дослідниками була передчасно припинена (C.A. Portell et al., 2021). Таким чином, результати дослідження обнадійливі за показниками ПВ, ЗВ і ВБП, проте висока частота ПР ≥3 ступеня та виникнення опортуністичних інфекцій дають підстави вважати, що ця комбінація може бути занадто токсичною для зазначеної популяції пацієнтів.
Нещодавно були опубліковані результати 6-річного спостереження рандомізованого клінічного дослідження III фази RELEVANCE, у якому порівнювали дві тактики лікування раніше не лікованих пацієнтів з ФЛ: леналідомід + ритуксимаб з хіміотерапією (n=517) або без неї (n=513). Згідно з отриманими даними, 6-річна ВБП у групі пацієнтів, які отримували леналідомід + ритуксимаб та хіміотерапію, склала 59%, а в групі без хіміотерапії – 60%, 6-річна ЗВ в обох групах – 89%. Однією із вторинних кінцевих точок дослідження було оцінювання відповіді на терапію після прогресування/рецидиву хвороби. Так, частота загальної відповіді (ЧЗВ) у групі без хіміотерапії становила 61%, у групі, де пацієнти разом з леналідомідом та ритуксимабом отримували хіміотерапію, – 59% (F. Morschhauser et al., 2021).
 У дослідженні ІІ фази GALEN були продемонстровані обнадійливі результати застосування комбінації обінутузумабу та леналідоміду у раніше не лікованих пацієнтів із запущеною ФЛ. При медіані спостереження 3,7 року 3-річна ВБП і ЗВ становили 82 та 94% відповідно, повна метаболічна відповідь досягнута у 80% хворих, ЧЗВ дорівнювала 94% (рис. 2; E. Bachy et al., 2022).
У дослідженні ІІ фази GALEN були продемонстровані обнадійливі результати застосування комбінації обінутузумабу та леналідоміду у раніше не лікованих пацієнтів із запущеною ФЛ. При медіані спостереження 3,7 року 3-річна ВБП і ЗВ становили 82 та 94% відповідно, повна метаболічна відповідь досягнута у 80% хворих, ЧЗВ дорівнювала 94% (рис. 2; E. Bachy et al., 2022).
 Професор кафедри гематології та трансфузіології Національного університету охорони здоров’я України імені П.Л. Шупика, завідувачка відділення гематології Медичного центру імені Ю.П. Спіженка (м. Київ), доктор медичних наук Тетяна Петрівна Перехрестенко свою доповідь присвятила розширеним можливостям терапії рецидивної/рефрактерної (р/р) ФЛ (за матеріалами ASH-2021).
Професор кафедри гематології та трансфузіології Національного університету охорони здоров’я України імені П.Л. Шупика, завідувачка відділення гематології Медичного центру імені Ю.П. Спіженка (м. Київ), доктор медичних наук Тетяна Петрівна Перехрестенко свою доповідь присвятила розширеним можливостям терапії рецидивної/рефрактерної (р/р) ФЛ (за матеріалами ASH-2021).
– Згідно з останніми оновленнями клінічних настанов Національної онкологічної мережі США (NCCN, версія 3.2022) щодо лікування ФЛ І-ІІ стадій, у 2-й лінії терапії слід віддати перевагу схемам бендамустин + обінутузумаб або ритуксимаб (не рекомендується, якщо раніше пацієнт отримував бендамустин); CHOP (циклофосфамід + доксорубіцин + вінкристин + преднізолон) + обінутузумаб або ритуксимаб; CVP (циклофосфамід + вінкристин + преднізон) + обінутузумаб або ритуксимаб; леналідомід + ритуксимаб. До інших рекомендованих належать ібритумумаб тіуксетан, леналідомід (у хворих, які не є кандидатами на терапію моноклональними антитілами анти-CD20); леналідомід + обінутузумаб; обінутузумаб; ритуксимаб. У деяких ситуаціях, наприклад при ранньому рецидиві ФЛ у молодих пацієнтів з групи високого ризику, можна розглянути застосування високодозової терапії з подальшою трансплантацією гемопоетичних стовбурових клітин (ТГСК). Як 3-ю лінію лікування пропонується використовувати інгібітори фосфоінозитид-3-кінази (PI3K), інгібітори EZH2, анти-CD19 CAR-Т-клітинну терапію.
Сьогодні активно вивчається ефективність застосування обінутузумабу у комбінації з різними препаратами при р/рФЛ. Зокрема, хороші результати забезпечує схема обінутузумаб + атезолізумаб + леналідомід. За даними відкритого багатоцентрового дослідження Іb/II фази при використанні цієї схеми при р/рФЛ була досягнута висока частота об’єктивної відповіді (84,4%), в тому числі ПВ – у 75,0% пацієнтів (за даними дослідників). За даними незалежного комітету частота об’єктивної відповіді та ПВ склали та 78,1 та 71,9% відповідно (F. Morschhauser et al., 2021).
На зустрічі ASH-2021 також були представлені результати дослідження Ib фази, які демонструють обнадійливу ефективність та контрольований профіль безпеки комбінації мозунетузумабу (біспецифічне антитіло CD20×CD3) з леналідомідом у пацієнтів з р/рФЛ (n=29), які отримали щонайменше одну лінію терапії. При медіані спостереження 5,4 міс ПР, пов’язані з введенням мозунетузумабу/леналідоміду, виникли у 100% пацієнтів, 3-4 ступеня – у 44,8% хворих, ПР з летальним наслідком не було. Лише у одного пацієнта було прийнято рішення про припинення лікування через ПР на тлі прийому леналідоміду. Найчастішою ПР 3-4 ступеня була нейтропенія. Слід окремо зазначити про таку ПР, як синдром вивільнення цитокінів (СВЦ). У цьому дослідженні СВЦ 1-2 ступеня мав місце у 27,6% пацієнтів, усі вони не потребували застосування кортикостероїдів, тоцилізумабу чи припинення лікування мозунетузумабом. У всіх хворих СВЦ був усунений.
У загальній популяції пацієнтів спостерігали високу ЧЗВ (89,7%) та повної метаболічної відповіді (65,5%). Найкраща відповідь за даними позитронної емісійної комп’ютерної томографії (ПЕТ-КТ) досягнута у пацієнтів з POD24, рефрактерністю до анти-CD20 терапії, подвійною рефрактерністю. На момент публікації результатів дослідження у 25 (86,2%) учасників відповідь на лікування утримувалася, у всіх пацієнтів, які досягли повної метаболічної відповіді, вона зберігається, у двох пацієнтів відповідь покращилася (рис. 3; F. Morschhauser et al., 2021).
Таким чином, комбінація мозунетузумаб + леналідомід, яка не містить хіміотерапевтичних компонентів, може стати перспективною схемою амбулаторного лікування р/рФЛ.
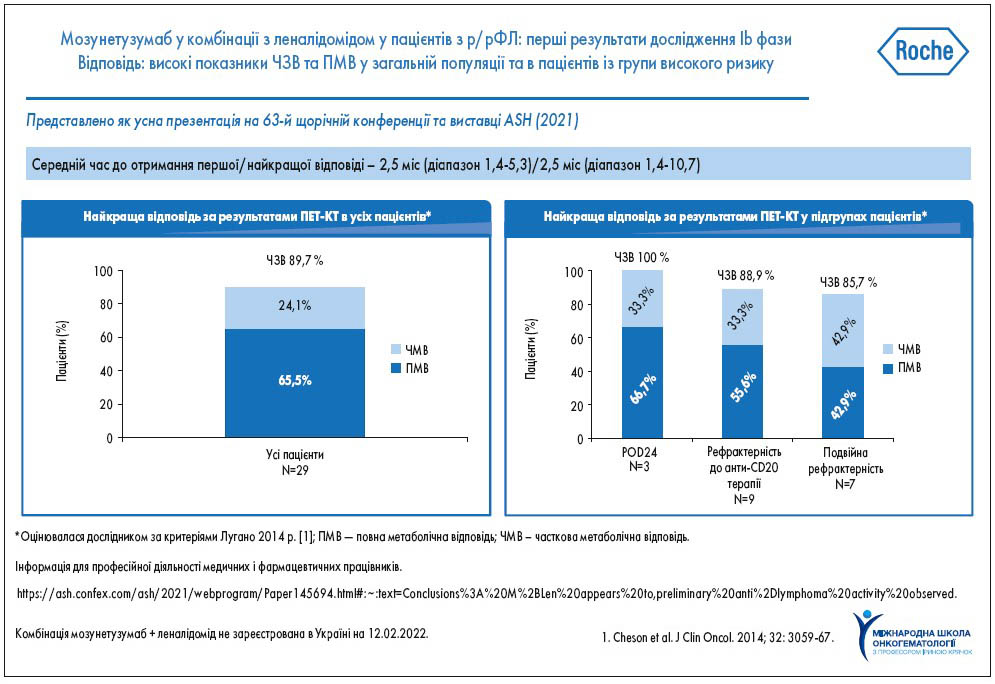 Рис. 3. Ефективність комбінації мозунетузумабу з леналідомідом у пацієнтів з р/рФЛ згідно з першими даними дослідження Ib фази
Рис. 3. Ефективність комбінації мозунетузумабу з леналідомідом у пацієнтів з р/рФЛ згідно з першими даними дослідження Ib фази
 Клінічний випадок лікування пацієнта з ФЛ представила завідувачка Обласного лікувально-діагностичного гематологічного центру КНП «Черкаський обласний онкодиспансер» Черкаської обласної ради Олена Володимирівна Лук’янець.
Клінічний випадок лікування пацієнта з ФЛ представила завідувачка Обласного лікувально-діагностичного гематологічного центру КНП «Черкаський обласний онкодиспансер» Черкаської обласної ради Олена Володимирівна Лук’янець.
Клінічний випадок
Пацієнт А., 46 років.
Липень 2020 року – звернувся до лікаря зі скаргами на збільшення ЛВ шиї та пахвинної ділянки. Вперше помітив збільшення ЛВ рік тому. Інші симптоми відсутні.
Аналіз крові від 07.07.2020: еритроцити – 5,22 Г/л, лейкоцити – 6,7 Г/л, рівень гемоглобіну – 149 г/л, тромбоцити – 159 Г/л, паличкоядерні – 5%, сегментоядерні – 43%, лімфоцити – 44%, моноцити – 8%, ЛДГ – 149 ОД/л; HbsAg – негативний, антитіла до HCV відсутні; ДНК вірусу гепатиту В та РНК вірусу гепатиту не визначаються.
Комп’ютерна томографія (КТ) органів грудної клітки, черевної порожнини, малого таза та шиї від 08.07.2020: двобічне ураження шийних ЛВ (максимальний розмір 23×15 мм), медіастинальних (максимальний розмір 49×19 мм), парааортальних (максимальний розмір 24×18 мм), мезентеріальних (максимальний розмір 49×31 мм), пахвинних і здухвинних ЛВ (максимальний розмір 38×22 мм), гепатомегалія, спленомегалія (краніокаудальний розмір – 155 мм).
Імуногістохімічне дослідження ЛВ шиї від 20.07.2020: морфологічна картина ураження ЛВ і характер експресії маркерів відповідають фолікулярній лімфомі GRADE 2 із фолікулярним характером росту.
Аналіз аспірату кісткового мозку від 30.07.2020: цитоз 160 г/л, лімфоцити – 32,4%.
Біопсія кісткового мозку від 03.08.2020: у досліджуваному матеріалі ураження кісткового мозку лімфомою не виявлено.
Діагноз: неходжкінська фолікулярна лімфома GRADE 2, стадія IIIА, клінічна група 2; ураження шийних, медіастинальних, парааортальних, мезентеріальних, здухвинних, пахвинних ЛВ, спленомегалія; 2 бали за FLIPI-1, проміжний ризик.
Лікування: обінутузумаб 1000 мг у 1-й день + бендамустин 90 мг/м2 площі поверхні тіла у 1-2-й дні 28-денного циклу; 1-й курс – обінутузумаб 1000 мг у 1-й, 8, 15-й дні. З метою профілактики інфекцій були призначені бісептол 480 мг 1 раз/добу, ацикловір 400 мг 2 рази/добу.
Дані КТ після 3 курсів лікування від 03.11.2020: редукція пухлинної маси на 76%.
10.11.2020 пацієнт повністю завершив 4-й курс лікування, після чого захворів на COVID-19 з 60% ураженням легень та гіпертермією протягом 5 тижнів.
Січень 2020 року – звернувся в онкодиспансер. Для контролю гіпертермії приймав метилпреднізолон.
Аналіз крові на імуноглобуліни від 13.01.2021: IgG сироватки – 3 г/л. Було прийнято рішення відмінити прийом метилпреднізолону, призначено препарат імуноглобуліну людського.
Аналіз крові на імуноглобуліни від 23.01.2021: IgG сироватки – 9 г/л.
Дані ПЕТ-КТ від 16.02.2021: повна метаболічна відповідь, залишкова інфільтрація легень після перенесеного COVID-19.
З 27.02.2021 – гіпертермія 38 °С.
06.03.2021 – результат дослідження на цитомегаловірус методом полімеразної ланцюгової реакції (ПЛР) негативний, IgG сироватки – 3,82 г/л, рівень C-реактивного протеїну – 102 мг/л.
Призначено препарат імуноглобуліну людського.
10.03.2021 – підтверджена інфекція COVID-19 методом ПЛР. Пацієнт був госпіталізований в інфекційне відділення, де йому був призначений ремдесивір. Гіпертермія регресувала.
Імунний статус від 07.06.2021: Т-лімфоцити – 86%, В-лімфоцити – 6,5%, співвідношення Т-хелпери/Т-кілери – 0,22, В-лімфоцити CD19+ не виявлені.
Дані КТ від 06.09.2021: повна морфологічна відповідь, всі ЛВ <15 мм у найбільшому діаметрі. Регресування інфільтративних змін у легенях.
Хворий двічі вакцинований проти COVID-19. Заплановане введення бустерної дози.
Таким чином, застосування моноклональних антитіл у пацієнтів з ФЛ супроводжується імуносупресією, яка потребує контролю. У нашому відділені ми дотримуємося тактики відтермінування терапії у пацієнтів з ФЛ, яким необхідне застосування моноклональних антитіл, до вакцинації проти COVID-19.
.jpg) Завідувачка науково-дослідного відділення хіміотерапії гемобластозів та ад’ювантних методів лікування Національного інституту раку (м. Київ), доктор медичних наук, професор Ірина Анатоліївна Крячок представила доповідь «Узагальнення даних та результатів досліджень: що є релевантним для України?».
Завідувачка науково-дослідного відділення хіміотерапії гемобластозів та ад’ювантних методів лікування Національного інституту раку (м. Київ), доктор медичних наук, професор Ірина Анатоліївна Крячок представила доповідь «Узагальнення даних та результатів досліджень: що є релевантним для України?».
– Поява нових терапевтичних агентів, зокрема ритуксимабу, драматично вплинула на виживаність пацієнтів з ФЛ. Однак у 20% пацієнтів хвороба прогресує протягом 24 міс. Пацієнти з раннім прогресуванням захворювання значно гірше відповідають на терапію, що підтверджується результатами багатьох досліджень. Тому показник POD24 набув значного поширення як прогностичний маркер у хворих на ФЛ.
Згідно з рекомендаціями Європейського товариства медичної онкології (ESMO), основним принципом вибору терапії при ФЛ є визначення пухлинного навантаження. При низькому пухлинному навантаженні можна застосовувати місцеву променеву терапію, ритуксимаб або тактику спостереження. При виборі конкретної терапевтичної схеми також враховують вік хворого. Так, у молодих пацієнтів можливе застосування більшої кількості варіантів лікування, зокрема ТГСК.
У клінічних настановах NCCN запропоновані кілька комбінацій лікування ФЛ у 1-й та 2-й лініях, більшість із них в Україні сьогодні доступна. Однак запропоновані NCCN варіанти 3-ї лінії лікування (інгібітори PI3K, інгібітори EZH2, анти-CD19 CAR-Т-клітинна терапія) недоступні в нашій країні. У клінічних настановах ESMO після другого та наступних рецидивів рекомендують застосовувати імунотерапію (монотерапія ритуксимабом, ритуксимаб + леналідомід), променеву терапію, іделалісиб (пероральний селективний інгібітор PI3K, при подвійній рефрактерності), у молодих пацієнтів із раннім рецидивом хвороби можливе проведення алогенної/аутологічної ТГСК.
Перспективним препаратами є інгібітори PI3K. Сьогодні Управлінням із контролю якості харчових продуктів і лікарських препаратів США схвалені іделалісиб, дувелісиб для перорального застосування та копанлісиб для внутрішньовенного введення, які демонструють зіставну ефективність у терапії р/рФЛ.
Однією із доступних в Україні та ефективних терапевтичних опцій є комбінація обінутузумаб + бендамустин. У рандомізованому дослідженні ІІІ фази Gadolin порівнювали ефективність та безпеку схеми обінутузумаб + бендамустин і монотерапії бендамустином у пацієнтів із рецидивною індолентною неходжкінською лімфомою (іНХЛ), рефрактерною до ритуксимабу. Згідно з фінальними результатами, застосування схеми обінутузумаб + бендамустин сприяє зниженню ризику прогресування чи смерті у пацієнтів з іНХЛ на 43%, у хворих на ФЛ – на 49% порівняно з монотерапією бендамустином. У пацієнтів з іНХЛ медіана ЗВ у групі обінутузумаб + бендамустин склала 88,3 міс, у групі монотерапії бендамустином – 65,6 міс (зниження ризику смерті на 23%), у хворих на ФЛ у групі обінутузумаб + бендамустин медіана ЗВ не досягнута, у групі бендамустину – 60,3 міс (зниження ризику смерті на 29%). У групі комбінованої терапії у більшості пацієнтів був досягнутий MRD-негативний статус порівняно з монотерапією (рис. 4; L.H. Sehn et al., 2019).
 Рис. 4. Результати дослідження GADOLIN: фінальний аналіз ВБП при іНХЛ і ФЛ за оцінкою дослідника
Рис. 4. Результати дослідження GADOLIN: фінальний аналіз ВБП при іНХЛ і ФЛ за оцінкою дослідника
У дослідженні ІІ фази GALEN високу ефективність продемонструвала схема обінутузумаб + леналідомід у пацієнтів з CD20+ р/рФЛ. Протягом медіани спостереження 2,6 року загальна відповідь склала 79%, ПВ мали 38% учасників (F. Morschhauser et al., 2019).
Незважаючи на те що імунохіміотерапія значно покращує ЗВ у хворих на ФЛ, майже у 20% пацієнтів розвивається ранній рецидив, що асоціюється з гіршим прогнозом. Тому сьогодні у пацієнтів з р/рФЛ активно вивчають значення ТГСК. У ретроспективному багатоцентровому дослідженні було проаналізовано дані 397 хворих з ФЛ, які отримали стандартну імунохіміотерапію на основі ритуксимабу. Згідно з отриманими даними, протягом медіани спостереження 92 міс у 148 (37,3%) учасників розвинувся рецидив, з них у 82 (20,7%) – ранній рецидив (протягом ≤2 років). 48% хворих із рецидивом ФЛ була проведена аутологічна ТГСК. За отриманими даними, ЗВ була вищою у пацієнтів, які мали ранній рецидив і яким була проведена аутологічна ТГСК, ніж у тих, кому не була проведена аутологічна ТГСК. При пізньому рецидиві аутологічна ТГСК не впливала на ЗВ (M. Manna et al., 2017).
Серед нових можливостей лікування р/рФЛ, за попередніми результатами досліджень, високу ефективність демонструють CAR-T-клітинна терапія, інгібітори EZH2 при наявності мутації EZH2 (таземетостат), біспецифічні антитіла. Важливо також зазначити, що схеми лікування, які не містять хіміотерапевтичних компонентів, з представленими в Украні обінутузумабом, леналідомідом, атезолізумабом, венетоклаксом дають нам можливості підібрати найкращі опції для пацієнтів з ФЛ.
Таким чином, сьогодні в Україні достатньо терапевтичних опцій для пацієнтів з ФЛ у 1-й та 2-й лініях, однак можливості лікування при наступних рецидивах обмежені. Крім того, сьогодні на стадії клінічних випробувань знаходяться нові схеми та терапевтичні агенти, які уже демонструють високу ефективність і в перспективі можуть доповнити стандартні схеми лікування ФЛ.
Підготувала Ілона Цюпа
Матеріал підготовлено за підтримки ТОВ «Рош Україна».
Для розміщення у спеціалізованих виданнях, призначених для медичних закладів або спеціалістів охорони здоров’я.
Інформація для професійної діяльності медичних і фармацевтичних працівників.
Деякі схеми лікування можуть включати лікарські засоби, застосовані за межами їхніх показань та/або не зареєстровані в Україні.
Комбінація обінутузумаб-леналідомід не зареєстрована в Україні на 14.02.2022. Комбінація мозунетузумаб-леналідомід не зареєстрована в Україні на 14.02.2022.
Запит медичної інформації про продукти ТОВ «Рош Україна» ви можете надіслати на електронну адресу: ukraine.medinfo@roche.com.
ТОВ «Рош Україна», м. Київ, 03150, вул. Велика Васильківська, 139. Тел.: +380 (44) 354-30-40, факс: +380 (44) 354-30-41. www.roche.ua.
Багатомовна глобальна гаряча лінія для медичних працівників та пацієнтів за тел.: +36 146-182-58. WhatsApp/SMS: +36 707-177-394; e-mail: patientcare@roche.com.
Повідомити про побічні явища під час лікування препаратом ТОВ «Рош Україна» або поскаржитись на якість препарату ви можете за контактними реквізитами офісу або на електронну адресу: ukraine.safety@roche.com.
M-UA-00000590
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 1 (74)-2 (75) 2022 р.



