13 жовтня, 2022
Порівняльне вивчення ефективності Холоплант®‑Тау в лікуванні гіпомоторної дисфункції жовчного міхура, асоційованої з біліарним сладжем
Актуальність проблеми
 Однією з актуальних проблем сучасної гастроентерології є функціональні біліарні розлади (ФБР). Цей термін характеризує комплекс клінічних симптомів, які розвиваються в результаті моторнотонічної дисфункції жовчного міхура (ЖМ) та/або сфінктерного апарату жовчовивідних шляхів (ЖВШ) [2, 3]. Зазвичай ФБР проявляються такими симптомами, як відчуття тяжкості, дискомфорт або больовий синдром у правому підребер’ї, нудота, гіркота в роті, зниження апетиту, огида до жирної їжі, порушення випорожнення (закрепи чи проноси), метеоризм та/або флатуленція.
Однією з актуальних проблем сучасної гастроентерології є функціональні біліарні розлади (ФБР). Цей термін характеризує комплекс клінічних симптомів, які розвиваються в результаті моторнотонічної дисфункції жовчного міхура (ЖМ) та/або сфінктерного апарату жовчовивідних шляхів (ЖВШ) [2, 3]. Зазвичай ФБР проявляються такими симптомами, як відчуття тяжкості, дискомфорт або больовий синдром у правому підребер’ї, нудота, гіркота в роті, зниження апетиту, огида до жирної їжі, порушення випорожнення (закрепи чи проноси), метеоризм та/або флатуленція.
В індустріально розвинених країнах ФБР спостерігають у ≈5% усього дорослого населення, хоча в осіб віком від 60 років їхня частота зростає до ≈25%. ФБР значно частіше зустрічаються в жінок, ніж у чоловіків (20 і 8% відповідно).
В основі розвитку ФБР лежить порушення синхронності роботи ЖМ і сфінктерів ЖВШ унаслідок їхніх неузгоджених надмірних (гіперфункція) або недостатніх (гіпофункція) скорочень. Вважається, що важливу роль у розвитку ФБР відіграють психоемоційні перевантаження і соціальна дезадаптація, які в поєднанні з генетичною схильністю визначають формування дисмоторних порушень і вісцеральної гіперчутливості [8].
Виокремлюють первинні та вторинні функціональні розлади біліарної системи [3]. Первинні дисфункції відзначають у середньому в 10-15% випадків; вони трапляються переважно в жінок молодого віку (18-35 років) астенічної конституції тіла з емоційно лабільною психікою. Їхній розвиток пов’язують з порушеннями нервово-гуморальної регуляції моторики ЖВШ на тлі психоневротичних, конституціональних, ендокринних впливів, при цьому ознаки супутньої органічної патології (запалення, каменеутворення) відсутні. Первинні порушення скоротливості можуть мати вроджений (генетично детермінований) характер і бути пов’язані з порушенням чутливості посмугованих м’язів ЖМ до різних стимулювальних імпульсів, серед яких провідну роль відіграють холецистокінін, мотилін і вагусні парасимпатичні впливи [2, 8]. Вторинні дисфункції зустрічаються значно частіше – за супутньої органічної патології, деяких гормональних порушень та ендокринних захворювань (наприклад, передменструального та клімактеричного синдромів, вагітності, цукрового діабету, патології щитоподібної залози), системних захворювань, психоемоційних порушень. Вторинні дисфункції часто розвиваються при жовчнокам’яній хворобі (ЖКХ), навіть на її ранніх стадіях і за відсутності клінічних симптомів (до 80%), а також в умовах запалення [1, 3]. Нерідко вторинна гіпотонія ЖМ зумовлена порушенням відтоку жовчі та високим опором у протоках за функціонального (спазм) або органічного (стриктура, папіліт) ураження слизової оболонки.
Функціональний розлад ЖМ (ФРЖМ) – це порушення скоротливої функції ЖМ, що проявляється болем біліарного типу внаслідок первинних метаболічних (перенасичення жовчі холестерином) або рухових порушень за відсутності конкрементів і структурних змін з боку стінки ЖМ. ФРЖМ розподіляють на два типи – гіперкінетичну (гіпермоторну) та гіпокінетичну (гіпомоторну) дисфункцію ЖМ (ДЖМ) [7].
Перебіг ДЖМ частіше відбувається переважно за гіпокінетичним типом із порушенням його скоротливості чи спорожнення. Діагностичні критерії гіпомоторної ДЖМ відповідно до Римських критеріїв IV наведено в таблиці 1.
Важливу роль у ґенезі функціонального біліарного болю відіграють формування біліарного сладжу (БС) і подальша поява в жовчі мікролітів [1, 2, 9].
Як відомо, основні етапи холестеринового літоґенезу передбачають:
1) перенасичення жовчі холестерином;
2) нуклеацію і преципітацію кристалів холестерину;
3) агрегацію кристалів і формування мікролітів.
З теоретичного та практичного погляду найприйнятнішою є діагностика передкам’яної стадії ЖКХ на III етапі – агрегація кристалів моногідрату холестерину з подальшим формуванням мікролітів [1]. Зміна мікроструктури жовчі у вигляді мікролітів, що сформувалися, роблять їх макроскопічно видимими, що легко виявляється за допомогою трансабдомінальної ультрасонографії та трактується як різні варіанти БС, за наявності якого з метою запобігання утворенню більших жовчних каменів слід проводити профілактику препаратами урсодезоксихолевої кислоти (УДХК) та/або жовчогінними засобами.
БС, що містить мікроліти, може вільно проходити всією системою протоків, постійно подразнюючи численні больові рецептори слизової оболонки жовчних шляхів (особливо сфінктерного апарату), та зумовлювати виникнення больового синдрому. За останніми даними, він може бути причиною незрозумілого болю в правому підребер’ї у 83% хворих [1, 4, 7]. Причиною болю при БС є також дисфункції сфінктерного апарату жовчних шляхів, які в цій ситуації мають вторинний характер. Так, наприклад, дисфункція сфінктера Одді за БС виявляється в 50-93% випадків. Окрім того, тривала персистенція БС і постійний пасаж його в дванадцятипалу кишку може ускладнюватися розвитком стриктур термінального відділу загальної жовчної протоки та/або стенозувального папіліту. БС також розглядається як часта причина біліарного панкреатиту. Дослідженнями встановлено, що частота виявлення БС у хворих з ідіопатичним панкреатитом доволі висока та, за даними різних авторів, сягає 33-90% [4, 5]. Основні причини розвитку панкреатиту в разі БС зумовлені дисфункцією сфінктера Одді, що створює умови для біліарних рефлюксів у проточну систему підшлункової залози, стенозом сфінктера Одді та/або панкреатичної протоки. Рідкісніші ускладнення БС – розвиток гострого холециститу та холангіту. В окремих випадках за наявності замазкоподібної жовчі можливе відключення ЖМ унаслідок закупорювання міхурової протоки.
Висока поширеність БС у хворих із патологією біліарної системи (40-50% від усіх хворих) надала змогу накопичити значний клінічний матеріал, який свідчить про особливості його клінічного перебігу, прогноз, ускладнення, що обґрунтовує необхідність проведення якісної діагностики й ефективної терапії. Основне клінічне значення БС полягає у тому, що він є джерелом каменеутворення. Однак це аж ніяк не означає, що у всіх хворих із БС обов’язково утворюється каміння. Незважаючи на те, що БС є вихідним матеріалом для формування жовчних каменів, вони, за різними оцінками, утворюються тільки в 5-20% пацієнтів за 1-3-річний період. Це пов’язано з тим, що при зникненні причин, які сприяють утворенню БС, останній зникає спонтанно.
За клінічних ознак гіпомоторної ДЖМ і наявності в ЖМ БС для зниження літогенних властивостей жовчі з метою запобігання формуванню надалі жовчних конкрементів рекомендується прийом препаратів УДХК і жовчогінних засобів [9]. Однією з властивостей УДХК є здатність зменшувати насиченість жовчі холестерином за рахунок пригнічення абсорбції у кишечнику та пригнічення синтезу в печінці, що супроводжується зниженням його секреції у жовчі. У зв’язку із цим клінічний ефект препаратів УДХК при БС насамперед зумовлений зниженням літогенності жовчі, отже, й збільшенням часу нуклеації, що зрештою запобігає утворенню мікролітів, а також сприяє розчиненню холестеринових каменів. Курс лікування препаратами, що містять УДХК, залежить від форми БС. Для елімінації БС у вигляді суспензії гіперехогенних частинок зазвичай достатньо 1-місячного курсу лікування. В разі інших його форм курс лікування триваліший, але зазвичай не перевищує 3 міс. Ефективність лікування препаратами УДХК до 3 міс (залежно від виду БС) становить 75-85%.
Одним з інноваційних комбінованих препаратів, що містять УДХК і застосовуються для лікування БС і попередження формування холестеринових конкрементів, є Холоплант®-Тау. Цей комбінований препарат містить 4 компоненти: екстракт листя артишоку (200 мг), УДХК (100 мг), екстракт кореня дягелю китайського (50 мг) і таурин (100 мг). Останній являє собою амінокислоту, яка зв’язується з УДХК та іншими вільними жовчними кислотами, підвищуючи їхню біологічну активність, холеретичні й антиоксидантні властивості. Таке поєднання компонентів Холоплант®-Тау зменшує або усуває застій жовчі, зменшує БС, знижує імовірність утворення холестеринових конкрементів, зменшує / знімає спазм і запалення. Зазвичай застосовується по 1-2 капсули 3 р/день протягом ≥1 міс.
Мета дослідження – провести клінічне вивчення ефективності застосування Холоплант®-Тау за гіпомоторної ДЖМ, асоційованої з наявністю БС, порівняно з іншими комбінованими жовчогінними препаратами.
Матеріали та методи
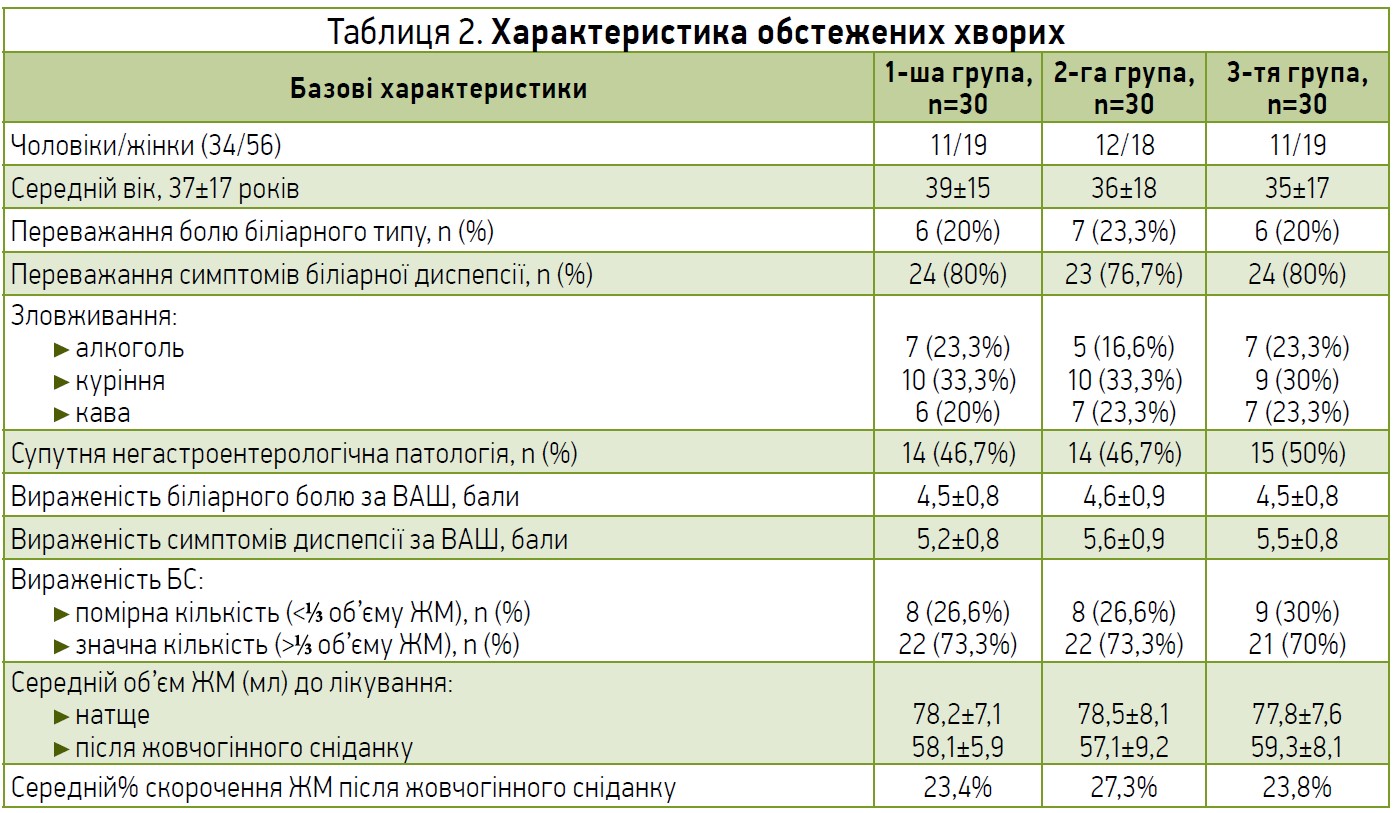
З цією метою обстежено 90 хворих (56 жінок, 34 чоловіків) із гіпомоторною ДЖМ і наявністю БС у ЖМ віком від 20 до 55 років (середній вік – 37±17 років), у яких за результатами додаткових лабораторних та інструментальних досліджень структурних змін із боку печінки, ЖМ і ЖВШ виявлено не було. Всі хворі були зіставними за віком і статтю. Діагноз гіпомоторної ДЖМ установлювали відповідно до Римських критеріїв IV. Усім хворим виконували загальноклінічні та біохімічні аналізи, зокрема дослідження печінкових проб і ліпідного спектра сироватки крові. Для виключення органічної патології усім хворим до лікування проводили верхню ендоскопію (ендоскопічна система Olympas Optera G‑140, Японія) та УЗД органів черевної порожнини (ультразвуковий сканер експертного класу Toshiba Aplio MX, Японія). Також усім хворим двічі (до і після курсового призначення терапії протягом 4 тиж) проводили динамічне УЗД ЖМ з автоматичним апаратним обчисленням його об’єму до і через 30 хв після жовчогінного сніданку (30 г сорбіту в 100 мл теплої води).
Залежно від схеми проведеного лікування всі пацієнти за допомогою комп’ютерного методу випадкових чисел у співвідношенні 1:1:1 були рандомізовані на 3 групи. До 1-ї групи залучили 30 хворих, які отримували традиційне базисне лікування, що передбачало дієту № 5, прийом рослинного жовчогінного та гепатотропного препарату Артіхол, який містить 200 мг сухого екстракту артишоку (по 1 таблетці 3 р/день протягом 4 тиж). Хворим 2-ї групи (30 пацієнтів) замість Артіхолу призначали Гепабене (комбінований гепатотропний і жовчогінний препарат рослинного походження, що містить екстракти рутки лікарської та розторопші плямистої) по 1 капсулі 3 р/день протягом 4 тиж. Хворим 3-ї групи (30 пацієнтів) призначали Холоплант®-Тау по 1 капсулі 3 р/день упродовж 4 тиж. За наявності нападоподібного болю в правому підребер’ї хворим усіх груп додатково призначали спазмолітик за потреби.
Базисну характеристику обстежених хворих наведено в таблиці 2.
Ефективність лікування в різних групах хворих оцінювали за динамікою клінічних симптомів і даними динамічного УЗД через 4 тиж після початку курсового лікування. Хорошими результатами лікування вважали зникнення або суттєве зменшення симптомів (на ≥5 балів) біліарної диспепсії та біліарного болю за візуально-аналоговою шкалою (ВАШ), зникнення УЗ-ознак БС чи його зменшення на >½ об’єму, поліпшення / нормалізація скоротливої функції ЖМ за результатами динамічного УЗД. Задовільними результатами лікування вважали зменшення вираженості симптомів біліарної диспепсії та біліарного болю (на 2-4 бали), зменшення БС у ЖМ на ⅓ об’єму, поліпшення скоротливої функції ЖМ за результатами динамічного УЗД.
Результати
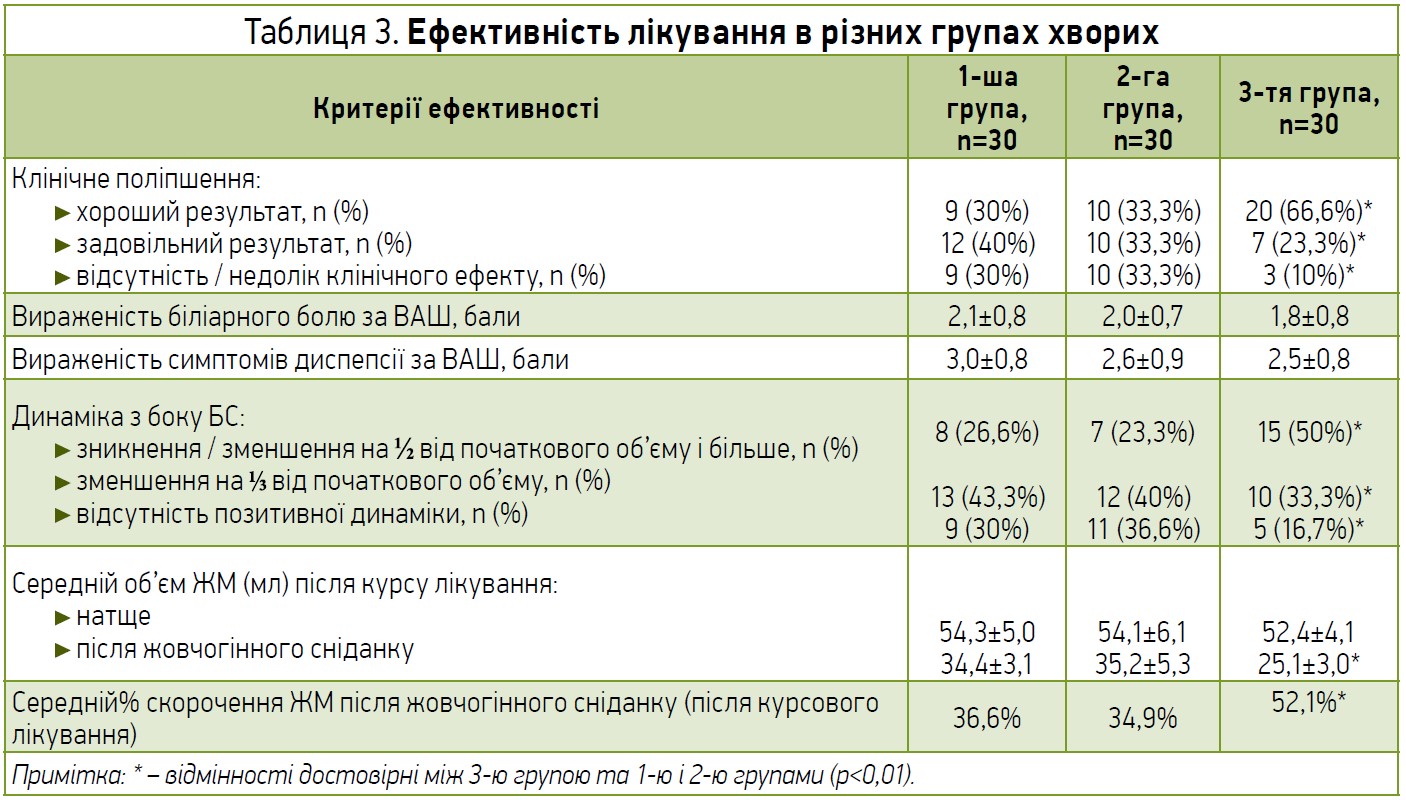
Отримані результати продемонстровано в таблиці 3. У більшості хворих усіх трьох груп 4-тижневий курс лікування супроводжувався достовірним зниженням інтенсивності біліарного болю і диспепсії порівняно з вихідним рівнем. Проте у хворих 3-ї групи, що застосовували Холоплант®-Тау, лікування супроводжувалося істотно вираженішим загальним клінічним ефектом порівняно з результатами лікування в 1-й і 2-й групах. Зокрема, у 3-й групі хороші та задовільні клінічні результати продемонстрували 20 (66,5%) і 7 (23,3%) хворих відповідно (загалом у 27 із 30 хворих, 90%), що було достовірно вищим, ніж у 1-й (21 із 30 хворих, 70%; р<0,01) та в 2-й групах (поліпшення у 20 із 30 хворих, 66,6%; р<0,01). Недостатня ефективність курсового лікування в 1-й і 2-й групах зафіксована в 30 і 33,3% випадків відповідно, тоді як у 3-й групі – тільки в 10% хворих (р<0,01). Крім того, курсове лікування препаратом Холоплант®-Тау супроводжувалося достовірною позитивною динамікою з боку БС. Так, у 1-й і 2-й групах хворих зникнення або зменшення об’єму БС на >½ об’єму ЖМ було приблизно однаковим і зафіксоване відповідно тільки в 26,6 і 23,3% хворих, що було достовірно нижчим, ніж серед хворих 3-ї групи (50% випадків, р<0,01).
У результаті застосування Холоплант®-Тау достовірно поліпшилася також і скорочувальна функція ЖМ. Так, після курсу лікування об’єм ЖМ натще в 3-й групі хворих достовірно зменшився, а його скорочувальна здатність у відповідь на приймання стандартного жовчогінного сніданку за результатами динамічного УЗД достовірно покращилася або нормалізувалася (середній об’єм ЖМ натще зменшився із 77,8±7,6 мл до 52,4±4,1 мл (р<0,05), а відсоток скорочення ЖМ після жовчогінного сніданку до і після лікування достовірно підвищився та становив 23,8 і 52,1% відповідно, р<0,01). У 1-й і 2-й групах хворих після лікування середній об’єм ЖМ хоча й зменшився, проте ступінь його скорочення після жовчогінного сніданку був достовірно нижчим, ніж у 3-й групі (34,9 і 36,6% відповідно проти 52,1%; р<0,01). Всі досліджувані параметри у хворих 3-ї групи були достовірно кращими, ніж у хворих 1-ї та 2-ї груп, у яких параметри, що порівнювалися, були приблизно зіставними. Кількість вжитих доз спазмолітиків за потреби виявилася зіставною у всіх групах порівняння. Будь-яких серйозних побічних ефектів, які б потребували скасування прийому Холоплант®-Тау, зафіксовано не було. Отже, курсове застосування Холоплант®-Тау (по 1 капсулі 3 р/день протягом 4 тиж) супроводжувалося істотним клінічним ефектом і поліпшенням скоротливої функції ЖМ, які були достовірно вищими, ніж при застосуванні інших гепатотропних і жовчогінних препаратів (Артіхол, Гепабене).
Висновки
Отже, проведене нами відкрите рандомізоване порівняльне дослідження свідчить при високу клінічну ефективність і безпеку препарату Холоплант®-Тау у хворих із гіпомоторною ДЖМ, асоційованою із БС.
Застосування Холоплант®-Тау по 1 капсулі 3 р/день протягом 4 тиж надало змогу досягти не лише клінічного поліпшення (зменшення / зникнення біліарного болю і біліарної диспепсії), а й покращити скорочувальну функцію ЖМ, зменшити БС та літогенний потенціал жовчі, отже, і ймовірність каменеутворення в переважної більшості хворих із гіпомоторною ДЖМ, що перевищувало ефективність застосування інших препаратів порівняння за аналогічними показниками. Саме тому Холоплант®-Тау слід розглядати як препарат вибору з метою монотерапії для лікування функціональної біліарної патології (насамперед гіпомоторної ДЖМ, асоційованої з БС).
Література
- Вовк Е.И. Желчнокаменная болезнь в XXI веке: лечение или профилактика? Consilium Medicum, 2010, 2: 37-44.
- Лоранская И.Д., Кукушкин М.Л., Малохова Е.В., Вишневская В.В. Дисфункции билиарного тракта: механизмы регуляции боли, диагностические критерии. Гепатология, 2004, 5: 10-15.
- Минушкин О.Н., Масловский Л.В. Диагностика и лечение функциональных расстройств билиарного тракта. РМЖ (Русский медицинский журнал), 2010, 18 (5): 277-279.
- Behar J., Corazziari E., Guelrud M. et al. Functional gallbladder and sphincter of Oddi disorders. Gastroenterol., 2006, 130: 1498-1509.
- Bennett E., Evans P., Dowsett J. et al. Sphincter of Oddi dysfunction: psychosocial distress correlates with manometric dyskinesia but not stenosis. World J Gastroenterol 2009; 15: 6080-5.
- Drossman D.A. Functional Gastrointestinal Disorders: History, Pathophysiology, Clinical Features, and Rome IV. Gastroenterology, 2016. – Vol 150 / – № 6. – P. 1262-1279.
- Goussous N., Kowdley G.C., Sardana N. et al. Gallbladder dysfunction: How much longer will it be controversial? Digestion 2014; 90: 147-154.
- Kurucsai G., Joo I., Fejes R. et al. Somatosensory hypersensitivity in the referred pain area in patients with chronic biliary pain and a sphincter of Oddi dysfunction: new aspects of an almost forgotten pathogenetic mechanism. Am J Gastroenterol 2008; 103: 2717-25.
- Rastogi A., Slivka A., Moser A.J. et al. Controversies concerning pathophysiology and management of acalculous biliary-type abdominal pain. Dig Dis Sci 2005; 50: 1391-401.
Медична газета «Здоров’я України 21 сторіччя» № 12 (529), 2022 р.