9 листопада, 2022
Рак нирки: еволюція медикаментозного лікування
Рак нирки сьогодні становить від 3 до 5% від усіх злоякісних новоутворень та уражає як чоловіків, так і жінок. Упродовж останніх років відзначається тенденція до підвищення частоти його поширення у популяції, щорічно захворюваність на рак нирки (РН) зростає на 2-4%. У 2018 р. за даними Globocan у світі було зареєстровано 403 262 випадки захворювання на нирковоклітинну карциному (НКК) та 175 098 випадків смерті. 22 червня цього року до Всесвітнього дня обізнаності про рак нирки проведено вебінар, у рамках якого провідні експерти галузі обговорювали нагальні питання ведення хворих на РН.
 Відкрив семінар головний лікар Національного інституту раку (м. Київ), кандидат медичних наук Андрій Петрович Безносенко.
Відкрив семінар головний лікар Національного інституту раку (м. Київ), кандидат медичних наук Андрій Петрович Безносенко.
– Незважаючи на всі обставини в нашій країні, платформа OncoHub відновлює серію вебінарів, семінарів і майстер-класів. Сьогоднішній вебінар присвячено Всесвітньому дню обізнаності про рак нирки, в рамках якого обговоримо актуальні питання онкоурології, зокрема стандарти медикаментозного та хірургічного лікування РН.
.jpg) Завідувачка відділення хіміотерапії № 1 КНП КОР «Київський міський клінічний онкологічний центр», доцент кафедри онкології Національного університету охорони здоров’я України імені П.Л. Шупика, кандидат медичних наук Ольга Володимирівна Пономарьова у своїй доповіді сфокусувалася на аспектах медикаментозного лікування РН.
Завідувачка відділення хіміотерапії № 1 КНП КОР «Київський міський клінічний онкологічний центр», доцент кафедри онкології Національного університету охорони здоров’я України імені П.Л. Шупика, кандидат медичних наук Ольга Володимирівна Пономарьова у своїй доповіді сфокусувалася на аспектах медикаментозного лікування РН.
– За сучасними даними частота НКК, яка визнана найпоширенішою формою РН, становить 2-3% від усіх злоякісних новоутворень у дорослих. При цьому саме на НКК припадає до 90% усіх випадків РН. За останні 20 років рівень захворюваності на НКК зріс на 2%, і сьогодні в Європі щорічно реєструють 84 тис. нових випадків [1, 2]. Що стосується випадків смерті внаслідок НКК, то у Європі смертність збільшувалася до початку 1990-х рр., проте завдяки впровадженню в клінічну практику сучасних алгоритмів медикаментозного лікування наразі ці показники стабілізувалися, а в подекуди зменшилися. І сьогодні у світі кількість випадків смерті внаслідок НКК сягає 102 тис., у Європі цей показник є ще меншим – до 34 тис. [3].
Ключовою проблемою ведення хворих з НКК є той факт, що у багатьох із них симптоми відсутні, навіть на пізніх стадіях захворювання. Класична тріада симптомів НКК, яка представлена болем у боці, гематурією та абдомінальним утворенням, наявна всього у 6-10% пацієнтів цієї групи. Безсимптомний перебіг НКК призводить до того, що на момент діагностики у 25-30% пацієнтів вже є метастази [4]. Найбільш поширене метастазування у легені, м’які тканини, кістки та печінку. П’ятирічна виживаність у разі поширеного захворювання є низькою та складає 70-95% для локалізованої, 10-65% – для місцево-поширеної та <5% для метастатичної форми [5].
Історія лікування НКК бере свій початок з 1992 р., коли ключовими його варіантами були такі біологічні агенти, як інтерферон-α та інтерлейкін-2 (рис. 1). З плином часу терапія НКК еволюціонувала: з початку 2000-х рр. включала застосування кількох різних молекул – інгібіторів тирозинкінази, зокрема сорафенібу, сунітинібу, темсиролімусу та ін. Проте всі ці варіанти терапії не забезпечували значного клінічного ефекту, і після 2010 р. науковий світ повернувся до проблеми пошуку нових варіантів лікування НКК.
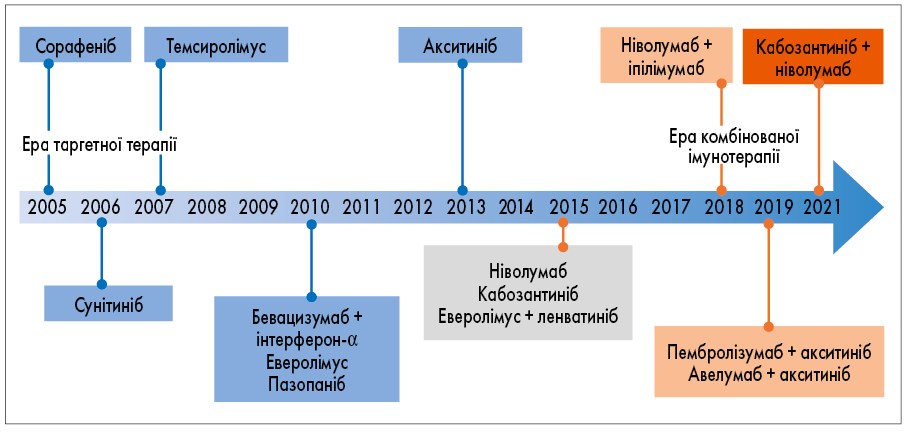 Рис. 1. Еволюція медикаментозної терапії НКК
Рис. 1. Еволюція медикаментозної терапії НКК
У 2015 р. у клінічну практику впроваджено потужний інгібітор тирозинкінази – кабозантиніб, а з 2016 р. на світовий фармацевтичний ринок активно почали виводити інгібітори контрольних точок, відомими представниками яких є ніволумаб і пембролізумаб. Після 2015 р. започатковано еру комбінованої медикаментозної терапії метастатичної НКК (мНКК), зокрема стали застосовувати такі поєднання, як ніволумаб та іпілімумаб, пембролізумаб та акситиніб, кабозантиніб та ніволумаб тощо [6].
Близько 50% хворих на РН потребують або потребуватимуть у майбутньому проведення системної терапії. Це пов’язано з тим, що майже 30% пацієнтів з РН на момент встановлення діагнозу вже мають метастази. Застосування лише радикального хірургічного втручання також не вирішує цю проблему: у 20-30% хворих після проведення операції розвивається активний метастатичний процес [7, 8].
Найпоширенішим варіантом РН є світлоклітинний рак, частота якого становить від 65 до 85%. Інші гістологічні типи раку, такі як папілярний (1 і 2 типів) та хромофорний є менш поширеними – 7-14 та 4-10% відповідно.
Наявні рекомендації регламентують, що ведення хворих на РН передбачає використання прогностичних моделей ризику – Меморіального онкологічного центру ім. Слоуна – Кеттерінга (MSKCC) та Міжнародного консорціуму з метастатичного нирковоклітинного раку (IMDC). Прогностичні моделі дають змогу розподілити всіх хворих на РН на три групи щодо прогнозу: сприятливий (відсутні прогностичні фактори ризику), сумнівний (1-2 фактори ризику) та несприятливий (≥2 факторів ризику). При цьому кількість факторів ризику прямо асоціюється з виживаністю пацієнтів. Відповідно хворі з групи несприятливого прогнозу мають найгірші показники загальної виживаності (ЗВ) порівняно з групою сумнівного та сприятливого прогнозу [9].
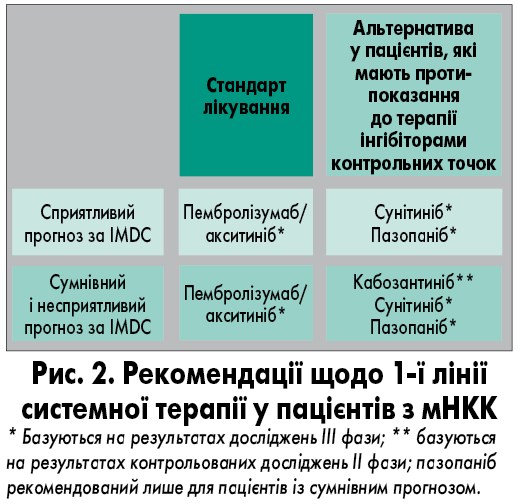 На основі міжнародних рекомендацій складено вітчизняний протокол надання медичної допомоги хворим на рак нирки [10]. Якщо проаналізувати рекомендації щодо системної терапії 1-ї та 2-ї ліній у пацієнтів з мНКК, можна помітити, що в обидві включено кабозантиніб (рис. 2, 3). Кабозантиніб також входить до останніх міжнародних настанов таких відомих медичних спільнот, як Національна онкологічна мережа США (NCCN) та Європейська асоціація урологів (EAU), як монотерапія, так і в комбінації з іншими препаратами.
На основі міжнародних рекомендацій складено вітчизняний протокол надання медичної допомоги хворим на рак нирки [10]. Якщо проаналізувати рекомендації щодо системної терапії 1-ї та 2-ї ліній у пацієнтів з мНКК, можна помітити, що в обидві включено кабозантиніб (рис. 2, 3). Кабозантиніб також входить до останніх міжнародних настанов таких відомих медичних спільнот, як Національна онкологічна мережа США (NCCN) та Європейська асоціація урологів (EAU), як монотерапія, так і в комбінації з іншими препаратами.
Кабозантиніб – низькомолекулярний інгібітор тирозинкінази, який пригнічує множинні VEGFR, зокрема MET, AXL та VEGFR-1-3, за рахунок того, що чинить вплив не лише на шлях VEGFR, а й мультитаргетний (багатоцільовий) вплив при лікуванні НКК. Це може допомогти при боротьбі з резистентністю до інгібіторів VEGFR. Результати нещодавно проведеного рандомізованого багатоцентрового відкритого дослідження II фази CABOSUN продемонстрували, що кабозантиніб є більш ефективним порівняно з сунітинібом: частота контролю захворювання дорівнювала 75 проти 47%, прогресування захворювання 18 проти 29% відповідно [11]. На фоні терапії кабозантинібом реєструвалося зниження ризику прогресування або смерті на 52% порівняно з сунітинібом [12]. Результати іншого дослідження, в якому оцінювали ефективність і безпеку застосування кабозантинібу при мНКК, засвідчили, що препарат є безпечним, характеризується прийнятною переносимістю та багатообіцяючою протипухлинною активністю у популяції пацієнтів з мНКК в умовах клінічної практики [13].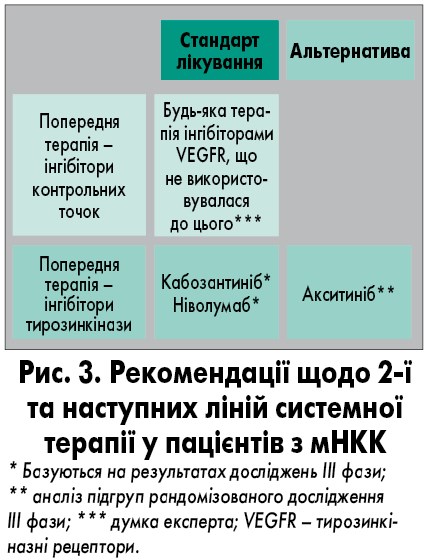
.jpg) Про варіанти хірургічного лікування РН розповів старший науковий співробітник відділення пластичної та реконструктивної онкоурології Національного інституту раку (м. Київ), кандидат медичних наук Олександр Едуардович Стаховський.
Про варіанти хірургічного лікування РН розповів старший науковий співробітник відділення пластичної та реконструктивної онкоурології Національного інституту раку (м. Київ), кандидат медичних наук Олександр Едуардович Стаховський.
– Відповідно до сучасних рекомендацій, стандартом лікування РН є системна терапія, проте у деяких випадках може бути доцільним хірургічне лікування. При відсутності даних, що підтверджують онкологічні переваги одного виду лікування над іншим, стратегії ведення пацієнтів із РН часто різняться. Наприклад, нефректомія показана при розмірі пухлини >4 см, тоді як при менших пухлинах, розміром <3 см, може бути розглянута тактика органозбережного лікування [14]. Остання опція пов’язана з тим, що сьогодні все більшого поширення набувають саме органозбережні операції, це відображено і в міжнародних рекомендаціях.
Водночас важливо розуміти, що функціональна паренхіма, яка залишається після проведення органозбережної операції, пов’язана з розміром пухлини та подальшим функціонуванням органа. Тобто чим більший розмір пухлини буде видалено, тим гіршою стане функція нирки, відповідно, чим більшу частину функціональної паренхіми буде залишено, тим кращою буде функція органа.
Ще однією важливою проблемою, з якою стикаються клініцисти при веденні пацієнтів із РН, є проблема вчасної діагностики захворювання. Відомо, що перебіг РН у 80% випадків є безсимптомним, захворювання зазвичай виявляють випадково при проведенні ультразвукового дослідження. Крім того, саме по собі оцінювання РН променевими методами діагностики є складним і багатофакторним процесом, що має свої обмеження. Враховуючи ці обмеження, група дослідників розробила новий метод діагностики РН – N.C.I.U. нефрометрію. Метод враховує локалізацію пухлини і дає більше шансів пацієнту на органозбережне лікування. Впровадження цього методу діагностики в клінічну практику дозволить об’єктивізувати та значно звузити показання до інвалідизуючої операції – нефректомії – у хворих на НКК. Це згодом сприятиме підвищенню ефективності лікування пацієнтів цієї групи за рахунок збереження функції нирок, відповідно – тривалості і якості життя хворих, а також зниженню частоти розвитку ниркової недостатності й інвалідизації. На базі Клініки пластичної та реконструктивної онкоурології Національного інституту раку виконано ретроспективний аналіз даних хворих на мНКК, яким проводили хірургічне лікування з 2008 по 2014 р. Загалом до аналізу були включені дані 116 осіб (86 чоловіків; 30 жінок; вік 55,9±6,4 року). Період спостереження становив 19,3±12 міс. Ключова мета дослідження – оцінювання ефективності циторедуктивної резекції як методу хірургічного лікування хворих на мНКК.
Результати дослідження продемонстрували, що у разі полярного чи латерального розміщення пухлини порогове значення об’єму функціонуючої паренхіми нирки, при якому доцільно виконувати резекцію, є >55%. При медіальному розташуванні злоякісного новоутворення основним показанням до проведення резекції нирки є розмір пухлини.
Таким чином, хоча сьогодні в арсеналі хірургів є декілька варіантів оперативного лікування РН, органозбережне втручання при локалізованій НКК має розглядатися як перша опція. Факторами, що впливають на органозбережну тактику лікування НКК, є розмір, локалізація пухлини, функція нирок, супутня патологія та поширеність процесу.
 Співзасновниця Благодійного фонду Inspiration Family Міла Реутова порушила нагальне питання необхідності розбудови пацієнторієнтованої онкологічної допомоги в Україні.
Співзасновниця Благодійного фонду Inspiration Family Міла Реутова порушила нагальне питання необхідності розбудови пацієнторієнтованої онкологічної допомоги в Україні.
– Inspiration Family – благодійний фонд підтримки дорослих онкопацієнтів. Фонд був створений у вересні 2020 р. Його засновницями стали п’ять жінок, котрі перенесли рак і тепер допомагають іншим. Ключова місія благодійного фонду полягає у розбудові пацієнторієнтованого надання онкологічної допомоги в Україні. Три основні напрями діяльності фонду охоплюють системні зміни у сфері «дорослої» онкології, інформаційну й емоційну підтримку дорослих онкопацієнтів, а також просвітницьку роботу.
Повномасштабна війна на території нашої країни внесла значні корективи в діяльність фонду, і сьогодні основні напрями діяльності Inspiration Family включають представлення України на міжнародному рівні, інформування міжнародної спільноти про лікування раку під час війни, збирання інформації від закордонних клінік і координування пацієнтів для виїзду на лікування за кордон, якщо таке лікування неможливо отримати у нашій країні.
Протягом всіх місяців війни фонд набув значного досвіду щодо координування пацієнтів у цих складних умовах. Координування онкохворих є вкрай важливим, оскільки допомагає пацієнтам отримати лікування й уникнути шахраїв.
Література
- Escudier B., Porta C., Schmidinger M. et al. Renal cell carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2014 Sep; 25 (suppl. 3): iii49-56. doi: 10.1093/annonc/mdu259.
- Ljungberg B., Bensalah K., Canfield S. et al. EAU guidelines on renal cell carcinoma: 2014 update. Eur Urol. 2015 May; 67(5): 913-24. doi: 10.1016/j.eururo.2015.01.005.
- NCCN. Clinical Practice Guidelines in Oncology. Kidney Cancer. 2016. Version 2.
- Linehan W.M., Pinto P.A., Bratslavsky G. et al. Hereditary kidney cancer. Cancer. 2009; 115 (is. S10): 2252-61.
- Delacroix S., Wood C., Jonasch E. et al. Renal Neoplasia. https://d2ogjlfjkptkow.cloudfront.net/putextbook/2.pdf.
- Klaassen Z. ASCO 2019: Evolving Front-Line Therapy in Metastatic Renal Cell Carcinoma. Urotoday. 2019.
- Patil S., Manola J., Elson P. et al. Improvement in overall survival of patients with advanced renal cell carcinoma: prognostic factor trend analysis from an international data set of clinical trials. J. Urol. 2012; 188: 2095-100. doi: 10.1016/j.juro.2012.08.026.
- Eggener S.E., Yossepowitch O., Pettus J.A. et al. Renal cell carcinoma recurrence after nephrectomy for localized disease: predicting survival from time of recurrence. J Clin Oncol. 2006 Jul 1; 24(19): 3101-6. doi: 10.1200/JCO.2005.04.8280.
- Manola J., Royston P., Elson P. et al. Prognostic model for survival in patients with metastatic renal cell carcinoma: results from the international kidney cancer working group. Clin Cancer Res. 2011; 17: 5443-50.
- Наказ МОЗ України від 20.06.2022 № 1061 «Про затвердження Уніфікованого клінічного протоколу первинної, вторинної (спеціалізованої) та третинної (високоспеціалізованої) медичної допомоги «Рак нирки».
- Choueiri T.K., Halabi S., Sanford B.L. et al. Cabozantinib Versus Sunitinib As Initial Targeted Therapy for Patients With Metastatic Renal Cell Carcinoma of Poor or Intermediate Risk: The Alliance A031203 CABOSUN Trial. J Clin Oncol. 2017 Feb 20; 35(6): 591-7. doi: 10.1200/JCO.2016.70.7398.
- Choueiri T.K., Hessel C., Halabi S. et al. Cabozantinib versus sunitinib as initial therapy for metastatic renal cell carcinoma of intermediate or poor risk (Alliance A031203 CABOSUN randomised trial): Progression-free survival by independent review and overall survival update. Eur J Cancer. 2018 May; 94: 115-125. doi: 10.1016/j.ejca.2018.02.012.
- Peverelli G., Raimondi A., Ratta R. et al. () Cabozantinib in Renal Cell Carcinoma With Brain Metastases: Safety and Efficacy in a Real-World Population. Clin Genitourin Cancer. 2019 Aug; 17(4): 291-8. doi: 10.1016/j.clgc.2019.05.002.
- Stakhovskyi O., Yap S.A., Leveridge M. et al. Small Renal Mass: What the Urologist Needs to Know for Treatment Planning and Assessment of Treatment Results. Amer J Roentgenol. 2011; 196: 1267-73. 10.2214/AJR.10.6336.
Підготувала Анна Хиць
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 4 (77) 2022 р.



