25 листопада, 2022
Багатоцентрове рандомізоване відкрите порівняльне дослідження ефективності назального спрея Аква Маріс® Екстра Стронг як симптоматичної терапії за відкладеного призначення антибіотиків у лікуванні гострого риносинуситу в дітей 6-11 років
Переклад оригінальної статті, розміщеної в American Journal of Otolaryngology–Head and Neck Medicine and Surgery
 Гострий риносинусит (ГРС) – найчастіша респіраторна інфекція. Поняття «риносинусит» (РС) почало широко використовуватися з 2005 року, оскільки було доведено, що запальний процес розвивається одночасно в порожнині носа та приносових пазухах [1]. У подальшому було проведено велику кількість присвячених ГРС досліджень, результати яких узагальнено в EPOS 2020 – європейському погоджувальному документі щодо діагностики й лікування гострого та хронічного риносинуситу і назальних поліпів [2]. Відповідно до сучасних поглядів, поняття ГРС включає три нозологічні форми: гострий вірусний РС, поствірусний РС і бактеріальний РС.
Гострий риносинусит (ГРС) – найчастіша респіраторна інфекція. Поняття «риносинусит» (РС) почало широко використовуватися з 2005 року, оскільки було доведено, що запальний процес розвивається одночасно в порожнині носа та приносових пазухах [1]. У подальшому було проведено велику кількість присвячених ГРС досліджень, результати яких узагальнено в EPOS 2020 – європейському погоджувальному документі щодо діагностики й лікування гострого та хронічного риносинуситу і назальних поліпів [2]. Відповідно до сучасних поглядів, поняття ГРС включає три нозологічні форми: гострий вірусний РС, поствірусний РС і бактеріальний РС.
1. Вступ
У сучасних посібниках ГРС визначають як раптову появу ≥2 типових клінічних симптомів тривалістю <12 тиж, один із яких має бути так званим великим: закладеність/обструкція носа або виділення з носа (ринорея чи постназальне затікання); а також другорядних симптомів: біль/тиск у ділянці обличчя, зменшення або втрата нюху, а в дітей – кашель (денний і нічний). Інші симптоми включають лихоманку, загальну слабкість і головний біль [2]. Гострий вірусний РС визначається як наявність симптомів тривалістю до 10 днів за відсутності їх посилення після 5 днів захворювання. Гострий поствірусний РС діагностується при посиленні симптомів після 5-го дня або за їх збереження після 10 днів захворювання [2]. У США при посиленні симптомів після 5-го дня або в разі їх збереження після 10 днів захворювання діагностується гострий невірусний РС [3]. Отже, як у європейських (EPOS), так і в американських погоджувальних документах терміни «гострий поствірусний РС» і «гострий невірусний РС» використовуються, щоб підкреслити, що в більшості випадків ГРС не є бактеріальним. Лише від 0,5 до 5% випадків захворювання можна охарактеризувати як гострий бактеріальний РС (ГБРС) [2, 3].
Дотепер не визначено жодного стандартного критерію для диференційної діагностики небактеріального (вірусного, поствірусного) РС і ГБРС. Традиційна рентгенографія неінформативна, томографічне дослідження не показане, за винятком випадків, коли патологічні симптоми персистують попри лікування або в разі підозри на ускладнення, а впровадження дослідження на реактивні білки, рекомендованого в EPOS 2012, не зменшило необґрунтованого призначення антибіотиків [2, 4, 5]. У зв’язку із цим ГРС є одним із найчастіших діагнозів, за яких застосовуються антибактеріальні засоби. Антибіотики призначаються в 4-9 разів частіше, ніж рекомендовано настановами, що є однією з основних причин глобальної антибіотикорезистентності [6, 8, 9]. Рушійною силою як невиправданого призначення антибіотиків лікарями, так і прагнення пацієнтів до антибіотикотерапії є бажання убезпечитися від потенційних ризиків, насамперед за наявності великих симптомів ГРС, як-от закладеність носа та слизово-гнійні виділення з носа [7].
Важлива стратегія скорочення непотрібних втручань – відкладене призначення антибактеріальних засобів. Пацієнти та лікарі можуть бути більш схильними погодити такий курс лікування порівняно з негайним призначенням або відсутністю призначення антибіотикотерапії в разі інфекцій дихальних шляхів [10].
У рамках цієї стратегії і з метою уникнення нераціонального застосування антибіотиків слід брати до уваги бажання позбутися слизово-гнійних виділень і закладеності носа, об’єктивні показання до антибактеріальної терапії та призначення лікування з доведеною ефективністю без додавання антибіотиків. При цьому такі широко використовувані препарати, як деконгестанти, антигістамінні засоби, гомеопатичні препарати та муколітики, не довели своєї ефективності в разі ГРС [1, 2].
З урахуванням цього постає необхідність застосування в системній і місцевій терапії препаратів із комплексною дією, які мають доказову базу ефективності при небактеріальних формах ГРС. Згідно з EPOS 2020, фармакотерапія небактеріальних форм ГРС (вірусного/поствірусного) з рівнем доказів 1b включає фітоекстракт 5 лікарських рослин BNO 1016 та лікувальні іригації ізотонічним розчином морської води [2, 11, 12]. Відповідно до рекомендацій більшості європейських й американських професійних асоціацій, морська вода, окремо або в поєднанні з іншими препаратами, відіграє важливу роль у лікуванні численних захворювань верхніх дихальних шляхів, насамперед гострих та хронічних РС, алергічного риніту в різних груп пацієнтів – від вагітних і дітей до дорослих [2, 13-15].
Механізм дії ізотонічних розчинів морської води базується на двох принципах – фізичному та фізіологічному. Перший принцип заснований на фізичному (механічному) ефекті очищення слизової оболонки носа від накопиченого секрету та хвороботворних мікроорганізмів. Другий принцип полягає у впливі іонів на слизову оболонку респіраторного тракту. Мікроелементи Ca, Mg активізують функцію миготливого епітелію, Na, Cl, Br забезпечують антисептичний ефект, Zn і Se стимулюють продукцію лізоциму, інтерферонів й імуноглобулінів, йод посилює вироблення захисного слизу келихоподібними клітинами [16-19].
Клінічні дані свідчать, що включення ізотонічної морської води до схеми терапії ГРС у дітей забезпечує поліпшення носового дихання, зменшення набряку слизової оболонки та кількості виділень із порожнини носа [20, 21]. Сукупність клінічних ефектів морської води в поєднанні з властивостями гіпертонічного розчину дозволяє при алергічному риніті додатково чинити осмолярну дію – вираженіше зменшувати набряк слизової оболонки [22, 23].
У світлі цих даних застосування гіпертонічних розчинів при ГРС могло б становити інтерес. У літературі зустрічаються нечисленні дані щодо ефективності гіпертонічних розчинів у лікуванні хронічного РС [24, 25]. Разом із тим валідних з погляду відповідності стандартам GCP багатоцентрових досліджень із вивчення застосування гіпертонічних розчинів морської води в лікуванні ГРС у дітей шкільного віку (6-11 років) раніше не проводилося. Підтвердження високої ефективності цього засобу в лікуванні ГРС у дітей, зіставної з його ефективністю в терапії інших респіраторних захворювань, дало б змогу оптимізувати схему лікування даної нозології та зменшити частоту необґрунтованого призначення антибіотиків.
Метою цього дослідження було оцінити ефективність використання гіпертонічного розчину морської води Аква Маріс® Екстра Стронг у рамках стратегії відкладеного призначення антибіотиків у дітей шкільного віку (6-11 років) порівняно зі стандартною симптоматичною терапією ГРС згідно з міжнародними та національними рекомендаціями [2, 26].
2. Матеріали та методи
2.1. Дизайн дослідження
Відкрите експлоративне порівняльне багатоцентрове рандомізоване проспективне, в паралельних групах, дослідження було проведене в 3 амбулаторних закладах України з вересня 2021 до лютого 2022 року. Дослідження виконувалося згідно зі стандартами GCP і принципами Гельсінської декларації. Дослідження було схвалене Комітетом з етики Івано-Франківського національного медичного університету в усіх дослідницьких центрах (протокол від 9.06.2021 № 122/21). Батьки кожної дитини надали письмову згоду на участь їхньої дитини в дослідженні.
2.2. Учасники
Для участі в дослідженні було відібрано 106 осіб, з них рандомізовано 100 амбулаторних пацієнтів віком 6-11 років, у яких було діагностовано ГРС. Оцінка діагностичних і диференційно-діагностичних критеріїв та призначення лікування відбувалися відповідно до рекомендацій європейських і національних клінічних настанов [2, 26]. Клінічний діагноз ГРС встановлювали на підставі наявності ≥1 великого симптому: закладеність/обструкція носа або виділення з носа (передня ринорея або постназальне затікання), та/або біль/тиск у ділянці обличчя, та/або кашель (денний і нічний) тривалістю <12 тиж.
→ Критерії включення:
- особи чоловічої та жіночої статі віком від 6 до 11 років, які перебувають на амбулаторному лікуванні з діагнозом ГРС;
- збереження симптомів упродовж 10 днів від початку захворювання або погіршення стану після 5-го дня лікування за відсутності діагностичних критеріїв ГБРС;
- загальна оцінка тяжкості симптоматики від 6 до 10 балів за шкалою Main Symptoms Severity (MSS): виділення з носа та їхній характер, закладеність носа, стікання виділень задньою стінкою глотки, лицевий біль, головний біль (0 – симптом відсутній; 1 – незначний прояв; 2 – помірний; 3 – сильний; 4 – дуже сильний);
- готовність і здатність пацієнта та/або батьків дотримуватися вимог протоколу дослідження;
- підписана інформована згода;
- відсутність критеріїв невключення.
→ Критерії невключення:
- застосування однієї з форм досліджуваних препаратів упродовж 30 днів до початку ГРС;
- діагноз алергічного РС;
- непереносимість препаратів;
- понад 14 днів від початку захворювання;
- тяжкий перебіг, що потребує госпіталізації або терапії антибактеріальними засобами (оцінка за MSS >10 балів);
- наявність імунодефіцитних станів, хронічної патології й анатомічних аномалій остіомеатального комплексу, котрі можуть впливати на наслідок захворювання.
→ Критерії виключення:
- рішення пацієнта та/або батьків припинити участь у дослідженні й відкликання письмової інформованої згоди;
- втрата контакту з пацієнтом;
- індивідуальна непереносимість досліджуваного медичного виробу та базисної схеми лікування;
- виникнення в пацієнта серйозних та/або непередбачуваних побічних явищ/реакцій у ході дослідження;
- виникнення ускладнень основного захворювання, котрі, на думку лікаря, вимагають виключення пацієнта з випробування;
- недотримання пацієнтом процедур, передбачених протоколом дослідження.
В основну групу рандомізовано 50 пацієнтів, які отримували ендоназальну іригаційну терапію Аква Маріс® Екстра Стронг з моменту встановлення діагнозу ГРС та симптоматичне лікування комплексним фітопрепаратом BNO 1012 (per os).
У контрольну групу рандомізовано 50 пацієнтів, які отримували ендоназальну іригаційну терапію ізотонічним сольовим розчином із моменту встановлення діагнозу ГРС і симптоматичне лікування комплексним фітопрепаратом BNO 1012 (per os).
До основної групи (n=50) увійшли 25 (50,0%) хлопчиків і 25 (50,0%) дівчаток (середній вік – 8,16±1,72 року); до контрольної (n=50) – 30 (60,0%) хлопчиків і 20 (40,0%) дівчаток (середній вік – 8,12±1,84 року). Пацієнти обох груп були зіставні за статтю, віком, клінічними проявами захворювання (р<0,05).
2.3. Втручання
Усі пацієнти від моменту рандомізації отримували терапію комплексним фітопрепаратом BNO 1012 (per os) і, за наявності показань, симптоматичні препарати (парацетамол). Пацієнтам контрольної групи додатково призначали терапевтичне зрошення порожнини носа ізотонічним сольовим розчином по 1-2 інстиляції в кожну ніздрю 3-4 р/добу. Пацієнтам основної групи додатково призначали терапевтичне зрошення порожнини носа назальним спреєм Аква Маріс® Екстра Стронг з однієї партії по 1-2 інстиляції в кожну ніздрю 3-4 р/добу. Аква Маріс® Екстра Стронг – назальний спрей гіпертонічного стерильного розчину морської води Адріатичного моря, що містить натуральні солі та мікроелементи, в балоні з дозуючим пристроєм. Виробник – Jadran – Galenski Laboratorij D. D. (Хорватія). Медичний виріб зареєстрований в Україні та доступний без рецепта. Склад, виготовлення, упаковка та маркування медичного виробу відповідають принципам Належної виробничої практики та чинним регуляторним вимогам України. Детальний опис всіх аспектів якості та безпеки спрея Аква Маріс® Екстра Стронг є частиною відповідних характеристик продукту. В Україні затвердженими показаннями до застосування Аква Маріс® Екстра Стронг є необхідність розрідження та поліпшення відтоку густого слизу при набряку та закладеності носа, зменшення місцевого запального процесу та зниження ризику ускладнень при гострих і хронічних захворюваннях порожнини носа (риніти, синусити).
До участі в дослідженні були залучені практичні спеціалісти оториноларингологи зі стажем роботи не менш ніж 5 років.
2.4. Критерії ефективності
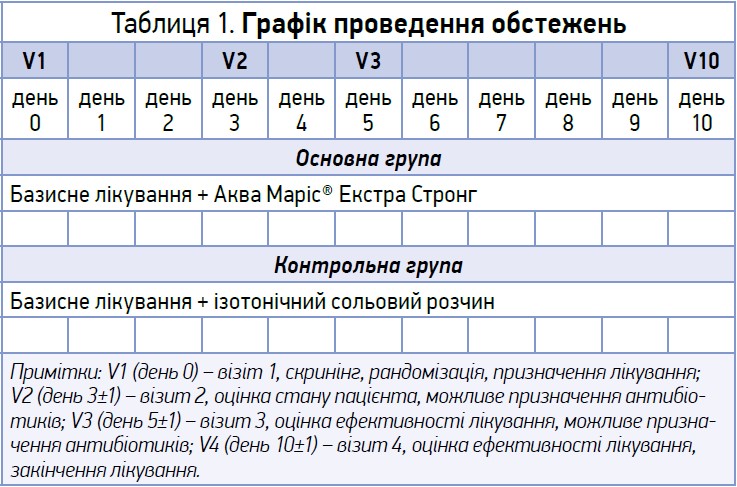
Усі дані оцінювалися напочатку дослідження і впродовж 10 днів (табл. 1).
Оцінку симптомів виконували лікарі та пацієнти. Лікарі в рамках кожного візиту оцінювали основні симптоми відповідно до шкали MSS (від 0 до 4 балів для кожного симптому): ринорея, закладеність носа, постназальне затікання, а також лицевий і головний біль. Крім того, пацієнти та їхні батьки щодня в щоденнику оцінювали скарги (ринорея, закладеність носа, стікання слизу задньою стінкою глотки, лицевий і головний біль) за 10-бальною візуальною аналоговою шкалою.
На візитах 2-3 лікар визначав стан пацієнта згідно з критеріями оцінки та самооцінки та спільно з пацієнтом та/або його батьками приймав рішення щодо необхідності призначення антибактеріальної терапії. Тривалість спостереження пацієнта становила 10±1 день.
Головним критерієм ефективності були зменшення вираженості симптомів захворювання за MSS на кожному візиті порівняно з візитом 1, динаміка самооцінки симптомів ГРС, динаміка прийому нестероїдних протизапальних препаратів (НПЗП), частота призначень антибіотиків.
2.5. Розмір вибірки
Клінічне дослідження було сплановано, щоб отримати достовірний опис ефективності активного застосування in vivo спрея Аква Маріс® Екстра Стронг порівняно зі стандартним лікуванням у рамках методики відкладеного призначення антибактеріальних препаратів. Залежно від даних проведено кілька пробних описових і статистичних оцінок; відтак, біометрична оцінка розміру вибірки не потрібна. Однак, щоб гарантувати достатній розмір вибірки для аналізу отриманих даних, обрано розмір вибірки n=100. Пацієнтів розподіляли в співвідношенні 1:1.
2.6. Рандомізація
Клінічна частина рандомізованого дослідження була відкритою, без процедури засліплення. Суб’єкти із симптомами ГРС випадковим чином були розподілені для отримання одного з двох можливих методів лікування відповідно до базового списку рандомізації. Рандомізація виконувалася з використанням програмного забезпечення (StatSoft – генератор випадкових чисел). Рандомізації підлягав кожний пацієнт, який підписав інформовану згоду.
2.7. Статистичні методи
Для аналізу однорідності груп використовували методи описової статистики для відображення вихідного стану основної та контрольної груп (для кількісних параметрів – n, середнє арифметичне, медіана, стандартне відхилення, мінімальне та максимальне значення; для якісних параметрів – частота і частка у відсотках). Перевірку розподілу даних у групах відповідності стандартам проводили за кількісними параметрами за допомогою критерію Шапіро-Вілка. Якщо дані в групах демонстрували нормальний розподіл за певними параметрами, групи порівнювали за цими параметрами за допомогою критерію Ст’юдента для незалежних вибірок. В іншому випадку (якщо розподіл даних відрізнявся від нормального) порівняння груп проводили за критерієм Манна-Вітні. Для категоріальних параметрів групи порівнювали за допомогою χ2-критерію Пірсона або точного критерію Фішера.
Для аналізу ефективності в кожній групі розраховували параметри описової статистики (n, середнє арифметичне, медіана, стандартне відхилення, мінімальне та максимальне значення) для всіх візитів відповідно до схеми обстеження пацієнтів.
Аналіз динаміки зазначених параметрів у кожній групі проводили методом двостороннього дисперсійного аналізу (ANOVA) за такою схемою: фактор «візит» є фіксованим (рівні: візит 1… візит n); фактор «суб’єкти» є випадковим.
Результати подальших візитів порівнювали з даними візиту 1 за допомогою контрастного аналізу з використанням простих контрастів.
Порівняння між групами в динаміці досліджуваних параметрів проводили за різницями dTi = (ТВізит n – ТВізит 1) оцінюваних параметрів за допомогою критерію Манна-Вітні.
Рівень довіри для критерію Шапіро-Вілка прийнято рівним 0,01, а для решти критеріїв – 0,05.
Аналіз значимості впливу терапії спреєм Аква Маріс® Екстра Стронг на зниження частоти прийому антибіотиків виконувався методом прогнозування на основі регресійного аналізу за допомогою нейронної мережі: оцінювалася ймовірність того, що аналізована (залежна) перемінна набуде значення за заданих значеннях факторів (моделюється лінійна комбінація факторів). У цьому випадку регресія розглядалася як окремий випадок нейромережі.
Аналіз було виконано за допомогою програмного забезпечення IBM SPSS 22.0.
3. Результати
3.1. Досліджувана вибірка
Скринінг для участі в дослідженні пройшли 106 осіб. У дослідження було рандомізовано 100 амбулаторних пацієнтів віком 6-11 років (рис. 1).
Рис. 1. Пацієнти, котрі пройшли скринінг і рандомізацію
Зі 106 відібраних пацієнтів 6 (5,6%) не включено до дослідження з причин невідповідності критеріям включення: вік поза зазначеним критерієм (n=2); небажання пацієнта та/або його батьків дотримуватися вимог протоколу (n=4). З-поміж 100 включених у дослідження пацієнтів 50 були рандомізовані в основну групу, решта 50 – у контрольну. Всі рандомізовані пацієнти (n=100; 100%) пройшли необхідні процедури відповідно до протоколу дослідження, їхні дані було включено до аналізу.
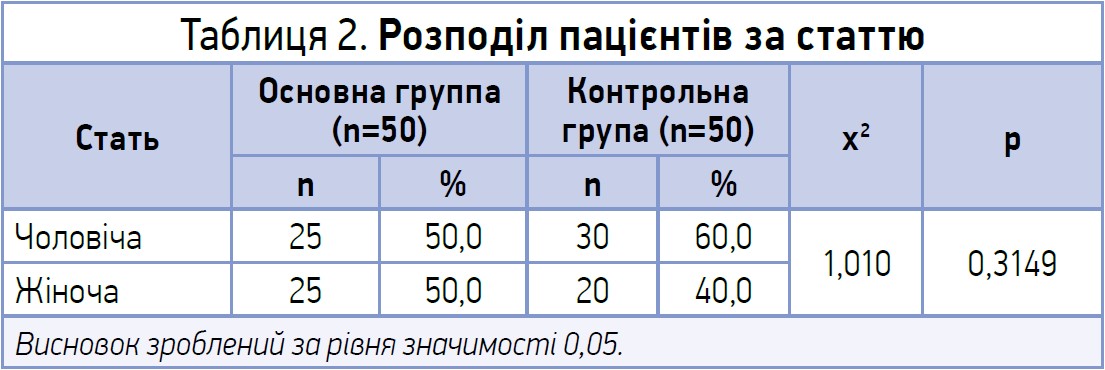
У таблиці 2 представлено розподіл пацієнтів обох груп за статтю: в основній групі з-поміж 50 пацієнтів 25 (25%) були хлопчики та 25 (25%) – дівчатка; у контрольній з-поміж 50 пацієнтів 30 (60%) були хлопчики, 20 (40%) – дівчатка.
Загалом за статевою ознакою сформовані групи були статистично однорідними.
Загалом суттєвих відмінностей за демографічними характеристиками між пацієнтами основної та контрольної груп на вихідному рівні (день 1) не відзначалося.
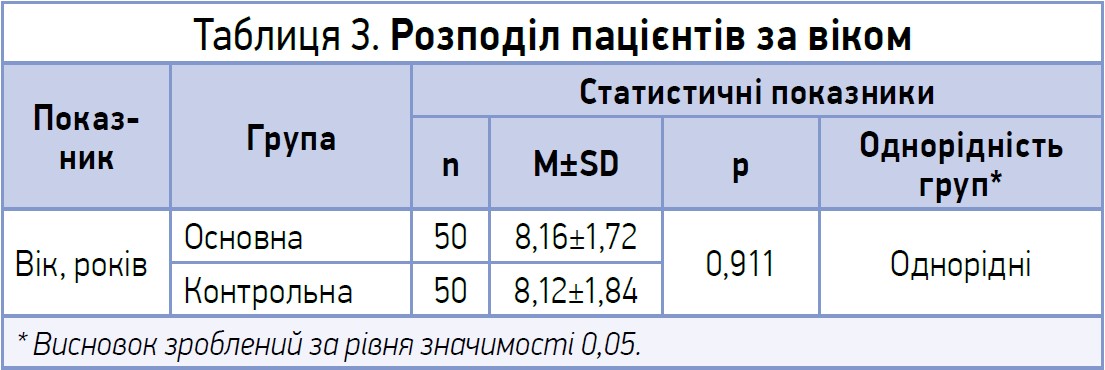
У таблиці 3 подано розподіл пацієнтів обох груп за віком: середній вік пацієнтів основної групи становив 8,16±1,72 року, контрольної – 8,12±1,84 року. За віковим критерієм сформовані групи були статистично однорідними.
Загалом суттєвих відмінностей за демографічними характеристиками між пацієнтами основної та контрольної груп на вихідному рівні (день 1) не відзначалося.
3.2. Клінічні результати та оцінка
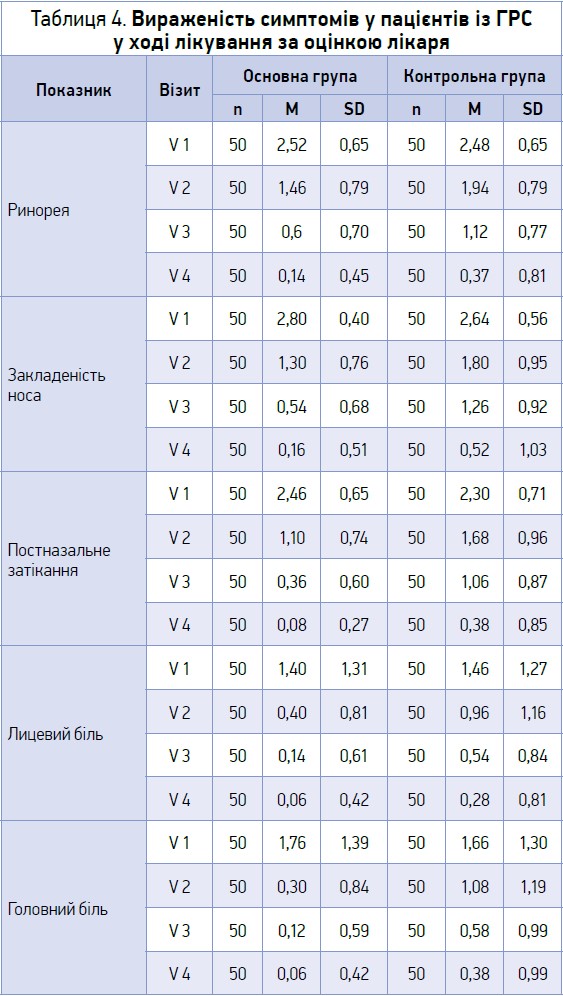
Типовими клінічними симптомами ГРС є виділення з носа (ринорея або постназальне затікання), закладеність/обструкція носа, лицевий біль і головний біль. У таблиці 4 представлена динаміка вираженості основних симптомів, які оцінювалися лікарем за 4-бальною шкалою, у пацієнтів основної та контрольної груп.
При оцінці лікарем такого симптому, як виділення з носа (ринорея), обидві групи продемонстрували зіставні показники на візиті 1: 2,52 бала в основній групі та 2,48 – у контрольній. У ході лікування на візиті 2 відзначалося зменшення вираженості ринореї в пацієнтів обох груп: з 2,52 до 1,46 бала в основній групі та з 2,48 до 1,94 бала – в контрольній. На візиті 3 спостерігалося подальше зменшення ринореї в пацієнтів обох груп: до 0,6 бала в основній та до 1,12 – в контрольній. На візиті 4 вираженість ринореї становила 0,14 бала в пацієнтів основної групи та 0,81 бала – в учасників контрольної. При цьому в основній групі відзначалася тенденція до вираженішої регресії симптому.
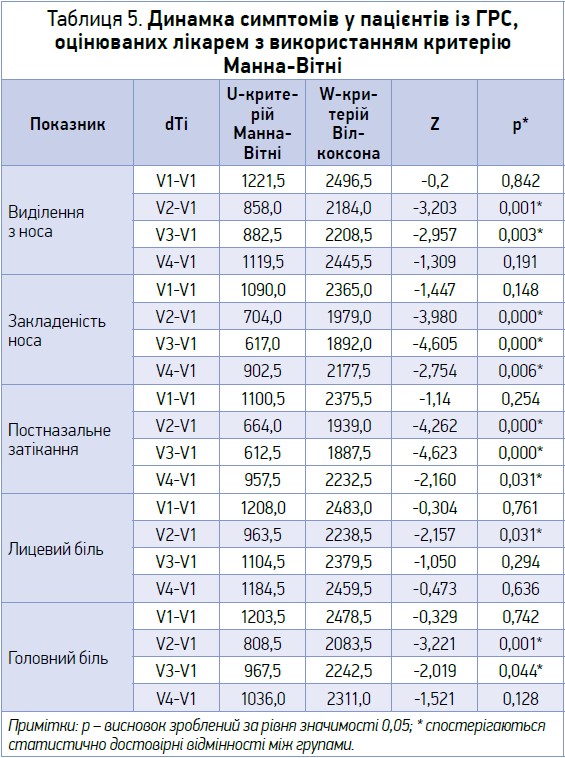
У таблиці 5 представлено порівняльну оцінку вираженості оцінюваних лікарем основних симптомів у пацієнтів із ГРС в основній і контрольній групах у ході лікування (з використанням критерію Манна-Вітні). Порівняння вираженості ринореї на візиті 1 показує відсутність достовірних відмінностей між групами. Оцінка регресії симптому показує достовірні порівняно з візитом 1 відмінності між групами на візитах 2 і 3 (р<0,05) та недостовірну різницю на візиті 4 (р>0,05).
При оцінці лікарем симптому закладеності носа на візиті 1 обидві групи продемонстрували зіставні за вираженістю показники: 2,80 бала в основній групі та 2,64 – у контрольній (різниця не достовірна) (табл. 4, 5). У ході лікування на візиті 2 відзначалося зменшення вираженості симптому закладеності носа в пацієнтів обох груп: з 2,80 до 1,30 бала в основній та з 2,64 до 1,80 – в контрольній. На візиті 3 спостерігалося подальше зменшення закладеності носа в пацієнтів обох груп: до 0,54 бала в основній та до 1,26 – в контрольній. На візиті 4 закладеність носа оцінювалася в 0,16 бала в пацієнтів основної групи та 0,52 бала в учасників контрольної (табл. 4). При порівняльній оцінці регресії цього симптому між групами за допомогою критерію Манна-Вітні відзначається достовірна різниця на візиті 2 (р<0,05), натомість на візитах 3 і 4 достовірних відмінностей не зафіксовано (p>0,05) (табл. 5).
При оцінці лікарем вираженості постназального затікання на візиті 1 обидві групи продемонстрували зіставні показники: 2,46 бала в основній групі та 2,30 – в контрольній (різниця не значима) (табл. 4, 5). У ході лікування на візиті 2 відзначалося зменшення вираженості постназального затікання в пацієнтів обох груп: з 2,46 до 1,10 бала в основній і з 2,30 до 1,68 – в контрольній. На візиті 3 спостерігалася подальша регресія постназального затікання в пацієнтів обох груп: до 0,36 бала в основній і до 1,06 – в контрольній. На візиті 4 вираженість постназального затікання становила 0,08 бала в пацієнтів основної групи та 0,38 бала в учасників контрольної групи. Мала місце тенденція до вираженішого зменшення симптому в основній групі (табл. 4). Порівняльна оцінка регресії постназального затікання між групами за допомогою критерію Манна-Вітні показала достовірну різницю на візиті 2 (р<0,05), натомість на візитах 3 і 4 достовірних відмінностей не зафіксовано (p>0,05) (табл. 5).
При оцінці лікарем вираженості лицевого болю на візиті 1 обидві групи продемонстрували зіставні показники: 1,40 бала в основній групі та 1,46 – в контрольній, різниця не достовірна (табл. 4, 5). У ході лікування на візиті 2 в пацієнтів обох груп відзначалося зменшення вираженості лицевого болю: з 1,40 до 0,40 бала в основній та з 1,46 до 0,96 – в контрольній. На візиті 3 спостерігалася подальша регресія вираженості цього симптому в пацієнтів обох груп: до 0,14 бала в основній та до 0,54 – в контрольній. На візиті 4 вираженість лицевого болю становила 0,06 бала в пацієнтів основної групи та 0,28 бала в учасників контрольної групи (табл. 4). Порівняльна оцінка зменшення лицевого болю між групами за допомогою критерію Манна-Вітні показала достовірну різницю на візиті 2 (р<0,05), натомість на візитах 3 і 4 достовірних відмінностей не зафіксовано (p>0,05) (табл. 5).
При оцінці лікарем вираженості головного болю на візиті 1 обидві групи продемонстрували зіставні показники: 1,76 бала в основній групі та 1,66 – в контрольній, різниця не достовірна (табл. 4, 5). У ході лікування на візиті 2 відзначалося зменшення вираженості головного болю в пацієнтів обох груп: з 1,76 до 0,30 бала в основній та з 1,66 до 1,08 – в контрольній. На візиті 3 спостерігалося подальше зменшення головного болю в пацієнтів обох груп: до 0,12 бала в основній та до 0,58 – в контрольній. На візиті 4 вираженість головного болю становила 0,06 бала в пацієнтів основної групи та 0,38 бала в учасників контрольної групи (табл. 4). Порівняльна оцінка зменшення вираженості головного болю між групами за допомогою критерію Манна-Вітні показала достовірні відмінності на візитах 2 і 3 (р<0,05), натомість на візиті 4 достовірної різниці не зафіксовано (p>0,05) (табл. 5).
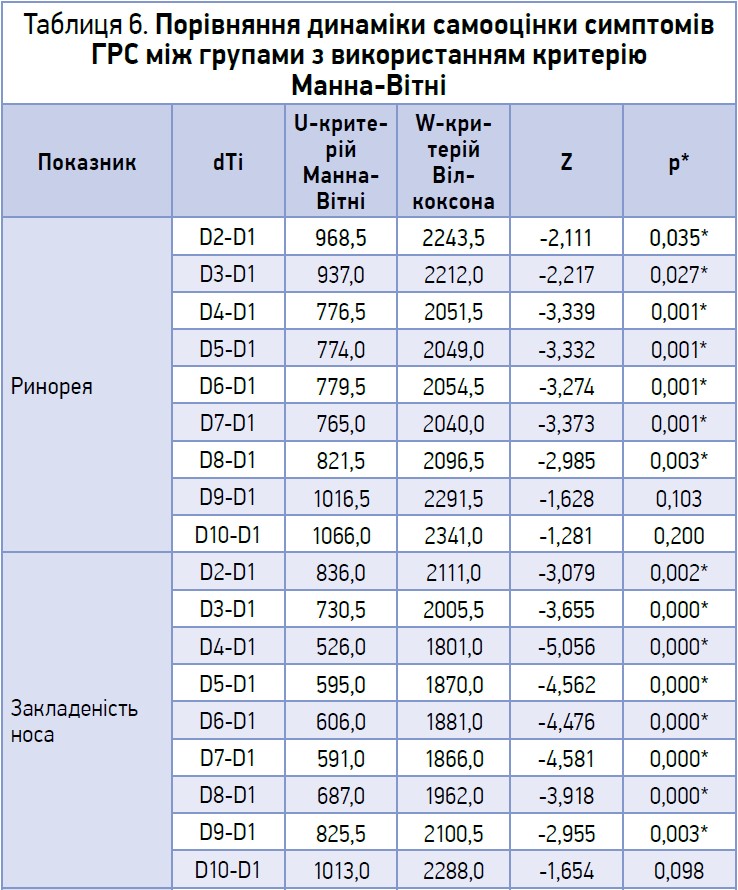
Пацієнти 6-11 років самостійно або за допомогою батьків щодня оцінювали основні скарги за 10-бальною візуальною аналоговою шкалою. Оскільки групи були однорідними за вираженістю основних симптомів на початку дослідження, було обчислено індивідуальні відмінності dTi = Тдень 2 – Тдень 1, … Тдень 10 – Тдень 1 для кожного учасника та симптому. Подальше порівняння між групами проводилося за динамікою самооцінки основних симптомів ГРС (відмінності в dTi) з використанням критерію Манна-Вітні (табл. 6).
Згідно із самооцінкою, починаючи з 2-го для лікування і до 8-го відзначалася суттєва різниця у зменшенні вираженості ринореї в пацієнтів основної групи порівняно з контрольною. На 9-10-й день різниця у вираженості ринореї була недостовірною (табл. 6).
Простежено динаміку самооцінки закладеності носа. В пацієнтів основної групи спостерігалося вираженіше (достовірне) зменшення цього симптому з 2-го до 9-го дня. На 10-й день різниця у вираженості ринореї була недостовірною.
Порівняння між групами показників регресії постназального затікання (згідно із самооцінкою пацієнта) з використанням критерію Манна-Вітні показує достовірні відмінності починаючи з 2-го і до 8-го дня. На 9-10-й день різниця у вираженості цього симптому була недостовірною.
Самооцінка пацієнтами лицевого болю відображає значну різницю у вираженості симптому тільки на 2-й день. Від 3-го дня лікування і до 10-го різниця у вираженості лицевого болю була недостовірною. Самооцінка вираженості головного болю показує значну різницю між основною та контрольною групою з 2-го до 6-го дня. Починаючи із 7-го дня і до 10-го різниця між групами не є достовірною.
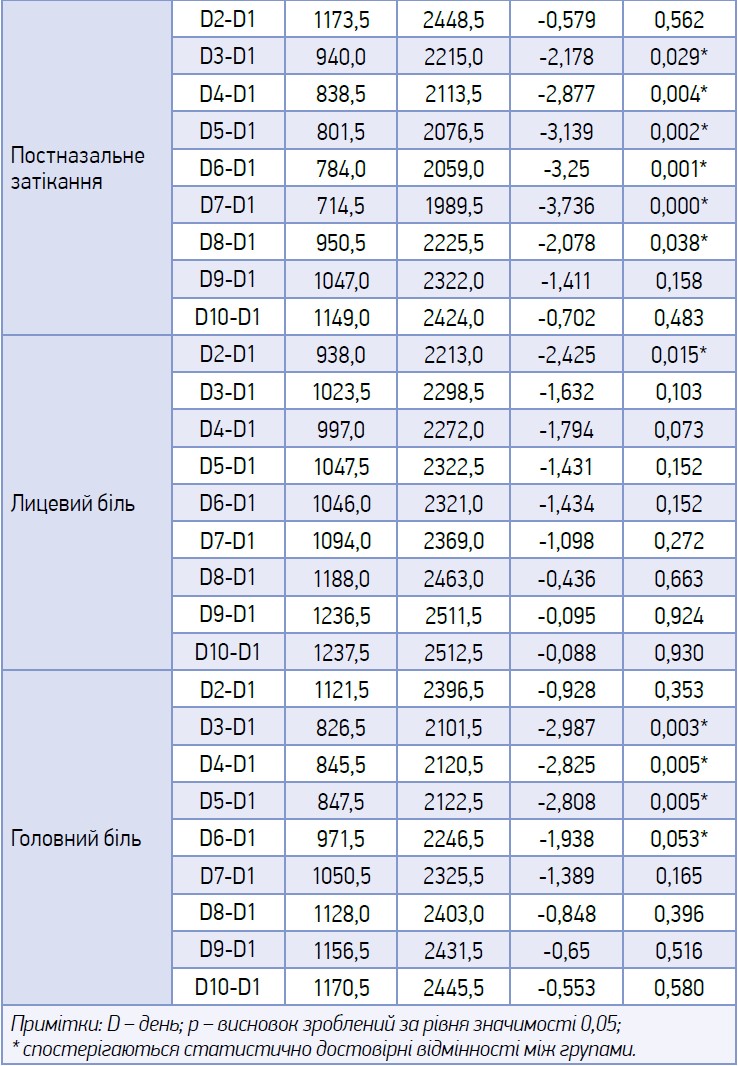
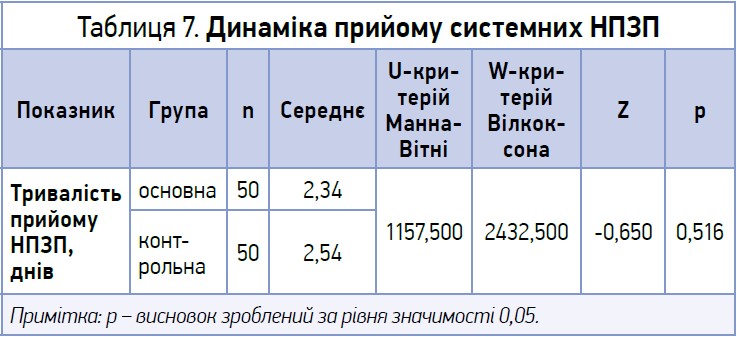
Відомо, що наявність такого симптому, як гіпертермія, є важливим критерієм оцінки тяжкості перебігу захворювання й одним з основних показань для прийому НПЗП. Нами проаналізовано динаміку тривалості прийому НПЗП. Враховувався день останнього прийому препарату (табл. 7).
Як видно з представлених даних, динаміка прийому НПЗП в обох групах була зіставною.
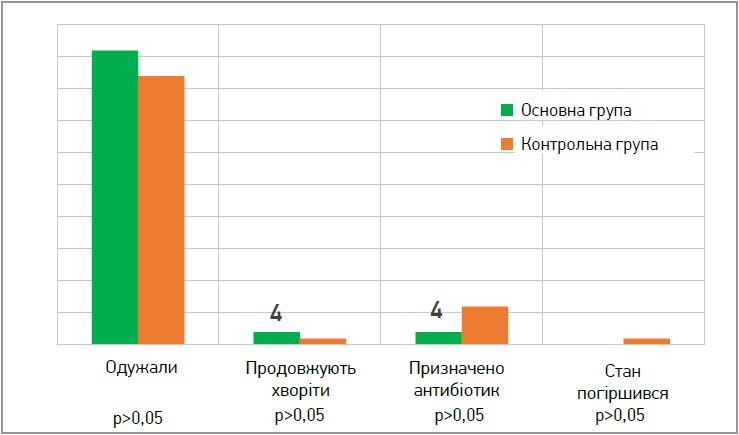
На візиті 4 було проведено порівняння наслідків лікування ГРС між групами (рис. 2). З-поміж 50 пацієнтів основної групи одужали 46 (92,0%), натомість з-поміж 50 учасніків контрольної – 42 (84,0%).
Рис. 2. Результати лікування на візиті 4
Різниця між групами була недостовірною – р=0,357 (>0,05). Продовжували хворіти 2 (4,0%) пацієнти основної групи та 1 (2,0%) учасник контрольної, мало місце погіршення стану в одного пацієнта контрольної групи. Різниця між групами в обох випадках була недостовірною – р=1,000 (>0,05).
Згідно з дизайном дослідження, на контрольних візитах проводилася комплексна оцінка стану пацієнта та приймалося рішення про необхідність призначення антибактеріальної терапії (рис. 2). Антибіотики було призначено 2 (4,0%) пацієнтам основної групи та 6 (12,0%) – контрольної. Різниця між групами була недостовірною – р=0,269 (>0,05).
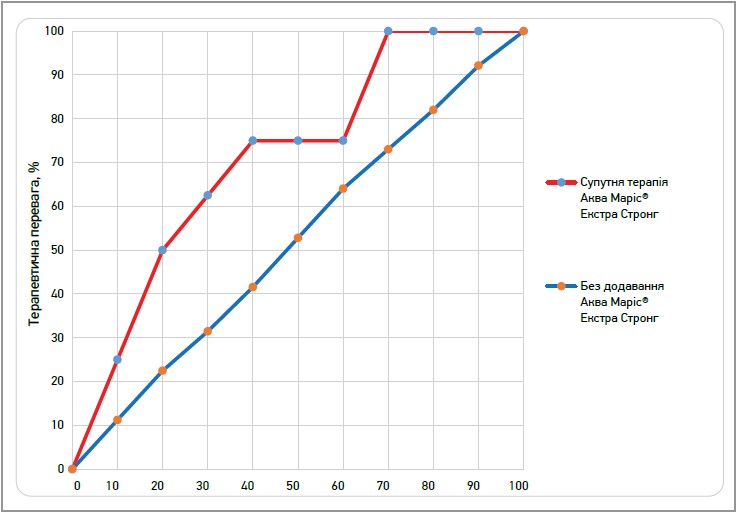
За відсутності достовірної різниці між групами щодо призначення антибактеріальної терапії нами проведено аналіз тенденції застосування антибіотиків залежно від використання в схемі лікування спрея Аква Маріс® Екстра Стронг. Аналіз виконано за допомогою нейромережевого моделювання (рис. 3).
Рис 3. Аналіз впливу призначення Аква Маріс® Екстра Стронг на зниження частоти прийому антибіотиків
Як видно з рисунка 3, застосування Аква Маріс® Екстра Стронг значно знизило частоту призначення антибіотиків в основній групі порівняно з контрольною.
3.3. Безпека та переносимість
Аналіз показав, що в усіх випадках лікування переносилося добре або дуже добре. Жодних побічних ефектів у ході лікування не було зареєстровано.
4. Обговорення
З-поміж усіх випадків ГРС частка ГБРС становить від 0,5 до 5% [2, 3]. Саме такій кількості хворих показано антибактеріальну терапію. Однак у разі ГРС антибіотики призначаються в 4-9 разів частіше, ніж рекомендується [6]. З погляду застосування стратегії відкладеного призначення антибіотиків стартове лікування має бути дуже ефективним, особливо щодо великих симптомів ГРС – закладеності носа та слизово-гнійних виділень із носа [7]. За недостатньої ефективності стартової терапії при повторному огляді як лікарі завжди розглядають необхідність призначення антибіотиків, так і пацієнти або їхні батьки висловлюються на користь призначення антибактеріальної терапії [6].
Згідно з дизайном, до нашого дослідження включалися пацієнти з діагностичними критеріями гострого небактеріального РС, а вираженість симптомів між групами в перший день була зіставною (р>0,05). У дослідженні було показано, що застосування гіпертонічного розчину морської води на додачу до стандартної терапії ГРС має доведений терапевтичний ефект із перших днів лікування.
Відповідно до оцінки лікарем великих симптомів ГРС, показник вираженості ринореї показує достовірне порівняно з візитом 1 зменшення на візитах 2 і 3 (р<0,05) і недостовірну різницю між групами на візиті 4 (р>0,05). При порівняльній оцінці зменшення закладеності носа та постназального затікання між групами відзначалися достовірні відмінності на візитах 2-4 (р<0,05).
Спостерігалися також достовірні відмінності щодо самооцінки пацієнтом інтенсивності ринореї та закладеності носа вже на 2-й день і постназального затікання на 3-й день лікування (p<0,05). Достовірні відмінності зберігалися до 9-10-го дня, тобто до закінчення лікування, коли різниця в показниках оцінки інтенсивності симптомів була недостовірною (p>0,005).
Отже, при застосуванні іригаційної терапії гіпертонічним розчином морської води в пацієнтів основної групи порівняно з учасниками контрольної групи відзначалася достовірна терапевтична перевага щодо зменшення вираженості великих симптомів ГРС, як-от ринорея, закладеність носа та постназальне затікання, вже в перші дні лікування, коли ухвалюється рішення про відкладене призначення антибактеріальних препаратів.
Наші результати узгоджуються з даними, які показують доведений клінічний ефект застосування ізотонічного розчину для лікування гострих респіраторних інфекцій [13-15]. Однак у контексті нашого дослідження більшу цінність мають нечисленні дані щодо того, що іригаційна терапія ізотонічним розчином у дітей із ГРС забезпечує поліпшення носового дихання та зменшення кількості виділень із носа. Показники опитувальника самооцінки якості життя підтверджувалися даними обстежень, які фіксували зменшення набряку слизової оболонки та показників пікової назальної швидкості видиху [20, 21]. Цей клінічний ефект узгоджується з раніше отриманими даними про покращення реологічних властивостей назального слизу та стимуляцію мукоциліарного кліренсу під впливом ізотонічного розчину морської води [16-18]. У нашому дослідженні ці ефекти потенціюються додатковим застосуванням фітоекстракту BNO 1016, котрий має схожі властивості [7].
Один із важливих симптомів ГРС – біль, як головний, так і лицевий. При ГРС больовий синдром пов’язаний переважно з токсичною дією вірусів, набряком слизової оболонки приносових пазух і блокадою співусть. У нашому дослідженні обидві групи продемонстрували зіставні за вираженістю показники лицевого та головного болю як за оцінкою цих симптомів лікарем на візиті 1, так і за самооцінкою симптомів пацієнтами в 1-й день (р>0,05). При порівняльній оцінці лікарем зменшення вираженості лицевого болю відзначалися достовірна різниця на візиті 2 (р<0,05) і відсутність достовірних відмінностей на візитах 3 і 4 (р>0,05); щодо зменшення вираженості головного болю мали місце достовірні відмінності на візитах 2 і 3 (р<0,05) та відсутність таких на візиті 4 (р>0,05).
Самооцінка пацієнтами лицевого болю показує достовірну різницю у вираженості симптому на 2-й день (р<0,05). Від 3-го дня лікування і до 10-го різниця у вираженості симптомів була недостовірною (р>0,05). Самооцінка вираженості головного болю відображає достовірну різницю між основною та контрольною групою з 2-го до 6-го дня. Починаючи із 7-го дня і до 10-го різниця між групами не є достовірною.
Менш виражену динаміку зменшення лицевого та головного болю порівняно з іншими симптомами ГРС можна пояснити мінімальним впливом ендоназального зрошення на стан слизової оболонки приносових пазух за цього захворювання. Проведені дослідження не показали статистично достовірного покращення показника рентгенографії навколоносових пазух [20].
Отже, важливий і цікавий висновок проведеного дослідження полягає в тому, що застосування гіпертонічного розчину морської води Аква Маріс® Екстра Стронг у пацієнтів із ГРС забезпечує достовірне зменшення вираженості таких симптомів, як ринорея, постназальне затікання, закладеність носа, лицевий і головний біль, до першого контрольного візиту (візит 2) пацієнта (p<0,005).
Як відомо, наявність больового синдрому в поєднанні з гіпертермією збільшує ймовірність необґрунтованого призначення антибактеріальних препаратів. У подібних випадках рекомендується призначення НПЗП. У дослідженні показано, що в пацієнтів основної та контрольної груп відсутня достовірна різниця в тривалості прийому НПЗП. Це дозволяє зробити висновок, що отримані результати в динаміці симптомів ГРС можна пояснити клінічними ефектами застосування назального спрея Аква Маріс® Екстра Стронг.
Згідно з дизайном, до нашого дослідження не включалися пацієнти з діагностичними критеріями ГБРС, які потребують негайного призначення антибактеріальної терапії. Рішення про призначення антибіотиків приймалося після оцінки динаміки симптомів на візитах 2-3. У таких випадках антибактеріальна терапія вважалася обґрунтованою, оскільки лікування, призначене на візиті 1, не демонструвало достатньої ефективності. Антибактеріальну терапію було призначена 2 (4,0%) із 50 пацієнтів основної групи та 6 (12,0%) із 50 учасників контрольної групи. Така низька частота призначення відповідає чинним рекомендаціям щодо антибактеріальної терапії ГРС [2, 26]. Відзначалася тенденція до зменшення кількості призначень в основній групі, однак різниця між групами не є достовірною (р>0,05). Невеликий обсяг вибірки пацієнтів не дозволив зробити статистично достовірні висновки за допомогою стандартних статистичних методик. Тому було проведено аналіз тенденції призначення антибіотиків за допомогою нейромережевого моделювання. Показано, що застосування назального спрея Аква Маріс® Екстра Стронг значно знизило частоту призначення антибіотиків в основній групі порівняно з контрольною.
Відтак, важливий висновок проведеного дослідження полягає в тому, що застосування гіпертонічного розчину морської води в пацієнтів із ГРС знижує необхідність проведення антибактеріальної терапії в рамках стратегії відкладеного призначення антибіотиків. Водночас, згідно з даними літератури, необґрунтована антибактеріальна терапія призначається набагато частіше, ніж необхідно [6]. Доведена висока ефективність лікування ГРС з погляду помітного зменшення вираженості симптомів у перші дні дозволить ширше реалізовувати стратегію відкладеного призначення антибіотиків і в багато разів знизити кількість необґрунтованих призначень антибактеріальних препаратів при першому зверненні пацієнта.
Дизайн передбачав порівняльне дослідження, що не дозволило здійснити плацебо-контроль. Однак порівняння проводилося між групами, які отримували лікування відповідно до клінічних рекомендацій, тому терапевтичний ефект можна вважати аналогічним [2, 26]. У зв’язку із цим всі відмінності в результатах лікування можна віднести за рахунок клінічних ефектів гіпертонічного розчину морської води Аква Маріс® Екстра Стронг, оскільки за характеристиками групи були зіставні.
5. Висновки
Було показано, що додавання призначення гіпертонічного розчину морської води до стандартної симптоматичної терапії BNO 1012 забезпечує суттєвий клінічний ефект у перші дні лікування ГРС. Порівняно з контролем достовірно зменшуються клінічні симптоми захворювання. Терапевтичний ефект у перші дні лікування зменшує необхідність призначення антибактеріальних препаратів. Включення медичного виробу до схеми лікування може бути рекомендовано пацієнтам із ГРС у рамках стратегії відкладеного призначення антибіотиків.
У подальших дослідженнях доцільно вивчити ефективність медичного виробу в пацієнтів із бактеріальним РС.
Список літератури знаходиться в редакції.
Popovych V. I., Koshel I. V., Piletska L. I. et al. Multicenter, randomized, open-label, comparative study of the effectiveness of nasal spray Aqua Maris Extra Strong as a symptomatic therapy in the technology of delayed antibiotic prescription in the treatment of acute rhinosinusitis in children aged 6-11 years. American Journal of Otolaryngology–Head and Neck Medicine and Surgery. Available online 25 September 2022.
Медична газета «Здоров’я України 21 сторіччя» № 12 (529), 2022 р.