5 лютого, 2023
Уніфікований клінічний протокол первинної, вторинної (спеціалізованої), третинної (високоспеціалізованої) медичної допомоги «Менопаузальні порушення та інші розлади в перименопаузальному періоді»*
ЗАТВЕРДЖЕНО
Наказ Міністерства охорони здоров’я України 17 червня 2022 року № 1039
Вступ
Мультидисциплінарну робочу групу для розробки медико-технологічних документів за темою «Менопаузальні порушення та інші розлади в перименопаузальному періоді» створено наказом Міністерства охорони здоров’я України від 18.08.2020 р. № 1908 (у редакції наказу Міністерства охорони здоров’я України від 16.02.2021 р. № 265).
Уніфікований клінічний протокол первинної, вторинної (спеціалізованої), третинної (високоспеціалізованої) медичної допомоги (УКПМД) «Менопаузальні порушення та інші розлади в перименопаузальному періоді» розроблений на основі клінічної настанови «Менопаузальні порушення та інші розлади в перименопаузальному періоді», яка ґрунтується на принципах доказової медицини з урахуванням сучасних міжнародних рекомендацій, відображених у клінічній настанові Recommendations on women’s midlife health and menopause hormone therapy Міжнародного товариства з менопаузи (The International Menopause Society, IMS) 2016 р., що більшою мірою відповідає специфіці надання медичної допомоги в нашій країні. Крім того, робочою групою для синтезу клінічної настанови використані інші документи, зокрема:
1. Menopause: diagnosis and management (NG23). National Institute for Health and Care Excellence (NICE) guideline, 2019;
2. Clinical guidance Managing menopausal symptoms. The Royal Australian and New Zealand College of Obstetricians and Gynaecologists (RANZCOG), 2020;
3. The genitourinary syndrome of menopause. The North American Menopause Society (NAMS), 2020;
4. The British Menopause Society & Women’s Health Concern recommendations on hormone replacement therapy in menopausal women, British Menopause Society (BMS) Women’s Health Concern, 2020.
Ознайомитися з клінічною настановою «Менопаузальні порушення та інші розлади в перименопаузальному періоді» можна за посиланням https://www.dec.gov.ua/cat_mtd/galuzevi-standarti-taklinichni-nastanovi.
В УКПМД запропоновані методи та алгоритми діагностики й лікування асоційованих із менопаузою розладів в Україні; основна мета — створення єдиної комплексної та ефективної системи надання медичної допомоги пацієнткам із симптомами менопаузи.
У закладі охорони здоров’я має бути наявний внутрішній документ (клінічний маршрут пацієнта), що уніфікує медичну допомогу пацієнткам із менопаузальними порушеннями на локальному рівні.
Перелік скорочень, що використовуються у протоколі
АМГ – антимюллерів гормон
АТ – артеріальний тиск
БЕ – біопсія ендометрія
ВМС-ЛНГ – внутрішньоматкова система, що вивільняє левоноргестрел
ВС – вазомоторні симптоми
ВТЕ – венозна тромбоемболія
ГУМС– генітоуринарний менопаузальний синдром
ЗОЗ – заклад охорони здоров’я
ІМ – інфаркт міокарда
ІМТ – індекс маси тіла
ІХС – ішемічна хвороба серця
КМП – клінічний маршрут пацієнта
КОК – комбіновані оральні контрацептиви
МГТ – менопаузальна гормональна терапія
РЕ – рак ендометрія
ССЗ – серцево-судинні захворювання
УЗД – ультразвукове дослідження
ФСГ – фолікулостимулюючий гормон
ХХН – хронічна хвороба нирок
ХС – холестерин
ЦД – цукровий діабет
ШКФ – швидкість клубочкової фільтрації
DEXA – метод подвійної енергетичної рентгенівської абсорбціометрії (Dual-Energy X-ray Absorptiometry)
Е2 – естрадіол
MRS – шкала оцінки менопаузи (The Menopause Rating Scale)
SERM – селективні модулятори рецепторів естрогенів
SCORE – системна оцінка коронарного ризику (Systematic Coronary Risk Estimation)
STRAW – Робоча група з вивчення стадій репродуктивного старіння жінок (Stages of Reproductive Aging Workshop)
І. Паспортна частина
1.1. Діагноз:
1.2. Коди захворювання відповідно до Національного класифікатора України НК 025:2021 «Класифікатор хвороб та споріднених проблем охорони здоров’я»:
N95 Менопаузальні та інші перименопаузальні розлади.
1.3. Для кого призначений протокол
Протокол призначений для лікарів загальної практики – сімейних лікарів, лікарів акушерів-гінекологів, гінекологів-онкологів, онкологів, хірургів-онкологів, кардіологів, ендокринологів, ортопедів-травматологів, інших медичних працівників, які надають медичну допомогу жінкам із менопаузальними порушеннями.
1.4. Мета протоколу
Мета протоколу: забезпечити організацію надання медичної допомоги, встановити єдині вимоги щодо діагностики та лікування пацієнток із симптомами менопаузи, рекомендувати використання критеріїв STRAW+10 2011 року щодо періодів клімактерію усім спеціалістам охорони здоров’я.
1.5. Дата складання протоколу: 2022 рік.
1.6. Дата перегляду протоколу: 2026 рік.
1.7. Список осіб, які брали участь у розробці протоколу
Татарчук Тетяна Феофанівна – заступник директора з наукової роботи, завідувач відділення ендокринної гінекології ДУ «Інститут педіатрії, акушерства і гінекології ім. академіка О.М. Лук’янової НАМН України», експерт Міністерства охорони здоров’я України, чл.‑ кор. НАМН України, д. мед. н., професор, заступник голови робочої групи з клінічних питань
Анікусько Микола Федорович – завідувач хірургічного відділення комунального некомерційного підприємства «Київський міський онкологічний центр», к. мед. н.
Булавенко Ольга Василівна – завідувач кафедри акушерства і гінекології № 2 Вінницького національного медичного університету ім. М.І. Пирогова, д. мед. н., професор
Горбань Наталія Євгеніївна – завідувач відділення медичних та психосоціальних проблем здоров’я сім’ї ДУ «Інститут педіатрії, акушерства і гінекології ім. академіка О.М. Лук’янової НАМН України», к. мед. н.
Долженко Марина Миколаївна – завідувач кафедри кардіології Національного університету охорони здоров’я України ім. П.Л. Шупика, д. мед. н., професор
Дубоссарська Юліанна Олександрівна – завідувач кафедри акушерства, гінекології та перинатології факультету післядипломної освіти Дніпровського державного медичного університету, д. мед. н., професор
Жилка Надія Яківна – професор кафедри акушерства, гінекології та перинатології Національного університету охорони здоров’я України ім. П.Л. Шупика, д. мед. н.
Занько Олена Василівна – старший науковий співробітник відділу репродуктивного здоров’я ДНУ «Центр інноваційних медичних технологій НАН України», к. мед. н.
Ісаєва Ганна Сергіївна – завідувач відділу комплексного зниження ризику хронічних неінфекційних захворювань ДУ «Національний інститут терапії ім. Л.Т. Малої НАМН України» (м. Харків), д. мед. н.
Калугіна Людмила Вадимівна – провідний науковий співробітник відділення ендокринної гінекології ДУ «Інститут педіатрії, акушерства і гінекології ім. академіка О.М. Лук’янової НАМН України», д. мед. н.
Камінський В’ячеслав Володимирович – завідувач кафедри акушерства, гінекології та репродуктології Національного університету охорони здоров’я України ім. П.Л. Шупика, академік НАМН України, д. мед. н., професор
Косей Наталія Василівна – завідувач відділу репродуктивного здоров’я ДНУ «Центр інноваційних медичних технологій НАН України», д. мед. н., професор
Малишевська Юлія Євгеніївна – заступник директора Департаменту оцінки медичних технологій, адміністрування державних реєстрів та моніторингу цін ДП «Державний експертний центр Міністерства охорони здоров’я України»
Медведь Володимир Ісаакович – завідувач відділення внутрішньої патології вагітних ДУ «Інститут педіатрії, акушерства і гінекології ім. академіка О.М. Лук’янової НАМН України», чл.‑ кор. НАМН України, д. мед. н., професор
Мітченко Олена Іванівна – завідувач відділу дисліпідемій ДУ «Національний науковий центр “Інститут кардіології ім. академіка М.Д. Стражеска НАМН України”», д. мед. н., професор
Педаченко Наталія Юріївна – завідувач кафедри акушерства, гінекології та перинатології Національного університету охорони здоров’я України ім. П.Л. Шупика, д. мед. н., професор
Регеда Світлана Іванівна – завідувач гінекологічного відділення ДНУ «Центр інноваційних медичних технологій НАН України», к. мед. н., старший науковий співробітник
Єфіменко Ольга Олексіївна – старший науковий співробітник відділу репродуктивного здоров’я ДНУ «Центр інноваційних медичних технологій НАН України», д. мед. н.
Методологічний супровід та інформаційне забезпечення
Гуленко Оксана Іванівна – начальник відділу стандартизації медичної допомоги Департаменту оцінки медичних технологій, адміністрування державних реєстрів та моніторингу цін ДП «Державний експертний центр Міністерства охорони здоров’я України», заступник голови робочої групи з методологічного супроводу
Електронна версія документа знаходиться на офіційному сайті Міністерства охорони здоров’я України: www.moz.gov.ua та у Реєстрі медико-технологічних документів: https://www.dec.gov.ua/mtd/home/.
Рецензенти:
Грищенко Ольга Валентинівна – завідувач кафедри акушерства та гінекології медичного факультету Харківського національного університету ім. В.Н. Каразіна, д. мед. н., професор
Громова Антоніна Макарівна – завідувач кафедри акушерства і гінекології № 1 Полтавського державного медичного університету, заслужений діяч науки і техніки України, д. мед. н., професор
ІІ. Загальна частина
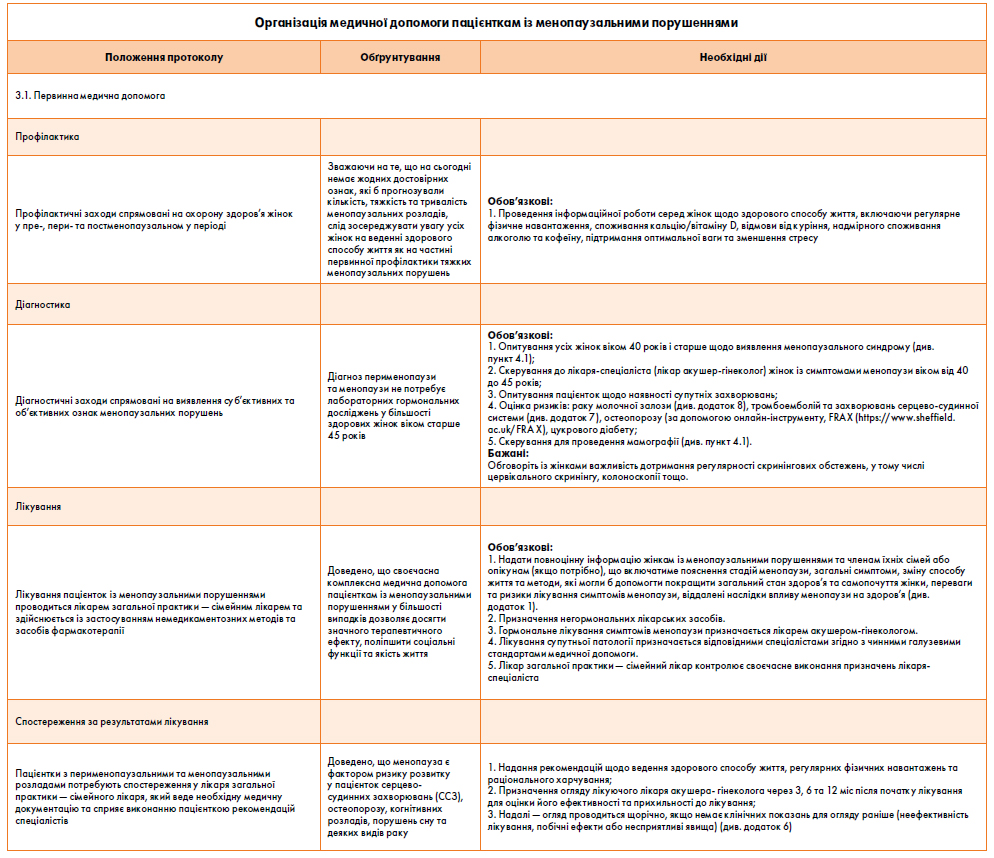
Діагноз менопаузального синдрому та станів, пов’язаних із менопаузальними та перименопаузальними порушеннями, встановлюється у закладах охорони здоров’я (ЗОЗ), що надають первинну та вторинну (спеціалізовану) медичну допомогу на основі скарг, огляду та лабораторних методів дослідження.
Лікарі загальної практики — сімейні лікарі поряд із лікарями акушерами-гінекологами жіночої консультації відіграють одну з ключових ролей в організації діагностики та лікування ранніх та пізніх менопаузальних порушень. На сьогоднішній день менопаузальна гормональна терапія (МГТ) залишається найбільш ефективною терапією менопаузальних порушень.
Перед початком лікування, з метою індивідуалізації терапії та вибору оптимального її методу, необхідно врахувати анамнез супутніх захворювань і факторів ризику серцево-судинної патології, гінекологічних онкологічних захворювань та ризиків раку молочної залози.
Необхідно зазначити, що застосування деяких лікарських засобів, ефективність яких при лікуванні менопаузального синдрому доведена численними дослідженнями і є визнаним методом фармакотерапії, в Україні може мати обмеження, оскільки показання до застосування лікарських засобів при менопаузальному синдромі відсутні в інструкціях для медичного застосування, затверджених Міністерством охорони здоров’я України.
Перелік термінів
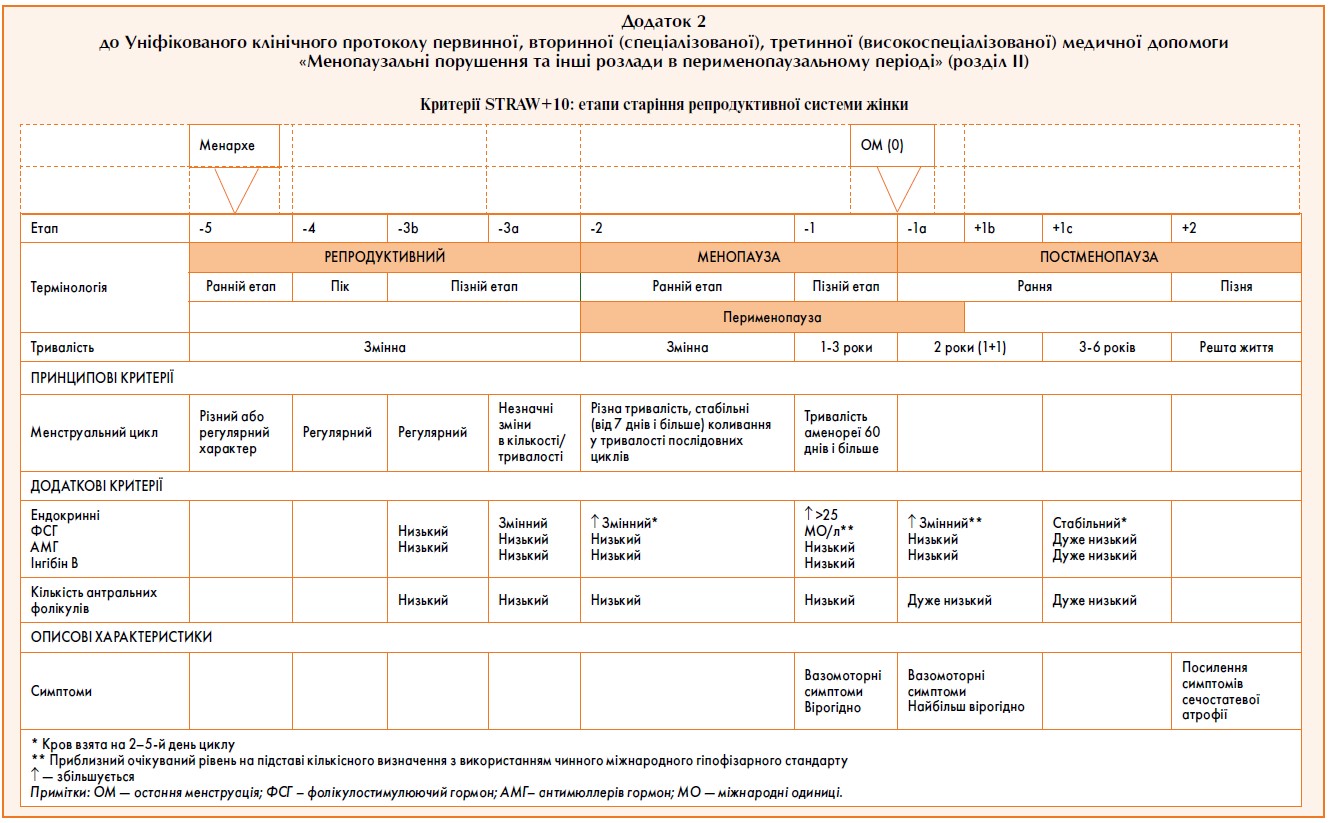
Клімактерій (від грец. climacteric – «щабель сходів») – це фізіологічний перехідний період у житті жінки, впродовж якого на фоні вікових змін в організмі домінують інволютивні процеси в репродуктивній системі, що характеризуються зниженням репродуктивної і менструальної функцій внаслідок генетично запрограмованого згасання та припинення функціонування яєчників. Згідно з критеріями STRAW+10 (Stages of Reproductive Aging Workshop), виділяють 4 періоди клімактерію: період менопаузального переходу, менопауза, перименопауза і постменопауза (див. додаток 2).
Період менопаузального переходу характеризується варіабельністю менструальних циклів, починається у віці 40-45 років і закінчується з настанням менопаузи. На фоні порушень менструального циклу можуть з’являтися вазомоторні симптоми (ВС) та психоемоційні симптоми дефіциту естрогенів, відзначаються варіабельні рівні фолікулостимулюючого гормона (ФСГ), естрадіолу (Е2), зниження рівнів прогестерону, інгібіну В і антимюллерового гормона (АМГ).
Менопауза – це остання самостійна менструація в житті жінки, її дата оцінюється ретроспективно через 12 міс відсутності менструацій.
Менопаузальний синдром – комплекс симптомів, які можуть супроводжувати клімактерій.
Ятрогенна менопауза – припинення менструальної функції в результаті хірургічного видалення обох яєчників (із видаленням матки або без) або іншого способу припинення функції яєчників (радіоактивне опромінення, хіміотерапія).
Виділяють передчасну недостатність яєчників (до 40 років), ранню менопаузу (40-45 років), своєчасну менопаузу (46-54 роки) і пізню менопаузу (від 55 років).
Перименопауза включає період менопаузального переходу від появи перших симптомів та 12 міс після останньої самостійної менструації.
Постменопауза – період після настання менопаузи до закінчення життя жінки. Розрізняють фази ранньої та пізньої постменопаузи. Фазі ранньої постменопаузи, яка у більшості жінок триває протягом 5-8 років, притаманні симптоми клімактеричного синдрому. У фазі пізньої постменопаузи на перший план виходить соматичне старіння жінки, зокрема кардіоваскулярні захворювання, остеопороз і генітоуринарний менопаузальний синдром. ВС менш виражені, але можуть персистувати протягом тривалого часу.
ІІІ. Основна частина
ІV. Опис етапів медичної допомоги
4.1. Діагностика
1. Анамнез
Збір анамнезу та фізикальне обстеження допомагають визначити провідні симптоми менопаузи, скерувати жінку на обстеження, визначити/уточнити тактику ведення пацієнтки.
Для уточнення стадій репродуктивного старіння доцільно використовувати критерії Робочої групи з визначення стадій репродуктивного старіння жінок (STRAW+10) (див. додаток 2).
Критерії STRAW+10 не можуть застосовуватись у жінок із синдромом полікістозних яєчників, передчасною недостатністю яєчників, у жінок, яким введено внутрішньоматкову систему з левоноргестрелом (ВМС-ЛНГ), а також після видалення: ендометрія, одного яєчника та/або тотальної гістеректомії. До таких жінок необхідно застосовувати додаткові критерії для визначення репродуктивного етапу.
Наступні стани діагностуються без лабораторних досліджень у здорових жінок віком старше 45 років:
- перименопауза — на основі ВС та нерегулярних менструацій;
- менопауза — у жінок, які не мали менструацій принаймні 12 міс і при цьому не використовували гормональних контрацептивів, або на основі появи симптомів у жінок, у яких проведена гістеректомія.
Менопаузальні симптоми:
- ВС (припливи та пітливість);
- психоемоційні симптоми (перепади настрою, проблеми зі сном);
- урогенітальні симптоми (дискомфорт та сухість піхви);
- сексуальні розлади (знижене лібідо);
- симптоми з боку опорно-рухової системи (біль у суглобах та м’язах).
Для усіх жінок, старше 40 років, які прийшли на прийом, доцільно задати 6 запитань для виявлення менопаузального синдрому.
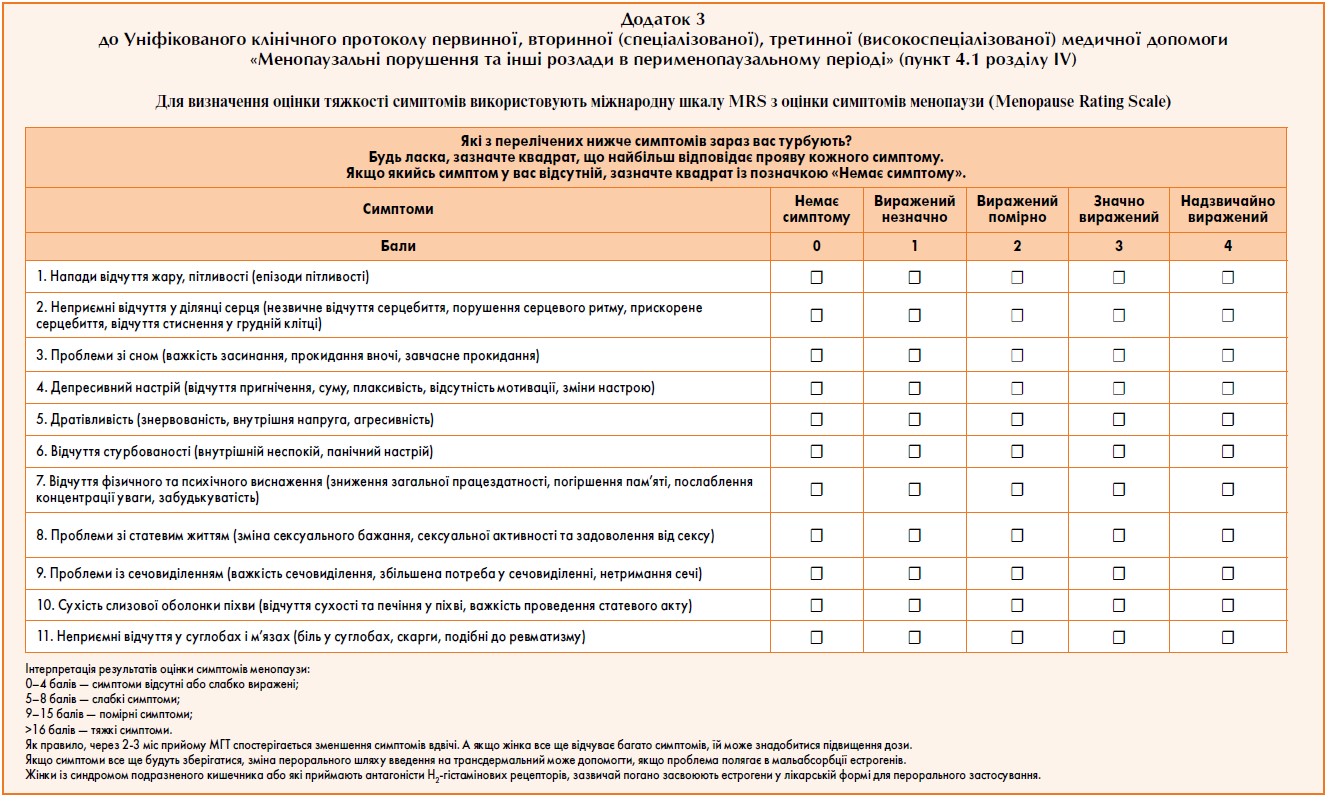
Для визначення тяжкості симптомів менопаузи доцільно використовувати міжнародну шкалу MRS з оцінки симптомів менопаузи (див. додаток 3).
Одним із важливих симптомів менопаузи є генітоуринарний менопаузальний синдром (ГУМС). ГУМС включає симптоми й ознаки, зумовлені впливом дефіциту естрогенів на сечостатеві шляхи жінки, включаючи піхву, статеві губи, уретру та сечовий міхур. Цей синдром включає:
- симптоми вагінальної сухості, печіння та подразнення;
- сечові симптоми та стани дизурії;
- гострі та рецидивуючі інфекції сечовивідних шляхів;
- дискомфортні відчуття болю та сухості під час статевого акту.
Фізичні зміни та ознаки різноманітні. Жінки можуть відчувати деякі або усі симптоми та ознаки, які визначають ГУМС. Слід виключити інші причини подібних ознак та симптомів, включаючи вульвовагінальний дерматоз, інфекцію або рак вульви та піхви.
На відміну від ВС, які зазвичай зменшуються із часом, ГУМС, як правило, прогресує без ефективної терапії.
Менопаузу слід розглядати як фактор ризику розвитку ССЗ, що запускає цілий каскад патологічних змін в організмі жінки, включаючи розвиток артеріальної гіпертензії, дисліпідемії, ожиріння за абдомінальним типом, виникнення інсулінорезистентності, збільшення симпатоадреналового тонусу, порушення ендотеліальної функції, запальні судинні реакції.
Базовий ризик ішемічної хвороби серця (ІХС) та інсульту у жінок менопаузального віку варіюється залежно від наявності чинників ризику. Визначення ризику ССЗ у жінок середнього віку проводиться згідно системи таблиці SCORE (див. додаток 7) або з використанням електронного інтерактивного інструменту для прогнозування та управління ризиком інфаркту та інсульту http://www.HeartScore.org у вигляді електронного калькулятора в модифікації для країн Європи з високим кардіоваскулярним ризиком.
З метою визначення критеріїв для діагностичного пошуку супутньої соматичної патології та подальшого вибору оптимального обсягу обстежень, крім оцінки ризиків ССЗ, доцільно з’ясувати особистий анамнез супутніх захворювань та факторів ризику виникнення:
- раку молочної залози (слід зазначити, що базовий ризик раку молочної залози для жінок менопаузального віку варіює залежно від наявності основних факторів ризику) (див. додаток 8);
- остеопорозу (за допомогою онлайн-інструменту, такого як FRAX) https://www.sheffield.ac.uk/FRAX;
- цукрового діабету;
- ВТЕ;
- наявності сімейного й особистого анамнезу раку ендометрія, яєчників та кишечника (наприклад, синдром Лінча);
- абсолютних або відносних протипоказань для МГТ (див. додаток 4).
2. Фізикальне обстеження
У ході фізикального обстеження важливе значення має визначення ІМТ, окружності талії, виявлення артеріальної гіпертензії, оскільки ожиріння та гіпертонічна хвороба є суттєвими чинниками ризику кардіоваскулярних ускладнень МГТ.
Обстеження органів малого таза включає проведення дослідження шийки матки в дзеркалах, бімануальне дослідження.
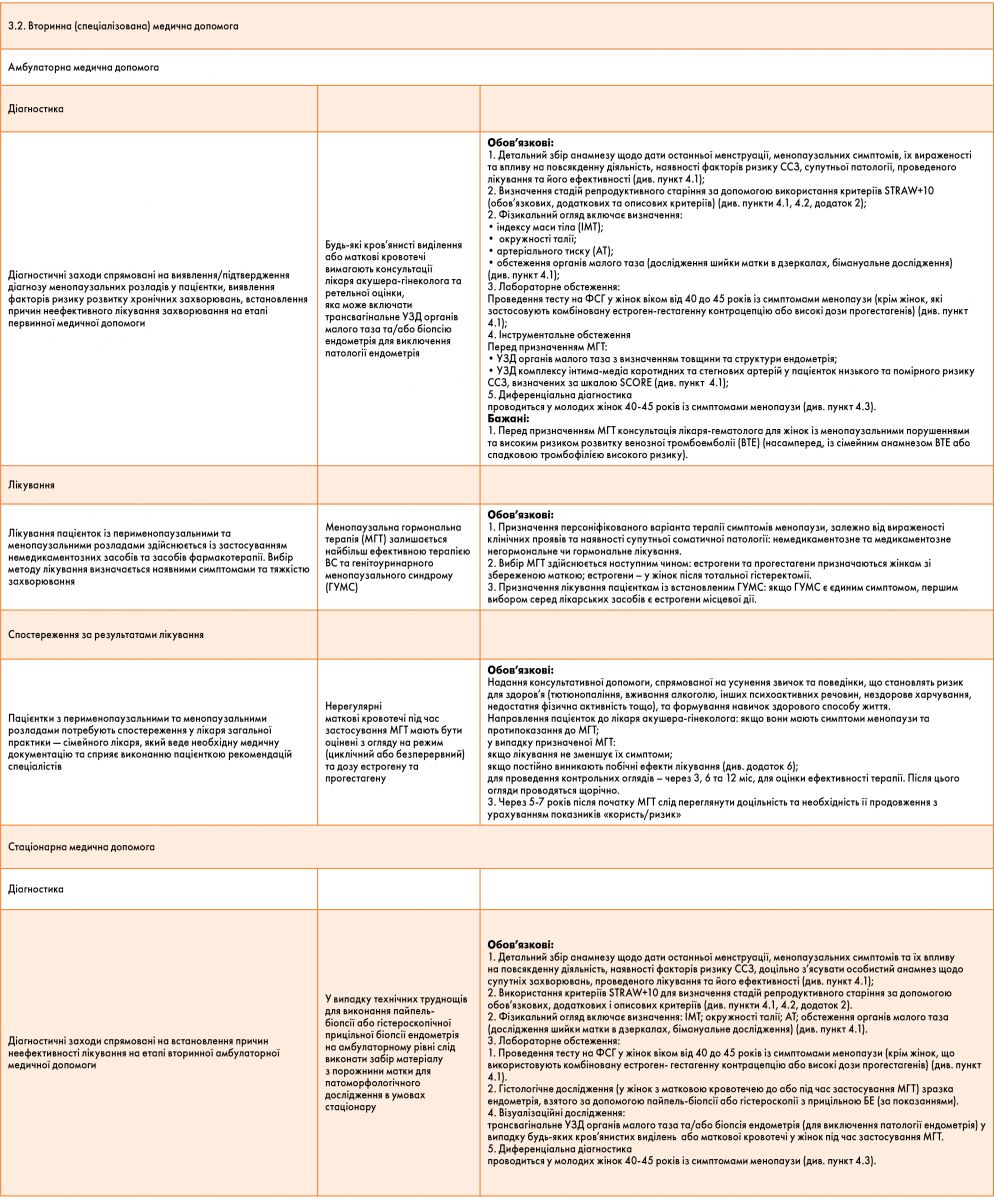
Для діагностики менопаузи використовується тест на фолікулостимулюючий гормон (ФСГ):
- у жінок віком від 40 до 45 років із симптомами менопаузи, включаючи зміни менструального циклу;
- у жінок віком до 40 років, у яких підозрюється передчасна недостатність яєчників.
Для діагностики менопаузи у жінок, які застосовують комбіновану гормональну контрацепцію або високі дози прогестагенів, не використовується тест на сироватковий ФСГ.
Для діагностики менопаузи у більшості здорових жінок віком старше 45 років не потрібно лабораторних гормональних досліджень.
Перед призначенням МГТ необхідне визначення загального рівня холестерину як одного з важливих лабораторних маркерів визначення кардіоваскулярного ризику згідно зі шкалою SCORE.
За наявності факторів ризику супутньої соматичної патології обсяг обстежень визначається відповідними чинними галузевими стандартами медичної допомоги.
Слід дотримуватись чинних галузевих стандартів медичної допомоги щодо цитологічного та мамографічного скринінгу.
4. Інструментальні методи обстеження
У жінок із підвищеним ризиком остеопорозу та переломів, згідно з опитувальником FRAX, визначення мінеральної щільності кісткової тканини здійснюється за допомогою методу подвійної енергетичної рентгенівської абсорбціометрії (DEXA).
4.1. Перед призначенням МГТ необхідно:
- провести УЗД органів малого таза з визначенням товщини та структури ендометрія;
- рекомендоване УЗД із доплерометрією каротидних та стегнових артерій із вимірюванням комплексу інтима-медіа (індивідуально, за наявності факторів ризику) в осіб із низьким і помірним кардіоваскулярним ризиком за шкалою SCORE.
4.2. Формулювання діагнозу
У діагнозі потрібно вказувати період клімактерію: перименопауза або постменопауза, менопауза (як спонтанна, так і ятрогенна), а також провідні симптоми менопаузи.
4.3. Диференціальна діагностика проводиться на основі клінічної оцінки та лабораторних досліджень:
- причини аменореї у молодих жінок — вагітність, гіперпролактинемія, захворювання щитоподібної залози, аменорея гіпоталамічного генезу, нервова анорексія, синдром полікістозних яєчників та ін.;
- поширені причини втоми, зміни настрою — захворювання щитоподібної залози, залізодефіцитна анемія, цукровий діабет 2-го типу, системні захворювання;
- причини припливів — захворювання щитоподібної залози, інфекції, іноді онкологічні захворювання, прийом певних лікарських засобів, а саме: тамоксифену при лікуванні раку молочної залози, деяких лікарських засобів для лікування остеопорозу та деяких антидепресантів.
4.4. Лікування
Порушення якості життя слід обговорювати й оцінювати разом із ризиками розвитку остеопорозу, ССЗ, тромбоемболії та деменції, пов’язаних із старінням, що виникають одночасно з менопаузою.
Варіанти лікування симптомів менопаузи включають немедикаментозне, медикаментозне негормональне та гормональне лікування.
1. Немедикаментозне лікування
Слід зосереджувати увагу на здоровому способі життя як частині первинної профілактики, включаючи регулярне фізичне навантаження, споживання кальцію/вітаміну D, відмову від куріння, надмірного споживання алкоголю та кофеїну, підтримання оптимальної ваги та зменшення стресу.
Контрольоване дихання, когнітивно-поведінкова терапія, тренування усвідомленості, акупунктура, гіпноз та блокування зірчастих гангліїв можуть бути корисними методами, які слід враховувати при лікуванні ВС, особливо у випадках, коли МГТ протипоказана.
2. Менопаузальна гормональна терапія
МГТ необхідно розглядати як частину загальної стратегії, включаючи рекомендації з модифікації способу життя відносно правильного харчування, регулярного фізичного навантаження, припинення куріння та безпечного рівня споживання алкоголю для підтримки здоров’я жінок у період пери- та постменопаузи.
Мета МГТ — частково компенсувати знижену функцію яєчників при дефіциті статевих гормонів, використовуючи оптимальні дози гормональних препаратів, які покращують якість життя та загальний стан пацієнток, забезпечують профілактику пізніх обмінних порушень.
МГТ залишається найбільш ефективною терапією ВС та ГУМС. Інші скарги, пов’язані з менопаузою, наприклад біль у суглобах та м’язах, коливання настрою, порушення сну та статева дисфункція (включаючи знижене лібідо), можуть зменшуватись під час застосування МГТ.
Ризики та переваги застосування МГТ відрізняються для жінок у період менопаузального переходу порівняно із жінками старшого віку. Якщо терапія була призначена жінці з менопаузальними симптомами у віці до 60 років або протягом перших 10 років постменопаузи, то переваги такої терапії значно перевищують ризики.
Жінки, які мають спонтанну або ятрогенну менопаузу у віці молодше 45 років, і зокрема до 40 років, піддаються високому ризику розвитку ССЗ, остеопорозу та підвищеному ризику афективних розладів та деменції. МГТ може зменшити симптоми й зберегти мінеральну щільність кісток і рекомендована принаймні до досягнення середнього віку менопаузи, приблизно до 51 року. Для більшості жінок віком >50 років тривалість МГТ має становити близько 5 років постійного застосування (короткостроковий прийом) для полегшення/усунення симптомів менопаузи.
Жінки в перименопаузі можуть потребувати контрацепції, найбільш безпечним методом є прийом комбінованих оральних контрацептивів (КОК) із натуральним естрогеном у режимі динамічного дозування (естрадіол/дієногест). Жінкам слід продовжувати застосовувати контрацепцію протягом 1 року після останньої менструації, якщо вік складає >50 років, та протягом 2 років у віці до 50 років.
МГТ необхідно індивідуалізувати та адаптувати відповідно до симптомів, особистого та сімейного анамнезу, результатів відповідних досліджень, побажань та очікувань жінок. Прийом індивідуалізованої МГТ може покращити сексуальність та загальну якість життя. Індивідуалізація МГТ — це диференційований підбір терапії з урахуванням стану здоров’я жінки та її супутніх захворювань, а також режиму МГТ (типу, дози, шляху введення та можливих побічних ефектів).
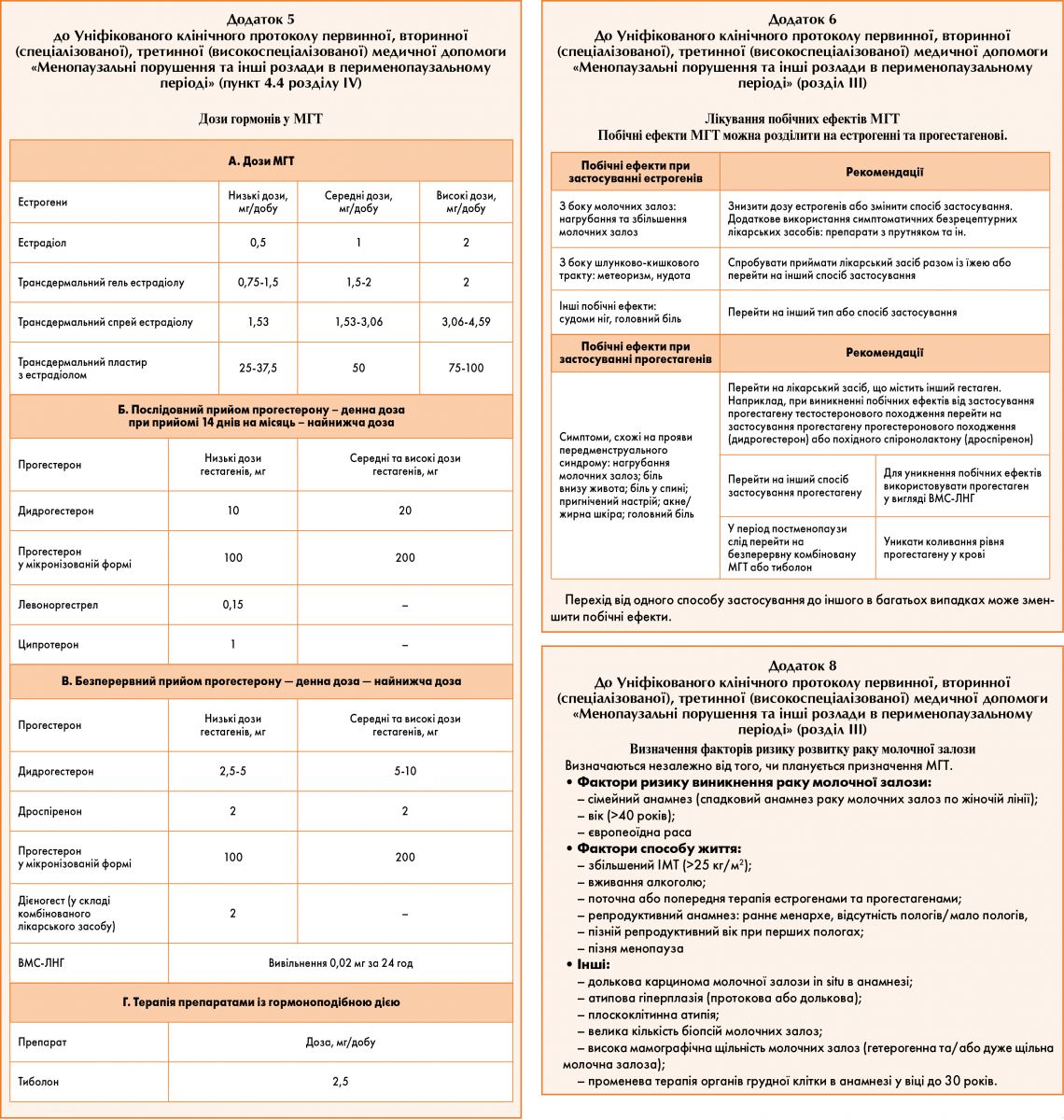
Вибір дозування препаратів МГТ необхідно проводити шляхом титрування до мінімально ефективної дози. Дози гормонів у складі МГТ наведені у додатку 5.
Початок МГТ у постменопаузі переважно починається з найбільш низької дози естрогенів (0,5 мг естрадіолу). За наявності ризику остеопорозу згідно зі шкалою FRAX доцільно починати з більш високої дози (1 мг естрадіолу). У випадку неефективності лікування препаратами з мінімальною дозою естрогенів доцільно розглянути перехід на лікарські засоби з вищою дозою.
Нерегулярні маткові кровотечі є поширеним побічним ефектом МГТ протягом перших 3 міс лікування, але про це слід повідомляти жінок при призначенні МГТ і на огляді лікаря акушера-гінеколога через 3 міс від початку терапії. Необхідно призначити негайну консультацію лікаря акушера-гінеколога, якщо позапланова маткова кровотеча з’явилася після перших 3 міс застосування МГТ.
Не існує причин для встановлення обов’язкових обмежень тривалості МГТ. Дані, отримані у дослідженні «Ініціатива з підтримки здоров’я жінок», та дані інших досліджень підтверджують безпечне застосування МГТ протягом 5 років у здорових жінок, які розпочали лікування у віці до 60 років. Рішення щодо продовження або припинення терапії повинна приймати жінка та її лікуючий лікар, залежно від конкретних цілей та об’єктивної оцінки індивідуальних переваг та ризиків.
Не слід рекомендувати МГТ без чітких показань до застосування, тобто значимих симптомів або фізичних ознак дефіциту естрогенів.
Для лікування ГУМС у жінок із протипоказаннями до системної МГТ можливе призначення естрогенів у лікарській формі вагінальних супозиторіїв або вагінального крему. Препарати естрогенів у жінок з гінекологічним гормон-залежним раком слід застосовувати з обережністю. Призначення естрогенів місцевої дії у жінок, які приймають тамоксифен або інгібітори ароматази, вимагає ретельного обговорення з пацієнткою та консультації лікаря-онколога.
Лікування естрогенами знижує рівень рН вагінального середовища, усуває мікробіологічні зміни, які виникають після менопаузи, та є ефективним у профілактиці рецидивів інфекцій сечовивідних шляхів. Якщо вагінальні естрогени не полегшують симптоми ГУМС, слід розглянути можливість підвищення дози.
Не рекомендований рутинний моніторинг товщини ендометрія під час місцевого лікування ГУМС. Однак жінки з підвищеним ризиком розвитку раку ендометрія внаслідок ожиріння або цукрового діабету можуть потребувати динамічного спостереження за станом ендометрія згідно із чинними галузевими стандартами медичної допомоги.
Тривалість лікування ГУМС вагінальними естрогенами (включаючи жінок, що використовують системну МГТ) може подовжуватися до полегшення симптомів.
Якщо є нетипові ознаки або якщо вульвовагінальні симптоми не вдається усунути після застосування естрогенів у лікарській формі вагінальних супозиторіїв або вагінального крему, слід розглянути проведення бактеріоскопічного дослідження, кольпоскопії, біопсії вульви та піхви.
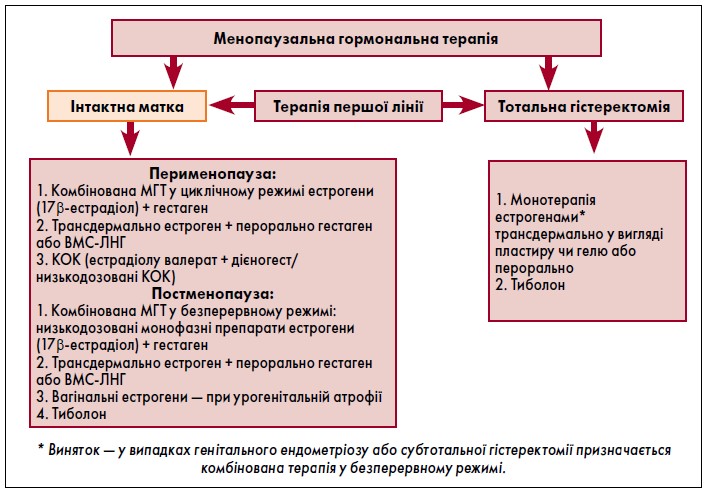
3. Режими менопаузальної гормонотерапії
I — монотерапія естрогенами або прогестагенами
Монотерапія естрогенами трансдермально або перорально призначається жінкам після тотальної гістеректомії, однак при субтотальній гістеректомії та при гістеректомії з приводу ендометріозу рекомендовані естроген-гестагенні препарати для МГТ.
Монотерапія прогестагенами призначається у фазі менопаузального переходу для регуляції менструального циклу. Можливе введення ВМС-ЛНГ із контрацептивною та лікувальною метою. ВМС-ЛНГ 52 мг мінімізує системні побічні ефекти застосування прогестагенів шляхом прямого вивільнення прогестагену в ендометрій.
II — комбінована терапія (естрогени з прогестагенами) у циклічному режимі
Двофазні пероральні лікарські засоби призначаються на стадії менопаузального переходу або в перименопаузі:
- естрадіол 1 мг (14 днів), потім естрадіол 1 мг + дидрогестерон 10 мг (14 днів);
- естрадіол 2 мг (14 днів), потім естрадіол 2 мг + дидрогестерон 10 мг (14 днів);
- естрадіол 2 мг (14 днів), потім естрадіол 2 мг + прогестерон у мікронізованій формі 200 мг (14 днів);
- естрадіол 2 мг (11 днів), потім естрадіол 2 мг + ципротерон 1 мг (10 днів) та 7 днів перерви;
- естрадіол 2 мг (9 днів), потім естрадіол 2 мг + левоноргестрел 0,15 мг (12 днів) та 7 днів перерви.
У разі застосування естрогенів у вигляді трансдермального гелю, спрею або пластиру безперервно слід обов’язково додавати прогестагени протягом останніх 12-14 днів на кожні 28 днів циклічного режиму (дидрогестерон 10 мг/добу або прогестерон у мікронізованій формі 200 мг/добу) або застосувати ВМС-ЛНГ 0,02 мг/добу:
- трансдермальний гель з естрадіолом 0,75-1,5 мг (14 днів), потім трансдермальний гель з естрадіолом 0,75-1,5 мг + дидрогестерон 10 мг або прогестерон у мікронізованій формі 200 мг протягом 12-14 днів;
- трансдермальний спрей з естрадіолом 1,53-4,59 мг (14 днів), потім трансдермальний спрей з естрадіолом 1,53-4,59 мг + дидрогестерон 10 мг або прогестерон у мікронізованій формі 200 мг протягом 12-14 днів;
- трансдермальний пластир із середньою швидкістю вивільнення естрадіолу 50 мкг на добу містить естрадіолу 4 мг, застосовувати 1 пластир з інтервалом у 3-4 дні (у середньому 2 рази на тиждень), потім трансдермальний пластир із середньою швидкістю вивільнення естрадіолу 50 мкг на добу містить естрадіолу 4 мг, застосовувати 1 пластир з інтервалом у 3-4 дні (у середньому 2 рази на тиждень) + дидрогестерон 10 мг або прогестерон у мікронізованій формі 200 мг протягом 12-14 днів.
III — монофазна комбінована терапія (естрогени з прогестагенами) у безперервному режимі в постменопаузі
Жінкам у постменопаузі з інтактною маткою призначаються комбіновані монофазні низькодозовані пероральні лікарські засоби (естрадіол + дидрогестерон 1/5 мг, 0,5/2,5 мг; естрадіол 1 мг + дроспіренон 2 мг; естрадіол 2 мг + дієногест 2 мг), а також тиболон 2,5 мг.
У випадку використання естрогенів трансдермально (спрей, пластир або гель) прогестагени додають у безперервному режимі у зниженій дозі (дидрогестерон 5 мг/добу, або прогестерон у мікронізованій формі 100 мг/добу, або ВМС-ЛНГ 0,02 мг/добу).
Ризик розвитку раку ендометрія у жінок із позаплановою матковою кровотечею, які отримують МГТ, значно нижчий, ніж при постменопаузальних кровотечах у жінок, які не отримують МГТ, особливо у жінок, у яких не спостерігалися кровотечі до початку МГТ та які застосовують прогестагени.
Проривні маткові кровотечі, які виникають після 4-6 міс від початку МГТ, вимагають проведення обстеження, а саме УЗД органів малого таза та/або біопсії ендометрія.
Стани, при яких необхідно віддавати перевагу гістероскопії з прицільною біопсією ендометрія порівняно з пайпель-біопсією:
- неінформативний зразок ендометрія за результатами пайпель-біопсії;
- якщо за результатами трансвагінального УЗД органів малого таза, біопсії ендометрія підозрюються внутрішньоматкові структурні аномалії (наприклад, поліпи);
- наявність зразка ендометрія доброякісного характеру у поєднанні з іншими ознаками, що вказують на високу ймовірність підозри на гіперплазію ендометрія або рак ендометрія;
- наявність хронічної аномальної маткової кровотечі;
- наявність стенозу шийки матки, при якому не вдалося виконати біопсію ендометрія;
- больовий синдром.
У більшості жінок із позаплановою матковою кровотечею, які отримують МГТ, коригування схеми застосування прогестагенів часто сприяє контролю кровотечі, особливо у жінок із позаплановими матковими кровотечами протягом перших місяців від початку МГТ.
У випадку застосування циклічних схем МГТ можна підвищити дозу прогестагенів або збільшити тривалість застосування прогестагенів (прогестаген протягом 14 днів/міс або протягом 21 дня при 28‑денній схемі МГТ).
У разі застосування безперервних комбінованих схем МГТ також можна підвищувати дозу прогестагенів, особливо в комбінації зі схемами застосування естрогенів у високих дозах. До комбінованих схем МГТ, що містять прогестагени у комбінованому препараті або ВМС-ЛНГ, можна додати пероральну форму прогестагену. У випадку продовження позапланових маткових кровотеч схему МГТ можна змінити на циклічну схему прогестагенів.
Схема. Алгоритм призначення менопаузальної гормональної терапії
Жінкам, у яких проривні маткові кровотечі продовжуються більше 6 міс незважаючи на коригування схеми застосування прогестагенів або за наявності занепокоєння щодо клінічного стану чи об’єму/характеру кровотечі, слід призначити УЗД органів малого таза з оцінкою стану ендометрія, пайпель-біопсію ендометрія або гістероскопію з біопсією ендометрія.
Якщо проривна маткова кровотеча настає після переходу на безперервну комбіновану МГТ і не рецидивує через 3-6 міс, жінка може повернутися до послідовної схеми принаймні ще на один рік.
4. Ризики та довгострокові переваги менопаузальної гормональної терапії
Серцево-судинні захворювання
Наявність серцево-судинних факторів ризику не є протипоказанням до МГТ, якщо вони оптимально лікуються та якщо підібрано оптимальне лікування основного захворювання.
Жінки в пери- й постменопаузі та медичні працівники, які займаються їх лікуванням, повинні розуміти, що МГТ не збільшує ризик ССЗ у жінок віком до 60 років та ризик смерті від ССЗ.
Останні дані свідчать, що застосування МГТ не пов’язане з підвищенням АТ. Більше того, МГТ не протипоказана жінкам з артеріальною гіпертензією, і їм може бути призначена гормональна терапія, якщо рівень АТ контролюється антигіпертензивними препаратами.
МГТ та селективні модулятори естрогенних рецепторів (SERM) не слід використовувати для первинної або вторинної профілактики ССЗ. МГТ тільки естрогеном пов’язана із відсутністю або зменшенням ризику ІХС. МГТ естрогеном та прогестагеном асоціюється із незначним або взагалі відсутнім збільшенням ризику розвитку ІХС.
Перед початком МГТ слід провести оцінку факторів кардіоваскулярного ризику за шкалою SCORE (див. додаток 7):
- жінкам із низьким та помірним кардіоваскулярним ризиком (SCORE ≥1% та <5%) перед призначенням МГТ рекомендується УЗД каротидних та стегнових артерій для визначення наявності атеросклеротичних бляшок;
- жінкам із високим кардіоваскулярним ризиком рекомендована консультація лікаря кардіолога (див. додаток 7), проте жінкам із дуже високим кардіоваскулярним ризиком (у тому числі після події ССЗ) застосування МГТ протипоказане.
Венозна тромбоемболія
ВТЕ — узагальнене поняття, що включає тромбоз глибоких вен, тромбофлебіт і тромбоемболію легеневої артерії або її гілок.
Ризик ВТЕ, пов’язаний із трансдермальною МГТ, що застосовується у стандартних терапевтичних дозах, не перевищує вихідний популяційний ризик. Ризик збільшується на тлі застосування пероральної МГТ порівняно з базовим популяційним ризиком і є більшим, ніж для трансдермальних форм лікарських засобів. Комбінація трансдермального естрогену та прогестерону у мікронізованій формі або дидрогестерону є безпечнішим варіантом, який несуттєво збільшує ризик розвитку ВТЕ відносно індивідуального ризику для пацієнтки.
У жінок у пери- та постменопаузі, які мають підвищений ризик розвитку ВТЕ, у тому числі з ІМТ понад 30 кг/м2, рекомендують застосування трансдермальної, а не пероральної МГТ. Віддається перевага застосуванню прогестерону у мікронізованій формі або дидрогестерону у жінок із ризиком розвитку ВТЕ, оскільки ці лікарські засоби не збільшують ризик венозного тромбозу порівняно з іншими препаратами прогестагенів.
Жінок у пери- та постменопаузі з високим ризиком розвитку ВТЕ (наприклад, тих, хто має у сімейному анамнезі ВТЕ або спадкову тромбофілію високого ризику) перед призначенням МГТ необхідно направляти для обстеження до лікаря-гематолога.
Профілактика тромбозу у госпіталізованих жінок, які отримують МГТ, та жінок, які госпіталізуються для планової операції:
- якщо жінку госпіталізують для проведення хірургічного втручання або діагностики супутніх захворювань, також повинна проводитися оцінка ризику розвитку ВТЕ;
- якщо жінок, які отримують МГТ, госпіталізують, вони повинні, за необхідності, отримувати профілактику тромбозу і їм не слід припиняти МГТ;
- якщо запланована операція, можна продовжувати МГТ як трансдермальними, так і пероральними лікарськими засобами, доки проводиться відповідна профілактика тромбозу;
- жінки із додатковими факторами ризику розвитку ВТЕ, які отримують МГТ, що містить пероральний естрадіол, можуть перейти на застосування трансдермальної форми естрадіолу.
Інсульт
Базовий ризик розвитку інсульту серед жінок віком до 60 років дуже низький.
Прийом пероральних (але не трансдермальних) естрогенів пов’язаний із незначним збільшенням ризику розвитку інсульту. Цей ефект, ймовірно, залежить від дози, тому слід призначати МГТ у найнижчій ефективній дозі.
У жінок старше 60 років або більше 10 років після менопаузи, які застосовують монотерапію пероральними естрогенами або комбіновану МГТ, ризик інсульту підвищений. Підвищений ризик обмежується ішемічним інсультом і, ймовірно, пов’язаний із тромбоемболічним ризиком.
Трансдермальний естрадіол не збільшує ризик розвитку інсульту вище вихідного ризику для жінки. Тому слід розглянути можливість трансдермального введення естрадіолу у жінок із факторами ризику або в осіб старше 60 років, за умови призначення естрадіолу в лікарській формі для трансдермального застосування в дозі ≤50 мкг.
Тип прогестагену, що застосовується при МГТ, може впливати на ризик розвитку інсульту. Слід розглянути можливість застосування прогестерону в мікронізованій формі або дидрогестерону в комбінації з трансдермальним естрадіолом у жінок із підвищеним ризиком інсульту.
Мігрень
Коливання рівня естрогенів та порушення менструального циклу пов’язані зі збільшенням поширеності мігрені під час перименопаузи. Тому ефективне лікування ВС може також призвести до зменшення симптомів мігрені.
Мігрень з аурою призводить до підвищення ризику інсульту у 2-2,5 раза протягом усього життя. У жінок із частими мігренями слід проводити аналіз на наявність інших факторів кардіоваскулярного ризику й, за необхідності, застосовувати стратегії зменшення ризику.
Мігрень з аурою не є протипоказанням для призначення МГТ.
Перевага віддається менш тромбогенним гормональним засобам, тобто естрогенам у трансдермальних лікарських формах (пластир, спрей або гель), за необхідності призначення МГТ жінкам з мігренню та аурою у постменопаузі.
Необхідно використовувати найнижчу дозу естрогену, яка ефективно контролює ВС для мінімізації ризиків небажаних побічних ефектів у жінок, які страждають на мігрень з аурою або без неї (див. додаток 6).
У випадку необхідності призначення прогестагенів рекомендується постійне їх введення у вигляді ВМС-ЛНГ чи прогестерону у мікронізованій формі.
Жінки з мігренню та ВС, які не бажають застосовувати МГТ або яким естрогени протипоказані, можуть мати позитивний ефект від використання есциталопраму або венлафаксину.
Цукровий діабет 2‑го типу
Застосування МГТ для лікування симптомів менопаузи у жінок із цукровим діабетом 2‑го типу необхідно розглядати після врахування супутніх захворювань та консультації лікаря-ендокринолога.
Прийом МГТ (перорально або трансдермально) не пов’язаний із підвищеним ризиком розвитку цукрового діабету 2‑го типу. МГТ, як правило, не пов’язана з негативним впливом на рівень глюкози у крові.
У жінок із цукровим діабетом 2‑го типу та супутніми факторами ризику ССЗ, такими як ожиріння, можливе застосування трансдермальних естрогенів.
У жінок із цукровим діабетом 2‑го типу та низьким ризиком ССЗ можливе застосування пероральних естрогенів у складі МГТ.
Серед прогестагенів рекомендується застосування лікарських засобів з нейтральною дією на метаболізм глюкози, таких як прогестерон у мікронізованій формі або дидрогестерон.
Рак молочної залози
МГТ тільки естрогенами пов’язана з незначним підвищенням або взагалі незмінним ризиком виникнення раку молочної залози.
МГТ естрогенами та прогестагенами може бути пов’язана зі збільшенням ризику виникнення раку молочної залози. Підвищений ризик захворювання на рак молочної залози пов’язаний перш за все з додаванням синтетичного прогестагену медроксипрогестерону до терапії естрогенами й залежить від тривалості застосування. Ризик інвазивного раку молочної залози може бути нижчим при використанні прогестерону в мікронізованій формі або дидрогестерону, ніж при застосуванні синтетичних прогестагенів.
Будь-яке збільшення ризику раку молочної залози пов’язане з тривалістю лікування та зменшується після припинення МГТ. Зокрема, використання МГТ протягом 10 років призводить до підвищення ризику раку молочної залози приблизно вдвічі порівняно з 5‑річним застосуванням.
Додатковий ризик, пов’язаний із МГТ, подібний до ризиків, пов’язаних із «сидячим» способом життя, ожирінням та вживанням алкоголю.
Можливе збільшення ризику виникнення раку молочної залози при МГТ може бути частково знижено шляхом призначення МГТ жінкам із більш низьким індивідуальним ризиком, включаючи низьку мамографічну щільність молочних залоз, та шляхом забезпечення жінок інформацією щодо профілактичних заходів відносно способу життя (зниження маси тіла, споживання алкоголю та підвищення фізичної активності).
Застосування вагінальних естрогенів у низьких дозах не підвищує ризик виникнення раку молочної залози у жінок, які не мають раку молочної залози в анамнезі. Залишається невідомим, чи можна безпечно застосовувати цей режим МГТ у жінок із раком молочної залози в анамнезі.
Жінки повинні регулярно проходити огляди, включаючи клінічне обстеження молочних залоз та мамографію відповідно до чинних галузевих стандартів та терміново звертатися за медичною допомогою у випадку виявлення змін.
Через збільшення ризику раку молочної залози у випадку тривалої МГТ рекомендується щорічний перегляд доцільності її застосування. Продовження МГТ після 5-7 років має базуватися на індивідуальних потребах кожної жінки щодо переваг та ризиків продовження МГТ.
Застосування МГТ при раку молочної залози протипоказане.
Остеопороз
Під час застосування МГТ ризик переломів кісток та розвитку остеопорозу зменшуються. Ця перевага зберігається під час лікування, але зменшується після його припинення й може тривати довше у жінок, які приймали МГТ більш тривалий час.
Деменція
Ймовірність впливу МГТ на ризик розвитку деменції не відома.
ВІЛ-позитивні жінки
МГТ у ВІЛ-позитивних пацієнток із менопаузальними порушеннями проводиться за загальними стандартами й не потребує додаткового обстеження та особливих підходів.
Втрата м’язової маси та сили
Є обмежені дані, що МГТ може збільшувати м’язову масу та силу. М’язова маса та сила підтримуються завдяки фізичній активності у щоденному житті. Для мобілізації вісцерального жиру достатньо близько 300 хв помірної фізичної активності на тиждень або 150 хв більш інтенсивної фізичної активності. Для активації метаболізму фізична активність може бути розділена на кілька коротких проміжків тривалістю мінімум 10 хв. Загальна рекомендація для населення становить щонайменше 150 хв помірної аеробної активності на тиждень, що еквівалентно ходьбі зі швидкістю 5-6 км/год. Ходьба залишається найкращим фізичним навантаженням/вправою як для жінок із нормальною/надмірною масою тіла, так і для пацієнток з ожирінням.
5. Негормональне медикаментозне лікування
Лікування ВС без застосування гормональних препаратів можливе й може бути єдиним варіантом у жінок із протипоказаннями до терапії естрогенами або прогестагенами.
Лікарські засоби на основі сангвінарії канадської можуть полегшити ВС. Дані препарати впливають на продукцію, метаболізм і біологічну активність статевих гормонів та внутрішньоклітинних ферментів — ароматаз, що регулюють позагонадне утворення гормонів. Завдяки слабкій естрогенній дії вони зменшують ступінь тяжкості клімактеричного синдрому, не впливаючи при цьому на проліферативні процеси в ендометрії.
Лікарські засоби на основі циміцифуги — найбільш широко вивчені й ефективні фітофармацевтичні препарати для лікування менопаузальних симптомів. Тритерпенові глікозиди циміцифуги мають ефекти, подібні до дії селективних модуляторів рецепторів естрогенів (SERM) — антиоксидантні, протизапальні та серотонінергічні. Не мають естрогенних властивостей, але здійснюють виражений позитивний вплив на зниження ВС, мають помірний позитивний вплив на кісткове ремоделювання та незначний позитивний вплив на вагінальний епітелій, при цьому практично не впливають або діють як антиестрогени на ендометрій, молочні залози, фактори згортання крові.
До лікарських засобів, які мають заспокійливу дію при ВС, відносяться селективні інгібітори зворотного захоплення серотоніну (СІЗЗС) (пароксетин, флуоксетин та ін.) та інгібітори зворотного захоплення серотоніну та норадреналіну (ІЗЗСН) (венлафаксин, дулоксетин та ін.), клонідин, деякі протиепілептичні препарати та інші лікарські засоби центральної дії. Однак вони не застосовуються як терапія першої лінії за наявності лише ВС.
Жінки з раком молочної залози в анамнезі є важливою категорію пацієнток, у яких негормональні методи лікування корисні для купірування ВС. СІЗЗС/ІЗЗСН зменшують припливи у цих пацієнток до 50%, що є прийнятним у більшості випадків. Слід уникати призначення пароксетину жінкам, які отримують тамоксифен.
У пацієнток із посиленням припливів у нічний час, із нічним потовиділенням та повторюваними пробудженнями може бути особливо корисним габапентин завдяки його седативному ефекту. Пацієнткам із такими симптомами рекомендується приймати разову дозу габапентину перед сном. Такий графік лікування може допомогти зменшити побічну дію габапентину.
Для лікування припливів жару та інших ВС також може використовуватися бета-аланін. Його дія спрямована на регуляцію просвіту судин шляхом пригнічення вивільнення гістаміну, збільшення утворення карнозину та активації рецепторів гліцину. Також лікарський засіб діє як антагоніст нікотинової кислоти, що дозволяє застосовувати його для зменшення кількості та інтенсивності припливів, покращення сну. Задовільна переносимість та відсутність залежності дозволяють застосовувати препарат без обмеження в тривалості.
Лікування ГУМС слід починати якомога раніше, до того, як відбулися незворотні атрофічні зміни. Терапію необхідно продовжувати для збереження позитивних результатів.
Лікарські засоби, що застосовуються в урології (оксибутинін) у комбінації з місцевими естрогенами становлять фармакологічне лікування першої лінії у жінок після менопаузи із симптомами гіперактивності сечового міхура.
Лікарські засоби з гормоноподібною дією
Тиболон — синтетичний стероїд, що володіє андрогенними, гестагенними та естрогенними властивостями та виділений в окремий клас терапії — STEAR (тканиноселективний регулятор естрогенної активності).
Тиболон не відрізняється за ефективністю від традиційної МГТ у лікуванні ВС та урогенітальних симптомів, збільшує мінеральну щільність кісткової тканини й ефективний у профілактиці остеопорозу.
Тиболон слід застосовувати лише жінкам >12 міс після менопаузи, оскільки він може спричинити нерегулярні кровотечі у молодих жінок.
4.5. Перегляд призначень та звернення до суміжних спеціалістів
Для кожного варіанта лікування короткочасних симптомів менопаузи необхідно оцінити ефективність та переносимість лікування через 3, 6 та 12 міс, після чого огляд проводити щорічно, якщо немає клінічних показань для огляду раніше (таких, як неефективність лікування, побічні ефекти або несприятливі явища).
Слід направляти жінок до лікаря акушера-гінеколога, якщо лікування не зменшує симптомів менопаузи або якщо виникають побічні ефекти (див. додаток 6).
V. Ресурсне забезпечення виконання протоколу
На момент затвердження цього протоколу засоби матеріально-технічного забезпечення дозволені до застосування в Україні. При розробці та застосуванні клінічних маршрутів пацієнток необхідно перевірити реєстрацію в Україні засобів матеріально-технічного забезпечення, що включаються до клінічних маршрутів пацієнток, та відповідність призначення лікарських засобів Інструкції для медичного застосування лікарського засобу, яка затверджена Міністерством охорони здоров’я України.
Державний реєстр лікарських засобів України знаходиться за електронною адресою: http://www.drlz.kiev.ua.
5.1. Первинна медична допомога
Кадрові ресурси: лікарі загальної практики — сімейні лікарі, середній медичний персонал.
Матеріально-технічне забезпечення:
Оснащення: відповідно до табеля оснащення.
Лікарські засоби:
Засоби, що застосовуються в гінекології: сангвінарія канадська, циміцифуга, бета-аланін.
Вітаміни та мікроелементи: вітамін D, кальцій.
5.2. Вторинна (спеціалізована) медична допомога
Кадрові ресурси: лікарі акушери-гінекологи, середній медичний персонал, інші медичні працівники, які беруть участь у наданні вторинної медичної допомоги пацієнткам із симптомами менопаузи.
Матеріально-технічне забезпечення:
Оснащення: відповідно до табеля оснащення.
Лікарські засоби (порядок розташування не впливає на порядок призначення):
- гормони статевих залоз та засоби, які застосовують при патології статевої сфери:
- естрогени: естрадіол (також у складі комбінованих лікарських засобів), естріол, тиболон;
- прогестагени: прогестерон у мікронізованій формі, дидрогестерон, дроспіренон, дієногест, левоноргестрел (також у складі комбінованих лікарських засобів та у формі ВМС 52 мг);
- антиандрогени: ципротерон (у складі комбінованих лікарських засобів).
- засоби, що застосовуються в гінекології: сангвінарія канадська, циміцифуга, бета-аланін;
- антигіпертензивні лікарські засоби: клонідин;
- вітаміни та мікроелементи: вітамін D, кальцій.
5.3. Третинна (високоспеціалізована) медична допомога
Кадрові ресурси: лікарі акушери-гінекологи, лікарі гінекологи-онкологи, середній медичний персонал, інші медичні працівники, які беруть участь у наданні третинної медичної допомоги пацієнткам із симптомами менопаузи.
Матеріально-технічне забезпечення:
Оснащення: відповідно до табеля оснащення.
Лікарські засоби (порядок розташування не впливає на порядок призначення):
- гормони статевих залоз та засоби, які застосовують при патології статевої сфери:
- естрогени: естрадіол (також у складі комбінованих лікарських засобів), естріол, тиболон;
- прогестагени: прогестерон у мікронізованій формі, дидрогестерон, дроспіренон, дієногест, левоноргестрел (також у складі комбінованих лікарських засобів та у формі ВМС 52 мг);
- антиандрогени: ципротерон (у складі комбінованих лікарських засобів);
- засоби, що застосовуються в гінекології: сангвінарія канадська, циміцифуга, бета-аланін;
- антигіпертензивні лікарські засоби: клонідин;
- засоби, що застосовуються в урології: оксибутинін;
- селективні інгібітори зворотного нейронального захоплення серотоніну (СІЗЗС): есциталопрам, пароксетин, флуоксетин;
- селективні інгібітори зворотного нейронального захоплення серотоніну та норадреналіну (СІЗЗСН): венлафаксин, дулоксетин;
- протиепілептичні засоби: габапентин;
- вітаміни та мікроелементи: вітамін D, кальцій.
VІ. Індикатори якості медичної допомоги
6.1. Перелік індикаторів якості медичної допомоги
1. Наявність у лікуючого лікаря загальної практики — сімейного лікаря, який надає первинну медичну допомогу, КМП із симптомами менопаузи.
2. Наявність у лікарів акушерів-гінекологів, лікарів гінекологів-онкологів, які надають вторинну (спеціалізовану), третинну (високоспеціалізовану) медичну допомогу, КМП з симптомами менопаузи.
6.2. Паспорти індикаторів якості медичної допомоги
1. Наявність у лікуючого лікаря загальної практики — сімейного лікаря, який надає первинну медичну допомогу, КМП із симптомами менопаузи.
Зв’язок індикатора із затвердженими настановами, стандартами та протоколами медичної допомоги:
Індикатор ґрунтується на положеннях УКПМД «Менопаузальні порушення та інші розлади в перименопаузальному періоді».
Зауваження щодо інтерпретації та аналізу індикатора: даний індикатор характеризує організаційний аспект запровадження сучасних протоколів медичної допомоги в регіоні. Якість медичної допомоги пацієнткам, відповідність надання медичної допомоги вимогам КМП, відповідність КМП чинному УКПМД даним індикатором висвітлюватися не може, але для аналізу цих аспектів необхідне обов’язкове запровадження КМП у ЗОЗ.
Бажаний рівень значення індикатора: 2022 рік — 90%; 2023 рік та подальший період — 100%.
Інструкція з обчислення індикатора:
Організація (ЗОЗ), яка має обчислювати індикатор: структурні підрозділи з питань охорони здоров’я місцевих державних адміністрацій.
Дані надаються лікарями загальної практики — сімейними лікарями, зареєстрованими на території обслуговування, до структурних підрозділів із питань охорони здоров’я місцевих державних адміністрацій.
Дані надаються поштою, у тому числі електронною поштою.
Метод обчислення індикатора: підрахунок шляхом ручної або автоматизованої обробки. Індикатор обчислюється структурними підрозділами з питань охорони здоров’я місцевих державних адміністрацій після надходження інформації від усіх лікуючих лікарів загальної практики — сімейних лікарів, зареєстрованих на території обслуговування. Значення індикатора обчислюється як відношення чисельника до знаменника.
Знаменник індикатора складає загальна кількість лікуючих лікарів загальної практики — сімейних лікарів, зареєстрованих на території обслуговування. Джерелом інформації є звіт структурних підрозділів з питань охорони здоров’я місцевих державних адміністрацій, який містить інформацію про кількість лікуючих лікарів загальної практики — сімейних лікарів, зареєстрованих на території обслуговування.
Чисельник індикатора складає загальна кількість лікуючих лікарів загальної практики — сімейних лікарів, зареєстрованих на території обслуговування, для яких задокументований факт наявності КМП із симптомами менопаузи. Джерелом інформації є КМП, наданий лікуючим лікарем загальної практики — сімейним лікарем.
Значення індикатора наводиться у відсотках.
2. Наявність у лікарів акушерів-гінекологів, лікарів гінекологів-онкологів, які надають вторинну (спеціалізовану), третинну (високоспеціалізовану) медичну допомогу, КМП з симптомами менопаузи.
Зв’язок індикатора із затвердженими настановами, стандартами та протоколами медичної допомоги: індикатор ґрунтується на положеннях УКПМД «Менопаузальні порушення та інші розлади в перименопаузальному періоді».
Зауваження щодо інтерпретації та аналізу індикатора: даний індикатор характеризує організаційний аспект запровадження сучасних протоколів медичної допомоги в регіоні. Якість медичної допомоги пацієнткам, відповідність надання медичної допомоги вимогам КМП, відповідність КМП чинному УКПМД даним індикатором висвітлюватися не може, але для аналізу цих аспектів необхідне обов’язкове запровадження КМП у ЗОЗ.
Бажаний рівень значення індикатора: 2022 рік — 90%; 2023 рік та подальший період — 100%.
Інструкція з обчислення індикатора:
Організація (ЗОЗ), яка має обчислювати індикатор: структурні підрозділи з питань охорони здоров’я місцевих державних адміністрацій.
Дані надаються лікарями акушерами-гінекологами, лікарями гінекологами-онкологами, розташованими на території обслуговування, до структурних підрозділів із питань охорони здоров’я місцевих державних адміністрацій.
Дані надаються поштою, в тому числі електронною поштою.
Метод обчислення індикатора: підрахунок шляхом ручної або автоматизованої обробки. Індикатор обчислюється структурними підрозділами з питань охорони здоров’я місцевих державних адміністрацій після надходження інформації від усіх лікарів акушерів-гінекологів, лікарів гінекологів-онкологів, зареєстрованих на території обслуговування. Значення індикатора обчислюється як відношення чисельника до знаменника.
Знаменник індикатора складає загальна кількість лікарів акушерів-гінекологів, лікарів гінекологів-онкологів, зареєстрованих на території обслуговування. Джерелом інформації є звіт структурних підрозділів з питань охорони здоров’я місцевих державних адміністрацій, який містить інформацію про кількість лікарів акушерів-гінекологів, лікарів гінекологів-онкологів, зареєстрованих на території обслуговування.
Чисельник індикатора складає загальна кількість лікарів акушерів-гінекологів, лікарів гінекологів-онкологів, зареєстрованих на території обслуговування, для яких задокументований факт наявності КМП з симптомами менопаузи. Джерелом інформації є КМП, наданий лікарями акушерами-гінекологами, гінекологами-онкологами.
Значення індикатора наводиться у відсотках.
VІІ. Перелік літературних джерел, використаних при розробці клінічного протоколу медичної допомоги
1. Електронний документ «Клінічна настанова, заснована на доказах «Менопаузальні порушення та інші розлади в перименопаузальному періоді», 2021.
2. Наказ МОЗ України від 14 лютого 2012 р. № 110 «Про затвердження форм первинної облікової документації та інструкцій щодо їх заповнення, що використовуються у закладах охорони здоров’я незалежно від форми власності та підпорядкування», зареєстрований в Міністерстві юстиції України 28 квітня 2012 р. за № 661/20974.
3. Наказ МОЗ України від 28 вересня 2012 р. № 751 «Про створення та впровадження медико-технологічних документів зі стандартизації медичної допомоги в системі Міністерства охорони здоров’я України», зареєстрований в Міністерстві юстиції України 29 листопада 2012 р. за № 2001/22313.
4. Наказ МОЗ України від 29 травня 2013 р. № 435 «Про затвердження первинної облікової документації та інструкцій щодо їх заповнення, що використовуються у закладах охорони здоров’я, які надають амбулаторно-поліклінічну та стаціонарну допомогу населенню, незалежно від підпорядкування та форми власності», зареєстрований в Міністерстві юстиції України 17 червня 2013 р. за № 990/23522.
5. Наказ МОЗ України від 21 січня 2014 р. № 59 «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги з питань планування сім’ї».
6. Наказ МОЗ України від 28 липня 2014 р. № 527 «Про затвердження форм первинної облікової документації та інструкцій щодо їх заповнення, що використовуються у закладах охорони здоров’я, які надають амбулаторно-поліклінічну допомогу населенню, незалежно від підпорядкування та форми власності», зареєстрований в Міністерстві юстиції України 13 серпня 2014 р. за № 959/25736.
7. Наказ МОЗ України від 02 листопада 2015 р. № 709 «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при залізодефіцитній анемії».
8. Наказ МОЗ України від 21 січня 2016 р. № 29 «Про внесення змін до первинних облікових форм та інструкцій щодо їх заповнення», зареєстрований в Міністерстві юстиції України 12 лютого 2016 р. за № 230/28360.
9. Наказ МОЗ України від 13 квітня 2016 р. № 353 «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при аномальних маткових кровотечах».
10. Наказ МОЗ України від 28 лютого 2020 р. № 587 «Деякі питання ведення Реєстру медичних записів, записів про направлення та рецептів в електронній системі охорони здоров’я», зареєстрований в Міністерстві юстиції України 05 березня 2020 р. за № 236/34519.
11. Наказ МОЗ України від 30 листопада 2020 р. № 2755 «Про затвердження Порядку ведення Реєстру пацієнтів в електронній системі охорони здоров’я», зареєстрований в Міністерстві юстиції України 13 січня 2021 р. за № 44/35666.
12. Наказ МОЗ України від 10 грудня 2020 р. № 2857 «Про внесення змін до Примірного табеля матеріально-технічного оснащення закладів охорони здоров’я та фізичних осіб-підприємців, які надають первинну медичну допомогу».
Генеральний директор
Директорату медичних послуг МОЗ України Олександра МАШКЕВИЧ
Тематичний номер «Акушерство. Гінекологія. Репродуктологія» № 5 (51) 2022 р.