27 березня, 2015
Перевод с габапентина на прегабалин в терапии периферической нейропатической боли
Периферическая нейропатия (ПН) встречается приблизительно у 2,4% людей в общей популяции и у 8% лиц старше 80 лет. ПН проявляется различными симптомами, в том числе онемением, парестезиями, покалыванием, нарушением координации и функции движения, а также нейропатической болью (НБ).
НБ может сопровождаться другими значимыми симптомами, такими как аллодиния, дизестезия или гиперестезия. Независимо от этиологии НБ ассоциируется с утратой трудоспособности, депрессией, снижением качества жизни (КЖ), а также нарушениями сна и настроения.
Более 85% больных с периферической НБ нуждаются в применении фармакотерапии. Противосудорожные средства габапентин (ГБП) и прегабалин (ПГБ) являются препаратами первой линии терапии НБ независимо от ее этиологии. Оба препарата связываются с a2-d-субъединицей потенциалзависимых кальциевых каналов, тем самым облегчая НБ. Однако ПГБ проще в применении, характеризуется более быстрым началом действия и рассматривается как более мощный ингибитор высвобождения нейромедиаторов по сравнению с ГБП. До настоящего времени не проводились прямые сравнительные исследования ГБП и ПГБ, поэтому выяснить, какой препарат имеет большую эффективность и переносимость, довольно сложно.
Целью данного исследования было определить потенциальную роль замены ГБП на ПГБ в лечении периферической НБ у больных, отвечающих на терапию ГБП или резистентных к ней. Было выдвинуто предположение, что лечение периферической НБ с помощью ПГБ позволит повысить обезболивающий эффект и будет лучше переносится по сравнению с ГБП.
Материалы и методы
Оценка состояния пациентов
С сентября 2005 по июнь 2008 года пациенты с впервые установленным диагнозом ПН и связанной с ней НБ направлялись в специализированные клиники боли при Университете г. Калгари. Для оценки клинической вероятности наличия НБ у больного использовался опросник DN4, характеризующийся высокой чувствительностью (83%) и специфичностью (90%). В исследование включались пациенты, набравшие не менее 4 баллов по опроснику DN4. Оценка клинического состояния пациентов проводилась с помощью шкалы TCSS (Toronto Clinical Scoring System) – простого инструмента, применяемого для скрининга диабетической ПН, который основан на анамнезе заболевания и обследовании пациента с акцентом на сенсорный дефицит. Несмотря на то что данный опросник предназначен в первую очередь для скрининга диабетической ПН, он также используется для количественной оценки других форм нейропатии. Диагноз ПН устанавливался при наличии у больного не менее 3 баллов по шкале TCSS и сенсорных нарушений в дистальных отделах нижних конечностей, выявленных при обследовании.
В исследование не включались пациенты с другой патологией нижних конечностей, в частности ревматологическими нарушениями или заболеваниями периферических сосудов. Пациенты с симптомами боли, проявляющимися только во время напряжения, также исключались из последующего наблюдения в связи с вероятностью наличия у них заболеваний периферических сосудов или нейрогенной перемежающейся хромоты.
Оценка ПН
Всем участникам проводили полное стандартизированное неврологическое и электрофизиологическое обследование, а также лабораторные исследования: полный анализ крови, определение содержания электролитов, мочевины, креатинина, аланинаминотрансферазы, аспартатаминотрансферазы, гамма-глутамилтранспептидазы, щелочной фосфатазы, общего билирубина, международного нормализованного отношения, уровня тиреотропного гормона; 2-часовый тест толерантности к глюкозе; определение уровня HbА1с, кобаламина, ревматоидного фактора, витамина В12, метилмалоновой кислоты и гомоцистеина, скорости оседания эритроцитов, содержания антинуклеарных антител; тест на выявление антител к экстрагированным ядерным антигенам; электрофорез сывороточных белков.
Замена ГБП на ПГБ и последующее наблюдение
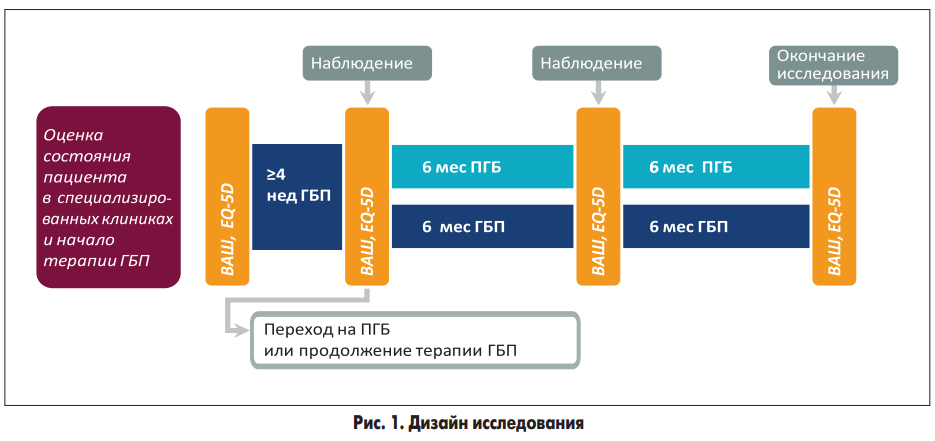
Во время оценки клинического состояния все пациенты начинали принимать ГБП. Во время последующих визитов (после появления ПГБ на фармацевтическом рынке Канады с сентября 2005 г.) всем участникам исследования, уже использующим в качестве монотерапии ГБП, было предложено перейти на терапию ПГБ. Необходимым условием был прием максимально переносимой дозы ГБП в течение как минимум 2 нед, при этом общая длительность терапии ГБП должна была превышать 4 нед. Появление побочных эффектов при использовании ГБП не рассматривалось как основание для перевода на прием ПГБ; в качестве причины для изменения терапии могла служить только неэффективность ГБП по оценке пациента. Из-за ограничений медицинского страхования не все пациенты имели возможность изменить фармакологическое лечение; эти больные исключались из дальнейшего наблюдения. Пациенты, которые для лечения НБ использовали несколько препаратов, в число которых входил ГБП, также исключались из исследования. Непосредственно перед переходом с терапии ГБП на ПГБ (начальная временная точка – 0 мес) у всех больных оценивали выраженность болевого синдрома по визуальной аналоговой шкале (ВАШ) и КЖ (рис. 1).
Сравнение результатов исследования проводилось между группой пациентов, которые переходили с ГБП на ПГБ, и группой непрерывной терапии ГБП. Последняя состояла из пациентов, которые не могли или не желали перейти на терапию ПГБ в связи с финансовыми ограничениями или по личным причинам.
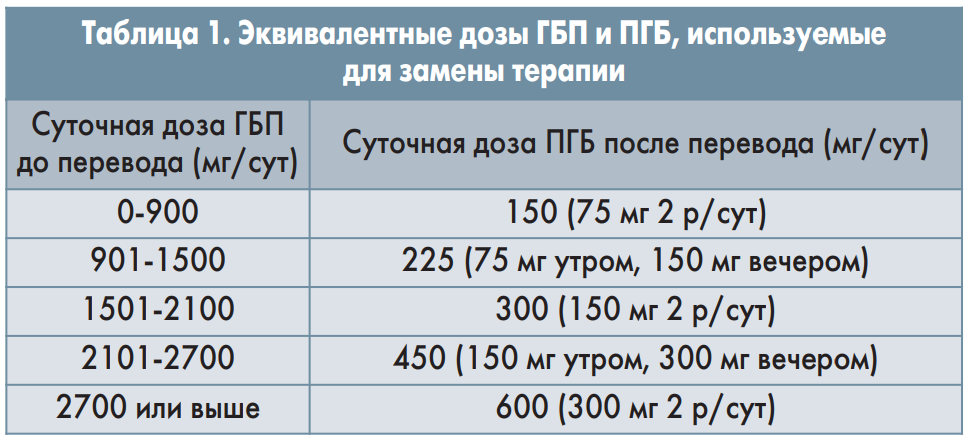
Прямое переключение терапии с ГБП на ПГБ осуществлялось следующим образом: вечером принималась последняя доза ГБП, а утром начинался прием ПГБ; доза последнего рассчитывалась в соответствии с таблицей 1. Через 1 нед после изменения терапии все пациенты сообщали о появлении любых новых или непереносимых нежелательных явлений (НЯ). Дополнительные визиты при последующем клиническом наблюдении проводились через 6 и 12 мес. На каждом визите оценивалась степень НБ по ВАШ (0 – отсутствие боли, 10 – невыносимая боль).
Вторичные конечные точки включали определение индекса здоровья и КЖ с использованием опросника EQ-5D (European Quality of Life-5 Domains), который заполнялся до начала терапии ГБП, по завершении (или продолжении) приема ГБП и через 6 и 12 мес терапии ПГБ или для мониторинга терапии ГБП. Опросник EQ-5D состоит из двух разделов. Первый раздел включает вопросы, позволяющие оценить качество жизни больного по 5 основным критериям: подвижности, способности к самообслуживанию, повседневной активности, интенсивности боли/дискомфорта, наличию тревоги/депрессии. Общий показатель (индекс здоровья) варьирует от -0,594, что свидетельствует о серьезной проблеме во всех аспектах, до 1, что указывает на отсутствие проблем. Второй раздел опросника используется для самооценки пациентом своего состояния по ВАШ (0 – наихудшее состояние здоровья, 100 – наилучшее).
Переносимость и НЯ
С целью определения переносимых и непереносимых НЯ во время или до начала визитов последующего наблюдения использовались стандартизированные формы; также регистрировались все НЯ, требовавшие прекращения терапии. К НЯ относили любой негативный, непреднамеренный и непрогнозируемый ответ на терапию, который, вероятно, был связан с применением препарата. Серьезное НЯ определялось как любая опасная для жизни реакция на фармакотерапию, которая требовала госпитализации, проведения дополнительного неотложного вмешательства или была причиной стойкой нетрудоспособности. Участники исследования должны были информировать о любых НЯ, которые они связывали с медикаментозной терапией. Если пациенты считали облегчение боли недостаточным или сообщали о появлении непереносимых НЯ, которые ограничивали их повседневную активность, дальнейшая тактика предусматривала прекращение лечения, замену препарата, увеличение дозы принимаемого лекарства или добавление второго препарата. Регистрация НЯ проводилась на каждом визите в начале исследования (0 мес), через 6 и 12 мес терапии.
Анализ данных
С целью оценки данных использовали метод дисперсионного анализа ANOVА. Для сравнения учитывались показатели выраженности боли до замены ГБП на ПГБ и полученные в ходе последующего наблюдения при приеме либо ГБП, либо ПГБ. Для проведения множественных сравнений между тремя клиническими группами применялась корректировка Бонферрони.
Результаты
В общей сложности было обследовано 146 пациентов, которым назначили монотерапию ГБП. 77 пациентов не пере- шли на терапию ПГБ, поскольку либо не могли, либо не желали прекратить прием ГБП, из них 47 больных продолжили прием ГБП и составили так называемую когортную группу непрерывного приема ГБП.
У 33 больных монотерапия ГБП в течение 4 нед привела к облегчению боли (группа пациентов, ответивших на терапию ГБП); у 36 пациентов монотерапия данным препаратом на протяжении этого периода не способствовала уменьшению болевого синдрома как минимум на 30% (группа больных, резистентных к терапии). Во всех случаях причиной для перехода на ПГБ была неэффективность ГБП (по субъективной оценке участников) в отношении снижения боли. Все эти 69 пациентов были переведены на терапию ПГБ и подлежали обследованию через 6 и 12 мес терапии.
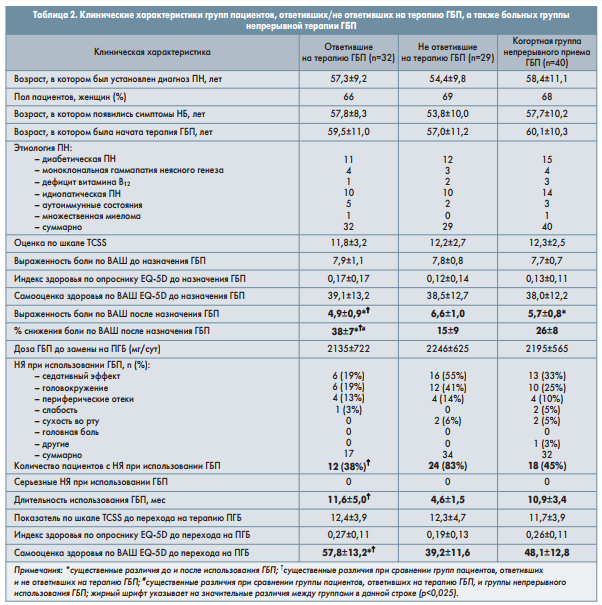
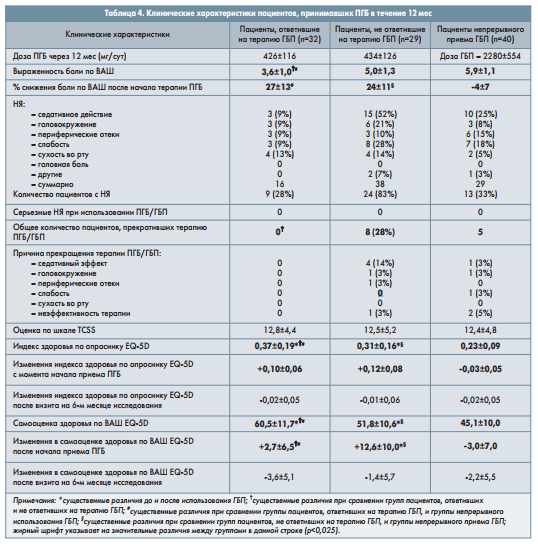
В когортную группу включили 47 пациентов с периферической НБ, получающих непрерывное лечение ГБП; период наблюдения за ними также составил 12 мес. Больные группы непрерывной терапии ГБП и пациенты, которые перешли на прием ПГБ, как ранее ответившие на терапию ГБП, так и нет, имели сходные клинические характеристики (табл. 2). Количество пациентов, досрочно прекративших лечение, в трех группах варьировало от 3 до 19%, при этом наивысшие показатели зарегистрированы в группе больных, ранее не ответивших на терапию ГБП. Ни один из больных трех групп не прекратил терапию после 6 мес наблюдения.
Пациенты всех групп были сопоставимыми по возрасту, полу, степени тяжести нейропатии и достигнутой дозе ГБП (табл. 2). Не было отмечено достоверных различий между группами пациентов, ответивших и не ответивших на ГБП, в отношении выраженности боли по ВАШ, оценке по ТCSS и EQ-5D перед использованием ГБП (табл. 2). Однако у больных, ответивших на терапию ГБП, наблюдалось значительное снижение выраженности боли (на 38%) по ВАШ по сравнению с исходными показателями, тогда как в группе пациентов, резистентных к ГБП, интенсивность боли снизилась на 15%, а в группе непрерывной терапии ГБП – на 26% (табл. 2).
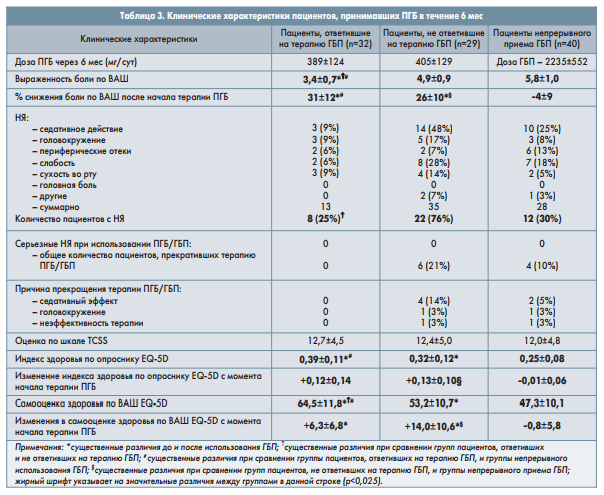
Лучшие показатели состояния здоровья по ВАШ (самооценка пациентами) были зарегистрированы в группе ответивших на терапию ГБП по сравнению с резистентными к ГБП и группой непрерывного приема ГБП, хотя индекс здоровья по опроснику EQ-5D достоверно не отличался между этими группами пациентов (табл. 2). Длительность терапии ГБП была значительно больше в группе больных, ответивших на терапию ГБП, тогда как разницы в максимальной дозе ГБП между тремя группами отмечено не было (табл. 2). Пациенты, резистентные к ГБП, чаще заявляли о появлении НЯ, связанных с приемом этого препарата (табл. 2). Достоверных различий в дозировке ПГБ после замены терапии между группами пациентов не наблюдалось (табл. 3). Доза ГБП в когортной группе непрерывного приема ГБП существенно не изменилась с течением времени (табл. 3 и 4).
Через 1 нед после замены ГБП на ПГБ пациенты, ранее ответившие на терапию ГБП, не отметили появления непереносимых НЯ. У 3 из 29 участников исследования, резистентных к терапии ГБП, был зарегистрирован чрезмерный седативный эффект, у 4 из 29 больных – легкое головокружение.
В группе пациентов, как ранее ответивших на терапию ГБП, так и резистентных к ней, через 6 и 12 мес после замены препарата отмечалось значительное снижение НБ по ВАШ (табл. 3 и 4). Не было показано существенных различий в индексе здоровья по опроснику EQ-5D между группами больных, ответивших и не ответивших на терапию ГБП. Однако через 6 и 12 мес лечения пациенты с хорошим терапевтическим ответом на ГБП, а также через 12 мес терапии лица, резистентные к ГБП, имели более высокий индекс здоровья по сравнению с группой непрерывной терапии ГБП (табл. 3 и 4).
Через 6 и 12 мес после начала приема ПГБ в группе пациентов, резистентных к ГБП, улучшилась самооценка здоровья по ВАШ опросника EQ-5D (табл. 3 и 4). Через 12 мес терапии было отмечено незначительное снижение самооценки здоровья по ВАШ опросника EQ-5D и индекса здоровья в группах участников, ранее ответивших и не ответивших на терапию ГБП, по сравнению с показателями, полученными через 6 мес лечения.
После замены ГБП на ПГБ во всех группах пациентов были выявлены НЯ (табл. 3 и 4), причем чаще они регистрировались среди больных, ранее не ответивших на терапию ГБП, по сравнению с пациентами, ответившими на ГБП (табл. 2-4). Большинство пациентов, отмечавших НЯ при использовании ГБП, отметили появление НЯ на фоне терапии ПГБ. В то же время серьезные НЯ не были выявлены ни в одной группе больных. Спустя несколько месяцев терапии пациенты, ранее не ответившие на терапию ГБП, чаще прекращали использование ПГБ, тогда как ни один пациент из группы ответивших на терапию ГБП не прекратил прием ПГБ (табл. 3 и 4).
Обсуждение
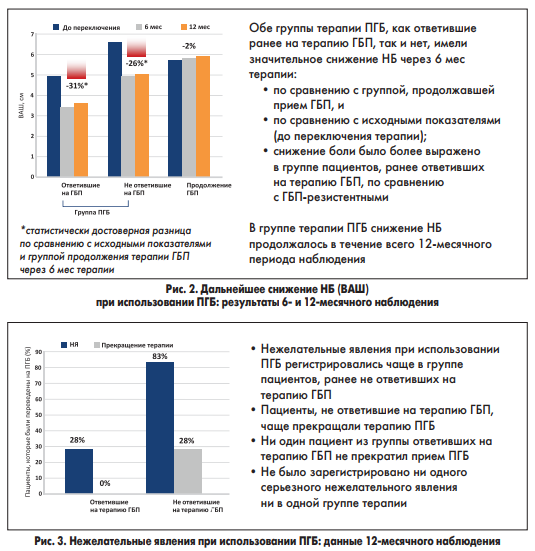
Облегчение НБ у пациентов с периферической НБ может быть наиболее эффективным подходом в улучшении их общего состояния здоровья и повышении КЖ. В данном проспективном исследовании замена ГБП на ПГБ способствовала усилению обезболивающего эффекта и снижению частоты НЯ, особенно в популяции пациентов, ответивших на терапию ГБП. Дальнейшее снижение тяжести НБ было достигнуто в обеих группах, хотя у резистентных к ГБП больных наблюдался относительно лучший ответ на терапию ПГБ. Более того, использование ПГБ у пациентов обеих групп привело к усилению обезболивающего эффекта по сравнению с группой непрерывной терапии ГБП (рис. 2).
В исследовании было показано повышение самооценки здоровья по ВАШ EQ-5D в группе больных, резистентных к ГБП, которые перешли на терапию ПГБ. Даже с учетом частоты прекращения терапии пациентами, резистентными к ГБП, исследование показало улучшение самооценки здоровья по ВАШ и повышение индекса здоровья при использовании опросника EQ-5D. Пациенты, которые отмечали появление НЯ или не переносили терапию ГБП (группа не ответивших на терапию ГБП), имели больше НЯ при использовании ПГБ, что позволяет предположить наличие у этой категории пациентов повышенной предрасположен- ности к НЯ или генетической предрасположенности к НЯ при использовании ГБП и/или ПГБ.
Терапия ПГБ, как правило, хорошо переносилась пациентами. В течение первой недели после замены препаратов появления НЯ в группе больных, ранее ответивших на лечение ГБП, отмечено не было, однако в группе резистентных к ГБП были зарегистрированы незначительные НЯ. Длительное использование ГБП ассоциировалось с лучшей переносимостью НЯ в группе ответивших на ГБП, но было связано с худшей непереносимостью и даже прекращением терапии в группе резистентных к ГБП (рис. 3).
ПГБ обладает несколькими потенциальными преимуществами по сравнению с ГБП у пациентов с НБ. Новые противосудорожные препараты, такие как ГБП и ПГБ, имеют меньший риск лекарственных взаимодействий, что особенно важно для пожилых пациентов, получающих терапию по поводу сопутствующих заболеваний.
Одной из наибольших проблем при использовании ГБП является назначение врачами недостаточной дозы препарата. Субоптимальное дозирование ГБП может привести к несоответствующему уровню снижения боли и ложному впечатлению о неэффективности лечения. Нелинейный профиль фармакокинетического действия ГБП может также затруднять титрование дозы препарата до эффективной с целью свести к минимуму риск НЯ. Новый препарат ПГБ обладает большей биодоступностью и линейным фармакокинетическим профилем действия при его назначении в дозе 150-600 мг/сут, что делает его эффективным обезболивающим средством в терапии НБ, связанной с диабетической ПН и постгерпетической нейропатией. Наконец, ПГБ может иметь большее сродство с α2-β-субъединицей потенциалзависимых кальциевых каналов, чем ГБП.
Существуют определенные ограничения при анализе результатов данного исследования. Основные ограничения связаны с невозможностью непосредственного сравнения эффективности и переносимости двух препаратов, назначаемых в качестве стартовой терапии. Исследование не являлось слепым и не имело оптимальной контрольной группы для сравнения с учетом отсутствия группы плацебо. Хотя всем пациентам было рекомендовано использовать консервативные методы лечения НБ, включая аэробные виды физических упражнений, контролировать их выполнение, как и прием пациентами безрецептурных препаратов, не представлялось возможным.
Необходимо учитывать, что пациенты, наблюдаемые в клиниках специализированной помощи, не могут представлять популяцию больных с ПН в целом. Наконец, в исследовании не проводился анализ дополнительных данных, включая нарушения настроения и сна. Данные, представленные в этом исследовании, нельзя приравнивать к результатам рандомизированного двойного слепого контролируемого исследования, непосредственно сравнивающего ПГБ и ГБП, но вероятность проведения такого исследования в будущем крайне низка.
Выводы
В популяции пациентов с периферической НБ использование ПГБ может обеспечить более выраженное купирование боли, чем ГБП, при этом реже вызывая НЯ. Было показано, что у пациентов, ответивших на терапию ГБП, после перевода на ПГБ удалось достичь дальнейшего снижения НБ без появления дополнительных НЯ, тогда как среди больных, резистентных к ГБП, назначение ПГБ позволило снизить выраженность боли.
Таким образом, были представлены доказательства целесообразности замены ГБП на ПГБ при лечении пациентов, не удовлетворенных результатами терапии ГБП, независимо от ее эффективности.
Статья печатается в сокращении.
Список литературы находится в редакции.
Pain Medicine 2010; 11: 456-465
Перевела с англ. Ольга Татаренко