28 квітня, 2017
Рекомендації щодо загального скринінгу та профілактики патології щитоподібної залози у вагітних
Захворювання щитоподібної залози (ЩПЗ) є дуже поширеними в усьому світі та чинять негативний вплив майже на всі функції організму людини в різні періоди її життя. Спочатку порушення функції ЩПЗ є непомітними, але через кілька місяців або років вони стають незворотними, а отже, потребують тривалого лікування та/або хірургічного втручання. Особливо чутливими до таких порушень є плід, діти і підлітки, вагітні та жінки, які годують груддю. Своєчасне виявлення і лікування тиреоїдних розладів, їх профілактика є запорукою подолання проблеми або контролю над нею.
Своєчасне виявлення у вагітних порушень функціонального стану ЩПЗ, так само як цукрового діабету, – це дуже важливе завдання, тому проведення тиреоїдних тестів (ТТГ, АТПО, АТТГ, рівень тиреоглобуліну) і визначення глікемії (рівень глюкози натще, пероральний тест толерантності до глюкози, вміст глікозильованого гемоглобіну) є обов’язковими для жінки при плануванні вагітності, контролю її розвитку, а іноді й після пологів.
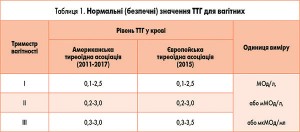
У нормі ЩПЗ синтезує низку гормонів, які впливають на всі без винятку клітини і тканини, від них залежить діяльність серцево-судинної, нервової та статевої систем тощо, процеси росту, дозрівання, фізичного та інтелектуального розвитку людини. Функція ЩПЗ регулюється гіпоталамусом і гіпофізом завдяки стимулюючому впливу тиреотропного гормону (ТТГ). Згідно з новими рекомендаціями Американської тиреоїдної асоціації (АТА) (American Thyroid Association, 2017) [1] нормальний рівень ТТГ для вагітних залежить від триместру вагітності (табл. 1).
При розвитку гіпотиреозу у невагітних жінок підвищується концентрація ТТГ у крові ≥4 мМОд/л, але у вагітних порушенням функції ЩПЗ вважається його рівень ≥2,5-3,5 мМОд, при якому зростає ризик безпліддя або викидня.
На щастя, більшість розладів ЩПЗ, які впливають на вагітність, можна легко діагностувати та скоригувати. Складність у таких випадках полягає в тому, щоб зрозуміти те, що наявні проблеми стосуються саме ЩПЗ, оскільки часто симптоми цих порушень є незначними та мають загальний характер: слабкість, підвищена втомлюваність, сонливість удень, безсоння вночі, порушення менструального циклу, коливання артеріального тиску. При гіпертиреозі спостерігаються тахікардія, погана переносимість спеки, при гіпотиреозі – сухість шкіри і/або закрепи.
 При виявленні у вагітних гіпотиреозу (субклінічного або маніфестного) їм призначають препарати L-тироксину, дозу яких підбирають індивідуально, з метою підтримувати рівень ТТГ у межах ідеальних значень – нижче 2,5 мМОд/л протягом усього періоду вагітності.
При виявленні у вагітних гіпотиреозу (субклінічного або маніфестного) їм призначають препарати L-тироксину, дозу яких підбирають індивідуально, з метою підтримувати рівень ТТГ у межах ідеальних значень – нижче 2,5 мМОд/л протягом усього періоду вагітності.
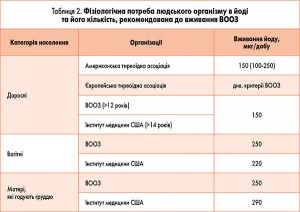
Від функціонального стану ЩПЗ залежить можливість самого зачаття, виношування і народження здорової дитини. Тиреоїдні гормони потрібні для розвитку головного мозку і серця майбутньої дитини, інших тканин її організму. Мікроелемент йод необхідний для синтезу цих гормонів, а його нестача зумовлює йододефіцитний стан у людей будь-якого віку – у плода, дітей та дорослих, у тому числі такий стан може негативно позначитися на інтелекті як людини зокрема, так і нації загалом (табл. 2).
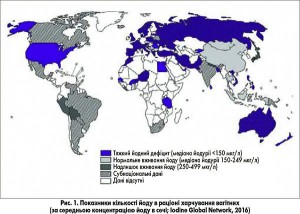
Експерти ВООЗ, ЮНІСЕФ та Міжнародного комітету з контролю йододефіцитних захворювань (WHO; UNICEF; Iodine Global Network; 2014) створили глобальну базу даних щодо поширеності йододефіцитних захворювань (рис. 1) [2]. Для цього вони використали відомості про вміст йоду в сечі – найбільш адекватному епідеміологічному індикаторі вживання йоду населенням у цілому. Вони були отримані з національних і субнаціональних досліджень, проведених у різних країнах світу з 1993 по 2016 рр. [3]. Згідно з даними Iodine Global Network, уточненими у 2016 р., більша частина території країн СНД та Європи, серед них і Україна, є найбільшою зоною дефіциту йоду (рис. 1).
У середньому дорослий українець отримує йод у кількості 50-80 мкг/добу, яка є нижчою за необхідну – 150 мкг/добу (у межах 100-250 мкг/добу).
Для вагітних і жінок, які годують груддю, добова потреба в йоді – вища, а саме 250 мкг, тому вони та їхні діти є найбільш уразливими групами населення.
Йод – мікроелемент, необхідний для вироблення гормонів ЩПЗ, діяльності шлунку і грудних залоз, інших тканин (шкіри, очей, головного мозку). Його можна отримати тільки з екзогенних джерел харчування.
Термін «йододефіцитні захворювання» запропонований ВООЗ у 2001 р. для позначення всіх патологічних станів, які розвиваються у популяції в результаті йодного дефіциту та можуть бути зворотними при нормалізації вживання йоду [2].
Ця проблема є актуальною орієнтовно для 40% населення планети (рис. 1) [3-4]. Йод, отриманий із їжею, легко проникає у кровообіг через слизову шлунково-кишкового тракту у вигляді йодиду і концентрується у ЩПЗ за допомогою натрій-йодат сімпортеру. У тиреоїдних фолікулах із йоду та тирозину синтезуються гормони – тироксин і трийодтиронін. Ці гормони необхідні, зокрема, для статевого розвитку і терморегуляції та енергообміну. Нестача йоду приводить до порушення усіх процесів у людському організмі. До 90% йоду екскретується із сечею, 10% – з жовчю.
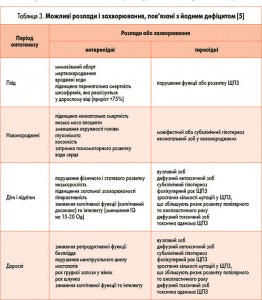
За даними ВООЗ, патологічні стани, викликані дефіцитом йоду, посідають 3-тє місце у переліку 38 найпоширеніших неінфекційних захворювань людини. До йододефіцитних захворювань та їх ускладнень відносять збільшення кількості мертвонароджених немовлят, передчасне переривання вагітності, безпліддя, глухоту і косоокість новонароджених, затримку фізичного, статевого та розумового розвитку дітей, зростання показників серцево-судинних захворювань та ін. Дефіцит йоду може також спричинити гіпотиреоз, у тому числі вроджений, дифузний нетоксичний зоб, вузловий зоб або дифузний токсичний зоб, психічні захворювання, депресію, низьку базальну температуру тіла (табл. 3).
Йододефіцитний стан може розвинутися у людини будь-якого віку. Частота цих станів не пов’язана ні зі статтю, ні з расою. Навіть незначний дефіцит йоду під час вагітності може привести до порушення розвитку головного мозку плода і таким чином негативно позначитися на інтелекті майбутньої дитини.
Загалом порушення функції ЩПЗ (гіпотиреоз, гіпертиреоз) діагностують нечасто – у 2-5% населення. Найбільша частота (до 12%) спостерігається серед вагітних та жінок, які не можуть завагітніти, а у тих, хто вдається до екстракорпорального запліднення, – до 20%.
У ранні терміни вагітності (до 3-4 міс) плід функціонує тільки за рахунок гормонів ЩПЗ матері. Цей період, особливо перші 4 тижні після зачаття, є критичним. У ці терміни вагітності трапляється найбільша кількість викиднів, пов’язаних із дефіцитом йоду або гіпотиреозом у матері.
Сьогодні в Україні виявляють значну кількість жінок із субклінічним гіпотиреозом, головною причиною якого є йодний дефіцит. Людині притаманна висока чутливість до дефіциту йоду і значна стійкість до його надлишку протягом тривалого часу. Тому, за рекомендацією ВООЗ, вагітні, особливо ті, які мешкають у йододефіцитних регіонах, мають упродовж усієї вагітності додатково приймати таблетовані препарати йоду. Для вагітних його потреба становить в середньому 250 мкг/добу. Безпечний рівень вживання йоду для жителів більшості регіонів світу – до 1000 мкг/добу сумарно. Поки що в нашій країні забезпечити щоденну потребу в йоді за рахунок їжі майже неможливо.
Враховуючи те, що в Україні дорослі фактично отримують йоду тільки 50-80 мкг/добу, оптимальна доза для вагітних становить 200 мкг оригінальних пігулок йодиду калію, які вживають щодня одноразово після прийому їжі у зручний час. Препарат рекомендований до застосування протягом усієї вагітності, періоду грудного вигодовування і за рік до запланованого зачаття. При цьому бажано здійснювати періодичний (кожні 4-6 міс) контроль тиреоїдних показників (ТТГ і тиреоглобуліну, іноді АТПО). На 4-му місяці внутрішньоутробного розвитку у плода починає функціонувати власна ЩПЗ, яка активно поглинає спожитий матір’ю йод і синтезує необхідну організму кількість тиреоїдних гормонів. Тому ефективність їх синтезу залежить від щоденного надходження йоду до материнського організму.
Під час I триместру вагітності материнські гормони ЩПЗ проникають через плаценту. До розвитку власної функціонуючої ЩПЗ вони – основне джерело цих важливих гормонів для плода і можуть становити 20-40% у його крові при народженні [6-7]. Низькі рівні гормонів ЩПЗ протягом ембріонального розвитку і раннього дитинства зумовлюють незворотні ураження головного мозку, зокрема приводять до розумової відсталості та неврологічних порушень. Метааналіз 18 досліджень показав, що йодний дефіцит (від помірного до тяжкого) пов’язаний зі зниженням середнього коефіцієнта інтелекту (IQ) на 13,5 балів.
 Велика поширеність серед населення клінічно важливої ендокринної патології в зоні йодного дефіциту або екологічного ризику, яка може перешкоджати зачаттю, нормальному розвитку вагітності і пологів, впливати на потомство в найближчому і віддаленому періоді після народження, зумовлює необхідність у виділенні деяких скринінгових гормональних маркерів, тобто таких, які є ефективними в більшості випадків та економічно доцільними (за критерієм «ціна – якість»). Скринінг-тести для їх визначення необхідно проводити усім – і здоровим, і хворим із будь-якою супутньою патологією. До таких маркерів належать глюкоза плазми крові натще і ТТГ. Додатковими, але не менш інформативними методами є визначення концентрації тиреоглобуліну у крові та проведення ультразвукової діагностики ЩПЗ.
Велика поширеність серед населення клінічно важливої ендокринної патології в зоні йодного дефіциту або екологічного ризику, яка може перешкоджати зачаттю, нормальному розвитку вагітності і пологів, впливати на потомство в найближчому і віддаленому періоді після народження, зумовлює необхідність у виділенні деяких скринінгових гормональних маркерів, тобто таких, які є ефективними в більшості випадків та економічно доцільними (за критерієм «ціна – якість»). Скринінг-тести для їх визначення необхідно проводити усім – і здоровим, і хворим із будь-якою супутньою патологією. До таких маркерів належать глюкоза плазми крові натще і ТТГ. Додатковими, але не менш інформативними методами є визначення концентрації тиреоглобуліну у крові та проведення ультразвукової діагностики ЩПЗ.
У кожної жінки, котра планує вагітність, стає на облік із приводу вагітності, у якої безпліддя, планує екстракорпоральне запліднення, стався викидень, слід з’ясувати рівні глюкози плазми крові і ТТГ. У 80-90% жінок в Україні виявляють підвищену концентрацію тиреоглобуліну (≥10 нг/мл) [5-7], що свідчить про значну поширеність йодного дефіциту та пов’язаних із ним ризиків.
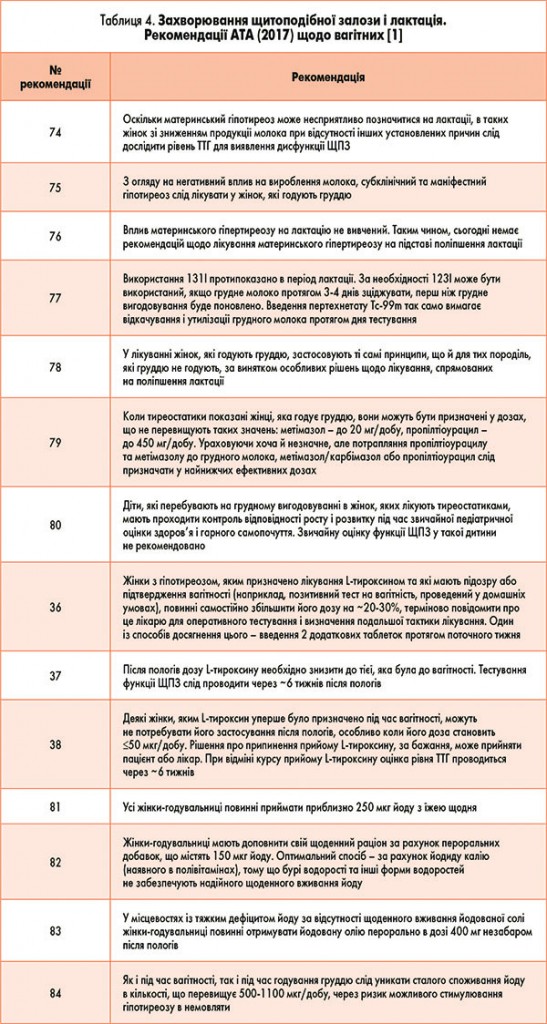
Досвід багатьох країн світу показує, що найбільш ефективним способом вирішення проблеми йодного дефіциту є проведення адекватної масової, групової та індивідуальної профілактики. Згідно з ВООЗ всі йододефіцитні захворювання можна попередити, на відміну від змін, зумовлених нестачею йоду на етапі внутрішньоутробного розвитку і в ранньому дитячому віці. Такі зміни є незворотними і майже невиліковними. Тому такі групи населення, передусім групи максимального ризику – жінки у період вагітності та діти на грудному вигодовуванні, потребують особливої уваги. У 2017 р. АТА оновила свої рекомендації щодо ведення вагітних [1]. Деякі принципові позиції цих рекомендацій наведено нижче (табл. 4).
 Недостатній вміст йоду в ґрунтах регіонів, віддалених від моря, гористих областей і місцевостей із частими повенями, низки берегових регіонів зумовлює його дефіцит у вирощуваній продукції. Поступове зменшення кількості йоду відбувається протягом тисячоліть через виморожування, комбіновану дію снігу, води та злив, які вимивають його з ґрунту. На додачу на вміст йоду у продуктах харчування впливають суміші, які використовують у іригації, виробництві добрив і вигодівлі худоби. Натомість йодофори, які застосовують для очищення каністр з-під молока і сосків корів у молочній промисловості, навпаки, можуть збільшити вміст йоду у такій продукції. Традиційно головні дієтичні джерела йоду в США, Європі та Австралії – хліб, молоко і морепродукти.
Недостатній вміст йоду в ґрунтах регіонів, віддалених від моря, гористих областей і місцевостей із частими повенями, низки берегових регіонів зумовлює його дефіцит у вирощуваній продукції. Поступове зменшення кількості йоду відбувається протягом тисячоліть через виморожування, комбіновану дію снігу, води та злив, які вимивають його з ґрунту. На додачу на вміст йоду у продуктах харчування впливають суміші, які використовують у іригації, виробництві добрив і вигодівлі худоби. Натомість йодофори, які застосовують для очищення каністр з-під молока і сосків корів у молочній промисловості, навпаки, можуть збільшити вміст йоду у такій продукції. Традиційно головні дієтичні джерела йоду в США, Європі та Австралії – хліб, молоко і морепродукти.
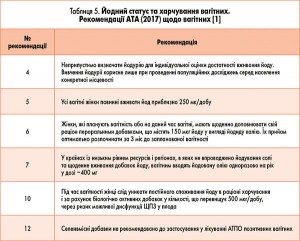
За визначенням ВООЗ, йодування – це найбільш дешевий та ефективний спосіб запобігання розвитку йододефіцитних захворювань. Йодний дефіцит не можна подолати раз і назавжди. Йодну профілактику слід здійснювати постійно, оскільки її проводять на території, якій притаманна нестача йоду в ґрунті та воді. У чинних регламентуючих документах наголошено, що для населення тієї місцевості, де існує дефіцит мікронутрієнтів, йодна профілактика має бути безперервною, щодобовою. Для вагітних єдиний спосіб надійного надходження йоду до організму – це прийом оригінального препарату йодиду калію у дозі 200 мкг/добу щоденно.
Висновки
- Порушення, зумовлені дефіцитом йоду в людському організмі, можуть з’явитися в будь-якому віці, але їм можна запобігти шляхом вживання йоду у фізіологічній кількості (для дорослих – приблизно 150 мкг/добу). У зоні йодного дефіциту (Україна – Європа) цього можна досягти лише за рахунок профілактичного прийому пігулок оригінального препарату калію йодиду в дозі 200 мкг/добу впродовж тривалого часу.
- Найбільш вразливі категорії, які є дуже чутливими до нестачі йоду, – це плід, діти та підлітки, вагітні та жінки, які годують груддю. Всім жінкам із першого дня вагітності та жінкам-годувальницям рекомендовано щодня приймати 200 мкг/добу оригінального препарату калію йодиду.
- Поширеність серед безплідних і вагітних жінок субклінічного гіпотиреозу, пов’язаного з йодним дефіцитом або аутоімунним тиреоїдитом, зумовлює порушення репродуктивної функції, зростання кількості спонтанних абортів, мертвонароджень, вроджених вад, підвищення перинатальної смертності, розвиток шизофренії, що реалізується у дорослому віці (приріст +75%), зниження інтелекту, а тому потребує своєчасного виявлення шляхом скринінгу ТТГ та застосування препаратів L-тироксину в індивідуальних дозах, що дозволяє утримувати рівень ТТГ нижче 2,5 мМОд/л.
Література
- Alexander E.K., Pearce E.N., Brent G.A. et al. 2017 Guidelines of the American Thyroid Association for the Diagnosis and Management of Thyroid Disease during Pregnancy and the Postpartum // http://online.liebertpub.com/doi/pdfplus/10.1089/thy.2016.0457
- Iodine Global Network (formerly ICCIDD Global Network) 2017. Global iodine scorecard and map, 2016 // http://www.ign.org/scorecard.htm
- Zimmermann M.B. Iodine deficiency in industrialised countries // Proc Nutr Soc. – 2009. – № 8. – P. 1-11.
- Bernal J. Thyroid Hormones in Brain Development and Function // Endotext [Internet], 2015 // http://www.ncbi.nlm.nih.gov/books/NBK285549
- Стандарти надання медичної допомоги хворим з патологічними станами щитоподібної залози в умовах дії негативних чинників довкілля / 2-ге вид., доп.; За ред. О.В. Камінського. – К.: Старт‑98, 2015. – 224 с.
- Rohner F., Zimmermann M., Jooste P. et al. Biomarkers of Nutrition for Development Iodine. Review // J Nutr. – 2014. – Vol. 144 (8). – H. 1322S‑1342S.
- Assessment of the Iodine Deficiency Disorders and monitoring their elemination: a gide for programme managers, 3rd ed. / WHO. – Geneva, 2007. – P. 1-98.
Тематичний номер «Гінекологія, Акушерство, Репродуктологія» № 1 (25), березень 2017 р.