7 червня, 2017
Ефективність та безпечність застосування препарату Метамакс у клінічній практиці
Ішемічна хвороба серця (ІХС) належить до числа найпоширеніших захворювань в економічно розвинених країнах. Серед усіх причин смертності населення також домінують хвороби серцево-судинної системи, де основною є частка ІХС. Вважають, що визначення реальної поширеності всіх форм ІХС становить певні труднощі через мультисимптомність захворювання. Однак абсолютно чітко відомо, що поширеність ІХС збільшується з віком. Її найпоширенішою формою вважають стабільну хворобу коронарних артерій. Згідно з офіційними даними, опублікованими у 2016 році, захворюваність на ІХС (усі форми) в нашій країні становить ~2% на рік. При цьому поширеність сягає ~24% дорослого населення.
Традиційно лікування стабільної хвороби коронарних артерій передбачає два напрями – вплив на прогноз захворювання та модифікація симптомів. До першої групи належить обов’язкова модифікація всіх факторів ризику та призначення медикаментів, які довели свій вплив на прогноз при лікуванні пацієнтів зі стабільною ІХС. Інші препарати використовують для зменшення проявів хвороби та покращення якості життя пацієнтів. Хоча слід зауважити, що в практичній медицині, принаймні в нашій країні, дуже рідко трапляються пацієнти лише зі стабільною хворобою коронарних артерій, без наявного ускладнення у вигляді серцевої недостатності (СН) або без супутньої патології. Насамперед це поєднання ІХС з артеріальною гіпертензією (АГ): за статистикою, в Україні таких хворих більш як 50%. Тому, обираючи лікування, необхідно раціонально комбінувати препарати з огляду на всі ланки патогенезу.
Відповідно до настанови з лікування ІХС оптимальна медикаментозна терапія має складатись як мінімум з одного препарату для зменшення симптомів стенокардії/ішемії плюс препарати для запобігання кардіальним подіям. Серед препаратів, що впливають на симптоми, останнім часом увагу знову привертають лікарські засоби метаболічної дії. Цей напрям лікування завжди був дискутабельним, але він знову й знову привертає до себе увагу. Впливаючи на ранні ланки патогенезу розвитку ІХС, ці препарати мають істотний вплив на перебіг захворювання.
Метаболічна терапія дає можливість кардіоміоцитам існувати в умовах ішемії. За достатнього надходження кисню до клітин найважливішим субстратом енергетичного метаболізму є жирні кислоти (ЖК). Вони надходять у цитозоль і мітохондрії завдяки переноснику L-карнітину. Далі, в результаті β-окислення ЖК утворюється ацетил-коензим А, який долучається до циклу Кребса, де й синтезується аденозинтрифосфат (АТФ). В умовах ішемії включається альтернативний синтезу АТФ анаеробний гліколіз. Але накопичення недоокислених метаболітів ЖК (ацилкарнітину й ацил-коензиму А) призводить до блокади транспорту вже синтезованого АТФ із мітохондрій у цитозоль, що, власне, і є причиною загибелі клітини.
Наявні метаболічні препарати впливають на різні етапи порушення синтезу АТФ в умовах ішемії. Одна група (триметазидин) частково пригнічує окислення ЖК завдяки iнгiбуванню довголанцюгової 3-кетоацил-КоА-тiолази (3-КАТ). Друга група препаратів (L-карнітин) посилює окислення вуглеводів у циклі Кребса та стимулює піруватдегідрогеназу. І, зрештою, один із сучасних напрямів метаболічної терапії – це зворотне пригнічення гамма-бутиробетаїнгідроксилази, зниження біосинтезу карнітину й у такий спосіб зупинка транспорту довголанцюгових ЖК крізь мембрану мітохондрій. Ці властивості притаманні мельдонію. Разом із тим мельдоній активізує NO-синтетазу, внаслідок чого зменшується периферичний опір судин та покращуються реологічні властивості крові. Тому раціональним підходом до корекції метаболічного стану є саме обмеження надходження ЖК до місця їх окислення, і найкращим підходом до вирішення цієї проблеми є блокування механізму переносу ЖК у мітохондрії.
Зважаючи на різні підходи до призначення препаратів, що впливають на симптоми ІХС, ми вирішили провести дослідження з використанням вітчизняного препарату Метамакс (мельдоній) у лікуванні пацієнтів з ІХС.
Мета дослідження – оцінити ефективність і переносимість препарату Метамакс при лікуванні пацієнтів зі стабільною хворобою коронарних артерій.
Об’єкт і методи дослідження
Було обстежено 60 пацієнтів середнього віку 58,2±1,4 року з верифікованим діагнозом ІХС, стабільної стенокардії ІІ-ІІІ функціонального класу (ФК) за класифікацією Канадської кардіологічної асоціації (Canadian Cardiovascular Society – CCS), які проходили лікування на клінічній базі Української військово-медичної академії. Контрольну групу становили 30 пацієнтів з аналогічним діагнозом, зіставні за віком і статтю, які не отримували додатково до базової терапії препарат Метамакс.
Критеріями включення пацієнтів у дослідження були, крім верифікованого діагнозу, наявність не менш як п’яти нападів стенокардії (що потребують прийому нітрогліцерину протягом тижня) та погіршення самопочуття. З дослідження виключали пацієнтів із нестабільними станами (специфічні зміни на електрокардіограмі – ЕКГ, біохімічні маркери ушкодження міокарда) та наявністю ознак вираженої СН.
Усі пацієнти були обстежені згідно з протоколом курації хворих на стабільну ІХС (Наказ МОЗ України від 02.03.2016 № 152).
Лабораторні дослідження включали загальний аналіз крові та сечі, а також визначення біохімічних показників (аспартатамінотрансфераза – АсТ, аланінамінотрансфераза – АлТ, глюкоза, білірубін, лужна фосфатаза – ЛФ, гамма-глутамілтранспептидаза – ГГТП, креатинін із підрахунком швидкості клубочкової фільтрації за формулою ЕРІ, ліпідограма). Додатково до обов’язкових інструментальних методів обстеження всім учасникам дослідження виконували добове моніторування ЕКГ (НТО «БЕТА», РИТМ‑2000).
Хворі були розподілені на дві групи. Пацієнтам першої групи (n=30) призначали повноцінну стандартну медикаментозну терапію (відповідно до настанови з лікування ІХС 2016 року), що включала в себе ацетилсаліцилову кислоту, статини, блокатори β-адренорецепторів і за показаннями інгібітори ангіотензинперетворювального ферменту. Другу групу (n=30) становили хворі на ІХС, яким до базової терапії додавали мельдоній (Метамакс).
У дослідження не включали хворих, котрі приймали (та продовжували приймати) інші метаболічні препарати (триметазидин, ранолазин, тіотриазолін, L-аргінін, L-карнітин). Пацієнти були поінформовані про проведення дослідження. Усі учасники підписали письмову згоду на призначення додаткового лікування та оброблення й оприлюднення результатів, отриманих у ході дослідження. Тривалість лікування становила 4 тиж.
Було проведено ступеневу терапію мельдонієм. Спершу мельдоній (Метамакс) застосовували внутрішньовенно в дозі 1000 мг 1 раз на добу протягом 14 днів із переходом на пероральний прийом у дозі 500 мг 2 рази на добу.
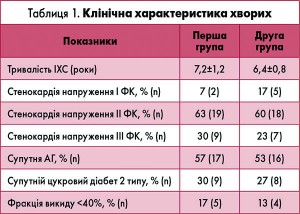
Показники клінічних характеристик хворих відображено в таблиці 1.
На початку та наприкінці проведення терапії оцінювали такі параметри: максимальна відстань, яку може пройти пацієнт до розвитку нападу стенокардії, кількість нападів стенокардії та потреба в прийомі нітрогліцерину, частота епізодів ішемії (больових і безбольових), сумарна тривалість епізодів депресії сегмента ST >1 мм, зафіксованих під час добового моніторування ЕКГ. Ураховували також показники ехокардіографії (фракцію викиду лівого шлуночка).
Переносимість препарату оцінювали як за суб’єктивними даними, так і за об’єктивними показниками.
Статистичну обробку даних проводили з використанням програм Statistica 6.0 та Microsoft Excel 2003.
Результати та їх обговорення
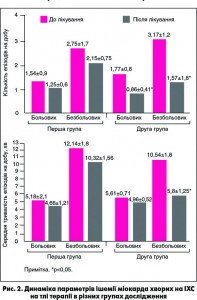
У результаті проведеного лікування в обох групах відзначали покращення як суб’єктивного стану, так і показників об’єктивного стану обстежуваних пацієнтів. Зменшилися загальна кількість нападів стенокардії та кількість нападів, які потребували прийому нітрогліцерину. Всі зміни клінічного перебігу підтверджувалися покращенням результатів дослідження. Проте результативність лікування різнилася залежно від призначеної терапії. Клінічно значущий результат лікування відзначали у 48 і 73% пацієнтів першої та другої групи відповідно. Так, у групі пацієнтів, які отримували додатково Метамакс, істотно зменшилася частота нападів стенокардії на тиждень: цей показник становив 7,1±1,3 до лікування та 3,8±0,9 після терапії (р<0,05), у першій (контрольній) групі – 6,2±0,9 та 4,9±1,8 відповідно. Скоротилася й потреба в прийомі нітрогліцерину. В групі хворих, що додатково приймали Метамакс, після проведеної терапії призначали 1,7±1,2 таблетки нітрогліцерину на тиждень, а в групі порівняння – 3,86±1,6 (рис. 1).
У ході аналізу даних добового моніторування ЕКГ було отримано такі результати.
У пацієнтів, котрі отримували додатково до базової терапії Метамакс, як кількість, так і тривалість епізодів ішемії істотно відрізнялися від хворих, що отримували лише базову терапію. Особливо це стосувалося епізодів безбольової ішемії (рис. 2).
Збільшення або зникнення депресії сегмента ST відзначали у другій групі у 56% пацієнтів та в контрольній групі – у 48%.
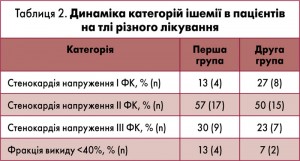
Істотне зменшення проявів ішемії в пацієнтів, які приймали Метамакс, відобразилося в зміні структури ФК серед обстежуваних хворих. Не виявлено змін щодо кількості пацієнтів, які належали до ІІІ ФК, а серед інших отримано позитивну динаміку. Так, у результаті застосування препарату Метамакс у групі стенокардії ІІ ФК відзначено зменшення кількості пацієнтів із 60 до 50%, тоді як у групі порівняння цей показник становив 63% до лікування та 57% – після (табл. 2).
Принципове зменшення ішемії міокарда в разі застосування препарату Метамакс привело до вираженіших позитивних змін систолічної функції лівого шлуночка.
Отже, наше дослідження вкотре підтвердило ефективність препарату Метамакс у лікуванні пацієнтів з ІХС.
Терапія препаратом Метамакс характеризувалася хорошою переносимістю, випадків виникнення побічних реакцій та відмови пацієнтів від лікування не зареєстровано.
Висновки
1. Терапія препаратом Метамакс у хворих на ІХС супроводжується додатковим антиангінальним та антиішемічним ефектами.
2. Додавання препарату Метамакс до базової терапії зумовлює швидше покращення клінічного стану та істотно підвищує ефективність базової терапії.
3. Призначати Метамакс доцільно на ранніх стадіях ІХС як для підвищення ефективності основної терапії, так і для гальмування прогресування захворювання.
4. Метамакс поєднує в собі основні вимоги до сучасних препаратів – ефективність та безпечність.