15 березня, 2017
Многофакторная профилактика атеросклероза и его осложнений: от выбора гиполипидемической терапии до контроля метаболических рисков

23 ноября 2016 г. в рамках X ежегодного заседания Украинского общества атеросклероза «Многофакторная профилактика атеросклероза и его осложнений» ведущие специалисты в области кардиологии, эндокринологии и других дисциплин обсуждали различные аспекты первичной и вторичной профилактики сердечно-сосудистых заболеваний (ССЗ), выявления и контроля множественных факторов риска – от артериальной гипертензии (АГ) до нарушений функции щитовидной железы (ЩЖ).
 Руководитель отдела дислипидемий ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, доктор медицинских наук, профессор Елена Ивановна Митченко охарактеризовала проблему семейной гиперхолестеринемии (СГХ) в мире и в Украине в частности.
Руководитель отдела дислипидемий ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, доктор медицинских наук, профессор Елена Ивановна Митченко охарактеризовала проблему семейной гиперхолестеринемии (СГХ) в мире и в Украине в частности.
СГХ – самое распространенное аутосомнодоминантное наследственное заболевание человека, вызванное нарушением функции генов рецепторов к липопротеинам низкой плотности (ЛПНП), которые удаляют частицы ЛПНП из крови. В результате уровень холестерина ЛПНП значительно повышается с рождения. СГХ ускоряет развитие атеросклероза и связанных с ним ССЗ, в первую очередь преждевременной ишемической болезни сердца (ИБС). Подсчитано, что из всех случаев ИБС в возрасте <60 лет 5% приходится на лиц с СГХ, несмотря на то что ее распространенность в общей популяции составляет ≤0,5% (J.L. Goldstein et al., 2009).
В 2016 г. Европейское общество по изучению атеросклероза и Европейское общество кардиологов для привлечения внимания общественности, специалистов и спонсоров к данной проблеме объявили с 19 по 25 сентября Неделю семейной гиперхолестеринемии. Многие люди даже не подозревают о своем заболевании и вследствие отсутствия своевременной диагностики рано становятся инвалидами или погибают от преждевременного инфаркта. Эксперты заявляют о необходимости внедрения национальных скрининговых программ и создании реестров пациентов с СГХ для определения потребности в ресурсах здравоохранения и поиска способов эффективного лечения. При этом ожидается существенный экономический эффект от профилактики ранней ИБС.
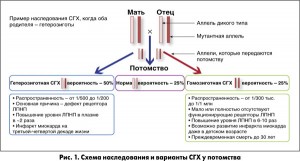
СГХ характеризуется менделевским типом наследования и может быть гетерозиготной и гомозиготной. Эти две формы существенно различаются по распространенности в популяции и по прогнозу для жизни (рис. 1).
Основными методами диагностики СГХ являются лабораторный и клинико-анамнестический. Генетическое тестирование пока не получило широкого распространения. Наследственный характер гиперхолестеринемии следует заподозрить при значениях общего холестерина плазмы ≥8 ммоль/л у взрослых пациентов и ≥6 ммоль/л у детей. В семейном анамнезе у таких пациентов можно выявить родственников с преждевременным развитием ИБС и инфаркта миокарда. Преждевременной считается ИБС в возрасте <55 лет у мужчин и <60 лет у женщин. Гетерозиготная СГХ, как правило, не имеет ярких клинических проявлений, в то время как для носителей гомозиготной формы заболевания характерны сверхвысокие уровни холестерина (18-31 ммоль/л) и внешние признаки липидных отложений в периферических тканях в виде туберозных и сухожильных ксантом, липоидной дуги роговицы.
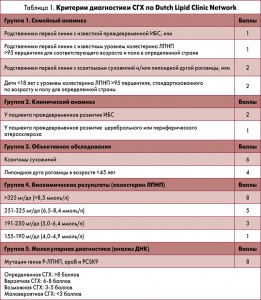
Разными группами экспертов разработаны диагностические критерии СГХ. Критерии Голландских липидных клиник (Dutch Lipid Clinic Network) приняты в последних европейских рекомендациях по ведению пациентов с дислипидемиями (ESC/EAS, 2016), а также Ассоциацией кардиологов Украины (табл. 1).
Также широко применяются более простые диагностические критерии Simon Broome. Основной критерий – уровни холестерина ЛПНП и общего холестерина крови (табл. 2).
При превышении указанных пределов следует уделить внимание сбору семейного анамнеза и поиску внешних проявлений гиперхолестеринемии.
Критерии определенной СГХ:
– ксантомы сухожилий или сведения об их наличии у родственников первой или второй степени родства
или
– мутация гена рецептора к холестерину ЛПНП, семейный дефект гена аполипопротеина B или мутация гена PCSK9 по данным анализа ДНК.
Критерии возможной СГХ:
– инфаркт миокарда в семейном анамнезе у родственника второй степени родства в возрасте <50 лет или у родственника первой степени родства в возрасте <60 лет
или
– повышение концентрации общего холестерина в семейном анамнезе >7,5 ммоль/л у взрослых родственников первой или второй степени родства; >6,7 ммоль/л у детей или подростков в возрасте <16 лет.
Эпидемиология СГХ в Украине специально не изучалась. Исследование распространенности факторов сердечно-сосудистого риска в городской популяции, проведенное в г. Днепр, выявило 81 случай повышения уровня холестерина ЛПНП ≥5 ммоль/л на 1000 населения.
Исходя из общей численности населения (45 млн 553 тыс. жителей по состоянию на 1 января 2013 г.) и данных о распространенности СГХ в мире, можно рассчитать, что в нашей стране – 46 больных с гомозиготной СГХ и около 120 тыс. с гетерозиготной формой СГХ. Однако, учитывая данные упомянутого выше популяционного исследования, в Украине может быть более 2 млн лиц с СГХ.
Специфическое лечение СГХ в настоящее время активно разрабатывается. Принципы помощи пациентам с высоким уровнем холестерина или установленным диагнозом СГХ заключаются в последовательном наращивании гиполипидемической терапии статинами и другими доступными липидоснижающими препаратами для достижения и поддержания целевых уровней холестерина ЛПНП: <2,5 ммоль/л – для взрослых, <3,5 ммоль/л – для детей, <1,8 ммоль/л – при наличии ССЗ.
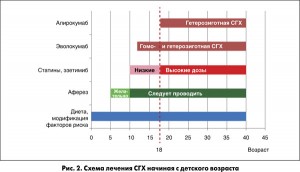
Важно начинать лечение сразу после постановки диагноза, в идеале – с детства (рис. 2). Базовыми составляющими являются диета и терапия статинами в максимально переносимых дозах. В случае необходимости могут быть назначены эзетимиб, фибраты, никотиновая кислота. Плазмаферез для удаления из крови ЛПНП следует начинать с 5-летнего возраста, но не позднее 8 лет. Процедуры проводятся каждые 1 или 2 нед.
Новые перспективы фармакотерапии тесно связаны с исследованиями и внедрением ингибиторов PCSK9. Их механизм действия отличается от механизма действия статинов. Ингибирование пропротеиновой конвертазы субтилизин-кексинового типа 9 (PCSK9) предотвращает разрушение рецепторов к ЛПНП. В настоящее время продолжаются клинические испытания двух представителей нового класса: алирокумаба и эволокумаба. В Украине эти препараты еще не зарегистрированы.
В связи с резистентностью к терапии и негативным влиянием на прогноз всех пациентов с подозрением на наследственную гиперхолестеринемию следует направлять в экспертно-консультативный центр для подтверждения диагноза и индивидуального подбора лечения. Единственный такой в Украине центр функционирует на базе отдела дислипидемий ННЦ «Институт кардиологии им. Н.Д. Стражеско».
 Член-корреспондент НАМН Украины, руководитель отдела реанимации и интенсивной терапии ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, доктор медицинских наук, профессор Александр Николаевич Пархоменко актуализировал проблему СГХ у пациентов с острым коронарным синдромом (ОКС).
Член-корреспондент НАМН Украины, руководитель отдела реанимации и интенсивной терапии ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, доктор медицинских наук, профессор Александр Николаевич Пархоменко актуализировал проблему СГХ у пациентов с острым коронарным синдромом (ОКС).
ОКС становится первым клиническим проявлением у многих пациентов с СГХ, которые не знают о своем заболевании. Сведения о встречаемости СГХ в этой группе больных немногочисленны, показатели варьируют в широких пределах, в зависимости от применявшихся критериев диагностики СГХ.
В исследовании EUROASPIRE IV при анализе популяции 7044 пациентов с ИБС из разных европейских стран были получены следующие показатели распространенности СГХ по критериям Dutch Lipid Clinic Network: вероятная (определенная) СГХ – 8,3%, возможная СГХ – 31,6%. Согласно данным многоцентрового когортного исследования, проведенного в Швейцарии (D. Nanchen et al., 2015), среди 4778 пациентов с ОКС из четырех университетских клиник распространенность СГХ составила от 1,6% (вероятная/определенная) до 17,8% (возможная). Когда в анализ включили только 1451 пациента с преждевременным ОКС (у мужчин <55 лет и у женщин <60 лет), то по тем же критериям были получены показатели 4,8 и 47,1% соответственно.
Лектор также привел данные наблюдений в клинике Института кардиологии им. Н.Д. Стражеско, согласно которым гетерозиготная форма СГХ выявляется ориентировочно у 6% больных ОКС. Около 50% пациентов с ОКС в возрасте до 60 лет имеют на момент поступления нормальный уровень холестерина.
Дальнейший анализ результатов швейцарского исследования предоставил ценную информацию о клинической роли СГХ и возможностях лечения. Так, у пациентов, которые принимали (n=1425) и не принимали статины (n=3353) на момент госпитализации по поводу ОКС, выявляемость СГХ существенно не различалась. Поскольку основным критерием диагностики СГХ является повышенный уровень холестерина, это свидетельствует о том, что даже терапия статинами не всегда обеспечивает нормализацию липидного профиля у пациентов с СГХ.
Дальнейшее медикаментозное и инвазивное лечение ОКС также не различалось в зависимости от того, сколько баллов набирали пациенты по датским критериям СГХ или шкале Simon Broome. Высокие дозы статинов назначали в 70-78% случаев.
Липидный профиль пациентов повторно анализировали через год после ОКС. У пациентов с вероятной/определенной СГХ согласно критериям Dutch Lipid Clinic Network (>5 баллов) целевой уровень холестерина ЛПНП <1,8 ммоль/л достигался только в 4,6% случаев. У пациентов с промежуточными оценками 3-5 баллов (возможная СГХ) данный целевой уровень был достигнут в 22,4% случаев. Действительно, наследственные формы гиперхолестеринемии ставят перед врачами сложную терапевтическую задачу, доступные средства фармакотерапии не дают возможности так быстро снизить уровень холестерина ЛПНП в 3 раза при исходных 6 ммоль/л и выше.
А.Н. Пархоменко обратил внимание на то, что через год после перенесенного ОКС только 10% пациентов прекратили принимать высокие дозы статинов. С учетом того, что эти данные получены в условиях реальной практики, следует констатировать высокую приверженность к гиполипидемической терапии. Трансформируется ли это в улучшение прогноза?
В 2016 г. эта же группа авторов опубликована данные о частоте повторных коронарных и сердечно-сосудистых событий у 1369 пациентов с преждевременной ИБС, которых продолжали наблюдать. Было установлено, что даже на фоне интенсивной липидоснижающей терапии частота повторных инфарктов и инсультов была в 2-3 раза выше у пациентов, у которых диагностировали СГХ, по сравнению с больными, которые не отвечали критериям СГХ. Различия между указанными подгруппами по частоте повторных событий начинали проявляться в первые 2-3 мес после первичного ОКС. «Это говорит о том, что у нас есть некоторое время на подбор липидоснижающей терапии у пациентов с СГХ. Мы обязаны с первых суток в стационаре назначить таким пациентам высокие дозы статинов, а в первые 2 мес проконтролировать их эффективность», – заключил А.Н. Пархоменко. Возможно, пациенты с СГХ нуждаются и в оптимизации антитромбоцитарной терапии, однако это предмет будущих исследований.
Основываясь на результатах швейцарского исследования, можно сделать важные выводы для практики:
1. При использовании клинических критериев диагностики СГХ, предлагаемых различными группами экспертов, распространенность СГХ среди пациентов с ОКС достигает 5-6%.
2. Несмотря на то что почти всем пациентам с СГХ при выписке были назначены статины (в основном высокие дозы), немногие достигали рекомендованных целевых уровней холестерина ЛПНП через год после ОКС.
3. У пациентов с СГХ риск развития повторного коронарного события в течение первого года после ОКС в среднем в 2 раза выше, чем у пациентов без СГХ.
4. Уровень холестерина ЛПНП следует определять с первых суток пребывания больного в стационаре, кроме того, внедрять систематический скрининг на СГХ у пациентов с ОКС. Надлежащее выявление пациентов с СГХ после ОКС необходимо для индивидуализации подходов к лечению гиперхолестеринемии и вторичной профилактики сердечно-сосудистых катастроф. Это означает необходимость подбора статинов, обеспечивающих максимальный липидоснижающий эффект, и проведение соответствующей мотивационной работы с пациентами. В настоящее время продолжаются исследования новых липидоснижающих препаратов, которые, возможно, позволят быстрее достигать целевых уровней липидов у пациентов с СГХ.
В рамках конференции состоялось секционное заседание «Сахарный диабет и дисфункция щитовидной железы – эндокринные предикторы манифестации атеросклероза»
 Доктор медицинских наук, профессор кафедры клинической иммунологии, аллергологии и эндокринологии Буковинского государственного медицинского университета, заведующий отделом профилактики эндокринных заболеваний Украинского научно-практического центра эндокринной хирургии, трансплантации эндокринных органов и тканей МЗ Украины Владимир Иванович Панькив напомнил о сочетанных кардиометаболических рисках при коморбидности ССЗ, сахарного диабета (СД) и заболеваний ЩЖ. Специалист отметил, что для нынешней эпидемиологической ситуации в Украине характерно сочетание ССЗ, СД 2 типа, ожирения, субклинической патологии ЩЖ и состояний, связанных с дефицитом витамина D у значительной части населения. Распространенность СД 2 типа оценивается в 1,5 млн человек, а еще 4 млн не подозревают, что у них есть нарушения углеводного метаболизма. У 40% женщин в возрасте 20-65 лет и у 36% мужчин имеется инсулинорезистентность – универсальный фактор риска для ССЗ и метаболических расстройств. Вся территория Украины относится к йододефицитным регионам, что обусловливает высокую встречаемость заболеваний ЩЖ. Распространенность гипотиреоза в популяции – от 0,1 до 15% (выше у женщин старшего возраста). Среди пациентов с ИБС субклинический гипотиреоз выявляют у 15% женщин и 4,3% мужчин. К этому лектор добавил, что у 93% населения Украины отмечается дефицит витамина D как фактор риска ССЗ и остеопороза.
Доктор медицинских наук, профессор кафедры клинической иммунологии, аллергологии и эндокринологии Буковинского государственного медицинского университета, заведующий отделом профилактики эндокринных заболеваний Украинского научно-практического центра эндокринной хирургии, трансплантации эндокринных органов и тканей МЗ Украины Владимир Иванович Панькив напомнил о сочетанных кардиометаболических рисках при коморбидности ССЗ, сахарного диабета (СД) и заболеваний ЩЖ. Специалист отметил, что для нынешней эпидемиологической ситуации в Украине характерно сочетание ССЗ, СД 2 типа, ожирения, субклинической патологии ЩЖ и состояний, связанных с дефицитом витамина D у значительной части населения. Распространенность СД 2 типа оценивается в 1,5 млн человек, а еще 4 млн не подозревают, что у них есть нарушения углеводного метаболизма. У 40% женщин в возрасте 20-65 лет и у 36% мужчин имеется инсулинорезистентность – универсальный фактор риска для ССЗ и метаболических расстройств. Вся территория Украины относится к йододефицитным регионам, что обусловливает высокую встречаемость заболеваний ЩЖ. Распространенность гипотиреоза в популяции – от 0,1 до 15% (выше у женщин старшего возраста). Среди пациентов с ИБС субклинический гипотиреоз выявляют у 15% женщин и 4,3% мужчин. К этому лектор добавил, что у 93% населения Украины отмечается дефицит витамина D как фактор риска ССЗ и остеопороза.
Профессор В.И. Панькив описал клинический портрет среднего украинца с СД 2 типа: возраст – 50 лет, индекс массы тела – 30 или выше, АГ 1-2 степени, дислипидемия, низкий уровень тестостерона, высокий уровень иммунореактивного инсулина, повышен уровень тиреотропного гормона (ТТГ), но при этом человек не предъявляет никаких жалоб. Действительно, как СД, так и другие метаболические расстройства длительное время протекают бессимптомно. В среднем через 7 лет от начала заболевания человек с СД попадает в поле зрения врачей. Инфаркт миокарда часто становится первым сосудистым проявлением метаболического расстройства.
Явные формы гипертиреоза и гипотиреоза также встречаются крайне редко. Чаще диагностируются субклинические формы, индикатором которых является уровень ТТГ. Диапазон нормальных концентраций ТТГ – от 0,4 до 4,0 мЕд/л (при планировании беременности – до 2,5 мЕд/л). Значения от 4,0 до 10,0 мЕд/л соответствуют субклиническому гипотиреозу, >10,0 мЕд/л указывают на манифестный гипотиреоз. Значения <0,1 мЕд/л означают подавление ТТГ, что соответствует гиперфункции ЩЖ.
Гипотиреоз вносит свой вклад в патогенез нарушений углеводно-жирового обмена, АГ, атеросклероза, ускоряя их прогрессирование, появление поражений органов-мишеней, затрудняя лечение. До 13% пациентов с дислипидемиями имеют скрытый гипотиреоз. Лечение гипотиреоза препаратами тиреоидных гормонов способствует нормализации липидного профиля и снижает риск развития сердечно-сосудистых осложнений. Поэтому профильные американские ассоциации рекомендуют проводить скрининг на гипотиреоз у всех пациентов с впервые диагностированной дислипидемией до начала липидоснижающей терапии.
Структурно-функциональные изменения сердечно-сосудистой системы при гипотиреозе носят системный характер: поражаются миокард, артерии крупного и среднего калибра, микроциркуляторное русло. Для сочетания АГ с субклиническим гипотиреозом характерно повышение пульсового артериального давления – АД (потеря эластичности артерий), нарастание вариабельности систолического и диастолического АД, нарушение суточного ритма систолического АД с увеличением доли нон-дипперов (пациентов, у которых АД не снижается ночью). Субклинический гипотиреоз снижает эффективность лечения АГ. Уровень ТТГ ≥5 мЕд/л ассоциируется с выявлением скрытой неконтролируемой АГ.
Нередко гипотиреоз сочетается с СД 2 типа, что усугубляет кардиометаболические риски. Профессор В.И. Панькив привел данные собственного исследования 115 пациентов с СД 2 типа и ожирением (72 женщины и 42 мужчины среднего возраста 57,2 года). Первую группу составили пациенты без тиреоидной дисфункции (N=55), вторую – пациенты с явным или субклиническим гипотиреозом (N=60). В обеих группах выявлена высокая распространенность АГ – 81,9 и 71,7% соответственно. У пациентов с СД и гипотиреозом по сравнению с пациентами первой группы отмечались повышенные показатели массы тела, ЛПНП, более высокая частота развития гипертриглицеридемии. Получена положительная корреляционная связь между уровнями ТТГ и триглицеридов крови.
«Вылечить гипотиреоз или СД нельзя, но можно взять под контроль кардиометаболические риски, увеличить продолжительность жизни больных и повысить ее качество», – отметил профессор В.И. Панькив. Целью лечения должны быть не цифры глюкозы, а профилактика инфарктов, инсультов и других сосудистых осложнений. Это достигается комплексной пожизненной терапией с назначением сахароснижающих, антигипертензивных препаратов, статинов и заместительной терапии L-тироксином при выявлении гипотиреоза.
 Старший научный сотрудник отдела дислипидемий ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины Вадим Юрьевич Романов более детально рассмотрел проблему кардиометаболических осложнений гипофункции ЩЖ. Связь гипотиреоза с атеросклерозом и ИБС известна более 100 лет. В классических опытах Теодора Бильрота (1829-1894) полное удаление ЩЖ у овец и коз приводило к резкому увеличению уровня холестерина и атеросклерозу артерий, в том числе коронарных.
Старший научный сотрудник отдела дислипидемий ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины Вадим Юрьевич Романов более детально рассмотрел проблему кардиометаболических осложнений гипофункции ЩЖ. Связь гипотиреоза с атеросклерозом и ИБС известна более 100 лет. В классических опытах Теодора Бильрота (1829-1894) полное удаление ЩЖ у овец и коз приводило к резкому увеличению уровня холестерина и атеросклерозу артерий, в том числе коронарных.
В общей популяции субклинический гипотиреоз можно выявить у 8% взрослого населения. Особенно часто он встречается у женщин, в возрастной группе старше 60 лет распространенность достигает 20%. Поэтому тиреоидологические ассоциации США рекомендуют рутинный скрининг функции ЩЖ начиная с 50 лет.
В роттердамском исследовании с участием 1149 женщин среднего возраста 69 лет повышенный уровень ТТГ ассоциировался с двукратным повышением частоты развития инфаркта миокарда и обнаружения кальциноза аорты по сравнению с эутиреоидными участницами. Если же высокий уровень ТТГ сопровождался наличием аутоантител к пероксидазе (аутоиммунный тиреоидит – самая частая причина гипотиреоза), то риск развития инфаркта увеличивался еще в 1,5 раза (A.E. Hak et al., 2000).
Согласно данным крупного популяционного исследования, проведенного в Тайване (эндемичный по йодному дефициту регион, более 1800 лиц с субклиническим гипотиреозом, 119 тыс. – с эутиреозом, средний возраст – 40 лет), наличие бессимптомной гипофункции ЩЖ ассоциируется с достоверным повышением общей и сердечно-сосудистой смертности (F.Y. Tseng et al., 2012).
Позже подтвердилось, что причиной худшего прогноза у лиц с гипотиреозом является ускоренное прогрессирование коронарного атеросклероза. К неожиданным выводам привел метаанализ зависимости исходов ИБС у пациентов с субклиническим гипотиреозом от возраста: оказалось, что смертность от ИБС при наличии гипотиреоза повышается на 37% у лиц 40-70 лет, а у лиц старше 70 лет риск увеличивается незначительно – на 9% (Razvi et al., 2008).
Предикторами развития и прогрессирования атеросклероза при гипотиреозе являются атерогенная дислипидемия, диастолическая гипертензия, инсулинорезистентность, эндотелиальная дисфункция, повышение жесткости артериальной стенки, повышенный уровень С-реактивного белка. Поскольку основной причиной гипотиреоза является аутоиммунный тиреоидит, в последнее время изучается вклад в патогенез ИБС и такого фактора, как аутоиммунная агрессия, ведущая к активации провоспалительных цитокинов, свертывающей системы крови. Рецепторы к ТТГ обнаружены в печени, сонных и коронарных артериях, предсердиях и желудочках сердца. По данным экспериментальных исследований, повышение уровня ТТГ может инициировать пролиферацию гладкомышечных клеток в сонных и коронарных артериях.
В.Ю. Романов представил результаты исследования, выполненного в отделе дислипидемий Института кардиологии им. Н.Д. Стражеско, которое демонстрирует, как лечение сопутствующего гипотиреоза помогает снизить общий сердечно-сосудистый риск. Из 134 женщин среднего возраста 56,8 года с гипертонической болезнью II стадии, 1-2 степени сформировали четыре группы в зависимости от тиреоидного статуса:
1) 33 женщины с впервые выявленным субклиническим гипотиреозом (средний уровень ТТГ – 5,5 мЕд/л);
2) 32 женщины с субклиническим гипотиреозом, компенсированным приемом левотироксина натрия в средней дозе 76,9 мкг/сут (средний уровень ТТГ – 2,16 мЕд/л);
3) 34 женщины с впервые выявленным манифестным гипотиреозом (средний уровень ТТГ – 10,9 мЕд/л);
4) 35 женщин без патологии ЩЖ (средний уровень ТТГ – 1,6 мЕд/л).
 Почти у 90% пациенток с впервые выявленным и манифестным гипотиреозом наблюдалась гиперхолестеринемия. Уровни общего холестерина у пациенток с субклиническим и манифестным гипотиреозом были достоверно выше, чем у женщин с эутиреоидным состоянием и тех, которые получали заместительную гормональную терапию. Корреляционный анализ выявил сильную связь между уровнем ТТГ и уровнями общего холестерина и холестерина ЛПНП. Отсюда можно сделать практический вывод, что у всех женщин с гиперхолестеринемией необходимо исследовать функцию ЩЖ.
Почти у 90% пациенток с впервые выявленным и манифестным гипотиреозом наблюдалась гиперхолестеринемия. Уровни общего холестерина у пациенток с субклиническим и манифестным гипотиреозом были достоверно выше, чем у женщин с эутиреоидным состоянием и тех, которые получали заместительную гормональную терапию. Корреляционный анализ выявил сильную связь между уровнем ТТГ и уровнями общего холестерина и холестерина ЛПНП. Отсюда можно сделать практический вывод, что у всех женщин с гиперхолестеринемией необходимо исследовать функцию ЩЖ.
Наличие как манифестного, так и субклинического гипотиреоза ассоциировалось с более частым выявлением инсулинорезистентности и эндотелиальной дисфункции, которые являются факторами риска раннего развития атеросклероза.
Инсулинорезистентность выявлена у 66,7% пациенток 1-й группы и 88,2% пациенток 2-й группы; эндотелиальная дисфункция – у 54,5 и 79,4% соответственно. Также было показано, что наличие тиреоидной недостаточности у женщин с АГ ассоциируется с более выраженной манифестацией ранних маркеров атеросклероза в виде утолщения комплекса интима-медиа общей сонной артерии и снижения лодыжечно-плечевого индекса АД.
Таким образом, у женщин с гипертонической болезнью наличие субклинического или манифестного гипотиреоза ассоциируется с признаками раннего прогрессирования атеросклеротического процесса, что свидетельствует о значительном атерогенном потенциале гипофункции ЩЖ еще на доклинической стадии и необходимости назначения терапии левотироксином или консультации эндокринолога.
Подготовил Дмитрий Молчанов