17 квітня, 2017
В-клетки как важное звено аутоиммунного воспаления и новая терапевтическая мишень при рассеянном склерозе
Рассеянный склероз (РС) – хроническое неврологическое заболевание с дебютом, как правило, в молодом возрасте, которое характеризуется воспалением в центральной нервной системе (ЦНС), демиелинизацией нервных волокон, глиозом и потерей аксонов. Аксональная дегенерация лежит в основе прогрессирующего неврологического дефицита. Наиболее характерный возраст появления первых симптомов – между 20 и 40 годами. На момент дебюта примерно у 80% пациентов диагностируют рецидивирующе-ремиттирующий РС, который со временем в 60% случаев переходит во вторично-прогрессирующий РС. У 10-15% пациентов отмечается первично-прогрессирующий РС, характеризующийся постоянным нарастанием неврологической симптоматики с самого начала заболевания. Прогноз при этом типе течения РС, как правило, носит неблагоприятный характер за счет неуклонного накопления неврологического дефицита, ведущего к стойкой инвалидизации.
Комментарий специалиста
 Заведующая кафедрой неврологии Национального медицинского университета им. А.А. Богомольца, доктор медицинских наук, профессор Лариса Ивановна Соколова
Заведующая кафедрой неврологии Национального медицинского университета им. А.А. Богомольца, доктор медицинских наук, профессор Лариса Ивановна СоколоваОбщепринятая концепция патогенеза РС рассматривает эту патологию как аутоиммунно опосредованное повреждение миелина в предрасполагающих условиях уязвимого организма. С 90-х годов прошлого века в первой линии терапии РС начали применять бета-интерфероны и глатирамера ацетат. Будучи разными по направленности иммунного воздействия – антиген-неспецифическими и антиген-специфическими соответственно, они были призваны оказывать разностороннее влияние на иммунную систему: подавление пролиферации Т-клеток и активности макрофагов, снижение уровня экспрессии молекул адгезии на эндотелиальных клетках, повышение продукции противовоспалительных цитокинов и подавление активности провоспалительных цитокинов, а также обеспечение конкуренции и замены основных нейробелков в механизмах антигенпрезентации и некоторые другие эффекты.
Вместе с тем постоянно велись поиски более избирательной терапии по мере появления новых данных о патогенезе РС. Наиболее прогрессивным оказалось создание моноклональных антител, позволяющих воздействовать на отдельные рецепторы иммунокомпетентных клеток и таким образом ограничивать их участие в иммунопатологическом процессе. За последние годы получено достаточно данных, подтверждающих возможность и необходимость воздействовать на рецепторы не только Т-лимфоцитов, но и В-лимфоцитов. Основные достижения этого направления, а также данные о роли В-лимфоцитов как важного иммунологического драйвера патогенеза РС и перспективной мишени для таргетной терапии приведены в предлагаемом обзоре.
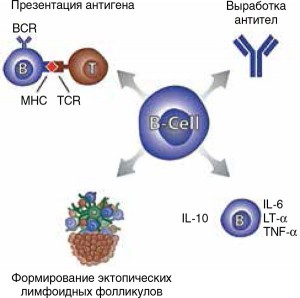
В-лимфоциты выполняют эффекторные функции в иммунной системе как антигенпредставляющие клетки: поглощают антиген путем эндоцитоза или фагоцитоза, а затем на своей поверхности презентуют его фрагменты Т-хелперам. В-клетки дифференцируются в плазмоциты, которые активно вырабатывают антитела, а также сами являются регуляторами иммунного ответа, секретируя про- и противовоспалительные цитокины, участвуют в формировании эктопических лимфоидных тканей. Все перечисленные функции В-клеток, по современным представлениям, участвуют в патогенезе РС (рис. 1).
Исторически при изучении патофизиологии РС внимание исследователей было сфокусировано преимущественно на Т-лимфоцитах. Их роль обосновывалась тем, что в эксперименте заболевание можно было вызвать путем переноса активированных Т-клеток от больной мыши к здоровой. Поэтому и поиски специфического лечения изначально основывались на контроле популяций Т-клеток. Однако модель экспериментального аутоиммунного энцефалита на мышах не могла объяснить прогрессирующий характер заболевания. Вместе с тем уже несколько десятилетий было известно, что присутствие в цереброспинальной жидкости (ЦСЖ) олигоклональных иммуноглобулинов, продуцируемых В-клетками и определяемых как олигоклональные линии (oligoclonal bands, ОСВ), является характерным биомаркером РС (A.G. Solimando и A. Tomasicchio, 2016). Долгое время не удавалось определить роль этих В-клеточных иммуноглобулинов в патогенезе, но они были настолько характерным феноменом при РС, что закономерно возникал вопрос: могут ли В-клетки быть новой мишенью терапии? Рассмотрим более детально роль каждой из функций В-клеток при РС.
Презентация антигенов: «свои против своих»
! Аутоиммунное воспаление при РС развивается вследствие аномальной активации и экспансии Т-клеток в ответ на антигены собственной нервной ткани, которые представляют им В-клетки.
Активация Т-клеток в ответ на презентацию чужеродных антигенов В-клетками — это нормальный процесс, лежащий в основе иммунной защиты организма. Однако при РС В-клетки начинают презентовать собственные антигены как чужеродные (S.J. Ireland et al., 2012). С конца 1990-х годов все больше исследователей признавали важную роль антигенпредставляющей функции В-клеток в запуске аутоиммунного процесса, направленного против миелин-олигодендроцитарного гликопротеина — важной молекулы, участвующей в миелинизации нервных волокон ЦНС, а также основного белка миелина (J.A. Lyons, 1999; M.S. Weber, 2010; N. Molnarfi, 2013). В экспериментах на культивированных линиях лимфоцитов только В-клетки от пациентов с РС запускали пролиферацию Т-клеток после инкубации с собственными антигенами нервной ткани. В то же время В-клетки от пациентов с РС и здоровых лиц вызывали нормальную активацию Т-лимфоцитов в ответ на чужеродные антигены, такие как вирус паротита или столбнячный токсин (C.T. Harp et al., 2010; S.J. Ireland et al., 2012).
Еще предстоит ответить на вопросы, как и почему В-клетки начинают презентовать собственные антигены нервной ткани Т-клеткам. Контроль аутоиммунного потенциала В-клеток, развивающихся в костном мозге, по-видимому, остается незатронутым у большинства пациентов с РС. Нарушаются механизмы В-клеточной толерантности, которые регулируют аутоиммунные свойства В-лимфоцитов, циркулирующих между периферическими лимфоидными тканями (H.-C. von Budingen et al., 2016). Миелин-реактивные В-клетки памяти могут обнаруживаться в периферической крови пациентов с РС (C.T. Harp et al., 2010; S.J. Ireland et al., 2012).
Шейные лимфатические узлы, возможно, являются местами поддержки ЦНС-направленной аутоиммунной агрессии у людей и мышей (K. Berer et al., 2011; J.N. Stern et al., 2014).
Выработка цитокинов — сигнальных молекул иммунного каскада
! В-клетки у пациентов с РС секретируют относительно больше провоспалительных, чем противовоспалительных цитокинов. Это приводит к аномальной активации других иммунных клеток или нарушает способность к регуляции иммунных ответов (A. Bar-Or et al., 2010; R.P. Lisak et al., 2012).
Например, установлено, что при РС В-клетки секретируют повышенные уровни интерлейкина‑6 (ИЛ‑6) по сравнению со здоровыми лицами. Вероятнее всего, повышенная продукция ИЛ‑6 связана с антиген-обученными В-клетками памяти. В-клетки памяти также эффективно поддерживают Т-клеточные иммунные механизмы: их истощение сопровождается снижением продукции ИЛ‑17 лимфоцитами периферической крови, что доказывает участие В-клеток в поддержании провоспалительного ответа Т-хелперов 17 типа (Th17) (H.-C. von Budingen et al., 2016).
Противоречивые данные получены в отношении субпопуляции В-лимфоцитов, ответственных за секрецию ИЛ‑10. В одном исследовании обнаружены ИЛ‑10-экспрессирующие В-клетки среди активированных В-клеток памяти, что подтверждает антигенспецифические регуляторные функции В-клеток. Повышенное количество ИЛ‑10-продуцирующих клеток было обнаружено у пациентов с аутоиммунным воспалением, несмотря на то что большинство больных РС в этом исследовании получали лечение иммуносупрессивными или иммуномодулирующими препаратами (Y. Iwata et al., 2011). В другом исследовании показано, что секреция ИЛ‑10 — это функция преимущественно наивных (не встречавшихся с антигенами) В-клеток и что переключение с регуляторной на провоспалительную функцию может происходить при созревании в клетки памяти (M. Duddy et al., 2006).
Продукция повреждающих аутоантител
! В-клетки сами способны вырабатывать аутоантитела, которые вызывают повреждение нервной ткани, активируют макрофаги и натуральные киллеры (M.K. Storch et al., 1998; C.P. Genain et al., 1999).
У более чем 95% пациентов с РС антитела в повышенном количестве вырабатываются в пределах ЦНС (H. Link, Y.-M. Huang, 2006). Олигоклональные антитела, продуцируемые немногочисленными мутировавшими клонами В-клеток, могут накапливаться в ЦСЖ (M. Colombo et al., 2000). Их обнаружение при исследовании ликвора подтверждает диагноз РС. Выработка аутоантител происходит в соматически гипермутированных В-клетках. Соматическая гипермутация (СГМ) — запрограммированный процесс мутаций в В-клетках, являющийся частью адаптации иммунной системы для борьбы против новых чужеродных элементов. При активации B-клетка начинает часто делиться, и при каждом делении в участок ДНК, который кодирует вариабельный регион антитела, вносятся все новые мутации (замена нуклеотидов).
B-клетки, лучше распознающие антиген, чаще активируются, и в итоге появляются B-клетки, антитела которых идеально распознают какой-то антиген. В конечном итоге B-лимфоцит становится плазматической клеткой, которая начинает производить антитела в больших количествах, а после того, как угроза миновала, становится клеткой памяти, способной произвести подходящие антитела через значительный промежуток времени. СГМ названа так потому, что возникает значительно чаще, чем соматические мутации нормального уровня (примерно в 10 тысяч раз). СГМ в норме реализуется в зародышевых центрах периферических лимфоидных органов.
На сегодняшний день патологическое значение антител при РС остается неясным. Тот факт, что при быстром ответе на анти-В-клеточную терапию уровни антител остаются практически без изменений, вызвал предположение, что антитела играют менее важную патогенетическую роль. Вместе с тем известно, что аутоантитела против ЦНС требуют благоприятной воспалительной среды или, по крайней мере, функционирующей системы комплемента, для того чтобы реализовывать свои патогенетические функции. Элиминация антител-независимых функций В-лимфоцитов (презентации антигенов, активации Т-клеток, образования медиаторов воспаления) путем истощения В-клеток, по-видимому, подавляет эффекторные механизмы воспаления в паренхиме мозга до такой степени, при которой антитела не могут вызвать существенного повреждения нервной ткани
(H.-C. von Budingen et al., 2016).
Эктопические лимфоидные фолликулы — центры аутоиммунной агрессии в ЦНС
! В-клетки могут образовывать в мозговых оболочках фолликулоподобные скопления, связанные с активацией микроглии, локальным воспалением и нейрональными потерями в близлежащей ткани коры головного мозга (B. Serafini et al., 2004; R. Magliozzi et al., 2011).
В настоящее время не только установлено, что ЦНС является мишенью аутоиммунной агрессии при РС, но также идентифицированы отделы и ткани (например, паренхима мозга, ЦСЖ, менингеальная ткань), поддерживающие созревание иммунной компетентности В-клеток (рис. 2). Анализ В-лимфоцитов, выделенных из ЦСЖ пациентов с РС, показал, что эти клетки проходят все этапы созревания и дифференцировки внутри ЦНС, что в норме происходит только в периферических лимфоидных органах (Corcione et al., 2004).
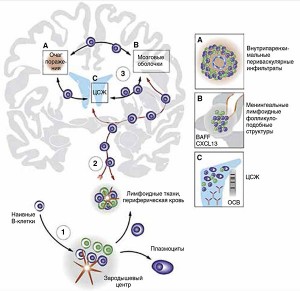 Рис. 2. В-клетки как иммунологически активное cвязующее звено между периферией и ЦНС (по H.-C. von Budingen и соавт., 2016) Наивные В-клетки выходят из костного мозга (1), проходят первоначальную антиген-тренировку и созревание в периферических зародышевых центрах и превращаются в В-клетки памяти. В-клетки памяти могут быть дополнительно стимулированы в периферических лимфоидных тканях и/или мигрируют в ЦНС (2), где участвуют в иммунологической атаке на ткани мозга (A) и менингеальные ткани, как в виде диффузно рассредоточенных клеток, так и в виде лимфоидных фолликулоподобных образований (B). ЦСЖ также вовлечена в иммунологический ответ и циркуляцию (3) зрелых В-клеток (C). Зрелые B-клетки с рецепторами, предполагающими постоянную антиген-стимуляцию, могут быть обнаружены во всех трех отделах ЦНС (очаги, мозговые оболочки, спинномозговая жидкость) и на периферии, что указывает на активацию иммунитета при РС по обе стороны гематоэнцефалического барьера. B-клетки показаны синим, Т-клетки — зеленым.
Рис. 2. В-клетки как иммунологически активное cвязующее звено между периферией и ЦНС (по H.-C. von Budingen и соавт., 2016) Наивные В-клетки выходят из костного мозга (1), проходят первоначальную антиген-тренировку и созревание в периферических зародышевых центрах и превращаются в В-клетки памяти. В-клетки памяти могут быть дополнительно стимулированы в периферических лимфоидных тканях и/или мигрируют в ЦНС (2), где участвуют в иммунологической атаке на ткани мозга (A) и менингеальные ткани, как в виде диффузно рассредоточенных клеток, так и в виде лимфоидных фолликулоподобных образований (B). ЦСЖ также вовлечена в иммунологический ответ и циркуляцию (3) зрелых В-клеток (C). Зрелые B-клетки с рецепторами, предполагающими постоянную антиген-стимуляцию, могут быть обнаружены во всех трех отделах ЦНС (очаги, мозговые оболочки, спинномозговая жидкость) и на периферии, что указывает на активацию иммунитета при РС по обе стороны гематоэнцефалического барьера. B-клетки показаны синим, Т-клетки — зеленым.В посмертных исследованиях при РС в ткани мозга были обнаружены эктопические лимфоидные фолликулоподобные структуры (третичные лимфоидные органы), состоящие преимущественно из В-лимфоцитов, сходные по структуре с периферическими лимфоидными фолликулами (Serafini et al., 2004, 2007; Magliozzi et al., 2010, 2011). Подобно вторичной лимфоидной ткани, эти структуры имеют зародышевые центры, где происходят размножение и созревание В-клеток, в том числе СГМ, пролиферация и конечная дифференцировка в антителопродуцирующие плазмоциты. Так, в исследовании R. Magliozzi и соавт.лимфоидные В-клеточные фолликулоподобные структуры обнаруживались в мозговых оболочках у 41% пациентов со вторично-прогрессирующим РС и ассоциировались с кортикальной потерей нейронов, демиелинизацией, быстрым прогрессированием неврологического дефицита, ранней инвалидизацией и смертью (рис. 3).
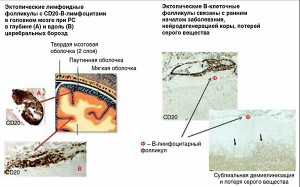 Рис. 3. Менингеальные B-клеточные фолликулы у пациентов с прогрессирующим РС ассоциируются с ранним началом заболевания и тяжелой кортикальной патологией.
Рис. 3. Менингеальные B-клеточные фолликулы у пациентов с прогрессирующим РС ассоциируются с ранним началом заболевания и тяжелой кортикальной патологией.По данным Magliozzi R. et al. Brain, 2007; 130: 1089-1104. Magliozzi R. et al. Аnn Neurol. 2010; 68: 477-493 (посмертный морфологический анализ ткани мозга пациентов с РС).
Патологическое значение этих эктопических В-клеточных фолликулов в аутоиммунной агрессии против ЦНС еще не до конца изучено. Вместе с тем присутствие CD35+ фолликулярных дендритных клеток и пролиферирующих В-лимфоцитов, а также экспрессия хемокина CXCL13, привлекающего В-клетки, и фактора, активирующего В-клетки (BAFF), дают основание утверждать, что третичные лимфоидные ткани в ЦНС при прогрессирующем РС обеспечивают активный интраменингеальный иммунный ответ. Более того, CXCL13 и BAFF также обнаруживались в очагах РС (M. Krumbholz et al., 2006), где указанные факторы могут служить медиаторами местного вовлечения В-клеток и их созревания в очагах активной демиелинизации.
Значение CD20-рецепторов для разработки таргетной терапии
В ходе созревания В-лимфоцитов на поверхности их мембран появляются специфические молекулы, называемые кластерами дифференциации. Они имеют значение для дифференциации В-клеток, передачи сигнала об антигенах, а также регуляции выработки цитокинов. Кластер дифференциации CD20 является специфическим маркером определенных субпопуляций В-клеток (P. Stashenko et al., 1980; M.R. Loken et al., 1987). Разные субпопуляции В-клеток в ходе их созревания выполняют разные функции в иммунной системе. В новых исследованиях изучается возможность селективного распознавания поверхностных маркеров, экспрессируемых на определенных этапах созревания В-лимфоцитов, для элиминации патогенных линий В-клеток при РС.
Ведущим методом лечения РС является иммуносупрессивная терапия. Современной тенденцией является переход от методов неселективной иммуносупрессии к использованию таргетных препаратов, нацеленных на определенные звенья иммунной системы. В последние годы в лечении широкого круга аутоиммунных заболеваний с успехом использовался подход, основанный на истощении пула CD20-положительных В-лимфоцитов (так называемая В-клеточная деплеция). В настоящее время изучаются возможности таргетной терапии, направленной на CD20-В-лимфоциты, в лечении РС.
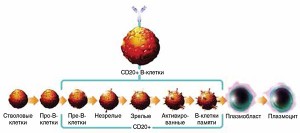
Выбор CD20 в качестве мишени для таргетной терапии связан с особенностями дифференцировки В-клеток. Рецепторы CD20 образуются только на определенных стадиях созревания В-клеток: от пре-В-клеток до зрелых В-лимфоцитов и клеток памяти (рис. 4). Стволовые, про-В- и плазматические клетки не содержат на своей поверхности CD20. Наивные В-лифоциты и В-клетки памяти играют важную роль в патогенезе РС, в то время как стволовые и прогениторные клетки необходимы для обновления всей популяции В-лимфоцитов (M.D. Pescovitz et al., 2006). Плазмоциты также являются важным компонентом гуморального иммунитета, носителями долгосрочной памяти о чужеродных антигенах (R. Warrington et al., 2011). Истощение пула В-клеток, несущих рецепторы CD20, не отменяет регенерацию В-лимфоцитов и не влияет на синтез иммуноглобулинов плазматическими клетками, что позволяет сохранить иммунологическую память.
! Таким образом, CD20-избирательная анти-В-клеточная терапия представляется эффективным подходом к подавлению аномального иммунного ответа и демиелинизирующего воспаления при РС, но при этом является безопасной для общей популяции В-лимфоцитов и не мешает реализации физиологических иммунных ответов.
Выводы и перспективы
В-клетки и продуцируемые ими иммуноглобулины, обнаруживаемые в ЦСЖ пациентов, больше не являются сугубо диагностическим маркером РС. Данные последних исследований заставляют пересмотреть значение В-клеток при данном заболевании. Становится все более очевидной их роль в иммунном воспалении и прогрессировании поражений ЦНС.
Согласно традиционной точке зрения В-клетки являются источником аутоантител, участвующих в процессе демиелинизации, а недавно была установлена их важная функция как антигенпрезентующих клеток, которые «обучают» Т-клетки, как начинать иммуновоспалительный каскад.
Иммунное воспаление, которое поддерживается в ЦНС скоплениями В-клеток, обусловливает прогрессирование заболевания и ассоциируется с худшим прогнозом.
Безусловно, не все В-клетки вовлечены в процессы разрушительного аутоиммунного воспаления при РС. Способность точно отличать патогенные В-клетки по кластеру дифференциации CD20 открывает путь к разработке целенаправленной терапии РС с улучшенным профилем эффективности и безопасности, позволит максимально приблизить ее к принципам персонализированного лечения.
Подготовил Дмитрий Молчанов
Подготовлено по заказу ООО «Рош Украина».
UA/NEUR/1704/0002