17 квітня, 2017
Эффективность десвенлафаксина в дозе 50 мг в сутки при длительном лечении большого депрессивного расстройства: рандомизированное двойное слепое исследование
Десвенлафаксин— ингибитор обратного захвата серотонина и норадреналина, одобренный в более чем 30 странах для лечения большого депрессивного расстройства (БДР) у взрослых. Несколько двойных слепых плацебо-контролируемых исследований продемонстрировали антидепрессивную эффективность десвенлафаксина в острой фазе (8 нед) в рекомендованной дозе 50 мг в сутки (P. Boyer et al., 2008; M.R. Liebowitz et al., 2008; B.W. Dunlop et al., 2011).
Долгосрочная эффективность десвенлафаксина изучалась в двойном слепом рандомизированном исследовании 3-й фазы длительностью 11 мес (J.Z. Rosenthal, P. Boyer, C. Vialet et al., 2013). Пациенты, которые ответили на терапию в ходе 8-недельной открытой фазы и у которых терапевтический эффект оставался стабильным в течение 12 дополнительных недель открытого приема десвенлафаксина в дозе 50 мг в сутки, были рандомизированы для продолжения приема препарата в такой же дозе или плацебо в течение 6 мес двойной слепой фазы. Первичным критерием эффективности служило время до рецидива. В результате частота рецидивирования за двойной слепой период исследования оказалась более чем в 2 раза выше в группе плацебо, чем в группе десвенлафаксина (30,2 против 14,3% соответственно; р<0,001).
Среди пациентов, которые отвечают на терапию депрессивного эпизода и остаются в ремиссии, многие, тем не менее, испытывают резидуальные симптомы (A.A. Nierenberg et al., 2010). Поэтому клиницисты часто задаются вопросом: как на самом деле чувствуют себя пациенты, долго находящиеся на поддерживающей терапии? Для ответа на этот вопрос в данном отчете представлены дополнительные результаты вышеупомянутого исследования венлафаксина по заранее запланированным вторичным исходам, которые не освещались в первой публикации (J.Z. Rosenthal, P. Boyer, C. Vialet et al., 2013).
Популяция исследования
В исследование включали взрослых амбулаторных пациентов 18 лет и старше с первичным диагнозом БДР или повторным эпизодом БДР без психотических проявлений согласно критериям DSM-IV. Симптомы депрессии должны были присутствовать 30 и более дней до скрининга с общими оценками по рейтинговой шкале Гамильтона (HDRS-17) ≥20 баллов, по части 1 шкалы HDRS-17 (сниженное настроение) ≥2 балла, по шкале глобального клинического впечатления о тяжести заболевания (CGI-S) ≥4 баллов. Разрешалось включать пациентов с коморбидным генерализованным тревожным расстройством, паническим или социальным тревожным расстройством, если БДР был первичным диагнозом. Исключалось участие пациентов, которые когда-либо принимали десвенлафаксин или имели суицидальный риск, основанный на клиническом мнении или оценке по части 3 шкалы HDRS-17 >3 баллов.
Конечные точки эффективности
Предусмотренные протоколом исследования вторичные критерии эффективности включали оценку по HDRS-17 и 6-пунктовой подшкале HDRS-6, шкалам общего клинического впечатления CGI-I и CGI-S, а также оценку доли пациентов, у которых достигалась ремиссия (общая оценка по HDRS-17 ≤7 баллов). HDRS-6 использовалась потому, что она обладает более высокой чувствительностью к изменениям ключевых характеристик депрессии по сравнению с HDRS-17 (P. Bech et al., 2010).
Оценка влияния на здоровье
Дополнительно оценивали, как пациенты воспринимают свою продуктивность на работе, с использованием опросника WPAI (Work Productivity and Activity Impairment), а также их самочувствие по 5-пунктовому индексу Всемирной организации здравоохранения (WHO-5).
WPAI— это 6-пунктовый опросник для оценки влияния тяжести симптомов на работоспособность и повседневную активность за последние 7 дней. Оцениваются четыре показателя: абсентеизм (количество пропущенного рабочего времени), презентеизм (сниженная эффективность труда), потеря продуктивности (абсентеизм + презентеизм) и нарушения повседневной активности. Чем выше балл, тем более выражено снижение функционирования по каждому из показателей.
WHO-5 оценивает частоту пяти характеристик, описывающих позитивное эмоциональное состояние («бодрый и в хорошем настроении», «спокойный и расслабленный», «активный и энергичный», «свежий и отдохнувший», «день наполнен событиями, которые мне интересны») по шкале от 0 (никогда) до 5 (все время) за последние 2 нед. Общая оценка (от 0 до 25) вычисляется путем суммирования оценок по пяти характеристикам.
Пациенты заполняли WPAI и WHO-5 в начале исследования, через 8 и 20 нед открытого лечения, а также через 14 и 26 нед двойного слепого периода или на последнем визите, если участник выбывал досрочно.
Результаты
Из 874 включенных пациентов 548 были рандомизированы к приему плацебо (n=276) или десвенлафаксина по 50 мг в сутки (n=272) в двойной слепой период исследования. 162 пациента выбыли досрочно; в обеих группах самой частой причиной была недостаточная эффективность (плацебо: n=67, десвенлафаксин: n=33). За двойной слепой период 57,2% пациентов группы плацебо и 54,4% пациентов группы десвенлафаксина сообщали о побочных эффектах.
HDRS-17
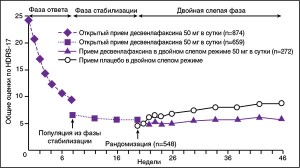
За время открытой фазы общие оценки по HDRS-17 улучшились: со средней (стандартное отклонение, SD) 24,21 балла (2,82) исходно до 9,29 (6,42) на 8-й неделе. Улучшения по HDRS-17 сохранялись на 20-й неделе (рис. 1). В двойную слепую фазу скорректированные средние оценки по HDRS-17 несколько повысились в обеих группах. Это повышение было более выраженным в группе плацебо, начиналось со 2-й недели двойной слепой фазы и продолжалось до 26-й недели. На 26-й неделе скорректированное среднее повышение по сравнению с исходным показателем в начале двойной слепой фазы было достоверно больше в группе плацебо, чем в группе терапии десвенлафаксином: скорректированная средняя разница 2,35; 95% доверительный интервал (ДИ) от 1,39 до 3,32; р<0,001.
HDRS-6
Средняя оценка по HDRS-6 снизилась с 12,83 (SD 1,63) балла исходно до 4,77 (3,64) балла на 8-й неделе открытой фазы, и это улучшение сохранялось на 20-й неделе открытой фазы. В ходе двойной слепой фазы средние оценки по HDRS-6 оставались преимущественно без изменений в группе десвенлафаксина, но повышались в группе плацебо. Статистически достоверная разница между группами наблюдалась на 2-й неделе двойной слепой фазы и сохранялась до 26-й недели. На 26-й неделе скорректированное среднее повышение по сравнению с исходным показателем в начале двойной слепой фазы было достоверно больше в группе плацебо, чем в группе терапии десвенлафаксином: скорректированная средняя разница 1,27 (95% ДИ 0,75-1,79); р<0,001.
Ремиссия
По окончанию 8-й недели открытой фазы 46,8% пациентов соответствовали критерию ремиссии (общая оценка по HDRS-17 ≤7 баллов). Доля пациентов, достигших ремиссии, выросла до 75,9% в конце фазы стабилизации открытого периода (на 20-й неделе). В начале двойной слепой фазы в группах плацебо и десвенлафаксина доли пациентов в состоянии ремиссии были сопоставимы (83,3 и 80,9% соответственно). За время двойного слепого лечения наблюдалось достоверно большее сокращение доли пациентов в состоянии ремиссии в группе плацебо по сравнению с группой десвенлафаксина, начиная со 2-й недели. На 26-й неделе двойной слепой фазы доля пациентов в состоянии ремиссии была достоверно больше в группе десвенлафаксина (р<0,0001).
Общее клиническое впечатление
В открытую фазу средние оценки по CGI-S улучшились с исходной 4,48 (SD 0,58) балла до 2,26 (1,11) балла на 8-й неделе. Затем они сохранялись всю фазу стабилизации открытого периода, со средней оценкой 1,68 (0,87) балла на 20-й неделе. На протяжении двойного слепого периода оценки по CGI-S преимущественно не изменились в группе десвенлафаксина, но достоверно повысились в группе плацебо, начиная с 3-й недели двойной слепой фазы. По завершению двойной слепой фазы (26-я неделя) скорректированный средний прирост по шкале CGI-S по сравнению с исходной оценкой в начале двойной слепой фазы был достоверно больше в группе плацебо, чем в группе десвенлафаксина (р<0,001).
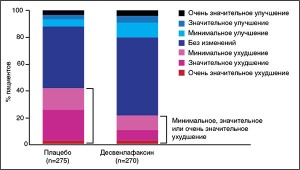
На 8-й неделе открытой фазы 55 и 27,7% пациентов имели оценку по CGI-I 1 (очень значительное улучшение) или 2 (значительное улучшение) соответственно (рис. 2). По завершению фазы стабилизации (20-я неделя) доля пациентов с такими оценками составила 77,5 и 16,1% соответственно. В конце двойной слепой фазы (20-я неделя) 78,1% пациентов группы десвенлафаксина и 57,1% пациентов группы плацебо имели оценки по CGI-I от 1 до 4. Пропорции пациентов с оценками 5 (минимальное ухудшение), 6 (значительное ухудшение) или 7 (очень значительное ухудшение) были выше в группе плацебо, чем в группе десвенлафаксина (р<0,001).
WPAI
Во время открытой фазы наблюдалось улучшение во всех четырех доменах WPAI (абсентеизм, презентеизм, потеря продуктивности и нарушения повседневной активности). На 8-й неделе открытой фазы наибольшее среднее изменение по сравнению с исходным отмечалось в домене нарушений активности: -31,0 (30,5) балла. Эти улучшения сохранялись на протяжении всей фазы стабилизации открытого периода. В ходе двойной слепой фазы достоверное превосходство десвенлафаксина над плацебо отмечалось на 14-й и 26-й неделях в доменах презентеизма, потери продуктивности и нарушения активности (для всех сравнений р≤0,041), но не в домене абсентеизма.
WHO-5
На протяжении открытой фазы оценки самочувствия по WHO-5 улучшались и удерживались: среднее изменение от исходного составило +8,35 (6,25) на 8-й неделе и +10,65 (6,20) на 20-й неделе. В ходе двойной слепой фазы достоверное превосходство десвенлафаксина над плацебо отмечались на 14-й и 26-й неделях (для обоих сравнений р<0,001). Средняя оценка по WHO-5 снизилась по сравнению с исходной в начале двойной слепой фазы в группе плацебо, но практически не изменилась к 26-й неделе в группе десвенлафаксина.
Обсуждение и выводы
Представленные здесь вторичные результаты исследования долгосрочной эффективности десвенлафаксина дополняют данные первичного анализа о снижении частоты рецидивов БДР и демонстрируют, что продолжение терапии за рамки 20 нед открытой фазы сопровождалось удержанием положительных эффектов в отношении симптомов депрессии и функциональных исходов по сравнению с плацебо.
Снижение продуктивности труда является главным функциональным нарушением, присущим БДР, и приводит к потере примерно 27 рабочих дней в год на одного пациента вследствие презентеизма и абсентеизма (R.C. Kessler et al., 2006). Результаты, полученные по опроснику трудоспособности WPAI, указывают на то, что пациенты группы плацебо продолжали ходить на работу, но их функционирование как на рабочем месте, так и при выполнении повседневных задач снижалось в ходе двойного слепого периода лечения, в то время как у пациентов, которые принимали десвенлафаксин, продуктивность, достигнутая за 20 нед открытой фазы терапии, сохранялась и в дальнейшем.
Индекс WHO-5 показал достоверное снижение самооценок самочувствия у пациентов группы плацебо в ходе двойной слепой фазы исследования по сравнению с участниками, которые продолжали принимать десвенлафаксин. В группе десвенлафаксина положительные результаты в эмоциональной сфере, достигнутые в начале двойной слепой фазы, практически не изменились.
Таким образом, антидепрессивная эффективность десвенлафаксина в дозе 50 мг в сутки сохранялась у пациентов, которые продолжали прием препарата дополнительно 6 мес после достижения стабильного терапевтического ответа, в то время как у пациентов группы плацебо наблюдалось усиление симптомов депрессии. Кроме того, продленная терапия десвенлафаксином в ходе двойной слепой фазы длительностью 6 мес способствовала удержанию положительных результатов по шкалам самочувствия и функционирования.
Prim Care Companion CNS Disord. 2015; 17 (4):
10.4088/PCC.14m01711.
Сокращенный перевод с англ. Дмитрия Молчанова