20 березня, 2017
Деркаст®: комплексний підхід в лікуванні пацієнтів з БА і ХОЗЛ на госпітальному етапі
Бронхіальна астма (БА) і хронічне обструктивне захворювання легень (ХОЗЛ) належать до тих захворювань дихальної системи, в лікуванні яких, на жаль, далеко не завжди вдається обійтися без стаціонарного етапу. Як правило, ургентна допомога таким хворим в стаціонарах надається з акцентом на усуненні небезпечного для життя стану – бронхоспазму. В той же час відомим є факт, що причина погіршення стану пацієнта при загостренні – прогресуюче запалення. Це зумовлює необхідність пошуку препаратів, які б забезпечували надійний контроль запалення при загостреннях БА та ХОЗЛ. Які ж особливості терапії таких пацієнтів на госпітальному етапі?
Хронічне запалення в патогенезі БА та ХОЗЛ
Згідно з положеннями консенсусу «Глобальна ініціатива щодо бронхіальної астми» (Global Initiative for Asthma, GINA, 2017) БА розглядається як гетерогенне захворювання, що характеризується хронічним запаленням дихальних шляхів і діагностується за респіраторними симптомами свистячого дихання, задишки, утруднення в грудях або кашлю, варіабельних за тривалістю та інтенсивністю в поєднанні з лабільною експіраторною обструкцією дихальних шляхів. У патогенезі ХОЗЛ (звіт «Глобальної ініціативи з ХОЗЛ» – Global Initiative for Chronic Obstructive Lung Disease, GOLD, 2017) також фігурує інформація стосовно того, що провідна роль у розвитку хвороби належить запальному процесу, а також дисбалансу протеїназ і антипротеїназ в легенях, окислювальному стресу.
При цьому хронічне запалення як у випадку БА, так і ХОЗЛ поширюється на всі відділи дихальних шляхів, паренхіму і судини легень. В результаті хронічного запалення дихальних шляхів розвиваються набряк слизової оболонки бронхів, гіперсекреція слизу, бронхоконстрикція, які проявляються обмеженням повітряного потоку (M. Roth, 2014). Таким чином, запальний процес відіграє важливу роль в патогенезі БА і ХОЗЛ. Очевидно, що патогенетична терапія має бути спрямована однаковою мірою на усунення хронічного персистуючого запалення і бронхоспазму. Про що ж свідчать сучасні рекомендації?
Сучасні принципи терапії БА та ХОЗЛ і їх прогалини
Як відомо, незважаючи на широкий спектр препаратів для терапії БА, загострення, при яких є необхідною госпіталізація, можуть розвинутися у будь-якого пацієнта незалежно від тяжкості і тривалості захворювання. Причинами втрати контролю при БА та госпіталізацій часто стають неадекватна базисна терапія і/або низька прихильність пацієнтів до дотримання щоденних рекомендацій, а також частий прийом КДБА (короткої дії β2-адреноміметиків), що призводить до збільшення хронічного запалення і розвитку загострень. Що стосується КДБА, то часте і тривале їх застосування на догоспітальному етапі є фактором ризику загострень, який провокує розвиток десенситизації адренергічних рецепторів; крім того, застосування цих препаратів
більше 1-2 разів на добу, особливо в денний час, вважається аргументом для перегляду базисної терапії. Використання КДБА понад 200 доз на місяць – фактор ризику смерті з причини БА.
Крім того, зворотною стороною медалі надмірного використання КДБА є розвиток електролітного дисбалансу. Так, в дослідженні A.N. Nagdeote, Y.R. Pawade (2011) взяли участь 50 дітей віком 2-12 років з БА. Всі діти були обстежені до початку лікування, яке включало сальбутамол та інгаляційний глюкокортикостероїд (ГКС), причому останній призначався тільки дітям з тяжкими симптомами захворювання. Через 15 днів терапії зразки крові були взяті повторно. Автори досліджували рівні калію і натрію в плазмі. Результати показали, що терапія сальбутамолом викликала значне зниження рівнів калію в крові пацієнтів незалежно від тяжкості перебігу БА. Рівні натрію достовірно не змінилися. Результати дослідження наведено в таблиці 1.
Таким чином, терапія КДБА може істотно впливати на електролітний склад плазми крові.
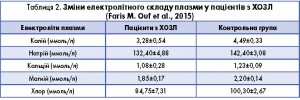
Слід взяти до уваги, що у пацієнтів з хронічною респіраторною патологією наявний фоновий дефіцит деяких мікроелементів, що підтверджено в дослідженні Faris M. Ouf і співавт. (2015). Дане дослідження, проведене за участю 60 дорослих пацієнтів з ХОЗЛ, дозволило виявити фонові зміни електролітного складу плазми у таких хворих. Автори відмічають, що пацієнти з ХОЗЛ мають значні порушення електролітного балансу навіть за відсутності терапії. Результати вимірювань рівнів електролітів плазми пацієнтів з ХОЗЛ до лікування наведено в таблиці 2.
У дослідженні також було вивчено динаміку змін електролітного балансу в ході стандартного лікування ХОЗЛ. Автори прийшли до висновку, що стандартна терапія ХОЗЛ може привести до подальшого посилення електролітного складу сироватки крові. Причому електролітні розлади є предиктором можливих ускладнень, а пацієнти з істотними коливаннями рівнів калію, магнію, хлору знаходяться в групі підвищеного ризику щодо потрапляння у відділення інтенсивної терапії.
Таким чином, призначаючи терапію пацієнтам з БА і ХОЗЛ на госпітальному етапі, слід пам’ятати про високу ймовірність гіпокаліємії та гіпомагніємії у таких хворих, особливо на тлі неконтрольованого застосування КДБА.
Шляхи оптимізації стаціонарного лікування хворих з БА та ХОЗЛ
В цілому для контролю БА як на до-, так і на госпітальному етапі повсюдно використовується комбінація ГКС/ТДБА (глюкокортикоїди / тривалої дії β2-агоністів) в SMART-режимі. Згідно з рекомендаціями GINA при погіршенні стану, який виникає внаслідок десенситизації β2-адренорецепторів, а також зниження чутливості пацієнтів до ГКС, у хворих з тяжким і середньотяжким перебігом БА виникає необхідність в комплексній терапії бронхоспазму і хронічного запалення дихальних шляхів із застосуванням препаратів другої лінії, основний напрямок дії яких – купірування бронхоспазму (іпратропію бромід, тіотропію бромід, теофілін). Рекомендації GOLD, які містять основні принципи ведення пацієнтів з ХОЗЛ, також поділяють лікування захворювання на 2 етапи. На госпітальному етапі внутрішньовенне введення препаратів другої лінії використовується з переважно бронхолітичною метою у випадках недостатнього ефекту від ГКС і короткодіючих бронхолітиків. Однак, як зазначалося вище, усунення бронхоспазму – тільки одна із цілей терапії БА та ХОЗЛ на госпітальному етапі. Комплексне лікування з обов’язковим усуненням і запалення, і бронхоспазму – ось патогенетично виправданий принцип у лікуванні загострень. З цїєї точки зору вартими уваги є препарати-інгібітори фосфодіестераз (ФДЕ). Інгібітори ФДЕ з раціональним складом здатні забезпечити таку комплексність лікування.Але що входить в поняття «раціональність» у цьому контексті? Спробуємо розібратися.
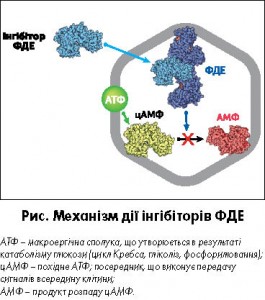
Необхідність призначати інгібітори ФДЕ в умовах стаціонару, як вже було описано вище, зумовлена зниженням чутливості β2-адренорецепторів до КДБА внаслідок частого їх застосування на догоспітальному етапі у зв’язку з погіршенням стану. В основі механізму дії інгібіторів ФДЕ лежить накопичення цАМФ за рахунок пригнічення процесу його перетворення в аденозинмонофосфат (АМФ) (рис.).
Накопичення цАМФ в клітинах гладких м’язів бронхів призводить до їх розслаблення і розвитку бронхолітичного ефекту. Протизапальна дія інгібітора ФДЕ реалізується за рахунок пригнічення вироблення лейкотрієнів, інтерлейкінів, гістаміну, фактора некрозу пухлини імунокомпетентними клітинами (нейтрофілами, Т-лімфоцитами, еозинофілами, макрофагами, тучними клітинами). Вкрай важливо відмітити, що інгібітори ФДЕ реалізують свої ефекти повною мірою лише в умовах наявності в організмі мікроелементів в концентраціях, близьких до нормальних. Це пов’язано з тим, що головний субстрат – цАМФ, відповідальний за розвиток біологічного (лікувального) ефекту інгібітора ФДЕ, утворюється з АТФ. Реакції з утворенням АТФ в результаті катаболізму глюкози потребують нормального вмісту есенціальних мікроелементів, в першу чергу магнію і калію. У разі дефіциту магнію і калію реакції утворення АТФ сповільнюються. Відомо, що магній є каталізатором 6 з 9 реакцій гліколізу, присутній в клітині у вигляді сполуки з АТФ (M. Faris, 2015), а також необхідний для кожної реакції циклу Кребса. Крім того, магній активує аденілатциклазу, яка контролює власне синтез цАМФ. Калій, в свою чергу, активує піруваткіназу, яка каталізує гліколіз з утворенням АТФ. Крім того, калій активує роботу ферментних систем, які беруть участь в утворенні АТФ в процесі окисного фосфорилювання (В.І. Мальцев, В.К. Казимирко, 2015). Таким чином, пацієнтам з БА і ХОЗЛ з їх фоновим дефіцитом калію і магнію в схему лікування препаратами другої лінії необхідно включати мікроелементи для нормалізації електролітного складу плазми. Це дозволить досягти бажаного терапевтичного ефекту від призначених препаратів-інгібіторів ФДЕ.
Отже, патогенетично обґрунтована схема терапії БА і ХОЗЛ на госпітальному етапі має передбачати:
- ефективне купірування бронхоспазму;
- надійний контроль запалення.
Парадоксально, але до теперішнього часу для пацієнтів із загостренням БА і ХОЗЛ на госпітальному етапі ринок не пропонував препарати комплексної дії, які б купірували одночасно і бронхоспазм, і запалення.
Прикладом сучасного підходу, що враховує патогенетичні особливості загострення БА та ХОЗЛ на госпітальному етапі, може виступати новий препарат Деркаст® (ТОВ «Юрія-Фарм», Україна). Це єдиний парентеральний інгібітор ФДЕ для лікування пацієнтів на госпітальному етапі, який одночасно купірує у пацієнтів із загостреннями БА та ХОЗЛ і бронхоспазм, і запалення, завдяки продуманому складу препарату.
Інгібуючи ФДЕ-3, ФДЕ-4, ФДЕ-5,
Деркаст® сприяє розвитку бронхолітичного і протизапального ефектів. Іони калію і магнію, що входять до складу препарату, забезпечують настання бажаного терапевтичного ефекту від застосування інгібітора ФДЕ. Деркаст® випускається у вигляді готового розчину для внутрішньовенної інфузії, що забезпечує швидкий і керований ефект. Ще раз необхідно підкреслити, що Деркаст® – принципово новий препарат, здатний одночасно впливати на основні ланки патогенезу загострення БА та ХОЗЛ.
Немає сумнівів стосовно того, що БА і ХОЗЛ є на сьогодні проблемою пульмонології № 1. Неухильне зростання поширеності, високий рівень смертності (щорічно від БА і ХОЗЛ помирають понад 3 млн осіб!), збільшення питомої ваги тяжких форм – ось причини, які зумовлюють високу медико-соціальну актуальність зазначених захворювань. Важливо відмітити, що основними причинами смерті хворих на БА та ХОЗЛ сьогодні називають як відсутність адекватного довгострокового лікування, так і несвоєчасне і неадекватне надання екстреної допомоги. Комплексний підхід до госпітального лікування хворих на БА та ХОЗЛ з використанням нового препарату Деркаст® – це не тільки патогенетично обґрунтований засіб підвищення ефективності терапії, але і спосіб зниження рівня смертності.
Підготувала Олександра Мєркулова