18 квітня, 2017
Сердечно-сосудистая безопасность целекоксиба, напроксена и ибупрофена при лечении артритов
Нестероидные противовоспалительные препараты (НПВП) начиная с 1960-х годов стали самыми популярными лекарственными средствами в мире; только в США ежегодно регистрируется более 100 млн назначений. НПВП уменьшают выраженность боли и воспаления путем ингибирования фермента циклооксигеназы (ЦОГ), который участвует в образовании воспалительных простагландинов. Однако ЦОГ также присутствует в слизистой оболочке желудка, где стимулирует образование гастропротективных простагландинов. Идентификация двух изоформ фермента — ЦОГ‑1 и ЦОГ‑2, а также открытие того факта, что противовоспалительный и аналгетический эффекты опосредованы ингибированием ЦОГ‑2, а гастротоксичность связана с подавлением ЦОГ‑1, привели к разработке селективных ингибиторов ЦОГ‑2, которые демонстрируют эффективность при меньшем риске развития побочных эффектов со стороны желудочно-кишечного тракта (B.J. Whittle, 2000).
Данные о неблагоприятных сердечно-сосудистых исходах, полученные в плацебо-контролируемом исследовании, послужили поводом к запрету продаж селективного ингибитора ЦОГ‑2 рофекоксиба в 2004 году. В другом исследовании на основании малого количества событий был сделан вывод, что кардиотоксичность целекоксиба могла быть обусловлена использованием более высоких доз, чем официально одобренные (S.D. Solomon et al., 2005). В итоге Управление по контролю качества продуктов питания и лекарственных средств США (FDA) разрешило продолжить продажи целекоксиба (единственного оставшегося на рынке селективного ингибитора ЦОГ‑2), но с требованием провести исследование сердечно-сосудистой безопасности. В исследовании PRECISION (Prospective Randomized Evaluation of Celecoxib Integrated Safety versus Ibuprofen or Naproxen) изучались сердечно-сосудистые, желудочно-кишечные, почечные и другие аспекты безопасности целекоксиба в сравнении с двумя неселективными НПВП.
Методы
PRECISION — рандомизированное многоцентровое двойное слепое исследование с запланированным анализом нон-инфериорности целекоксиба (для подтверждения или опровержения того, что целекоксиб не уступает препаратам сравнения по критериям безопасности). Более детально методы исследования и протокол были описаны в предыдущей публикации (M.C. Becker et al., 2009).
Спонсор исследования (Pfizer) участвовал в разработке дизайна и составлении протокола в сотрудничестве с исполнительным комитетом и при консультативной поддержке FDA. Спонсор также помогал при сборе данных и осуществлял поддержку базы данных исследования. Спонсор разделял операционные роли с Кливлендским координационным центром по проведению клинических исследований (C5Research) и несколькими контрактными исследовательскими организациями. После завершения исследования база данных была передана в C5Research для проведения статистического анализа. Исполнительный комитет исследования подготовил статью. Спонсору разрешалось редактировать и комментировать статью, но решение о публикации и о финальном содержании статьи принималось авторами без договорных ограничений права на публикацию.
В исследование включали пациентов в возрасте от 18 лет с ревматоидным артритом (РА) или остеоартритом (ОА), с установленными сердечно-сосудистыми заболеваниями или факторами риска и, по мнению врачей и самих пациентов, нуждались в ежедневном приеме НПВП для купирования артралгии. Пациентов случайным образом распределяли в соотношении 1:1:1 для приема целекоксиба (100 мг 2 раза в сутки), ибупрофена (600 мг 3 раза в сутки) или напроксена (375 мг 2 раза в сутки). Во время последующих визитов у пациентов с РА врачам разрешалось повышать дозу целекоксиба до 200 мг 2 раза в сутки, дозу ибупрофена — до 800 мг 3 раза в сутки, напроксена — до 500 мг 2 раза в сутки для достижения контроля симптомов. Что касается пациентов с ОА, то дозы ибупрофена или напроксена также разрешалось повышать, но доза целекоксиба для применения по данному показанию была ограничена регуляторным органом. В целях гастропротекции всем пациентам назначали эзомепразол в дозе 20-40 мг в сутки. Врачи, участвовавшие в исследовании, могли в полной мере использовать способы профилактики сердечно-сосудистых заболеваний, соответствующие местным стандартам и руководствам. Пациентам, которые принимали низкие дозы (≤325 мг) ацетилсалициловой кислоты (АСК), разрешалось продолжать эту терапию.
Первичная комбинированная конечная точка в анализе «время до события» включала исходы, которые соответствовали критериям Проекта исследований антитромбоцитарной терапии (Antiplatelet Trialists’ Collaboration, APTC), а именно: смерть по причине сердечно-сосудистых нарушений, в том числе от геморрагических осложнений, нефатальный инфаркт миокарда или нефатальный инсульт (Antiplatelet Trialists’ Collaboration. BMJ 1994; 308: 81-106). Вторичный комбинированный исход — большие неблагоприятные сердечно-сосудистые события, включая компоненты первичной конечной точки, а также коронарную реваскуляризацию или госпитализацию по поводу нестабильной стенокардии или транзиторной ишемической атаки. В качестве вторичных исходов также фиксировались клинически значимые желудочно-кишечные события. Третичные исходы включали клинически значимые почечные события, железодефицитную анемию желудочно-кишечного генеза и госпитализации в связи с сердечной недостаточностью или гипертензией. Интенсивность артралгии по визуальной аналоговой шкале (ВАШ) от 0 до 100 мм регистрировалась как незаявленный вторичный критерий эффективности; изменения более чем на 13,7 мм считались клинически значимыми (G.A. Hawker et al., 2011). Летальный исход от любых причин регистрировался как предварительно заданный третичный исход.
В статистическом анализе напроксен служил первичным препаратом сравнения для проверки нон-инфериорности целекоксиба. Также были запланированы анализы нон-инфериорности целекоксиба относительно ибупрофена и ибупрофена относительно напроксена. Для подтверждения нон-инфериорности требовалось показать соответствие четырем статистическим критериям: в оригинальном дизайне относительный риск (ОР) не более 1,12 с верхней границей одностороннего 97,5% доверительного интервала (ДИ) не более 1,33 в двух популяциях — подлежащих лечению (intention-to-treat, ITT) и реального лечения (on-treatment). Согласно расчету требовалось 762 события конечной точки, чтобы со статистической мощностью 90% подтвердить нон-инфериорность. При прогнозируемой частоте событий 2% в год и 40% выбывании пациентов расчетный размер выборки составил 20 тыс. пациентов. В действительности частота событий была ниже прогнозируемой, процент выбывания более высоким, а набор участников происходил медленнее, чем планировалось. Поэтому согласно рекомендации комитета мониторинга данных и безопасности и после консультации с FDA в протокол исследования были внесены изменения: статистическая мощность понижена до 80%, а верхний 97,5% ДИ для нон-инфериорности в популяции получавших лечение был изменен на 1,40.
Для расчета ОР и ДИ использовалась модель пропорциональных рисков Кокса с поправками на факторы стратификации. Односторонний p<0,025 был принят как пороговый показатель статистической достоверности нон-инфериорности для первичной конечной точки без поправки на множественность сравнений. Значения Р для анализов вторичных конечных точек в популяции ITT приводятся с описательной целью. Двусторонний p<0,05 был принят как порог статистической значимости без поправки на множественность сравнений.
Результаты
Популяция пациентов
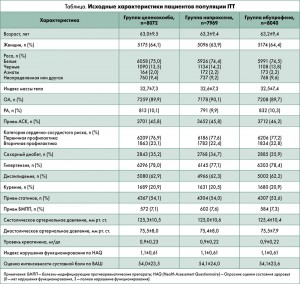
Скрининг для участия в исследовании прошли 31 857 пациентов; 24 222 были рандомизированы на базе 926 центров 13 стран между 23 октября 2006 года и 30 июня 2014 года. 141 участника исключили из анализа по причине фальсификации данных, в результате для анализа были доступны данные 24 081 пациента. 8072 участника включили в группу целекоксиба (средняя доза ± стандартное отклонение 209±37 мг), 7969 больных составили группу напроксена (852±103 мг), 8040 — группу ибупрофена (2045±246 мг). По исходным характеристикам пациентов группы были хорошо сбалансированы (табл.). Средние периоды лечения и наблюдения составили соответственно 20,3±16,0 и 34,1±13,4 мес для общей популяции пациентов: 20,8±16,0 и 34,2±13,4 мес — в группе целекоксиба, 20,5±15,9 и 34,2±13,3 мес — в группе напроксена, 19,6±16,0 и 33,8±13,6 мес — в группе ибупрофена. В ходе 10-летнего исследования 68,8% пациентов прекратили принимать исследуемые препараты, 27,4% вышли из-под наблюдения; 2,5% пациентов умерли, 8,3% отозвали согласие на участие в исследовании в письменном виде, 7,4% заявили о нежелании продолжать участие в устной форме, еще с 7,2% была утрачена связь до дня последнего визита.
Первичный исход по критериям APTC
В популяции первичная точка APTC была зафиксирована у 188 пациентов группы целекоксиба (2,3%), у 201 — группы напроксена (2,5%) и у 218 — группы ибупрофена (2,7%). ОР наступления данного исхода в группе целекоксиба по сравнению с группой напроксена составил 0,93 (95% ДИ от 0,76 до 1,13; p<0,001 для нон-инфериорности). ОР в группе целекоксиба по сравнению с ибупрофеном составил 0,85 (95% ДИ от 0,70 до 1,04; p<0,001 для нон-инфериорности); ОР в группе ибупрофена по сравнению с напроксеном — 1,08 (95% ДИ от 0,90 до 1,31; p=0,02 для нон-инфериорности).
В популяции пациентов, получавших лечение, первичная точка АРТС была зафиксирована у 134 пациентов группы целекоксиба (1,7%), у 144 — группы напроксена (1,8%) и у 155 — группы ибупрофена (1,9%). ОР наступления событий в группе целекоксиба по сравнению с группой напроксена составил 0,90 (95% ДИ 0,71-1,15; p<0,001 для нон-инфериорности); для целекоксиба против ибупрофена — 0,81 (95% ДИ 0,65-1,02; p<0,001 для нон-инфериорности); для ибупрофена против напроксена — 1,12 (95% ДИ 0,89-1,40; p=0,025 для нон-инфериорности).
Целекоксиб при сравнении как с напроксеном, так и с ибупрофеном отвечал всем четырем запланированным критериям нон-инфериорности (p<0,001 для нон-инфериорности по отношению к обоим препаратам сравнения). Ибупрофен в сравнении с напроксеном уложился в критерий нон-инфериорности (p=0,025).
Большие сердечно-сосудистые события и смертность
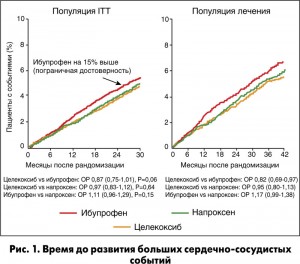
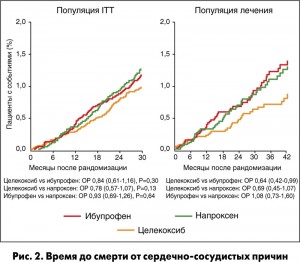
ОР наступления комбинированной конечной точки больших сердечно-сосудистых событий для целекоксиба против напроксена согласно результатам анализа в популяции ITT составил 0,97 (95% ДИ 0,83-1,12; p=0,64); ОР для целекоксиба против ибупрофена — 0,87 (95% ДИ 0,75-1,01; p=0,06) (рис. 1). При попарных сравнениях по компонентам первичной конечной точки, включая летальный исход от сердечно-сосудистых причин, различия между целекоксибом и напроксеном, а также между целекоксибом и ибупрофеном не достигли статистической достоверности (рис. 2). ОР смерти от любых причин составил 0,80 для целекоксиба против напроксена (95% ДИ 0,63-1,00; p=0,052). Частота развития нефатальных инфарктов миокарда была выше в группе ибупрофена, чем напроксена (ОР 1,39; 95% ДИ 1,01-1,91; p=0,04).
Исходы со стороны ЖКТ и почек
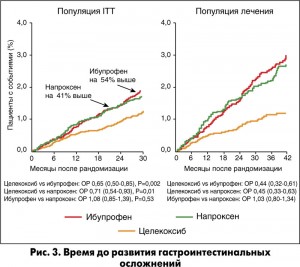
Частота наступления комбинированной конечной точки серьезных желудочно-кишечных событий в популяции ITT была ниже в группе целекоксиба, чем в группе напроксена (ОР 0,71; 95% ДИ 0,54-0,93; p=0,01), и ниже в группе целекоксиба, чем в группе ибупрофена (ОР 0,65; 95% ДИ 0,50-0,85; p=0,002). ОР желудочно-кишечных событий в группе ибупрофена против группы напроксена составил 1,08 (95% ДИ 0,85-1,39; p=0,53) (рис. 3). Серьезные почечные события происходили достоверно реже в группе целекоксиба по сравнению с группой ибупрофена (ОР 0,61; 95% ДИ 0,44-0,85; p=0,004), однако различия частоты этого исхода в группе целекоксиба против группы напроксена были недостоверными (ОР 0,79; 95% ДИ 0,56-1,12; p=0,19).
Другие исходы
Частота госпитализаций в связи с гипертензией была достоверно ниже в группе целекоксиба, чем в группе ибупрофена (ОР 0,60; 95% ДИ 0,36-0,99; p=0,04), но без достоверных различий между группами целекоксиба и напроксена. Что касается влияния терапии на качество жизни и симптомы артрита, то при оценке боли по ВАШ выявлено достоверное, но незначительное преимущество напроксена в сравнении с целекоксибом или ибупрофеном. Изменение по ВАШ от исходных оценок составило в среднем -9,3±0,26 мм в группе целекоксиба, -9,5±0,26 мм в группе ибупрофена и -10,2±0,26 мм в группе напроксена (p<0,001 для сравнения напроксена с целекоксибом, p=0,01 для сравнения напроксена с ибупрофеном).
Обсуждение
Исследование PRECISION планировалось после запрета рофекоксиба, на фоне научных и общественных предубеждений относительно сердечно-сосудистой безопасности селективных ингибиторов ЦОГ‑2. Предыдущие сведения об относительной безопасности селективных и неселективных ингибиторов ЦОГ были ограниченными, поскольку НПВП получали одобрение на основании небольших краткосрочных исследований, в которых, как правило, изучали их способность купировать боль, а также безопасность их применения. Обеспокоенность вызывало то, что целекоксиб, как и рофекоксиб, может оказывать неблагоприятные сердечно-сосудистые эффекты. Исследование PRECISION предоставило статистически достоверные доказательства того, что кардиоваскулярный риск при применении умеренных доз целекоксиба не выше, чем при назначении неселективных НПВП. В сравнении с двумя широко применяемыми неселективными НПВП — напроксеном и ибупрофеном — терапия целекоксибом ассоциировалась с численно меньшей частотой кардиоваскулярных событий, что в результате обеспечило значения p для нон-инфериорности менее чем 0,001. Результаты исследования не поддерживают широко распространенное мнение, что лечение напроксеном по сравнению с другими НПВП обеспечивает лучшие кардиоваскулярные исходы (C. Patrono, C. Baigent, 2014).
Для подтверждения того что целекоксиб не уступает препаратам сравнения (нон-инфериорности), согласно дизайну исследования требовалось показать соответствие запланированным критериям как в популяции подлежащих лечению (ITT), так и в популяции пациентов, которые в действительности получали лечение. Мы выбрали этот подход, поскольку два альтернативных вида статистического анализа обеспечивают взаимодополняющие данные о безопасности препарата. Анализ ITT — единственный, сохраняющий целостность рандомизации, но имеющий свойство «растворять» сигналы безопасности, если пациенты демонстрируют низкую приверженность к терапии исследуемым препаратом. Анализ в популяции находящихся на лечении учитывает только те события, которые происходили в то время, когда пациенты принимали исследуемый препарат, что усиливает показатели безопасности. Мы также запланировали анализ более обширного исхода — больших сердечно-сосудистых событий — в качестве вторичной комбинированной точки, чтобы повысить статистическую мощность для обнаружения различий между тремя ветвями терапии. В группе целекоксиба было зарегистрировано меньше больших сердечно-сосудистых событий, чем в группе ибупрофена, но различия не достигли уровня достоверности в популяции ITT (p=0,06). Уровень летальных исходов от любых причин была ниже в группе целекоксиба, чем в группе напроксена, хотя различия были также не достоверными (p=0,052). Мы призываем к осторожности при интерпретации этих данных, поскольку большие сердечно-сосудистые события были вторичной конечной точкой, а общая смертность — третичной, и эти исходы анализировались без поправки на множественность компонентов конечной точки. Кроме того, конечная точка «большие сердечно-сосудистые события» включала более субъективные компоненты, чем комбинированный исход по критериям APTC.
Хотя первичной задачей исследований было оценить кардиоваскулярные исходы, мы также запланировали анализ желудочно-кишечных и почечных осложнений, чтобы дать всеобъемлющую характеристику безопасности. Для сравнения трех препаратов мы составили двухкомпонентную конечную точку, включавшую клинически значимые желудочно-кишечные события и железодефицитную анемию желудочно-кишечного происхождения. По данному исходу достоверно меньше событий было зафиксировано в группе целекоксиба, чем в группах сравнения. Эти результаты были ожидаемыми на основании теоретических гастроинтестинальных преимуществ селективной блокады ЦОГ‑2. Различия были выявлены несмотря на то, что всем пациентам назначали ингибитор протонной помпы эзомепразол, хотя приверженность к этой терапии специально не отслеживалась. Частота развития почечных побочных эффектов и госпитализаций в связи с гипертензией также была достоверно меньшей в группе целекоксиба, чем в группе ибупрофена, хотя различия между группами целекоксиба и напроксена не достигли уровня достоверности.
Несмотря на то что пациенты, принимавшие напроксен, отмечали несколько лучшее купирование боли, чем в группах целекоксиба и ибупрофена, различия не достигали клинической значимости, которая определялась как изменение более чем на 13,7 мм по ВАШ.
Исследованию PRECISION присущи некоторые ограничения. Приверженность и удержание на терапии были хуже, чем в большинстве исследований по изучению кардиоваскулярных исходов, что отражает трудности длительного лечения болевого синдрома: пациентов часто не удовлетворяет эффективность, и они переходят на другую терапию или выбывают из исследования. Низкие урони приверженности и удержания также регистрировались в предыдущих исследованиях по лечению боли (R.A. Moore et al., 2008). Принимая во внимание схожесть результатов, полученных в популяциях ITT и реального лечения, можно предположить, что низкая приверженность, скорее всего, не повлияла на основные выводы, однако высокие уровни выбывания пациентов затрудняют интерпретацию.
Доза целекоксиба ограничена официальной инструкцией до 200 мг в сутки для большинства пациентов, что могло обусловить потенциальное преимущество по безопасности его применения, хотя следует заметить, что дозы обоих неселективных НПВП также были субмаксимальными. Наше исследование подтверждает безопасность умеренных доз целекоксиба, но это не означает, что высокие дозы также безопасны. Несмотря на то что ранее сообщалось о влиянии ибупрофена и напроксена на антиагрегантные эффекты АСК (F. Catella-Lawson et al., 2001), в нашем исследовании такой связи не обнаружено. Однако следует учитывать, что оценка влияния АСК на относительную безопасность НПВП специально не планировалась.
Результаты исследования отражают относительную безопасность только трех препаратов и не могут быть экстраполированы на эффекты более чем двадцати других НПВП, представленных на рынке. По этическим соображениям в исследовании не набиралась группа плацебо. Ацетаминофен не был выбран в качестве препарата сравнения, поскольку предыдущие исследования показали его неэффективность при лечении НПВП-зависимых пациентов с артритами (G.C. Machado et al., 2015).
Таким образом, исследование PRECISION подтвердило, что целекоксиб в умеренных дозах не уступает напроксену и ибупрофену по кардиоваскулярной безопасности в соответствии с критериями APTC. Кроме того, на фоне лечения целекоксибом реже, чем в группах сравнения, возникали желудочно-кишечные осложнения и реже, чем в группе ибупрофена, регистрировались ренальные побочные эффекты.
New England Journal of Medicine, 2016; 375 (26): 2519-2529.
Список литературы находится в редакции.
Сокращенный перевод с англ. Дмитрия Молчанова