14 березня, 2017
Сравнительная эффективность и безопасность препаратов для лечения подагры и гиперурикемии: результаты первого сетевого метаанализа
Гиперурикемия определяется как плазменная концентрация солей мочевой кислоты (МК) — уратов,
превышающая порог их растворимости во внеклеточной жидкости — 6,8 мг/дл. При преодолении
этого значения начинается отложение кристаллов моноурата натрия в мягких тканях вокруг
суставов, что рано или поздно приводит к развитию клинически манифестной подагры. В 2010 году
распространенность данного заболевания в мировой популяции оценивалась в 0,08%, а недавние
эпидемиологические исследования подтвердили рост этого показателя наряду с увеличением
распространенности бессимптомной гиперурикемии (E. Smith et al., 2014; E. Roddy, H. K. Choi, 2014).
Установлено, что постоянно повышенный уровень МК ассоциируется не только с риском развития
подагры, но и с коморбидными заболеваниями сердечно-сосудистой системы и почек.
Согласно последним рекомендациям Европейской противоревматической лиги (EULAR, 2016) уратоснижающую терапию (УСТ) следует предлагать всем пациентам с впервые установленным диагнозом подагры. УСТ показана пациентам с повторными приступами подагрического артрита, тофусами, уратной артропатией и/или почечными конкрементами. Начинать УСТ рекомендуется в ранние сроки после установления диагноза у пациентов молодого возраста (<40 лет), при очень высоком уровне МК крови (>8,0 мг/дл, или 480 мкмоль/л) и/или при наличии коморбидных состояний — поражения почек, артериальной гипертензии, ишемической болезни сердца, сердечной недостаточности. Концентрацию МК следует поддерживать на уровне <6 мг/дл (360 мкмоль/л). Более низкий целевой уровень (<5 мг/дл, или 300 мкмоль/л) рекомендуется достигать у пациентов с тяжелыми проявлениями подагры (частыми приступами, тофусами, артропатией) для ускорения растворения уратных отложений.
Уратоснижающие препараты классифицируются на три основные группы по механизму действия. Урикозурические средства действуют как ингибиторы синтеза МК. Из этой группы старой генерации широкое распространение получил пробенецид, а бензбромарон с 2003 года запрещен в большинстве европейских стран в связи с выраженной гепатотоксичностью.
Ингибиторы ксантиноксидазы — аллопуринол и фебуксостат рекомендованы EULAR и Американской коллегией ревматологов (ACR) в качестве уратоснижающих препаратов первой линии. Пуриновый аналог аллопуринол значительно дешевле, но ассоциируется с серьезными кожными побочными эффектами. С 2008 года в европейских странах, а с 2009 — в США зарегистрирован фебуксостат — мощный непуриновый селективный ингибитор ксантиноксидазы с альтернативными путями метаболизации (почки и печень), что позволяет применять его даже у пациентов с умеренной почечной недостаточностью. Наконец, в 2011 году на рынках Европы и США появился новый препарат для лечения рефрактерной подагры пеглотиказа — рекомбинантный полиэтиленгликолевый конъюгат фермента уриказы.
В 2014 году на международном совете 78 экспертов в области ревматических заболеваний были сформулированы 10 ключевых вопросов касательно диагностики и лечения подагры (F. Sivera et al., 2014). В их числе был вопрос о том, как объективно сопоставить безопасность, клиническую и экономическую эффективность различных препаратов для УСТ. В двух предыдущих метаанализах были получены данные о преимуществах фебуксостата перед аллопуринолом в отношении частоты достижения целевых значений МК (P. Ye et al., 2013; L.I. Faruque et al., 2013). С этими препаратами проведено наибольшее количество исследований. Но задачу усложняет дефицит прямых сравнительных исследований высокого методологического качества, которые могли бы служить материалом для попарных сравнений с другими препаратами. Выходом из ситуации стало проведение сетевого метаанализа, который позволяет оценить относительные различия в эффективности препаратов при отсутствии рандомизированных исследований с прямыми сравнениями (T. Lumley et al., 2002). Вооружившись этим методом, китайские исследователи впервые проанализировали эффективность и безопасность пяти основных уратоснижающих препаратов и ранжировали их по величине эффектов (Shu Li, Hongxi Yang, Yanan Guo et al., 2016).
Систематический обзор провели в соответствии с критериями PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-analyses) для метаанализов клинических исследований. В базах данных PubMed, Medline, Embase, ClinicalTrials.gov и библиотеке Кокрановского сотрудничества выполнен поиск публикаций рандомизированных контролируемых исследований (РКИ) УСТ по 16 января 2016 года. Критерии включения исследований были следующими: 1) взрослые пациенты с гиперурикемией, с или без хронической подагры; 2) УСТ одним из пяти препаратов — аллопуринол, бензбромарон, фебуксостат, пеглотиказа или пробенецид; 3) назначения в группах сравнения — плацебо или другой препарат из пяти перечисленных; 4) критерий (не)эффективности — (не)достижение целевого уровня МК (≤6 мг/дл, или 360 мкмоль/л); критерий безопасности — частота развития побочных эффектов.
Результаты
Авторы идентифицировали 15 РКИ с участием 7246 пациентов, которые включили в сетевой метаанализ. В семи исследованиях сравнивали аллопуринол с разными дозами фебуксостата (M.A. Becker et al., 2005; M.A. Becker et al., 2008; X. Huang et al., 2014; N. Kamatani et al., 2011; N. Kamatani et al., 2011; S. Xu et al., 2015; K.H. Yu et al., 2016), в двух — аллопуринол с бензбромароном (F. Perez-Ruiz et al., 1999; M.K. Reinders et al., 2009), в одном — бензбромарон с пробенецидом (M.K. Reinders et al., 2009). В трех РКИ фебуксостат сравнивали с плацебо (M.A. Becker et al., 2005; N. Kamatani et al., 2011; N. Kamatani et al., 2011). Только одно плацебо-контролируемое исследование проведено с пеглотиказой (J.S. Sundy et al., 2011). Еще одно исследование имело три ветви — с аллопуринолом, фебуксостатом и плацебо (H.R. Schumacher et al., 2008). Длительность терапии варьировала от 4 до 52 нед. Возраст пациентов составлял от 30 лет, мужчины преобладали во всех выборках (более 80%). У всех участников исходная концентрация МК в плазме крови превышала 8,0 мг/дл.
При попарном сравнении препаратов рассчитывались показатели отношения шансов (ОШ) недостижения целевого уровня МК с 95% доверительными интервалами (ДИ), а также развития побочных эффектов. Значения ОШ >1,0 при сравнении эффективности означают преимущество второго препарата над первым. Значения ОШ <1,0 при сравнении безопасности означают меньшую частоту развития побочных эффектов в ходе терапии первым препаратом по сравнению со вторым, и наоборот.
Эффективность. Согласно результатам сетевого метаанализа все изучавшиеся препараты показали убедительные преимущества перед плацебо по достижению цели лечения. Во всем диапазоне дозировок, кроме 20 мг/сут, фебуксостат был эффективнее аллопуринола.
Вероятность недостижения целевого уровня МК на терапии аллопуринолом по сравнению с разными дозировками фебуксостата:
– аллопуринол против фебуксостата 40 мг/сут: ОШ 1,52; 95% ДИ 1,15-1,99;
– аллопуринол против фебуксостата 80 мг/сут: ОШ 3,54; 95% ДИ 2,80-4,47;
– аллопуринол против фебуксостата 120 мг/сут: ОШ 5,95; 95% ДИ 4,15-8,52;
– аллопуринол против фебуксостата 240 мг/сут: ОШ 17,41; 95% ДИ 8,22-36,89.
Бензбромарон был эффективнее фебуксостата в дозе 20 мг/сут (ОШ 0,20; 95% ДИ 0,06-0,73), но уступал дозировкам фебуксостата 120 и 240 мг/сут:
– бензбромарон против фебуксостата 120 мг/сут: ОШ 4,37; 95% ДИ 1,47-12,93;
– бензбромарон против фебуксостата 240 мг/сут: ОШ 12,78; 95% ДИ 3,58-45,60.
Остальные попарные сравнения были статистически недостоверными.
Безопасность. Частота развития побочных эффектов была ниже на фоне приема фебуксостата в дозе 120 мг/сут по сравнению с аллопуринолом и фебуксостатом в дозе 40 мг/сут:
– фебуксостат 120 мг/сут против аллопуринола: ОШ 0,72; 95% ДИ 0,56-0,91;
– фебуксостат 120 мг/сут против фебуксостата 40 мг/сут: ОШ 0,73; 95% ДИ 0,56-0,95.
Пробенецид вызывал побочные эффекты чаще, чем аллопуринол, фебуксостат в дозах 40, 120 и 240 мг/сут и плацебо:
– пробенецид против аллопуринола: ОШ 8,40; 95% ДИ 1,00-70,21;
– пробенецид против фебуксостата 40 мг/сут: ОШ 8,56; 95% ДИ 1,02-72,01;
– пробенецид против фебуксостата 80 мг/сут: ОШ 9,62; 95% ДИ 1,15-80,86;
– пробенецид против фебуксостата 120 мг/сут: ОШ 11,71; 95% ДИ 1,38-99,29;
– плацебо против пробенецида: ОШ 0,11; 95% ДИ 0,01-0,95.
Остальные попарные сравнения были статистически недостоверными.
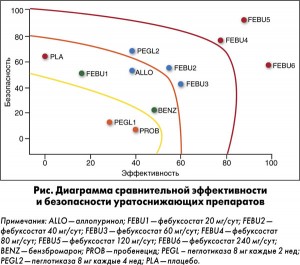
По результатам метаанализа была построена диаграмма, которая наглядно демонстрирует соотношения эффективности и безопасности сравниваемых препаратов для лечения подагры (рис.). Первое место в рейтинге занял фебуксостат с наиболее выгодными соотношениями эффективность/безопасность для доз 80 и 120 мг/сут. Бензбромарон и пробенецид обладают умеренной эффективностью, но часто вызывают побочные эффекты.
Выводы
• Фебуксостат превосходит другие уратоснижающие препараты по эффективности и безопасности, особенно в дозе 120 мг 1 р/сут.
• Риски развития побочных эффектов не перевешивают преимущества от применения любого из пяти изучавшихся препаратов, кроме пробенецида.
• Результаты метаанализа поддерживают действующие рекомендации EULAR и ACR относительно выбора фебуксостата и аллопуринола в качестве уратоснижающих препаратов первой линии.
• Требуется дальнейшее изучение пеглотиказы и схожих новых препаратов уриказы, так как доказательной базы недостаточно для определенных выводов.
Источник: www.nature.com/scientificreports.
DOI: 10.1038/srep33082.
Подготовил Дмитрий Молчанов