22 березня, 2017
Причини гетерогенності у дослідженнях, які повідомляли про підвищення смертності при застосуванні ГЕК 130/0,4 або 0,42 у пацієнтів з сепсисом: систематичний огляд і метааналіз
Завдяки більш швидкому відновленню гемодинамічної стабільності, покращенню мікроциркуляції, зменшенню оксидативного стресу і запальної відповіді гідроксиетилкрохмаль (ГЕК) в усьому світі широко застосовується для інфузійної терапії у пацієнтів із сепсисом. Проте деякі експериментальні дані вказали на те, що ГЕК, навіть найновішого покоління (ГЕК 130/0,4 або 0,42; далі – ГЕК 130/0,4), може викликати проліферації інтерстицію, макрофагальну інфільтрацію і пошкодження трубочок нирок з подальшим погіршенням ниркової функції. Крім того, у низці досліджень було продемонстровано, що порівняно з кристалоїдами ГЕК 130/0,4 асоціюється з підвищенням 90-денної смертності і потреби у нирковозамісній терапії у пацієнтів з тяжким сепсисом або септичним шоком. Відповідно, виникли значні побоювання щодо безпеки використання розчинів ГЕК для інфузійної терапії в цій популяції хворих.
Втім слід зазначити, що в рандомізованих контрольованих дослідженнях (РКД), в яких повідомлялось про ГЕК-асоційовану надмірну смертність порівняно з контрольними рідинами, спостерігалася значна гетерогенність. Наприклад, на відміну від дослідження Perner і співавт. (2012), у дослідженнях Myburgh і співавт. (2012) і Annane i співавт. ГЕК 130/0,4 не підвищував ризик смерті. Джерела цієї гетерогенності залишались нез’ясованими, але з високою ймовірністю вони зумовлені різницями у дизайні дослідження (тяжкість захворювання, осліплення, рандомізація тощо) і власне протоколі інфузійної терапії (показання, час, об’єм інфузованої рідини). Цікаво, що дози ГЕК, які застосовувались у РКД, не були ідентичними або навіть порівняними. До того ж в різних дослідженнях спостерігалися суттєві відмінності стосовно балансу рідини. Отже, мета цієї роботи – за допомогою систематичного огляду і метааналізу визначити, чи справді призначена доза ГЕК 130/0,4 або дельта балансу рідини є причинами гетерогенності ГЕК-асоційованої надмірної смертності порівняно з контрольними рідинами у пацієнтів з сепсисом – учасників згаданих РКД.
Методи
Систематичний огляд провели відповідно до Кокранівського керівництва і методології PRISMA. У базах даних PubMed, EMBASE і Кокранівському реєстрі контрольованих досліджень (CCRCT) здійснили пошук досліджень, які відповідали всім наступним критеріям: рандомізований контрольований дизайн; порівняння 6% ГЕК з молекулярною масою 130 кДа і коефіцієнтом молярного заміщення 0,4 або 0,42 vs будь-якої контрольної рідини (кристалоїдів або колоїдів); пацієнти віком 18 років і старше; діагноз сепсису на момент рандомізації; досліджувані рідини для інфузійної терапії визначались як рідини, необхідні для збільшення або підтримання внутрішньосудинного об’єму; повідомлення показника смертності. Дельта добового балансу рідини визначалась як середній добовий позитивний баланс у групі ГЕК мінус те саме в контрольній групі впродовж періоду спостереження.
Результати
Пошук виявив 327 досліджень, з яких 11 відповідали критеріям і були включені у метааналіз. Смертність і загальна доза ГЕК 130/0,4 повідомлялися в усіх дослідженнях, проте добовий баланс рідини – лише в 6 дослідженнях з 11.
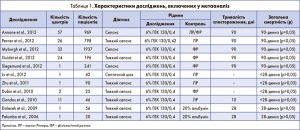
Характеристики досліджень, що увійшли у метааналіз, представлені в таблиці 1. Загалом в цих РКД взяли участь 4408 пацієнтів із сепсисом. ГЕК 130/0,4 порівнювався з лактатом Рінгера, 0,9% розчином NaCl, ацетатом Рінгера або людським альбуміном у якості контролю.
Аналіз методологічної якості досліджень показав, що лише 5 РКД мали низький ризик систематичної помилки за всіма категоріями. Три дослідження, які проводились у Китаї, Аргентині та Італії, мали високий ризик помилки, і ще в трьох РКД цей ризик був помірним.
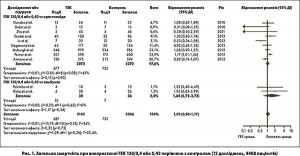
Узагальнений аналіз відношення ризиків (ВР) показав відсутність статистично значущої різниці в загальній смертності у пацієнтів, що отримували ГЕК 130/0,4, порівняно з хворими, яким призначалися контрольні рідини (ВР 1,02; 95% довірчий інтервал 0,90-1,17; р=0,73; I2=34%; рис. 1). В аналізі підгруп ГЕК 130/0,4 так само не асоціювався з підвищеною загальною смертністю порівняно з кристалоїдами (ВР 1,01; 95% ДІ 0,88-1,16; р=0,90; I2=42%) або з альбуміном (ВР 1,64; 95% ДІ 0,72-3,73; р=0,65; I2=0).
В 6 з 11 досліджень повідомлялося про надмірну смертність у пацієнтів групи ГЕК 130/0,4 порівняно з контрольними рідинами (кристалоїдами 4 у РКД і альбуміном у 2 РКД), проте статистична значущість мала місце лише в дослідженні Perner і співавт. (2012). В інших 5 дослідженнях, навпаки, повідомлялося про нижчу смертність у групі ГЕК порівняно з контролем (кристалоїдами в усіх 5 РКД), хоча і без статистичної значущості.
Під час оцінки смертності в загальній популяції було встановлено помірну гетерогенність (I2=34%; р=0,13; рис. 1). У підгрупі з кристалоїдами в якості контрольної рідини спостерігалася значна варіабельність з I2=42% (р<0,1), проте тест підгрупової різниці був статистично незначущим (χ2=1,29; р=0,26; I2=22,4%).
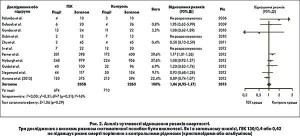
Після виключення 3 досліджень з високим ризиком систематичної помилки аналіз чутливості показав, що узагальнене ВР для ГЕК 130/0,4 стосовно смертності залишилося статистично незначущим порівняно з контрольними рідинами (ВР 1,06; 95% ДІ 0,95-1,17; р=0,29), хоча варіабельність між дослідженнями (I2) зменшилася з 34 до 16% (рис. 2).
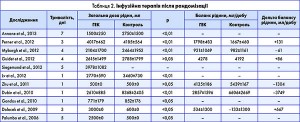
Загальна доза ГЕК 130/0,4 становила від 500±0 мл (упродовж 1 дня) до 4017±462 мл (упродовж 3 днів) (табл. 2). Дельта добового балансу рідини була позитивною (від 86 до 667 мл; тобто більш позитивний добовий баланс у групі ГЕК 130/0,4 порівняно з контролем) у 3 дослідженнях і негативною (від –61 до –3749 мл) у 3 інших дослідженнях (табл. 2). Метарегресійний аналіз не виявив статистично значущого зв’язку між ВР смертності і загальною дозою ГЕК 130/0,4, проте була продемонстрована тенденція до взаємозв’язку «доза-ефект» між дельтою добового балансу рідини і ВР смертності у пацієнтів, які отримували ГЕК 130/0,4.
Тест Еггера показав наявність систематичної помилки, пов’язаної з переважною публікацію досліджень з позитивними або негативними результатами (р=0,31).
Обговорення
На відміну від попередніх метааналізів отримані результати показали, що у пацієнтів із сепсисом ГЕК 130/0,4 не підвищує загальну смертність порівняно з контрольними рідинами (кристалоїдами і альбуміном). Було встановлено помірну гетерогенність в усіх дослідженнях (I2=34; р=0,73) і високу варіабельність у дослідженнях з кристалоїдами (I2=42%; p<0,1). Крім того, метарегресійний аналіз не підтвердив, що загальна призначена доза ГЕК 130/0,4 є джерелом гетерогенності. Цікаво, що таким джерелом могла бути дельта добового балансу рідини, яка з досить високою ймовірністю асоціювалась зі смертністю у пацієнтів, що отримували ГЕК 130/0,4 в цих дослідженнях (р=0,079).
Примітно, що лише в дослідженні Perner і співавт. повідомлялося про статистично значуще підвищення віддаленої (90-денної) смертності у пацієнтів із сепсисом у разі призначення ГЕК 130/0,4 порівняно з контрольними рідинами. Результати цього РКД мали високу вагу у попередніх метааналізах Haase і співавт. (2013) (31,3%) і Patel і співавт. (2013) (47,3%), які дійшли висновків про підвищення ВР смертності у групі ГЕК 130/0,4 (хоча в обох випадках різниця ледь досягла статистичної значущості). В обговорюваному метааналізі розмір вибірки за рахунок додаткових даних був суттєво збільшений (n=4408; 11 РКД) порівняно з метааналізами Haase і співавт. (n=3414; 9 РКД) і Patel і співавт. (n=3033; 6 РКД). Це свідчить про те, що попередні висновки стосовно підвищення смертності у разі застосування ГЕК 130/0,4 були помилковими, оскільки ґрунтувалися на обмежених даних.
Частим джерелом гетерогенності є методологічна якість досліджень. Втім аналіз чутливості, в якому було досягнуто суттєве зниження варіабельності між дослідженнями (I2) з 34 до 16%, показав, що дослідження з високим ризиком систематичної похибки не мали суттєвого впливу на отриманий узагальнений результат (рис. 2). Крім того, метарегресійний аналіз не виявив залежності між смертністю і дозою ГЕК 130/0,4. Це означає, що варіабельність результатів окремих РКД не пов’язана з якістю досліджень або дозою ГЕК 130/0,4 і зумовлена іншими факторами.
Цікаво, що дельта добового балансу рідини (тобто більш або менш позитивний добовий баланс рідини в групі ГЕК 130/0,4 порівняно з контрольною групою) варіював у широких межах від –3749 до +667 мл. На додаток до цього метарегресійний аналіз показав, що дельта добового балансу рідини позитивно корелює з ВР смертності у пацієнтів, які отримували ГЕК 130/0,4. Отже, баланс рідини – безпосередній наслідок інфузійної терапії – з високою ймовірністю був причиною підвищення смертності у групі ГЕК 130/0,4 порівняно з контролем.
Раніше було переконливо продемонстровано, що неадекватний баланс рідини асоціюється з гіршими результатами у пацієнтів с тяжким сепсисом або септичним шоком. Наприклад, в дослідженні за участю 198 відділень інтенсивної терапії (ВІТ) з 24 країн Європи середній баланс рідини в перші 72 год перебування у ВІТ був незалежним фактором ризику смерті у пацієнтів із сепсисом, при цьому з кожним підвищенням кумулятивного балансу рідини на 1 л ризик смерті збільшувався на 10%. В іншому дослідженні було встановлено, що у пацієнтів з негативним балансом рідини значно знижується 90-денна смертність (ВР 0,30; 95% ДІ 0,24-0,43; р<0,0001).
На сьогодні з’являється все більше доказів того, що у пацієнтів, які отримують зайву рідину, з більшою вірогідністю розвиваються ускладнення, пов’язані з перевантаженням рідиною (набряки тканин, дисфункція органів, у тому числі гостра ниркова недостатність, або навіть смерть). Дійсно, неадекватний баланс рідини з високою ймовірністю мав місце в дослідженнях з позитивною дельтою добового балансу в групі ГЕК. Це могло бути обумовленим декількома причинами. По-перше, протоколи інфузійної терапії в цих дослідженнях не були спрямовані на попередження введення зайвої рідини, незважаючи на те що всі протоколи були заявлені як такі, що відповідають рекомендаціям Surviving Sepsis Campaign. Наприклад, у дослідженні Perner і співавт. вихідні рівні центрального венозного тиску, центральної венозної сатурації киснем і лактату в обох групах свідчили про те, що більшість пацієнтів не мали тяжкого дефіциту внутрішньосудинного об’єму, тобто вони були високочутливими до перевантаження рідиною. По-друге, загальний об’єм інфузованої рідини в групі ГЕК був подібним або навіть перевищував такий у контрольній групі. Загалом ГЕК 130/0,4 забезпечує більшу експансію об’єму плазми порівняно з кристалоїдами. Отже, пацієнти з тяжким сепсисом або септичним шоком мали більший ризик отримати зайву рідину в групі ГЕК. По-третє, добова доза ГЕК 130/0,4 і дельта добового балансу рідини не корелювали між собою. Це означає, що причина позитивної дельти балансу рідини полягала не в ефектах ГЕК 130/0,4 на експансію плазми або потенційне порушення ниркової функції (яке може призводити до значного зниження діурезу), а у відсутності стандартизації протоколу стосовно контролю балансу рідини.
Висновки
Нещодавно виникли значні побоювання щодо безпеки розчинів ГЕК, у тому числі ГЕК 130/0,4 або 0,42, які використовуються для інфузійної терапії у пацієнтів із сепсисом. Проте систематичний огляд з метааналізом показав, що ГЕК 130/0,4 або 0,42 не асоціюється з підвищеною смертністю порівняно с контролем. Проаналізовані дослідження відрізнялися гетерогенністю стосовно відносних ризиків, яка була значною в дослідженнях з кристалоїдами як контрольними рідинами. Метарегресійний аналіз не виявив дозозалежного взаємозв’язку між ГЕК 130/0,4 або 0,42 і смертністю, але свідчив про те, що добова дельта балансу рідини з високою ймовірністю асоціюється зі смертністю у пацієнтів із сепсисом, які отримували ГЕК 130/0,4 або 0,42 в цих РКД. Отже, в дослідженнях, в яких порівнювали ГЕК 130/0,4 або 0,42 з контрольними рідинами для об’ємзамісної терапії у пацієнтів із сепсисом, неоднаковий баланс рідини був одним з важливих джерел гетерогенності стосовно ВР смертності.
Список літератури знаходиться у редакції.
Стаття друкується в скороченні.
Ma P. -L., Peng X.-X., Du B. et al. Sources of Heterogeneity in Trials Reporting Hydroxyethyl Starch 130/0.4 or 0.42 Associated Excess Mortality in Septic Patients: A Systematic Review and Meta-regression. Chin Med J (Engl).
2015 Sep 5; 128(17): 2374-2382.
Переклав з англ. Олексій Терещенко