22 березня, 2017
Место сбалансированных инфузионных растворов на основе лактата натрия в современной инфузионной терапии
Данный обзор посвящен проблеме использования сбалансированных полиионных растворов с носителем резервной щелочности – лактатом натрия, их месту в современной инфузионной терапии. Показано, что несмотря на относительно долгий период после открытия первых сбалансированных многокомпонентных солевых растворов с лактатом, они остаются актуальными и востребованными в клинической практике. Появление нового поколения полиионных многофункциональных растворов вызвало значительный интерес в среде клиницистов. Многие работы характеризуют их как эффективные и относительно безопасные лекарственные средства, нашедшие свое место в лечении критических и неотложных состояний.
Выдающиеся открытия в области теоретической и клинической медицины до неузнаваемости изменили и придали ей тот облик, к которому мы быстро привыкли за последние 20-30 лет.
Среди перечня громких побед очень редко упоминается инфузионная терапия, однако можно категорически утверждать, что без нее современной медицины не существовало бы.
Появление инфузионных сред в арсенале лекарственных препаратов дало мощный толчок и открыло новую эру в развитии медицины. Сбалансированные солевые среды берут свое начало с изобретения раствора Рингера в 1882 г. немецким фармакологом-гомеопатом Сиднеем Рингером. Среди созданных растворов с носителем резервной щелочности первый и на многие годы, вплоть до сегодняшних дней, снискавший славу как средство, спасающее жизни, – Рингера лактат (LR) [1].
Только благодаря развитию и доведению до совершенства принципов и методов инфузионной терапии удалось не только поднять до невиданных высот хирургию, но и создать принципиально новую медицинскую специальность – реаниматологию, а также добиться побед над многими заболеваниями, ранее считавшимися неизлечимыми [2].
Вместе с тем практически во всех других медицинских специальностях инфузионная терапия применяется как вспомогательный метод лечения, от которого тоже часто зависит его исход.
На сегодняшний день существует множество различных кристаллоидов, искусственных коллоидов и растворов альбумина, используемых для коррекции нарушений функционирования органов и систем как при критических состояниях, так и с целью профилактики нарушения гомеостаза в организме больного. Инфузионная терапия является агрессивным методом лечения с прямым вмешательством во внутреннюю среду организма. Правила ее проведения четко определены в Британском руководстве по жидкостной терапии 2013 г., что эквивалентно принятому в англоязычной литературе понятию четырех R – Resuscitation (жидкостная ресусцитация), Routine maintenance (рутинная поддержка), Replacement (восстановление патологических потерь), Redistribution (перераспределение жидкости) [3].
Какой должна быть оптимальная инфузионная среда? Tramble и соавт. заявили, что «…оптимальной жидкостью для проведения ресусцитации будет среда, сочетающая в себе свойство расширять и поддерживать внутрисосудистый объем, со способностью, как у крови, переносить кислород, не являться передатчиком трансмиссивных заболеваний. Кроме того, она должна восстановить и поддерживать нормальный состав и распределение жидкости в компартментах организма». Следующий шаг – идеальная жидкость обязана сочетать все вышеперечисленное с положительными иммунологическими и коагуляционными эффектами и быть стабильной, легко воспроизводимой, дешевой в производстве [4]. Все вышесказанное перекликается с современной концепцией Всемирной организации здравоохранения (ВОЗ), согласно которой основные лекарственные средства – это препараты, которые удовлетворяют приоритетные потребности здравоохранения популяции. Данные лекарства отбираются на основании релевантности (необходимости) для общественного здоровья, наличия доказательств эффективности и безопасности, а также сравнительных преимуществ с точки зрения соотношения «затраты – эффективность». Согласно концепции основных лекарственных средств такие препараты должны быть доступны в необходимом количестве, соответствующих (установленных) дозировках и лекарственных формах при наличии гарантированного качества с предоставлением соответствующей (установленной) информации о лекарствах, об их цене, доступной для пациента и сообщества.
Существуют различные классификации инфузионных растворов. В практической медицине наиболее часто используется рабочая классификация, согласно которой все внутривенно инфузируемые среды подразделяются на кристаллоиды, коллоиды, препараты компонентов крови. В Украине современную классификацию препаратов для инфузионной терапии представили Ю.И. Фещенко и М.И. Гуменюк (2010). Она сохраняет функциональность классификации И.Н. Мокеева (1998) и охватывает основные средства для инфузионной терапии [5]. Несмотря на все разнообразие классификаций и обилие препаратов на рынке, стоит отметить, что основной перечень жизненно необходимых лекарственных средств (18-е издание, апрель 2013 г.), утвержденных ВОЗ, в пункте 26.2 указывает на следующие рекомендованные растворы для коррекции водно-электролитных и кислотно-основных нарушений: глюкозу, глюкозу с натрия хлоридом, калия хлорид, натрия бикарбонат, натрия хлорид 0,9% изотонический и сложные растворы натрия лактата, соответствующие формуле LR.
В последние годы четко обозначились современные тенденции в инфузионной терапии – появление новых препаратов и постепенный уход от применения «старых знакомых» – инфузионных средств, эффективность которых считается низкой, а уровень безопасности недостаточным. Так, в группе кристаллоидов все реже используют известные и популярные ранее несбалансированные солевые растворы: дисоль, трисоль, ацесоль. Наблюдается общая тенденция к ограничению введения изотонического (0,9%) раствора натрия хлорида (Normal Saline) и растворов глюкозы. Однако шире используют многокомпонентные сбалансированные растворы кристаллоидов – раствор LR, во многих исследованиях принятый как стандартный раствор, по отношению к которому идут все сравнения.
Избыточное применение солевых растворов для инфузии зачастую приводит к развитию гиперхлоремического ацидоза. Этот вид ацидоза довольно подробно был описан в «British Consensus Guidelines» (2013), посвященном инфузионной терапии у хирургических больных. Инфузионные жидкости, не содержащие физиологическое буферное основание бикарбонат, создают дилюционный ацидоз, поскольку вливание подобного раствора уменьшает концентрацию HCO3– (буферного основания) во всем внеклеточном пространстве, тогда как парциальное давление CO2 (буферной кислоты) остается постоянным. Дилюционный ацидоз предсказуем, определяется как ятрогенное нарушение и логически описывается уравнениями кислотно-щелочного равновесия Хендерсона – Хасселбалха и Стюарта [7, 8]. Разбавление бикарбоната и слабых органических кислот, в том числе лактата, во всем внеклеточном пространстве приводит к гиперхлоремии или гипохлоремии – в зависимости от того, была ли гемодилюция вызвана вливанием гиперхлоремического или гипохлоремического раствора [8, 9].
В связи с тем, что бикарбонат с трудом можно поддерживать в стабильном состоянии в обычных инфузионных растворах или хранить во флаконах, в большинстве растворов он был заменен так называемыми предшественниками бикарбоната [10]. Кроме того, бикарбонат натрия нельзя использовать в инфузионных растворах, содержащих кальций, или смешивать с ним, поскольку быстро образуется осадок карбоната кальция. Дилюционный ацидоз можно предотвратить, используя адекватные концентрации предшественников бикарбоната – метаболизируемых анионов для замещения HCO3–. В качестве метаболизируемых оснований (носителей резервной щелочности) чаще всего используется анион молочной кислоты – лактат натрия, который, помимо всего прочего, является естественным метаболитом. Поглощая в процессе метаболизма ионы H+ и кислород, он метаболизируется в неповрежденной печени с получением HCO3–. Из каждого моля лактата получается один моль бикарбоната [8, 13]. Преимуществами лактата по отношению к другим носителям резервной щелочности являются менее выраженная вазодилатация и, следовательно, лучшая переносимость. Как альтернатива лактата натрия применяется ацетат натрия. Но надо помнить, что, попадая в организм, ацетат метаболизируется в мышечных клетках, поэтому способность организма к метаболизму ацетата напрямую зависит от развитости и функционирования мышечной системы тела. Очевидно, что мышечная масса у больных, длительно находящихся без активного движения, снижается, что затрудняет метаболизм ацетата в организме. Как следствие, возможны гипотония, тошнота и рвота.
В «British Consensus Guidelines on Intravenous Fluid Therapy for Adult Surgical Patients» абсолютно четко указано, что следует применять сбалансированные растворы кристаллоидов, а не солевые. «Из-за риска развития гиперхлоремического ацидоза в обычной клинической практике целесообразно применять лактат/ацетат Рингера, которые должны заменить 0,9% NaCl, кроме ситуаций, способствующих развитию гипохлоремии (например, рвота или большое количество отделяемого по назогастральному зонду). Уровень рекомендаций – 1 b» [12].
Сбалансированные кристаллоиды также широко применяются и имеют такую же эффективность, как и NaCl 0,9%, с точки зрения увеличения объема плазмы. Тем не менее у них действительно есть теоретическое преимущество в том, что они содержат несколько меньшую концентрацию ионов натрия и хлора, в их состав входят ионы калия, кальция. Поэтому применение сбалансированных кристаллоидов имеет приоритет по сравнению с 0,9% натрия хлоридом при использовании в реанимации или рутинной практике. Сбалансированные растворы, содержащие лактат натрия или другие буферы, также могут иметь преимущество в ситуациях с выраженным ацидозом [3, 4, 12].
Такой же тактики придерживаются авторы современных руководств по лечению кровотечений у взрослых [3, 12]: «Мы рекомендуем агрессивную и своевременную стабилизацию сердечной преднагрузки (1В). …Мы рекомендуем коррекцию рН для лечения и предупреждения ацидотической коагулопатии, хотя и коррекция рН самостоятельно не может немедленно исправить ацидозиндуцированную коагулопатию (1С). …Если пациенты нуждаются в инфузионной терапии, целесообразно использование кристаллоидов, которые содержат натрий в диапазоне 130-154 ммоль/л, в виде болюса 500 мл в течение менее чем за 15 мин (LR, раствор Хартмана и др.)».
Исследования O’Malley и соавт. [9] эффективности LR по сравнению с NaCl 0,9% показали, что пациенты во время трансплантации почек, получавшие инфузию LR, не нуждались в дальнейшей коррекции метаболического ацидоза, гиперкалиемии, и такая инфузионная поддержка была более безопасна для пациента. Концентрация бикарбоната была на 3,02 мэкв/л больше (95% доверительный интервал, ДИ 2,00-4,05) в группе LR, pH в среднем был выше на 0,07 ед., уровень иона Cl– в среднем на 9,93 ммоль/л был меньше (95%, ДИ 19,96-0,11), чем в группе NaCl 0,9%. Также было отмечено, что увеличение концентрации хлора на 12 ммоль/л выше нормы приводило к снижению клубочковой фильтрации на 20% и могло быть причиной гипотензии.
Руководство «Intravascular Volume therapy in Adult. Guidelines from the Association of the Scientific medical societies in Germany» (2016) [14] рекомендует использовать сбалансированные кристаллоидные растворы для замещения объема в периоперационном периоде (рекомендация 4а‑4) и с той же целью – в отделениях интенсивной терапии (рекомендация 4b‑4). Изотонический солевой раствор не следует применять для волемической поддержки у пациентов в отделениях интенсивной терапии (рекомендация 6b‑1). Аргументация: применение несбалансированных солевых растворов согласно суррогатным точкам исследований способствует развитию гиперхлоремического ацидоза в течение первых 48 ч после начала терапии (отношение опасности лечения – 0,28; 95% ДИ 0,11-0,70; р=0,006), возникновению смертности и других конечных точек, таких как инфекции и острое поражение почек (р<0,001), а также увеличивает потребность в заместительной почечной терапии (p=0,004). Высказывалось предположение, что гиперхлоремический ацидоз воздействует на гемостаз, функцию желудочно-кишечного тракта и когнитивный статус [8, 15].
LR и нормальные солевые растворы рекомендованы для проведения агрессивной жидкостной ресусцитации при лечении сепсиса у взрослых и детей [16, 17]. Большинство рандомизированных клинических исследований свидетельствуют о том, что внутривенная жидкостная терапия растворами, содержащими менее 120 ммоль/л хлорида, связана с более низкой смертностью, чем жидкостная поддержка растворами, содержащими более 120 ммоль/л хлорида. Рекомендовано использование кристаллоидов без глюкозы с содержанием натрия в диапазоне 131-154 ммоль/л в виде болюса 20 мл/кг менее чем за 10 мин для детей и 10-20 мл/кг в течение 10 мин для доношенных новорожденных.
В зарубежной литературе приводятся указания по лечению травматических поражений, боевых травм и геморрагического шока: жидкостную реанимацию рекомендуется проводить только при систолическом артериальном давлении <80-85 мм рт. ст., продолжающемся кровотечении или угнетении сознания без признаков травмы головы. При геморрагическом шоке кристаллоиды должны быть использованы через два катетера большого диаметра (1А), немедленно (1В), предпочтение отдавать LR / раствору Хартмана в связи с низкой себестоимостью и доступностью во многих странах [18-23].
Начальное жидкостное восполнение (10-20 мл/кг – 300-600 мл/м2) при лечении диабетического кетоацидоза ряд руководств рекомендуют проводить с использованием изотонических нормальных солевых растворов или LR с последующим восполнением в течение 48 ч, эквивалентным 1500 мл/м2 в сутки [24, 25]. «Themanagement of diabetic ketoacidosis in adults (September 2013)» рекомендует для снижения риска развития гиперхлоремического ацидоза использовать сбалансированные инфузионные растворы с обязательным контролем уровня калия. Гиперхлоремический ацидоз вследствие больших объемов NaCl 0,9% может привести к почечной вазоконстрикции и стать причиной олигурии.
Мировое признание, безопасность, эффективность, широкий спектр использования в современных схемах лечения пациентов, нуждающихся во внутривенной инфузионной терапии, обеспечили высокую потребность в растворах, содержащих лактат. Многие мировые фармацевтические корпорации продолжают их выпуск (табл.).
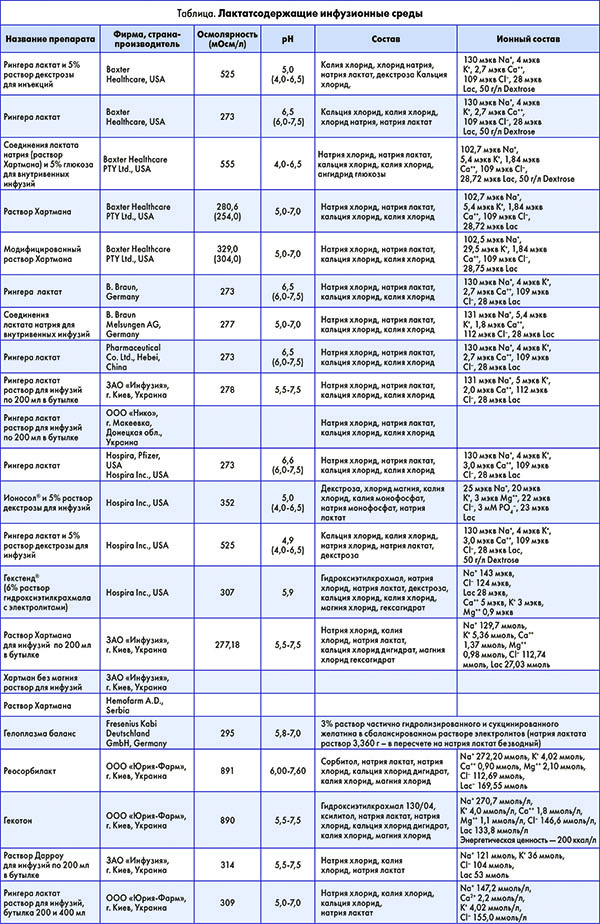
В заключение можно сделать следующие выводы. Современная философия жидкостного восполнения привела к постепенному вытеснению рутинных простых инфузионных сред полиионными сбалансированными и многофункциональными растворами. Происходит переход от традиционного режима инфузионной терапии, основанного на использовании физиологического 0,9% раствора NaCl, к режиму, в котором применяются электролитные растворы, сбалансированные по составу и содержащие носители резервной щелочности. Эта тенденция отражает стремление минимизировать отрицательное влияние на гомеостаз пациента в процессе лечения основной патологии, что не может не находить положительного отклика у врачей любой специальности, так или иначе связанной с проведением инфузионной терапии.
Несмотря на почти что вековую историю, раствор LR остается актуальным и востребованным препаратом, доказавшим свою эффективность, безопасность и незаменимость. Отечественные сбалансированные лактатсодержащие полиэлектролитные растворы полностью отвечают требованиям ВОЗ к средствам, необходимым для жизнеобеспечения. Они демонстрируют в клинических исследованиях высокую эффективность по сравнению с другими кристаллоидами. Все это позволяет современному врачу качественно и дифференцированно подойти к интенсивной терапии экстренных ситуаций и критических состояний.
Список литературы находится в редакции.


