18 липня, 2017
Микробиоценоз слизистой оболочки носоглотки у часто болеющих детей и возможности его коррекции
Острые респираторные вирусные инфекции (ОРВИ), на долю которых приходится более 90% всех болезней респираторной системы у детей, являются важной, социально значимой проблемой [2]. Повторные вирусные инфекции приводят к повреждению цилиарного эпителия слизистой оболочки дыхательной системы, нарушению целостности микробной биопленки, высвобождению большого количества свободных форм латентно персистирующих микробов. Развиваются дисбиотические нарушения, которые сохраняются после перенесенной ОРВИ в течение 1,5-2 мес. С увеличением количества обострений возрастает частота и расширяется спектр высеваемых микроорганизмов. Вторичные по своей природе сдвиги нормальной флоры могут брать на себя патогенетическое лидерство, инициируя развитие повторных респираторных заболеваний [1, 3].
Цель исследования: оценить состав микрофлоры слизистой оболочки носоглотки, определить влияние фитопрепарата Имупрет® на состояние микробиоценоза носоглотки и частоту острых респираторных заболеваний у детей дошкольного возраста.
Материалы и методы
Обследованы 128 детей (средний возраст 4,6±0,3 года). В исследование включались часто болеющие дети в соответствии с критериями, предложенными А.А. Барановым и В.А. Альбицким (1986). В основную группу вошли 57 (57%) мальчиков и 43 (43%) девочки. Контрольную группу составили 28 здоровых детей соответствующего возраста, эпизодически болеющих респираторными инфекциями. Обследование включало общеклинические методы согласно протоколам обследования и лечения данной группы детей. Изучение состава микрофлоры верхних дыхательных путей проводили с помощью общепринятого бактериологического исследования, которое включало посевы отделяемого носоглотки (мазки из зева и носа) на питательные среды. Микробиологическое исследование проводили дважды – в начале исследования и после применения препарата Имупрет® («Бионорика», Германия). Доза препарата соответствовала рекомендациям производителя: по 10 капель перорально 3 раза в день после еды в течение 5 нед. Аллергических реакций и отказов детей (по органолептическим свойствам) от приема препарата не было.
Статистическую обработку полученных данных проводили с использованием прикладных программ Excel, «Статистика 6.0».
Результаты исследования и их обсуждение
Бактериологическое исследование носо- и ротоглотки показало различные изменения микробного пейзажа этих двух отделов верхних дыхательных путей. У 39% детей носоглотка была заселена нормальной для данного биологического локуса микрофлорой. У 61% пациентов качественное и количественное содержание микрофлоры отличалось от нормальных значений. Микробный пейзаж носа был представлен монокультурой дифтероидов – грамположительных палочек группы Corynebacterium (19%), различными видами грамположительных кокков семейства Micrococcaceae: Staphylococcus saprophyticus (27%), Staphylococcus aureus (3%), Staphylococcus epidermidis (1%), а также Streptococcus haemolyticus (1%), Streptococcus viridens (3%) или ассоциациями бактерий группы Corynebacterium и семейства Micrococcaceae (7%). Выраженность дисбиотических изменений слизистой оболочки носа у 54% детей достигала I степени, у 7% – II степени.
Состав микрофлоры ротоглотки характеризовался присутствием большего количества и более разнообразного спектра патогенных бактерий и их ассоциаций. Лишь у 40% детей микробный пейзаж слизистой оболочки ротоглотки был представлен монокультурой бактерий, включая Staphylococcus aureus (12%), Streptococcus haemolyticus (6%) и Streptococcus viridens (22%). У большинства (60%) пациентов со слизистой оболочки ротоглотки выделялись сложные ассоциации бактерий, в состав которых наиболее часто входил золотистый стафилококк (25%). У 21% детей дисбиотические изменения полости ротоглотки были обусловлены комбинацией пневмококка и моракселлы. Грибы рода Candida в ротоглотке были у 8% детей, причем всегда в виде ассоциаций с грамположительными либо грамотрицательными бактериями. По результатам исследования, у детей с нарушениями микробного пейзажа наиболее часто обнаруживали: Staphylococcus aureus, S. viridens, S. haemolyticus, Streptococcus pneumoniae, Moraxella catarrhalis, Escherichia coli, Klebsiella pneumonia, K. ozaenae. В целом, изменения состава микрофлоры слизистых оболочек ротоглотки по степени дисбиотических сдвигов превосходили изменения микробного пейзажа полости носа, у 57% детей они соответствовали I степени дисбиоза, а у 43% – II степени.
С целью коррекции дисбиотических сдвигов в носоглотке, а также с целью иммуномодуляции назначали фитопрепарат Имупрет®. Один курс препарата в течение 5 нед получили 25 (25%) пациентов основной группы, 2 курса с интервалом 3 мес – 28 (28%) пациентов; 22 (22%) часто болеющим детям были назначены 3 курса лечения препаратом в течение года. Группу сравнения составили 25 детей основной группы, которые по различным причинам отказались от приема Имупрета, и 28 здоровых.
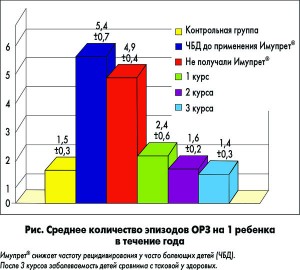
До начала исследования проведен ретроспективный анализ заболеваемости детей исследуемой и контрольной групп за 12 мес. Среднее количество острых респираторных заболеваний (ОРЗ), перенесенных одним ребенком за анализируемый период в основной группе, составило 5,4±0,7, в контрольной группе – 1,5±0,3 (р<0,05). Средняя продолжительность одного заболевания в исследуемой группе – 12,3±0,5 дня, в контрольной группе – 5,9±0,8 дня (р<0,05). Среднее количество дней, пропущенных по болезни одним ребенком в исследуемой группе, составило 52,4±3,5, в контрольной группе – 19,0±2,7 (р<0,05; рис.).
После применения препарата Имупрет® в профилактической дозе получено статистически значимое уменьшение количества случаев заболеваний (р<0,05). После 1 курса лечения число эпизодов ОРЗ на одного ребенка составило 2,4±0,6 дня, после 2 курсов – 1,6±0,2 и после 3 курсов в течение года – не отличалось от таковых в контрольной группе (1,4±0,3). На 46% снизилось и количество дней, пропущенных по болезни на одного ребенка. Таким образом, коэффициент эффективности препарата Имупрет® для профилактики ОРЗ равен 1,7, показатель профилактической защищенности – 41,2%.
Изменения, возникшие после применения препарата Имупрет®, уравняли исследуемые группы по качеству и количеству микроорганизмов, заселяющих слизистую оболочку ротоглотки. Достоверно уменьшилась частота у детей таких микроорганизмов, как S. aureus, коринебактерий, грибов рода Candida, элиминированы S. pneumoniae, S. vestibularis и грибы Aspergillus. Распространенность дисбиоза среди детей после 1 курса лечения препаратом Имупрет® снизилась в 2 раза (р<0,05), после 3 курсов – микробиоценоз слизистой оболочки не отличался от такового у здоровых детей.
Выводы
· Профилактическое назначение препарата Имупрет® у часто болеющих детей достоверно уменьшает число эпизодов респираторных инфекций уже после 1 курса применения, а после 3 профилактических курсов в течение года уровень заболеваемости равен таковому в контрольной группе.
· После применения препарата Имупрет® достоверно уменьшается среднее количество дней, пропущенных по болезни одним ребенком в течение года, с 52,4±3,5 до 22,3±1,9 дня (после 1 курса) и до 12,7±1,7 дня (после 3 курсов).
· Частота дисбиоза среди детей после первого курса применения препарата Имупрет® снизилась в 2 раза (p<0,05), нормализация биоценоза слизистой оболочки ротоглотки отмечена после 3 профилактических курсов.
Литература
1. Романова Ю.М. Бактериальные биопленки как естественная форма существования бактерий в окружающей среде и в организме хозяина / Ю.М. Романова, А.Л. Гинцбург // Журнал микробиологии, эпидемиологии и иммунобиологии. – 2011. – № 3. – С. 99-109.
2. Рябова М.А. Внесезонные ОРВИ – лечение и профилактика / М.А. Рябова // Лечащий врач. – 2011. – № 8. – С. 21-24.
3. Чернова Т.М. Возможности топической терапии тонзиллофарингитов у детей в практике участкового педиатра / Т.М. Чернова [и др.] // Педиатрическая фармакология. – 2012. – Т. 9, № 1. – С. 112-116.
Статья печатается в сокращении.
Семейная медицина, № 2(64), 2016 г.