1 квітня, 2015
Віковий андрогенодефіцит у чоловіків
 Віковий андрогенодефіцит, або пізній гіпогонадизм, – це біохімічний синдром, пов’язаний з віком, який характеризується дефіцитом продукції андрогенів за (або без) зменшення чутливості їх рецепторів, що супроводжується суттєвими змінами якості життя і несприятливим впливом на функцію багатьох органів і систем організму.
Віковий андрогенодефіцит, або пізній гіпогонадизм, – це біохімічний синдром, пов’язаний з віком, який характеризується дефіцитом продукції андрогенів за (або без) зменшення чутливості їх рецепторів, що супроводжується суттєвими змінами якості життя і несприятливим впливом на функцію багатьох органів і систем організму.
Прогресуюче, залежне від віку падіння концентрації тестостерону (Т) спричиняє виражене зниження енергії, втрату гарного самопочуття, порушення статевої функції, ендокринні й метаболічні зміни. Віковий гіпогонадизм асоціюється з вираженим погіршенням якості життя та дисгармонією в стосунках між партнерами.
Частота андрогендефіцитних станів у чоловіків, за різними даними, становить 7-30%. Підвищений ризик розвитку клімактеричних розладів спостерігається у пацієнтів з еректильною дисфункцією, зниженим лібідо, системними захворюваннями, метаболічним синдромом та його складовими, на тлі лікування різними препаратами (глюкокортикоїдами, антигіпертензивними, психотропними). За даними тривалих досліджень встановлено, що відсоток чоловіків зі зниженими та субнормальними рівнями Т в крові (менше 12 нмоль/л) зростає з віком: близько 1% в осіб до 40 років, понад 20% – до 60 років і більше 40% – до 80 років. Згідно з результатами іншого дослідження синдром дефіциту андрогенів спостерігається у 6-12% чоловіків після 45-річного віку, що спричиняє розвиток вікового гіпогонадизму (ВГ). Так, під час обстеження 2162 чоловіків на прийомі у лікарів первинної ланки дефіцит загального Т в крові (менше 10,5 нмоль/л) спостерігався в 39% випадків, причому він становив 34% у 45-54-річних і 50% – у 55-80-річних чоловіків. Детальні дослідження частоти дефіциту Т (менше 12,0 нмоль/л) у чоловіків 20-89 років подекадно засвідчили віковозалежне зростання відсотку чоловіків з андрогенодефіцитом у всіх вікових групах.
Вважають, що в основі розвитку ВГ лежить ураження центральної й периферичної ланок гіпоталамо-гіпофізарно-статевої системи, яке призводить до розвитку змішаного гіпогонадизму.
Тестостерон чинить важливі біологічні ефекти на метаболізм, кістки, м’язи, серцево-судинну систему та мозок. Дія Т забезпечується безпосередньо самим гормоном і його активними метаболітами – дигідротестостероном й естрадіолом.
Передбачають, що вірогідність настання, термін, ступінь прояву андрогендефіцитного стану в чоловіків є генетично детерміновані, оскільки спадкові чинники визначають рівень Т в організмі на 60%. Водночас чинники довкілля (переїдання, малоактивний спосіб життя, професійні й побутові шкідливості, тривале перенапруження, вібрація, шум, радіація, хімічні речовини) суттєво впливають і можуть сприяти більш ранньому розвитку ВГ. Крім того, індекс маси тіла, інсулінорезистентність, хронічні захворювання, прийом лікарських препаратів впливають на синтез і секрецію Т. З’являється все більше робіт, які демонструють зв’язок між зниженням концентрації Т в крові у чоловіків та розвитком метаболічного синдрому і його складових, у першу чергу вісцерально-абдомінального ожиріння, цукрового діабету (ЦД) 2 типу, гіпертензії, гіперліпідемії. За наявності вищеперерахованих захворювань рівень Т в крові у чоловіків на 10-15% нижчий, ніж у загальній популяції аналогічного віку, при цьому швидкість падіння рівня Т у них не відрізняється від такої у здорових чоловіків.
Стан біологічного старіння чоловічого організму супроводжується структурно-функціональними змінами в органах і тканинах з тенденцією до зменшення їх функціональних резервів.
Вікові зміни функціональної активності залоз внутрішньої секреції супроводжуються зниженням продукції та секреції низки гормонів, змінами метаболізму в органах-мішенях. Найважливіші прояви старіння чоловічого організму в цілому визначають вікові зміни в гіпоталамічних структурах центральної нервової системи, які призводять до розвитку порушення психіки й емоціональної сфери, зниження репродуктивної й сексуальної здатності, розумової й фізичної працездатності, рухливості, порушення регуляції гомеостазу і функцій внутрішніх органів.
Одна з найважливіших закономірностей старіння – множинність патологічних процесів, з віком збільшується кількість захворювань у чоловіків. Існує тісний взаємозв’язок між старінням чоловічого організму і такими захворюваннями, як серцево-судинні, артеріальна гіпертензія, ЦД, онкозахворювання, ожиріння. Клімактеричні розлади не лише перебігають на тлі перерахованих захворювань, а й самі створюють преморбідну ситуацію.
Старіння у здорових чоловіків традиційно асоціюється зі зниженням продукції й секреції Т статевими залозами. Вікове падіння рівня Т зумовлене низкою чинників: первинним ураженням тестостеронпродукуючих клітин яєчок, у результаті – зменшення кровопостачання яєчок, зниженням кількості рецепторів на поверхні цих клітин і підвищенням їх резистентності до лютропіну, гормону гіпофіза, який регулює синтез Т; підвищенням рівнів сексстероїдзв’язувального глобуліну й відповідно кількості зв’язаного з ним Т, що призводить до зменшення рівня біологічно активного Т; порушенням співвідношення тестостерон/естрогени та розвитком відносної гіперестрогенії, що є наслідком підвищеної ароматизації андрогенів. Естрогени, що пригнічують секрецію гонадотропінів, додатково зменшують синтез Т в яєчках.
У здорових чоловіків середнього віку приблизно 2% Т циркулює у вільній (активній) формі, 30% – зв’язані з сексстероїдзв’язувальним глобуліном, а 68% – з білком альбуміном.
Встановлено, що з віком у чоловіків спостерігається зниження рівня загального Т в крові на 0,4%, а вільного – на 1,2% на рік.
Дослідженнями, проведеними в ДУ «Інститут геронтології ім. Д.Ф. Чеботарьова НАМН України», було встановлено, що рівень Т в крові суттєво не змінюється до 50-55-річного віку, а потім спостерігається перше вірогідне зниження його рівнів, яке асоціюється з вірогідним підвищенням концентрації прогестерону в крові. Друге значиме падіння рівня Т в крові спостерігалося у чоловіків після 70 років. Було встановлено, що найвища концентрація Т в крові у чоловіків відмічається у віці 20-40 років, причому у 80% обстежених він перевищував 20,0 нмоль/л. Хоча в наступних вікових групах середній рівень гормону вірогідно не зменшувався, у 50% обстежених він був нижчим за 20,0 нмоль/л. Тобто, з віком у чоловіків скорочується варіабельність рівнів тестостерону.
Продукція інших гормонів ендокринної системи також суттєво порушується в разі старіння чоловіків. Спостерігається зниження секреції андрогенів у надниркових залозах. Рівень дегідроепіандростерон-сульфату (ДГЕА-С) у чоловіків 80-річного віку становить 20% від його рівня в крові 25-річних. Встановлено, що ДГЕА-С має антиатерогенні властивості, антиканцерогенну дію, може позитивно впливати на імунну систему, зменшує ожиріння.
Клінічні прояви симптому андрогенної недостатності у літніх чоловіків зумовлені змінами в центральній нервовій системі, серцево-судинній, сечо-статевій і кровотворній системах, опорно-руховому апараті, жировій тканині.
Основні симптоми клімактеричного синдрому у чоловіків
1. Сечостатеві розлади:
– зміни лібідо (ослаблення, зникнення імпульсивності, зниження гостроти та інтенсивності);
– еректильна дисфункція (повільне наставання ерекції, необхідність активної стимуляції, зниження ригідності статевого члена);
– зміни оргазму (ослаблення інтенсивності оргазму і сім’явиділення);
– легка переносимість статевих абстиненцій;
– подовження тривалості фрикційної стадії копулятивного циклу;
– зниження фертильності сперми;
– подовження рефрактерного періоду;
– зменшення природної потреби в еякуляції;
– яєчки піднімаються в мошонці приблизно наполовину і повільніше;
– зниження напруження скелетних м’язів під час статевого збудження;
– полакіурія (не зв’язана з доброякісною гіперплазією передміхурової
– залози).
2. Вегетосудинні розлади:
– раптова гіперемія обличчя, шиї («приливи»);
– коливання артеріального тиску;
– кардіалгії;
– головокружіння;
– відчуття нестачі повітря.
3. Психоемоційні розлади:
– підвищена подразливість;
– швидка втомлюваність;
– ослаблення пам’яті та уваги;
– безсоння;
– депресивні стани;
– зниження загального самопочуття і працездатності.
4. Соматичні розлади:
– зменшення сили і маси м’язів;
– зниження щільності кісткової тканини;
– гінекомастія;
– вісцеральне ожиріння;
– зменшення кількості андрогензалежного волосся;
– стоншення й атрофія шкіри.
5. Лабораторні дослідження:
– зниження рівнів Т;
– підвищення рівнів естрадіолу та сексстероїдзв’язувального глобуліну, підвищення рівнів ліпопротеїнів низької і дуже низької щільності;
– анемія.
Описані симптоми характерні для клінічної картини гіпогонадизму. Інтенсивність симптомів не завжди корелює з рівнем андрогенів у крові. Повний комплекс симптомів зустрічається далеко не у всіх пацієнтів, у кожному випадку поєднання симптомів формує різноманітну клінічну картину. Враховуючи поліморфізм проявів клімактеричного синдрому, розвиток їх на тлі супутніх захворювань, зростає вірогідність звернення пацієнтів до лікарів різних спеціальностей, що вимагає певних навичок у лікарів.
Метаболічні порушення проявляються зменшенням маси тіла та сили м’язів, вісцеральним ожирінням (переважне відкладання жиру в верхній і середній частинах тулуба), прогресуючим остеопорозом.
Встановлено зростання ризику смертності у чоловіків з рівнем Т в крові, меншим за 8,0 нмоль/л, на 68% порівняно з групою чоловіків з нормальним рівнем гормону. Низькі рівні загального і вільного Т в крові обернено пропорційно корелювали з ураженням коронарних артерій у чоловіків незалежно від віку й вісцерального ожиріння. У чоловіків з ангіографічно доказаною хворобою коронарних артерій рівень Т в крові був нижчим порівняно з контролем і відмічалася вірогідна зворотна кореляція між його рівнем та ступенем ураження артерій. Близько 25% чоловіків з підтвердженим ангіографічно ураженням коронарних артерій мали рівні загального Т в крові у межах нижньої границі нормальних коливань, а у 50% рівні гормону були нижчими 11,0 нмоль/л.
Проведеними нами дослідженнями встановлено, що у чоловіків з ЦД 2 типу частота дефіциту Т становила 39%. Водночас у чоловіків з рівнями загального і вільного Т в крові у нижньому квартилі є 4-кратне перевищення випадків ЦД порівнянно з чоловіками з рівнями Т у верхньому квартилі.
Встановлено, що низький рівень Т в крові у чоловіків середнього віку є предиктором ризику розвитку у літніх чоловіків метаболічного синдрому та його захворювань-складових, причому ризик розвитку абдомінального ожиріння у них зростає в 2,7, ЦД 2 типу – в 2,1, артеріальної гіпертензії – в 1,8, гіперліпідемії – в 1,5 раза порівняно з чоловіками з нормальною концентрацією Т в крові. Між тим у літніх чоловіків з абдомінальним ожирінням ВГ діагностується у 52,4%, ЦД 2 типу – у 50%, артеріальною гіпертензією – у 42,4%, гіперліпідемією – у 40,4%. Тобто, ВГ перебігає на тлі захворювань, асоційованих зі старінням і водночас він сам створює преморбідну ситуацію. Більше того, низький рівень Т є предиктором ЦД 2 типу, вісцерально-абдомінального ожиріння, серцево-судинних захворювань. Численними роботами доведений взаємозв’язок між секрецією інсуліну й Т. Інсулінорезистентність є одним із найважливіших патогенетичних чинників розвитку ЦД 2 типу, вісцерально-абдомінального ожиріння й метаболічного синдрому і розвивається до появи клінічної симптоматики. Інсулін бере участь у регуляції секреції андрогенів. Наведені захворювання асоціюються зі старінням чоловічого організму й розвиваються на тлі інволюційних змін, зумовлених падінням рівнів Т. Вважають, що ризик розвитку захворювань, асоційованих з віком, зростає у чоловіків з мутаціями гену андрогенового рецептора. Знайдені кореляційні зв’зки між кількістю повторів CAG (цитозин-аденін-гуанін) у гені андрогенового рецептора, рівнем Т і ризиком ровитку захворювань у пацієнтів старших вікових груп. Можливо, поліморфізм CAG-повторів є одним з пускових механізмів, які призводять до розвитку порушень андрогенного забезпечення організму чоловіка й метаболічних змін.
Спостерігається виражена залежність між частотою гіпогонадизму і частотою еректильної дисфункції у чоловіків, причому за даними
Масачусетського дослідження старіння чоловіків, вона є віковозалежною: виявляється у 40% 40-річних, 48% – 50-річних, 57% – 60-річних і у 67% – 70-річних чоловіків.
Діагностика. Діагноз клімактеричного синдрому в чоловіків має бути підтверджений гормональними й біохімічними дослідженнями, які доводять наявність гіпогонадизму. Постановка діагнозу тільки на основі клінічних симптомів у більшості випадків є важкою і ненадійною.
Необхідність і оптимальний об’єм проведення гормональних досліджень до цього часу є дискусійним питанням. Серед лабораторних методів діагностики провідне місце займає визначення концентрації статевих і гонадотропних гормонів у крові. Забір проб крові бажано проводити в ранкові години – о 8-11 год, причому, зважаючи на пульсуючий характер секреції гормонів гіпофізарно-статевої системи, забір проб крові необхідно проводити двічі з інтервалом у 20-30 хв. Концентрація загального Т в крові, нижча за 8,0 нмоль/л, свідчить про абсолютну андрогенову недостатність.
Якщо рівень гормону нормальний або на рівні нижньої границі нормальних коливань, то ще раз визначають концентрацію Т, лютеїнізуючого, фолікулостимулювального гормонів і пролактину в крові. Вважають, що рівні Т в крові, нижчі за 8,0 нмоль/л, свідчать про абсолютну андрогенну недостатність. Визначення біологічно активного Т і сексстероїдзв’язувального глобуліну є інформативним тестом, але ці аналізи не є рутинними дослідженнями. При визначенні рівнів гормонів у крові бажано забирати дві проби з інтервалом у 15 хв для підтвердження вірогідності результатів.
Визначення рівнів гонадотропінів і пролактину має допоміжне значення, оскільки вони можуть бути як нормальними, так і підвищеними і зниженими. Більш інформативними є функціональні тести (введення препаратів гонадоліберину, кломіфену цитрату, хоріонічного гонадотропіну), які дозволяють уточнити рівень ураження в гіпоталамо-гіпофізарно-статевій системі й резервні можливості окремих ланок системи.
Додаткові методи діагностики включають:
– визначення концентрації в крові дегідроепіандростерон-сульфату;
– біохімічні дослідження крові – визначення глюкози крові, інсуліну, загального холестерину й холестерину ліпопротеїдів, тригліцеридів;
– загальний аналіз крові;
– дослідження щільності кісткової тканини – денситометрію.
Неспецифічність клінічної картини клімактеричних розладів у чоловіків утруднює діагностику цього стану і вимагає проведення диференціальної діагностики з іншими захворюваннями, асоційованими з віковими змінами в організмі, зважаючи на множинність патологічних процесів в організмі старіючих чоловіків.
ВГ є недодіагностованим станом, і необхідні дослідження для розширення знань стосовно цієї патології й чіткої діагностики, що зумовлено декількома обставинами, а саме: симптоми гіпогонадизму неспецифічні і можуть спостерігатися за інших захворювань; відсутність чітких біохімічних критеріїв – якщо рівні Т не є значно нижчими нормальних, то це утруднює інтерпретацію; пацієнти вірять, що симптоми є наслідком старіння організму; інтенсивність симптомів не завжди корелює з рівнем андрогенів у крові; відсутня загальна клінічна усвідомленість наявності ВГ. У частини пацієнтів віком понад 50 років з симптомами андрогенодефіциту спостерігається рівень загального Т, нижчий 12,0 нмоль/л, тобто у частини чоловіків з явними клінічними симптомами андрогенодефіциту рівні загального Т знаходяться в межах нижньої границі коливань рівнів гормону у здорових чоловіків.
Лабораторна діагностика ВГ залишається серйозною проблемою, оскільки немає чітких біохімічних критеріїв діагностики – стандартні рівні Т в крові відрізняються в різних аналітичних лабораторіях, а за даними дослідницьких лабораторій в США показники нижньої границі нормальних коливань гормону варіюють від 4,0 до 15,6 нмоль/л, й різниця становить 450%. Немає чітких і переконливих даних стосовно величини порогових рівнів Т відносно віку чоловіків. Вважають, що з віком порогові величини Т підвищуються.
Тому передбачають, що, хоч у багатьох чоловіків старших вікових груп рівні Т в крові знаходяться в межах нормальних коливань, вони є недостатні для нормального функціонування статевої системи.
Показанням для проведення лікування є клінічні прояви андрогенодефіциту, підтверджені гормональними дослідженнями.
Основна мета терапії – усунення прогресуючої з віком андрогенної недостатності, корекція метаболічних порушень, покращення якості життя чоловіків. Синдром недостатності Т все більше розглядається з точки зору якості життя чоловіків старших вікових груп, і замісна терапія проводиться не тільки з лікувальною метою, а й для підтримання активного, творчого життя, фізичного, інтелектуального і сексуального здоров’я. Цілями лікування є також відновлення статевої функції (підвищення лібідо, почуття статевого задоволення), попередження або зменшення остеопорозу, вісцерального ожиріння, вегетосудинних і психологічних розладів, відновлення м’язової сили, фізичної активності.
Вік не є лімітуючим чинником початку андрогензамісної терапії (АЗТ) у літніх чоловіків. Необхідно ще раз відмітити, що крім явних медичних показань для АЗТ правомочними вважають і відносні («соціальні») показання, основним з яких є якість життя чоловіків.
АЗТ є базисною, вона переслідує довгострокові цілі й має бути ефективною.
Препарати Т для замісної терапії включають пероральні таблетки й капсули, ін’єкційні препарати короткої і тривалої дії, підшкірні імплантати, трансдермальні пластирі, нашкірні гелі.
Для проведення АЗТ у чоловіків із клімактеричним синдромом необхідно, щоб препарати були ефективними і здатними до відновлення рівня Т до його фізіологічних значень, не створювали супрафізіологічних рівнів Т в крові й не пригнічували продукцію гормонів яєчками, не чинили гепатотоксичний і гепатоканцерогенний вплив на організм, мали повний спектр андрогенної активності, були зручними для введення в організм.
Конкретна тактика лікування, схема АЗТ підбираються індивідуально і залежать від вираженості симптомів, концентрації Т в крові, поставлених цілей терапії й розвитку можливих побічних ефектів. Введені дози Т мають бути достатніми для підтримання рівнів гормону в межах фізіологічних коливань і не досягати супрафізіологічних концентрацій.
Позитивні ефекти прийому препаратів Т визначаються за динамікою клінічних проявів клімактеричного синдрому й лабораторних показників:
– підвищення лібідо та сексуальної задоволеності;
– покращення загального самопочуття, зменшення подразливості, втомлюваності, депресії;
– зменшення вираженості або зникнення вегетосудинних проявів;
– зниження маси тіла, зменшення вісцеральної й підшкірно-жирової тканини, збільшення м’язової маси та сили; підвищення щільності кісткової тканини;
– зниження рівнів атерогенних ліпідів, підвищення чутливості до інсуліну.
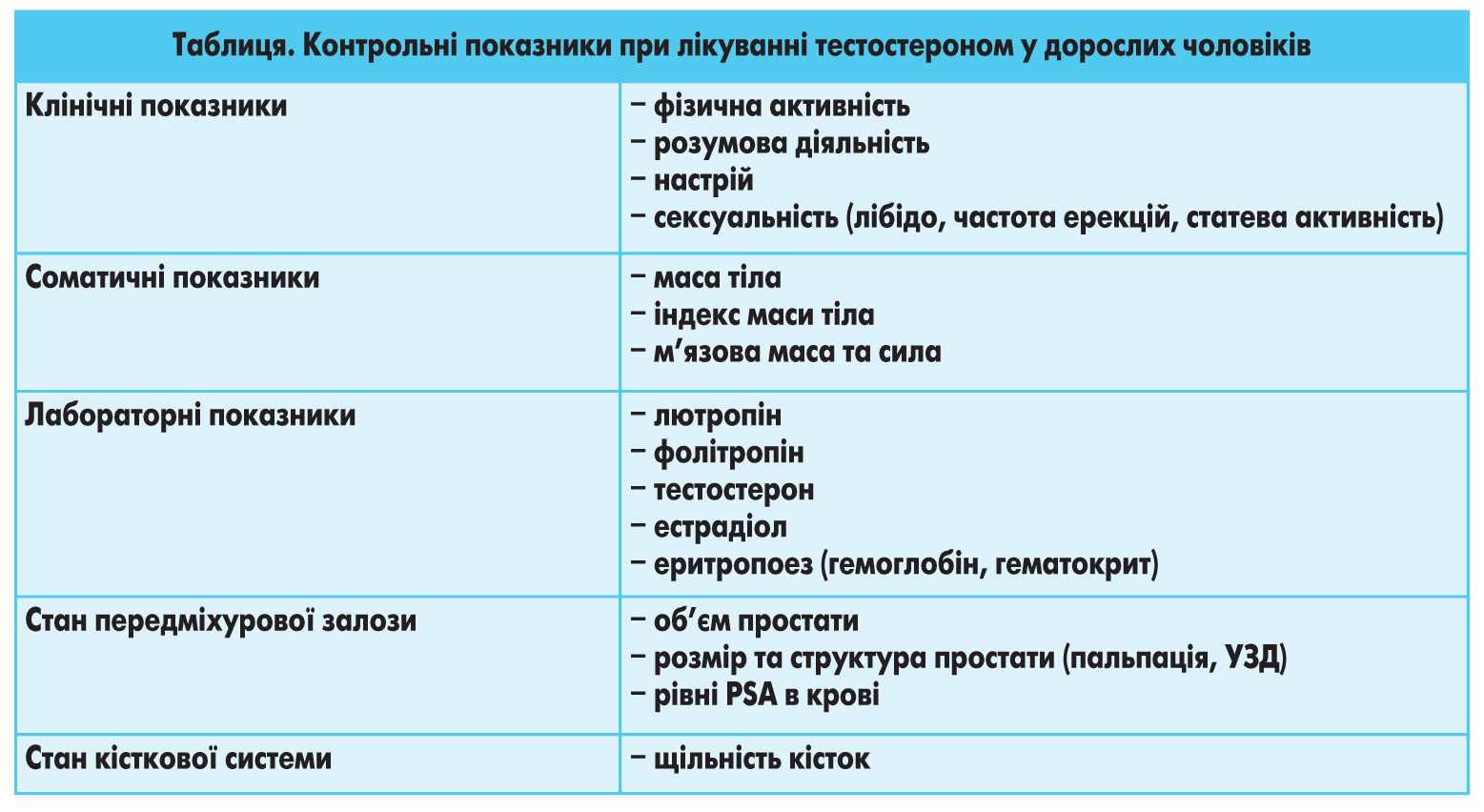
Оскільки прийом препаратів Т може бути тривалим, з метою моніторингу ефективності тестостеронзамісної терапії у чоловіків літнього віку необхідно визначати контрольні показники. Ефективність АЗТ у літніх пацієнтів визначають за динамікою клінічних симптомів та лабораторних досліджень.
Моніторинг у літніх чоловіків, які приймають АЗТ, здійснюється протягом усього терміну терапії, причому моніторування має бути пристосоване до показань та індивідуальних потреб пацієнта. Протягом першого року АЗТ моніторинг здійснюється 1 раз на 3 місяці, а пізніше – 1 раз на 6 місяців.
АЗТ у літніх чоловіків зумовлює підвищення сексуальної активності, покращення настрою і загального самопочуття, зменшення маси тіла, вісцеральної й підшкірної жирової тканини, збільшення м’язової маси та сили, підвищення щільності кісткової тканини, зниження рівня атерогенних ліпідів, підвищення чутливості до інсуліну.
Курс лікування препаратами тестостерону протягом трьох місяців у чоловіків з ЦД 2 типу та помірною андрогенною недостатністю призводить до зменшення маси тіла, коефіцієнту ОТ/ОС, маси жирової тканини, виражено покращує метаболічний контроль (знижується рівень HbА1с, причому не відмічалися побічні впливи АЗТ на гематологічні, біохімічні й ліпідні параметри.
Тривалий прийом Т у чоловіків з ЦД 2 типу і низьким рівнем Т підвищує інсулінову чутливість, зменшує рівень глюкози натще, індекс НОМА і рівень лептину, холестерину і тригліцеридів у крові.
Замісна терапія андрогенами у чоловіків з гіпогонадизмом і серцевою патологією чинить протекторний ефект на серцево-судинну систему через метаболічні зміни і прямий вплив на судини.
Підвищення рівня Т на одне стандартне відхилення приводить до вираженого зменшення ризику розвитку метаболічного синдрому. У групі пацієнтів, у яких спостерігалося більше підвищення рівнів Т, мала місце й редукція жирової маси в печінці (зменшення стеатозу). У обстежених чоловіків, які тривалий час приймали Т, не відмічалися зміни рівнів простатичного специфічного антигену (РSA).
Замісна терапія препаратами Т відновлює еректильну функцію у чоловіків з метаболічним синдромом і низькими рівнями Т в крові. Більше того, стандартна АЗТ покращує статеву функцію у чоловіків не тільки з рівнями Т в крові, меншими 7,0 нмоль/л (2,0 нг/мл), а й із рівнями Т в крові 7,0-12,0 нмоль/л (2,0-3,4 нг/мл). Hа ефект лікування впливає тип препарату Т, коморбідні стани (вісцеральне ожиріння, ЦД 2 типу, артеріальна гіпертензія, дисліпідемія).
Абсолютним протипоказанням для АЗТ є підозра або наявність у пацієнта раку передміхурової або грудної залози.
Прийом екзогенних препаратів необхідно призначати з урахуванням захворювань печінки у пацієнтів.
Обов’язковий моніторинг і спостереження кардіолога необхідні у чоловіків літнього віку з серцево-судинними захворюваннями.
Рідко АЗТ може призводити до розвитку гінекомастії, яка проходить у разі корекції дози Т.
Застосування екзогенних препаратів тестостерону може призводити до розвитку поліцитемії, тому необхідне періодичне визначення гематокриту і зниження дози препарату, якщо він перевищує 52%.
АЗТ може викликати апное (асфіксію) уві сні, але на цей час це питання є спірним.
Дуже рідко у чоловіків при прийомі АЗТ спостерігається затримка рідини в організмі.