1 жовтня, 2017
Феномен Рейно, дигитальные язвы и критическая ишемия при системной склеродермии: современные взгляды на проблему и менеджмент
Системная склеродермия (ССД) – это системное заболевание соединительной ткани, которое характеризуется фиброзом, повреждением сосудов и иммунологическими отклонениями с различной степенью вовлеченности внутренних органов. Несмотря на то что часто ССД клинически подразделяются на два подтипа по степени поражения кожи – диффузный и ограниченный (лимитированный), феномен Рейно и его осложнения являются универсальными признаками заболевания, которые встречаются более чем у 95% пациентов [19]. Хорошо известно, что ангиопатия при ССД вызывает нарушения микроциркуляции с ишемией органов, активацией фибробластов и последующим развитием обширного фиброза [3]. В связи с этим феномен Рейно является потенциально опасным симптомом, поскольку он довольно часто прогрессирует вплоть до изъязвлений (у 50% пациентов), приводя к гангрене конечности [12].
Серьезность ситуации связана с формированием структурных нарушений и функциональных сосудистых аномалий при феномене Рейно в рамках ССД в отличие от первичных (идиопатических) форм данного феномена, когда сосудистые отклонения являются полностью обратимыми и никогда не прогрессируют до необратимой травмы тканей. Таким образом, дигитальная васкулопатия является одним из факторов, приводящих к хронической ишемической боли и инвалидности у пациентов с ССД.
Первичный феномен Рейно является временным обратимым вазоспастическим явлением. Феномен Рейно представляет собой эпизоды преходящей ишемии вследствие вазоспазма артерий, прекапиллярных артериол и кожных артериовенозных анастомозов под влиянием холода и эмоционального стресса [5]. Чаще всего он затрагивает пальцы рук и ног, кончики ушей, нос и соски [27]. Как правило, изменения цвета кожи претерпевают три фазы: начальная бледность, цианоз и эритема как выражение компенсаторной вазодилатации. Клинические проявления феномена Рейно можно сгруппировать следующим образом [1]:
- наиболее часто изменения окраски наблюдаются на пальцах кистей;
- изменения начинаются на одном пальце, в дальнейшем распространяются на другие пальцы и становятся симметричными на обеих кистях;
- наиболее часто вовлекаются II-IV пальцы кистей, большой палец обычно остается нетронутым;
- изменение окраски кожи может отмечаться и на других участках – ушные раковины, кончик носа, лицо, над коленями;
- во время атак Рейно возможно появление сетчатого ливедо на конечностях, которое проходит после завершения вазоспазма;
- в редких случаях наблюдается поражение языка, что проявляется его онемением и преходящими нарушениями речи (речь становится невнятной, смазанной);
- значительная часть больных предъявляют жалобы на сенсорные нарушения (онемение, покалывание, боль) во время атаки.
Распространенность феномена Рейно составляет менее 10% в общей популяции [21]. N.A. Flavahan (2015) [8] в недавнем обзоре акцентирует внимание на терморегуляторных механизмах как основе для понимания феномена Рейно, подчеркивая роль артериовенозных анастомозов и повышенной активности α2-адреноблокаторов в снижении кровотока.
Феномен Рейно при ССД является следствием структурных и функциональных сосудистых нарушений с выраженной пролиферацией интимы дистальных артерий конечностей (дигитальных артерий). Сосудистые изменения имеют двоякий характер. С одной стороны, значительная пролиферация и фиброз интимы, эндотелиальное повреждение приводят к усилению высвобождения сосудосуживающих медиаторов и одновременному снижению уровней сосудорасширяющих молекул. С другой стороны, частые эпизоды вазоспазма приводят в конечном итоге к прогрессирующей ишемии тканей, продукции свободных супероксидных радикалов и еще больше усиливают патологические изменения в тканях [14]. Патофизиология феномена Рейно связана со сложными механизмами и предполагает взаимодействие между сосудистыми, внутрисосудистыми факторами и механизмами нервного контроля.
Диагноз феномена Рейно устанавливается в первую очередь на основании жалоб и клинических симптомов и считается достоверным при положительном ответе на три следующих вопроса [1]:
- Отмечается ли необычная чувствительность пальцев к холоду?
- Изменяется ли цвет пальцев под воздействием холода?
- Становятся ли они белыми и/или синеватыми?
При положительном ответе на все три вопроса диагноз феномена Рейно является достоверным.
Вторичный феномен Рейно наиболее часто встречается при системных заболеваниях соединительной ткани с наибольшей распространенностью при ССД (до 95% случаев), а также при системной красной волчанке (около 40%), дерматомиозите в рамках антисинтетазного синдрома (около 25%), ревматоидном артрите (10%). Диагностические критерии первичного и вторичного феномена Рейно представлены в таблице 1 [18].

Принято считать, что изъязвление кончиков (подушечек) пальцев является следствием ишемии, тогда как изъязвление на разгибательной поверхности пальцев имеет «травматический» характер. До сегодняшнего дня мы не обладали достаточным количеством доказательств данной теории [13]. Однако исследование B. Ruaro и соавт. (2015) [22], включившее 20 пациентов с ССД и язвами пальцев, продемонстрировало достоверное снижение кровотока в месте образования язв пальцев и улучшение его при заживлении. Ишемизация тканей также лежит в основе развития остеолиза, преимущественно ногтевых фаланг [2].
Возможности прогнозирования развития дигитальных язв имеют огромное клиническое значение, поскольку это позволит выделить группу пациентов, требующих целенаправленных профилактических воздействий. За последнее время в ходе нескольких исследований были описаны предикторы изъязвлений при ССД и прогностические факторы. В большом проспективном исследовании (n=623) с участием пациентов с ССД было установлено, что к наиболее сильным факторам риска развития новых дигитальных язв в течение последующих 6 мес относятся: плотность капилляров на среднем пальце доминирующей руки (анормальная капилляроскопическая картина), число язв пищеварительного тракта и наличие исходной критической ишемии [7]. К другим предикторам изъязвлений кончиков пальцев следует относить наличие антител к топоизомеразе (anti-Scl-70) [16, 29], наличие антител к рецептору типа А эндотелина-1 (ЭТ-1) [23], увеличение циркулирующих уровней ЭТ-1, а также тяжесть изменений термографии [4]. В систематическом обзоре PRISMA I. Silva и соавт. (2015) [24] суммировали факторы риска развития дигитальных язв, которыми являются: подтип диффузного поражения кожи при ССД, ранний дебют феномена Рейно, наличие антител к топоизомеразе (anti-Scl-70), анормальная картина капилляроскопии, повышение уровней ЭT-1 и низкий уровень фактора роста эндотелия сосудов (VEGF).
Одновременно признается, что наличие дигитальных язв связано с тяжелым течением болезни и даже повышенной смертностью. В многофакторном анализе 3196 пациентов из базы данных EUSTAR история дигитальных язв была достоверным прогностическим фактором смерти [20].
Механизм развития дигитальных язв при ССД объясняется несколькими факторами, которые включают повторяющиеся микротравмы, истончение кожи, ее сухость и наличие кальциноза. Считается, что 8-12% язв возникают на основе кальциноза кожи и подкожной клетчатки. Однако длительная ишемия вследствие феномена Рейно является наиболее важным механизмом [21]. Дигитальные язвы различаются размерами и границами, наличием обнаженных тканей (кость, сухожилие), кальциноза тканей. Язвы считаются острыми до 3 мес, хроническими – более 6 мес. Клинические исходы язв зависят от многочисленных факторов. Потеря мягких тканей и костей наблюдается примерно у 30% пациентов с ССД и дигитальными язвами. В ходе 7-летнего мониторинга осложнений у больных с язвами в 11% случаев выявлена гангрена; при неэффективности или отсутствии лечения, наличии рецидивирующих ишемических атак развитие гангрены впоследствии наблюдалось у 100% больных [25]; 12% пациентов с дигитальными язвами требовали госпитализации и хирургического вмешательства.
Критическая ишемия конечностей при ССД является ургентным состоянием и требует неотложных мероприятий. Поскольку в основе развития критической ишемии лежит необратимая ишемия (в отличие от феномена Рейно), то этот процесс может быстро привести к гангрене конечности и возможной потере пальцев. На рисунке 1 (а, б, в) представлены фотографии пациентов с дигитальными язвами и развившейся критической ишемией на фоне ССД.
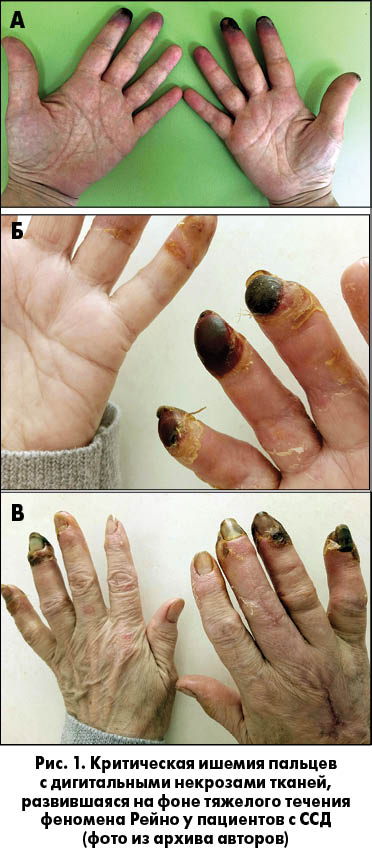
Возникновение критической ишемии сопровождается сильной болью, что иногда даже требует применения наркотических аналгетиков. Малейшие прикосновения и движения вызывают боль. Появлению критической ишемии предшествуют изменения окраски пальцев, стойкое побеление, позже посинение, возникает граница между «синей» и «белой» зонами пальцев. Обычное согревание рук не оказывает никакого положительного воздействия (что, возможно, было эффективно ранее). Обычно критическая ишемия развивается во II-IV пальцах рук. Несмотря на то что в основе васкулопатии при ССД лежит вазоокклюзионная болезнь, быстрые и решительные действия обладают реверсионным потенциалом и способны предупредить потерю мягких тканей и даже пальцев.
Ведение пациентов с феноменом Рейно, дигитальными язвами / некрозами при ССД включает нефармакологические, фармакологические подходы и хирургическое вмешательство (табл. 2). Используемые нефармакологические модальности включают избегание триггеров, провоцирующих эпизоды ишемии, в том числе холодовой контакт, эмоциональный стресс или лекарства, способствующие сужению сосудов, включая β-адреноблокаторы, антимигренозные препараты (такие как суматриптан и эрготамин), пероральные контрацептивы, некоторые химиотерапевтические агенты (такие как цисплатин, винбластин, таргетные блокаторы тирозинкиназы, др.) и амфетамины. Прекращение курения абсолютно необходимо для предотвращения дальнейшего сосудистого повреждения уже уязвимой ишемизированной ткани.

Вазоактивные методы терапии являются центральными в фармакологическом лечении сосудистых осложнений ССД. Е. Hachulla и соавт. (2007) [10] сообщают, что вазодилатационная терапия значительно задерживает развитие дистальных изъязвлений (отношение рисков, ОР 0,17; 95% доверительный интервал, ДИ 0,09-0,32).
Блокаторы кальциевых каналов (БКК) мало изучены в лечении/профилактике дигитальных язв, хотя многие клиницисты используют препараты этой группы (чаще всего нифедипин) в лечении тяжелого феномена Рейно [14]. В рандомизированном двойном слепом исследовании сравнивали пероральный нифедипин (30 мг ежедневно в течение 4 нед, а затем 60 мг ежедневно в течение 12 нед) и внутривенное введение илопроста для лечения тяжелого феномена Рейно. Согласно полученным результатам среднее количество дигитальных язв было уменьшено с 4,3 до 1,4 после 16 нед лечения нифедипином. При применении илопроста число дигитальных поврежений уменьшилось с 3,5 до 0,6. Повышение температуры рук и улучшение микроциркуляции было отмечено только при применении илопроста.
Несмотря на то что существует достаточно сильное терапевтическое обоснование роли ингибиторов ангиотензинпревращающего фермента (АПФ) при ССД и сосудистых осложнениях в качестве агентов ремоделирования сосудов (как и у пациентов с ишемической болезнью сердца), в настоящее время отсутствует доказательная база, подтверждающая эффективность этого вмешательства. В многоцентровом двойном слепом рандомизированном клиническом испытании, включавшем 210 пациентов с лимитированной ССД или аутоиммунным феноменом Рейно (с наличием специфических склеродермических аутоантител), трехлетнее лечение квинаприлом не ассоциировалось со значительным уменьшением числа новых дигитальных язв (ОР -0,08; 95% ДИ от -0,23 до 0,06) [9].
Ингибиторы фосфодиэстеразы 5 типа (ФДЭ-5) ингибируют деградацию (и, следовательно, увеличивают биодоступность) циклического гуанозинмонофосфата (ГМФ) с последующей вазодилатацией. В метаанализе эффективности терапии дигитальных язв, включавшем 31 рандомизированное контролируемое исследование, применение ингибиторов ФДЭ-5 (на основе трех рандомизированных клинических исследований, n=85) ассоциировалось с заживлением язв и улучшением состояния пациентов.
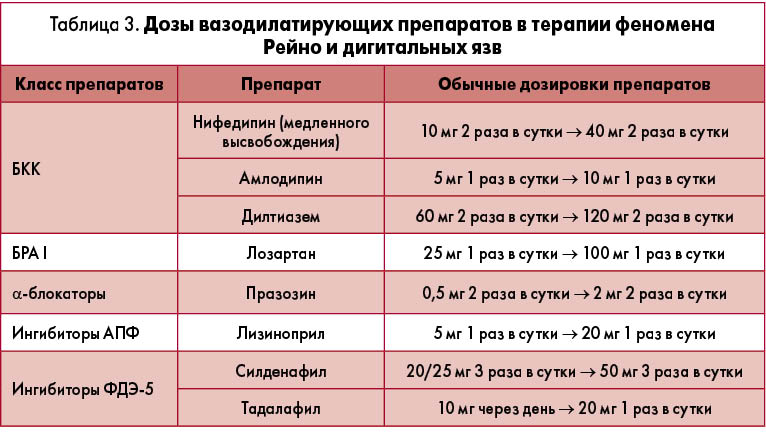
В недавнем многоцентровом двойном слепом рандомизированном контролируемом исследовании, в которое включили 84 пациента, лечение силденафилом в течение 12 нед сопровождалось значительным сокращением числа новых дигитальных язв (0,86 против 1,51). Тем не менее время заживления этих язв (основная конечная точка исследования) не уменьшалось [11]. Три коммерчески доступных ингибитора ФДЭ-5 включают силденафил, варденафил и тадалафил. Силденафил и варденафил имеют более короткий период полураспада – около 4 ч, в то время как период полувыведения тадалафила намного дольше – в течение 18 ч. Дозы оральных вазодилатирующих препаратов, которые наиболее часто используются в терапии феномена Рейно и его осложнений, представлены в таблице 3.
Простаноиды являются мощными вазодилататорами, а также ингибируют агрегацию тромбоцитов и пролиферацию клеток гладких мышц сосудов. Илопрост, одобренный в Европе для лечения дигитальных язв, связанных с ССД, представляет собой химически стабильный аналог простациклина с двойным вазодилататорным и тромбоцитарным эффектами [6]. Илопрост является синтетическим аналогом простациклина, вызывает подавление агрегации и активации тромбоцитов, дилатацию артериол и венул, повышает плотность капилляров и снижает повышенную сосудистую проницаемость, обусловленную медиаторами, такими как серотонин и гистамин, в системе микроциркуляции; активирует эндогенный фибринолиз, обеспечивает противовоспалительный эффект, подавляет адгезию и миграцию лейкоцитов после повреждения эндотелия, а также накопление лейкоцитов в ишемизированных тканях.
При внутривенном введении простаноидов отмечается достаточно высокая частота побочных эффектов и плохая переносимость препаратов, включая системную гипотензию, головокружение, приливы, желудочно-кишечные расстройства, боль в челюсти и миалгию, что отмечается у 92% пациентов.
Внутривенную терапию простаноидами следует рассматривать при рефрактерном течении феномена Рейно, особенно у пациентов с генерализованной формой ССД и в холодное время года. Наиболее часто используется внутривенный илопрост (3-5 дней лечения со скоростью 0,5-2 нг/кг/мин в течение 6 ч, повторные курсы каждые 4/6/8 нед в течение 52 нед) и эпопростенол.
Сообщалось также о внутривенной терапии простаноидами для улучшения заживления дигитальных язв и сокращения количества новых. В двух мультицентровых двойных слепых рандомизированных исследованиях внутривенная терапия простаноидами (илопрост 0,5-2,0 нг/кг/мин в течение 6 ч в течение 5 дней подряд) была связана со значительно большим заживлением дигитальных язв, чем в группе плацебо [28].
В тяжелых случаях течения васкулопатий, при рецидивирующих незаживающих язвах пациенты должны получать повторные курсы простаноидов; непрерывные или расширенные курсы внутривенной терапии следует рассматривать в клинически тупиковых ситуациях [15].
Необходимо отметить, что пероральные препараты простаноидов (илопрост, а также новые препараты – берапрост, цизапрост, трепростинил) не продемонстрировали какого-либо улучшения в заживлении дигитальных язв [26]. Другие аналоги простагландина – алпростадил – реже применяются в лечении феномена Рейно и дигитальных язв.
Празозин как антагонист α1-адренергического рецептора в двух рандомизированных исследованиях продемонстрировал благоприятное влияние на течение феномена Рейно [30]. Сообщалось, что применение празозина в дозе 1 мг 3 раза в сутки способствует улучшению течения заболевания и прогноза по сравнению с плацебо и сопряжено с меньшим количеством побочных эффектов по сравнению с использованием более высоких доз. К сожалению, опубликованных данных о его влиянии на дигитальные изъязвления очень мало.
Местные нитраты использовались для улучшения локального кровотока, однако относительно сложное применение и потенциальные побочные эффекты уменьшили энтузиазм в отношении их регулярного использования.
ЭТ-1 является не только мощным вазоконстриктором, но и оказывает выраженное пролиферативное действие на гладкомышечные клетки и фибробласты, действуя через два рецептора (ЭТA и ЭТB) [26]. В целом ЭТA и ЭТB, обнаруженные в клетках гладких мышц, способствуют вазоконстрикции и гиперплазии, в то время как ЭTB, который также находится на эндотелиальных клетках, способствует вазодилатации.
Бозентан является двойным антагонистом рецепторов ЭТ-1, лицензированным в Европе для лечения легочной артериальной гипертензии (ЛАГ) и профилактики рецидивирующих дигитальных язв. Два крупных многоцентровых двойных слепых рандомизированных контролируемых исследования продемонстрировали, что лечение бозентаном значительно сократило количество новых изъязвлений [17]. В рандомизированном двойном слепом плацебо-контролируемом исследовании влияния бозентана на заживление и профилактику ишемических дигитальных язв у пациентов с ССД, включившем 188 пациентов с ССД, 24-недельное применение бозентана (62,5 мг 2 раза в сутки 4 нед и 125 мг 2 раза в сутки) ассоциировалось с 30% снижением количества новых дигитальных язв [17]. Бозентан одобрен в Европе для профилактики дигитальных язв при склеродермии, однако Управлением по контролю качества продуктов питания и лекарственных средств США (FDA) после тщательного анализа одобрен не был. Бозентан может быть важным методом лечения, учитывая его пероральное применение и потенциально уникальную способность предотвращать образование новых дигитальных изъязвлений.
У пациентов с некурабельными упорными дигитальными язвами, рефрактерными к терапии ингибиторами ФДЭ-5 и внутривенным инфузиям простаноидов, антагонисты рецепторов ЭТ-1 могут быть особенно полезными.
На сегодняшний день для лечения ЛАГ в Европе утверждены два новых антагониста рецепторов ЭТ-1: мацитентан и амбризентан, которые проходят исследования в лечении дигитальных язв при ССД.
Кальциноз тканей, окружающих язву, может потребовать хирургической обработки, если другие меры по ее заживлению не увенчались успехом. Дигитальная (ладонная) симпатэктомия может принести значимую пользу пациентам, не ответившим на консервативные методы терапии [15]. Безусловным ограничением является то, что данная методика выполняется в отдельных специализированных хирургических центрах.
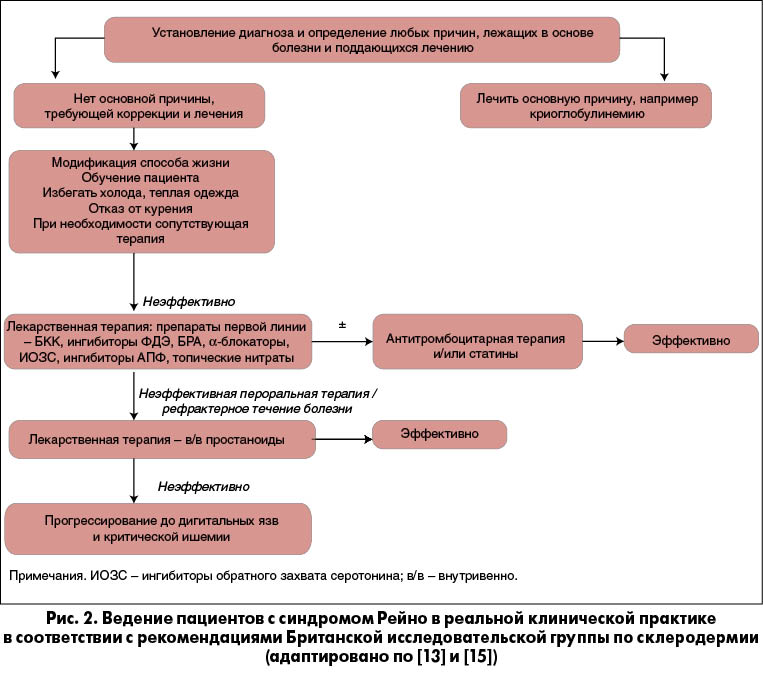
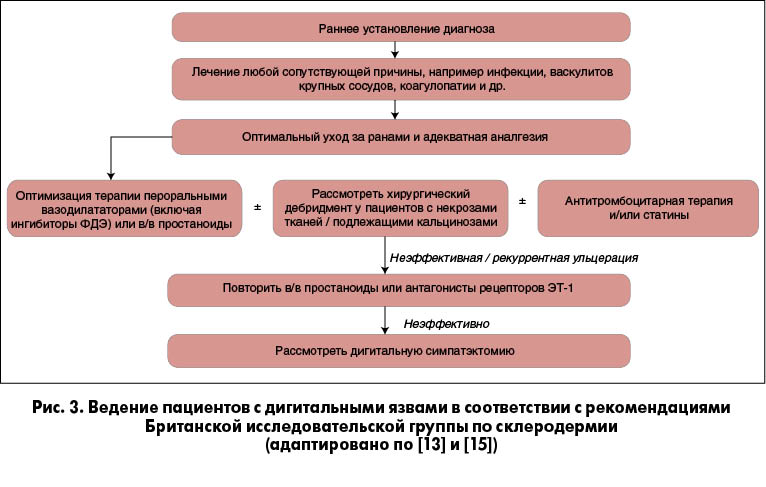
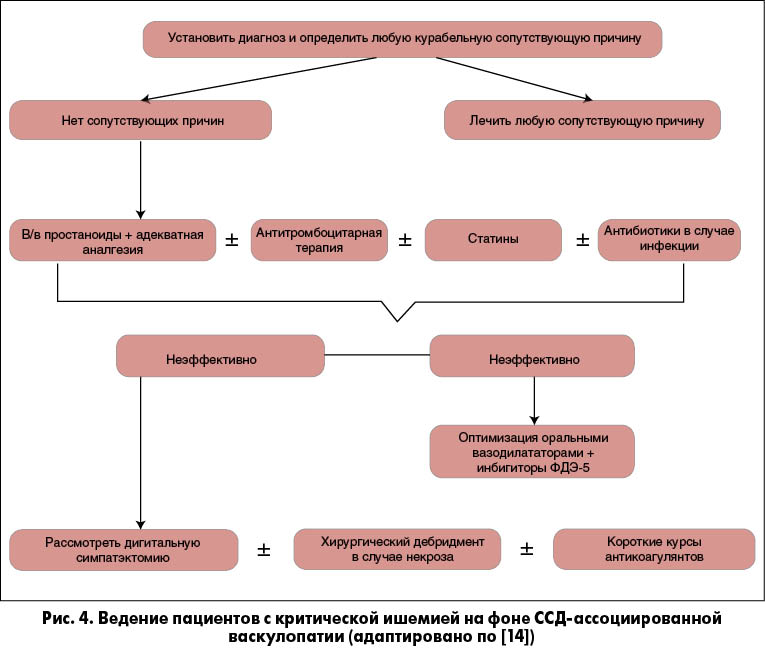
На рисунках 2, 3 и 4 представлены адаптированные рекомендации по ведению пациентов с феноменом Рейно, дигитальными изъязвлениями и критической ишемией. Они представляют ступенчатый вариант усиления терапии в зависимости от эффективности или неэффективности ранее проводимых мероприятий, основанных на передовой клинической практике.
 Таким образом, ССД-ассоциированная васкулопатия является серьезной и актуальной проблемой, которая значительно усугубляет течение ССД. В связи с этим поиск и разработка хорошо переносимых, недорогих, доступных терапевтических вариантов лечения феномена Рейно и его осложнений в виде дигитальных язв остается приоритетным направлением. Использование предложенного многогранного терапевтического подхода для оптимизации ведения пациентов с феноменом Рейно и дигитальными изъязвлениями позволит адекватно курировать таких пациентов и предотвратить образование новых повреждений для обеспечения пациентам достойного качества жизни.
Таким образом, ССД-ассоциированная васкулопатия является серьезной и актуальной проблемой, которая значительно усугубляет течение ССД. В связи с этим поиск и разработка хорошо переносимых, недорогих, доступных терапевтических вариантов лечения феномена Рейно и его осложнений в виде дигитальных язв остается приоритетным направлением. Использование предложенного многогранного терапевтического подхода для оптимизации ведения пациентов с феноменом Рейно и дигитальными изъязвлениями позволит адекватно курировать таких пациентов и предотвратить образование новых повреждений для обеспечения пациентам достойного качества жизни.
Литература
- Алекперов Р.Т. Синдром Рейно как мультидисциплинарная проблема. Альманах клинической медицины. 2014; 35: 94-100.
- Волков А.В., Юдкина Н.Н. Внутривенный илопрост в комплексной терапии сосудистых нарушений у пациентов с системными заболеваниями соединительной ткани. Современная ревматология. 2013; 2: 70-74.
- Синяченко О.В., Егудина Е.Д., Микукстс В.Я. и соавт. Ангиопатия при системной склеродермии. Украинский ревматологический журнал. 2017; 67 (1): 5-11.
- Blaise S., Roustit M., Carpentier P., et al. The digital thermal hyperemia pattern is associated with the onset of digital ulcerations in systemic sclerosis during 3 years of follow-up. Microvasc Res. 2014; 94: 119-122.
- Block J.A., Sequeira W. Raynaud’s phenomenon. Lancet. 2001; 357 (9273): 2042-2048.
- Botzoris V., Drosos A.A. Management of Raynaud’s phenomenon and digital ulcers in systemic sclerosis. Joint Bone Spine. 2011; 78 (4): 341-346.
- Cutolo M., Herrick A.L., Distler O., et al. Nailfold videocapillaroscopic and other clinical risk factors for digital ulcers in systemic sclerosis: a multicenter, prospective cohort study. Arthritis Rheumatol. 2016; 68 (10): 2527-2539.
- Flavahan N.A. A vascular mechanistic approach to understanding Raynaud phenomenon. Nat Rev Rheumatol. 2015; 11: 146-158.
- Gliddon A.E., Dore C.J., Black C.M., et al. Prevention of vascular damage in scleroderma and autoimmune Raynaud’s phenomenon: a multicenter, randomized, double-blind, placebo-controlled trial of the angiotensin-converting enzyme inhibitor quinapril. Arthritis Rheum. 2007; 56 (11): 3837-3846.
- Hachulla E., Clerson P., Launay D., et al. Natural history of ischemic digital ulcers in systemic sclerosis: single-center retrospective longitudinal study. J Rheumatol. 2007; 34: 2423-2430.
- Hachulla E., Hatron P.Y., Carpentier P., et al. Efficacy of sildenafil on ischaemic digital ulcer healing in systemic sclerosis: the placebo-controlled SEDUCE study. Ann Rheum Dis. 2016; 75 (6): 1009-1015.
- Herrick A.L. Management of Raynaud’s phenomenon and digital ischemia. Curr Rheumatol Rep. 2013; 15 (1): 303.
- Herrick A.L. Recent advances in the pathogenesis and management of Raynaud’s phenomenon and digital ulcers. Curr Opin Rheumatol. 2016; 28 (6): 577-585.
- Hughes M., Herrick A.L. Digital ulcers in systemic sclerosis. Rheumatology (Oxford). 2017; 56 (1): 14-25.
- Hughes M., Ong V.H., Anderson M.E., et al. Consensus best practice pathway of the UK Scleroderma Study Group: digital vasculopathy in systemic sclerosis. Rheumatology, 2015; 54: 2015-2024.
- Hunzelmann N., Riemekasten G., Becker M.O., et al. The Predict Study: low risk for digital ulcer development in patients with systemic sclerosis with increasing disease duration and lack of topoisomerase-1 antibodies. Br J Dermatol. 2016; 174: 1384-1387.
- Matucci Cerinic M., Denton C.P., Furst D.E., et al. Bosentan treatment of digital ulcers related to systemic sclerosis: results from the RAPIDS-2 randomised, double-blind, placebo-controlled trial. Ann Rheum Dis. 2011; 70 (1): 32-38.
- Maverakis E., Patel F., Kronenberg D., et al. International Consensus Criteria for the Diagnosis of Raynaud’s Phenomenon. J Autoimmun. 2014; 2: 60-65.
- Meier F.M., Frommer K.W., Dinser R., et al. Update on the profile of the EUSTAR cohort: an analysis of the EULAR Scleroderma Trials and Research group database. Ann Rheum Dis. 2012; 71: 1355-1360.
- Mihai C., Landewе R., van der Heijde D., et al. Digital ulcers predict a worse disease course in patients with systemic sclerosis. Аnn Rheum Dis. 2015; 75 (4): 681-686.
- Nitsche A. Raynaud, digital ulcers and calcinosis in scleroderma. Reumatol Clin. 2012; 8 (5): 270-277.
- Ruaro B., Sulli A., Smith V., et al. Short-term follow-up of digital ulcers by laser speckle contrast analysis in systemic sclerosis patients. Microvasc Res. 2015; 101: 82-85.
- Silva I., Almeida J., Vasoncelos C. A PRISMA-driven systematic review for predictive risk factors of digital ulcers in systemic sclerosis patients. Autoimmunity Rev. 2015; 14: 140-152.
- Silva I., Teixeira A., Oliveira J., et al. Endothelial dysfunction and nailfold videocapillaroscopy pattern as predictors of digital ulcers in systemic sclerosis: a cohort study and review of the literature. Clinic Rev Allerg Immunol. 2015; 49: 240-252.
- Steen V., Denton C.P., Pope J.E., Matucci-Cerinic M. Digital ulcers: overt vascular disease in systemic sclerosis. Rheumatology (Oxford). 2009; 4 Suppl. 3: 19-24.
- Tingey T., Shu J., Smuczek J., Pope J. Meta-analysis of healing and prevention of digital ulcers in systemic sclerosis. Arthritis Care Res (Hoboken). 2013; 65 (9): 1460-1471.
- Wigley F.M. Clinical practice. Raynaud’s phenomenon. N Engl J Med. 2002; 347: 1001-1008.
- Wigley F.M., Wise R.A., Seibold J.R., et al. Intravenous iloprost infusion in patients with Raynaud phenomenon secondary to systemic sclerosis. A multicenter, placebo-controlled, double-blind study. Ann Intern Med. 1994; 120 (3): 199-206.
- Wirz E.G., Jaeger V.K., Allanore Y., et al. Incidence and predictors of cutaneous manifestations during the early course of systemic sclerosis: a 10-year longitudinal study from the EUSTAR database. Ann Rheum Dis. 2016; 75: 1285-1292.
- Wollersheim H., Thien T., Fennis J., et al. Double-blind, placebo-controlled study of prazosin in Raynaud’s phenomenon. Clin Pharmacol Ther. 1986; 40 (2): 219.


