30 жовтня, 2017
Можливості місцевої імуномодулюючої та репаративної терапії в дітей з рекурентними захворюваннями респіраторного тракту і порожнини рота

На сьогодні в усьому світі найчастішою патологією в амбулаторній практиці педіатра та сімейного лікаря є гострі респіраторні інфекції (ГРІ). Розповсюдженість ГРІ становить 18 тис. випадків на 100 тис. дорослого населення, серед дітей цей показник в 3,6 раза вищий – більше 67 тис. випадків на 100 тис. [1, 4].
Основними збудниками ГРІ в дітей є віруси, серед яких переважають риновіруси (30-50%), на другому місці – віруси грипу та коронавіруси (5-15%), на третьому – віруси парагрипу, адено-, ентеро- та метапневмовіруси (5%) [15].
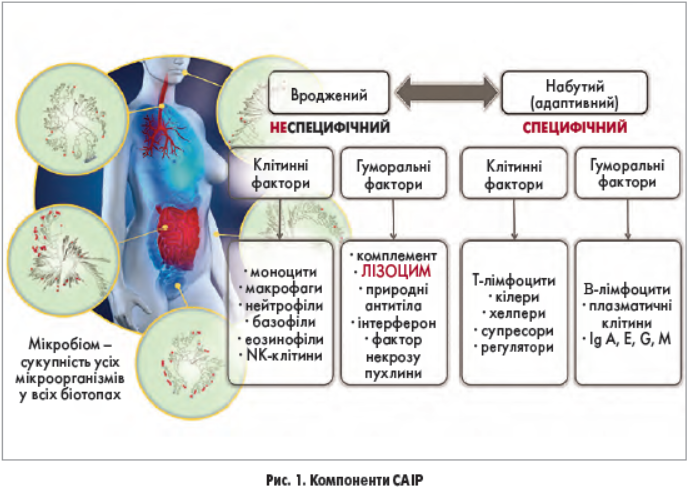
Найчастіше – до 5-7 разів на рік – на ГРІ хворіють діти раннього, дошкільного та молодшого шкільного віку. Схильність до повторних (рекурентних) респіраторних інфекцій (РРІ) у дітей перших 5-6 років життя пов’язана з фізіологічним віковим становленням імунної системи (ІС), особливо місцевого захисту слизових оболонок (СО) носової порожнини та порожнини рота (ПР), які є вхідними воротами для алергенів, харчових і мікробних антигенів [15]. Контроль (імунний нагляд) за підтриманням антигенного гомеостазу організму та рівнем обсіменіння СО носа і ПР різноманітними мікроорганізмами здійснюється системою антиінфекційної резистентності (САІР), яка представлена двома ланками, – мікробіологічною (усі компоненти мікробіому) та імунною (місцеві неспецифічні та специфічні фактори захисту) [5, 10], що схематично зображено на рисунку 1.
Морфофізіологічні та функціональні особливості СО
Для інфекційних агентів СО носа, ПР та глотки є найбільшою за площею контактною біологічною поверхнею (близько 200-250 см2), до складу якої, окрім епітеліоцитів, входять лейкоцити (гранулоцити), клітини Лангерганса, клітини Меркеля (містять гранули з нейромедіаторами, як-от вазоактивний інтестинальний пептид, субстанція Р та ін.). В lamina propria СОПР містяться макрофаги, опасисті, плазматичні і дендритні клітини, лімфоцити. Епітелій взаємодіє з цими клітинами через цито- та хемокіни, а також постійно злущується і швидко регенерує, за рахунок чого реалізує захисну функцію. Епітеліоцити разом із компонентами лімфоглоткового кільця (язичний, піднебінні, глоткові і трубні мигдалики) є морфологічним субстратом взаємодії епітеліоцитів, лімфоїдних і дендритних клітин. СО кореня язика утворює низку коротких слабко розгалужених крипт, у глибині яких відкриваються протоки слизових і дрібних слинних залоз. У криптах міститься величезна кількість мікроорганізмів, злущених епітеліоцитів, лімфоцитів, макрофагів, гранулоцитів. У крипти та інші ділянки СО відкриваються вивідні протоки великих та дрібних слинних залоз. Саме в них секретується sIgA і IgM, лізоцим, лактоферин, пероксидаза, альфа-амілаза, мальтаза, нуклеази; глікозаміноглікани, калікреїн, гормональні речовини і фактори росту, гістатини (мають бактерицидну і фунгіцидну активність проти Streptococcus mutans і Candida albicans), антимікробні пептиди дефензини і кателіцидини тощо. Перелічені захисні фактори в кооперації з представниками мікробіому беруть участь у переключенні імунної відповіді (з Th2 на Th1), забезпеченні толерантності до харчових і мікробних антигенів, управлінні протизапальними механізмами, сприяють формуванню і подальшому підтриманню активності фізіологічного мінімально інтенсивного запалення СО та ефективного функціонування ІС і САІР [10, 17].
Завдяки злагодженому функціонуванню обох ланок САІР здійснюється ефективний захист СО (так званих вхідних воріт) від дії екзогенних мікроорганізмів. Однак у перші 5-6 років життя дитини на тлі становлення мікробіому та ІС існує високий ризик розвитку РРІ та уражень СОПР. Це пов’язано з особливостями функціонування лімфоїдних структур, асоційованих зі СО: низьким рівнем секреторного IgA (sIgA), недостатньою активністю фагоцитозу, функції NK (природних кілерів), хемотаксису нейтрофілів, синтезу інтерферону і лізоциму в ротоглотковому секреті. Тому при рекурентних ураженнях ПР, мигдаликів та глотки доцільно використовувати місцеві лікарські засоби, що впливають на лімфоїдні тканини, асоційовані зі СО (mucosa-associated lymphatic tissue – MALT), через нормалізацію в ротоглотковому секреті специфічних (sIgA) та неспецифічних факторів захисту (альфа- і бета-дефензини, лактоферин, муцин, інгібітори протеолітичних ферментів, глікопротеїни, інтерферон, лізоцим).
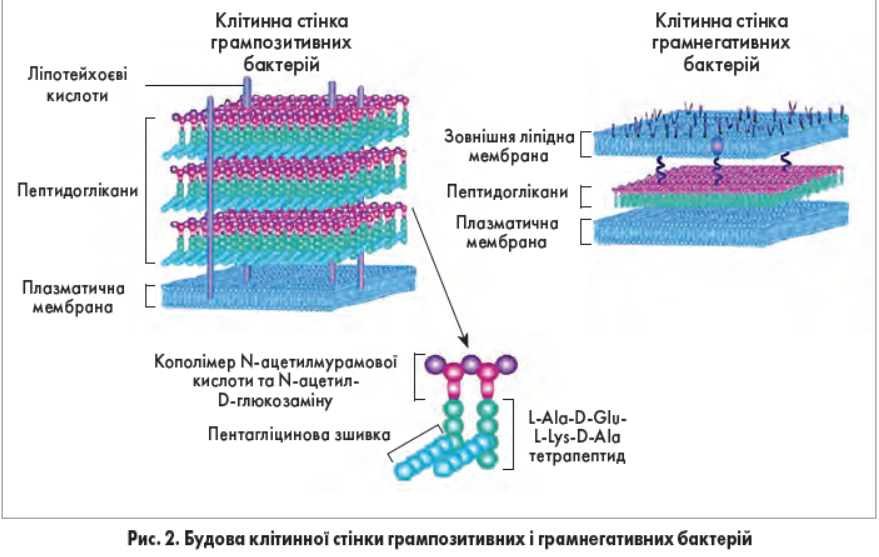
Лізоцим у високій концентрації міститься в слині і в ротоглотковому секреті здорових осіб [19]; він є важливим компонентом першої лінії захисту СО, оскільки бере участь у процесах розпізнавання характерних мікробних субстратів (пептидоглікан та ліпотейхоєві кислоти грампозитивних мікроорганізмів, бактеріальна ДНК, N-формілметіонін, двониткова РНК вірусів, мукополісахариди клітинних стінок грибів та ін.).
Доведено, що продукція лізоциму в організмі посилюється у відповідь на дію мікробних факторів, однак надалі, особливо при рекурентній патології, зростання активності місцевого імунітету змінюється його виснаженням, що потребує відповідної замісної терапії.
Лізоцим (мурамідаза, фермент класу гідролаз), відкритий у 1922 р. Александром Флемінгом [20].
!Лізоцим – природний антибактеріальний ензим, що руйнує клітинні стінки бактерій.
Руйнування клітинної стінки бактерій відбувається за рахунок гідролізу β-глікозидних зв’язків між залишками N-ацетилмурамової кислоти і N-ацетил-D-глюкозаміну, які становлять 50% клітинної стінки грампозитивних і 10% грамнегативних бактерій (рис. 2).
Лізоцим каталізує гідроліз (1,4-β)-глікозидного зв’язку між N-ацетилмурамовою кислотою та N-ацетил-D-глюкозаміном.
Пептидоглікан при цьому зв’язується з активним центром ферменту між двома його структурними доменами. Молекула субстрату в активному центрі набуває конформації, близької до такої перехідного стану. Відповідно до механізму Філіпса лізоцим зв’язується с гексасахаридом, переводить 4-й залишок у ланцюгу в конформацію твіст-крісла; у такому напруженому стані глікозидний зв’язок легко руйнується. При цьому надзвичайно важливими для функціонування ферменту є залишки глутамінової (Glu35) та аспарагінової кислот (Asp52), оскільки Glu35 є донором протона при розриві глікозидного зв’язку субстрату (руйнує зв’язок), а Asp52 відіграє роль нуклеофілу при утворенні проміжного глікозил-ферменту. Згодом глікозил-фермент взаємодіє з молекулою води і повертається у вихідний стан з утворенням продуктів гідролізу [16].
Окрім бактерицидної дії, лізоцим також реалізує противірусні ефекти щодо широкого спектра вірусів, у тому числі герпесвірусів [15]. Відомо, що під дією лізоциму активуються фактори імунітету, які перешкоджають розмноженню вірусів.
На сьогодні не викликає сумніву і антимікотична активність лізоциму [19]. Останній у великій кількості міститься в цитоплазматичних гранулах у макрофагах і поліморфноядерних лейкоцитах, у шкірі, селезінці, печінці, кістковому мозку, підшлунковій залозі, СО травного шляху (ТШ), а також у носоглотковому і травних секретах, слині, сироватці крові, сльозовій рідині та грудному молоці [19]. Зазначимо, що концентрація лізоциму в материнському молозиві і молоці значно вища, ніж у коров’ячому, та продовжує зростати через півроку після початку годування дитини [14]. Це відіграє важливу роль, адже лише до 6 місяців дитина має достатній запас материнських факторів захисту, а їх власна продукція ще є недосконалою [15, 20].
Лізоцим – універсальний неспецифічний фактор захисту, який тісно взаємодіє з іншими гуморальними ланками вродженого імунітету (β-лізин, пропердин та інші компоненти системи комплементу). З’ясовано, що при зниженні останніх зменшується і вміст лізоциму в сироватці крові. Доведено, що лізоцим активує інші компоненти гуморальної регуляції [3]. Місцевий імуномодулюючий ефект лізоциму реалізується завдяки стимуляції синтезу sIgA та потенціюванню активності комплексу sIgA з фракцією С3 системи комплементу. Лізоцим також зменшує проникнення чужорідних антигенів в організм завдяки стимуляції фагоцитозу, що сприяє реалізації функцій макрофагів і Т-лімфоцитів та здійсненню імуномодулюючого впливу.
! Дослідженнями доведено [2], що лізоцим пригнічує вільнорадикальне окислення, а також забезпечує мембраностабілізуючий ефект.
Протизапальні ефекти лізоциму реалізуються завдяки пригніченню калікреїн-кінінової системи та корекції активності α‑1-інгібітора еластази [1, 2].
Зменшення вмісту ендогенного лізоциму спостерігається під впливом забруднення атмосфери, стресів, інфекційних агентів, харчових і медикаментозних ксенобіотиків, алергічних та рекурентних захворювань, асоційованих з інфекціями [8].
Доведено, що дефіцит лізоциму в ТШ призводить до зниження протиадгезивних і біфідогенних властивостей травних секретів та порушення процесів травлення з активацією умовно патогенної мікрофлори і проникненням мікроорганізмів через фізіологічні бар’єри з розвитком ендогенної інфекції в дітей. Низький рівень лізоциму в ТШ є однією з причин хронізації алергічних та гастроентерологічних захворювань у дітей [2, 8].
Лізоцим добре проникає в різні тканини і повільно виводиться. Так, при внутрішньом’язевому застосуванні його максимальна концентрація спостерігається в крові, при інгаляційному – у легенях. У разі перорального прийому лізоцим визначається в сироватці крові і СО. На сьогодні є дані, що підтвердили можливість його використання в комбінації з антибактеріальними засобами для посилення їх протимікробної дії [15].
У медичній практиці використовують лізоцим білка курячого яйця. Існуюча ідентичність фізико-хімічних властивостей та антигенних структур ендогенного (людського) та екзогенного (білка курячого яйця) лізоциму дає можливість використання останнього в якості терапевтичного засобу з мінімальним ризиком виникнення побічних ефектів.
Ефект екзогенного лізоциму залежить не тільки від його дози, але й від функціонального стану організму, активності імунної системи. Стимуляція лізоцимом неспецифічної резистентності [12, 21] найбільш доцільна в дітей груп ризику РРІ та частої патології ПР. Таким пацієнтам слід призначати лізоцимвмісні препарати, зокрема Лісобакт®, який містить лізоциму гідрохлорид у комбінації з водорозчинним вітаміном В6.
Піридоксину гідрохлорид бере участь в обміні глутатіону, забезпечує антиоксидантний захист, зменшує ушкодження клітин, сприяє їх регенерації, контролює запальні реакції на фоні інфекційних процесів, коли потреба в піридоксині значно зростає; недостатність вітаміну В6 проявляється низкою симптомів, у тому числі ураженням СО [9, 13, 18].
При вивченні динаміки стану мікрофлори ротоглотки на фоні терапії Лісобактом реєструється зниження активності факультативних анаеробів, нормалізація балансу аеробів та анаеробів, відновлення процесів протеолізу та муциноутворення, а також нормалізація рівня sIgА в слині, що підтверджує доцільність використання препарату не тільки для лікування [11], а й з метою профілактики РРІ та уражень СОПР у дітей в осінньо-зимовий період [6, 7].
Чим обумовлюється вибір препарату?
По-перше, високим вмістом лізоциму (20 мг).
По-друге, його ефективністю щодо як грампозитивних, так і грамнегативних мікроорганізмів, а також грибів і вірусів та здатністю підвищувати чутливість бактерій до дії антибіотиків.
По-третє, піридоксину гідрохлорид, що входить до складу препарату, прискорює репаративні процеси та реалізує захисну дію на СОПР (попереджує розвиток афтозного і кандидозного стоматиту та ефективний у їх лікуванні).
По-четверте, піридоксину гідрохлорид каталізує процеси трансамінування і декарбоксилювання амінокислот, що сприяє нормалізації рН СОПР і посиленню активності лізоциму.
По-п’яте, доцільно застосовувати місцевий засіб Лісобакт® з огляду на його здатність прискорювати терміни одужання та покращувати якість життя пацієнтів.
По-шосте, використання сучасної технології мікрогранулювання та найменший діаметр льодяника Лісобакту (порівняно з іншими засобами цього напряму) забезпечують хороший комплаєнс.
Лісобакт® (льодяники пресовані) широко використовується в практиці отоларингологів, стоматологів, педіатрів та сімейних лікарів для ефективного лікування ГРІ (фарингіти, тонзиліти, тонзилофарингіти) та уражень СОПР (стоматити, гінгівіти, пародонтити). Після розсмоктування таблетки максимальна концентрація лізоциму в сироватці крові досягається через 1-1,5 години.
Отже, використання препарату Лісобакт® у дітей дає змогу підвищити локальний неспецифічний імунний захист та резистентність СО ротоглотки, прискорити репарацію епітелію, запобігти приєднанню вторинної інфекції, скоротити тривалість лікування. Препарат безпечний, простий у використанні, що обґрунтовує доцільність його включення до класичних схем терапії дітей з РРІ та ураженнями СОПР як у госпітальних, так і в амбулаторних умовах.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 19 (416), жовтень 2017 р.