2 листопада, 2017
Остеопластическая пневмопатия
 Остеопластическая пневмопатия – редкое заболевание неизвестной природы, в основе которого лежит образование в легких участков окостенения. Заболевание встречается крайне редко – в настоящее время в мире зарегистрировано около 200 случаев. Остеопластическую пневмопатию следует отличать от вторичной оссификации легких, образующейся в участках обызвествления в фокусах хронического воспаления (туберкулез, хронический абсцесс легкого и др.), интерстициального фиброза, в стенках сосудов при нарушениях легочного кровообращения.
Остеопластическая пневмопатия – редкое заболевание неизвестной природы, в основе которого лежит образование в легких участков окостенения. Заболевание встречается крайне редко – в настоящее время в мире зарегистрировано около 200 случаев. Остеопластическую пневмопатию следует отличать от вторичной оссификации легких, образующейся в участках обызвествления в фокусах хронического воспаления (туберкулез, хронический абсцесс легкого и др.), интерстициального фиброза, в стенках сосудов при нарушениях легочного кровообращения.
 Этиология заболевания неизвестна. Существуют гипотезы генетической детерминированности остеопластической пневмопатии – описаны семейные случаи заболевания [2, 6]. Вопросы патогенеза разработаны недостаточно. Костная ткань формируется постепенно из соединительной ткани: коллагеновые волокна соединяются в пучки, набухают, гиалинизируются, местами обызвествляются. Замурованные фибробласты претерпевают изменения: уменьшаются в размерах, приобретают угловатую форму. Костная ткань увеличивается в объеме за счет соединительной ткани. В дальнейшем в костные пластинки врастают кровеносные сосуды вместе с рыхлой соединительной тканью, богатой клетками, и дают начало образованию костномозговых полостей с элементами костного мозга [1].
Этиология заболевания неизвестна. Существуют гипотезы генетической детерминированности остеопластической пневмопатии – описаны семейные случаи заболевания [2, 6]. Вопросы патогенеза разработаны недостаточно. Костная ткань формируется постепенно из соединительной ткани: коллагеновые волокна соединяются в пучки, набухают, гиалинизируются, местами обызвествляются. Замурованные фибробласты претерпевают изменения: уменьшаются в размерах, приобретают угловатую форму. Костная ткань увеличивается в объеме за счет соединительной ткани. В дальнейшем в костные пластинки врастают кровеносные сосуды вместе с рыхлой соединительной тканью, богатой клетками, и дают начало образованию костномозговых полостей с элементами костного мозга [1].
Выделяют два гистологических типа легочной оссификации – узелковый и ветвистый [7, 8]. Узелковая форма характеризуется отложениями пластинок остеоидного материала в альвеолярных пространствах, чаще без элементов костного мозга.
 Узелковая форма обычно ассоциирована с заболеваниями сердечно-сосудистой системы, которые приводят к венозному застою крови в системе малого круга (митральный стеноз, хроническая левожелудочковая сердечная недостаточность, идиопатический гипертрофический субаортальный стеноз) [3, 4, 10].
Узелковая форма обычно ассоциирована с заболеваниями сердечно-сосудистой системы, которые приводят к венозному застою крови в системе малого круга (митральный стеноз, хроническая левожелудочковая сердечная недостаточность, идиопатический гипертрофический субаортальный стеноз) [3, 4, 10].
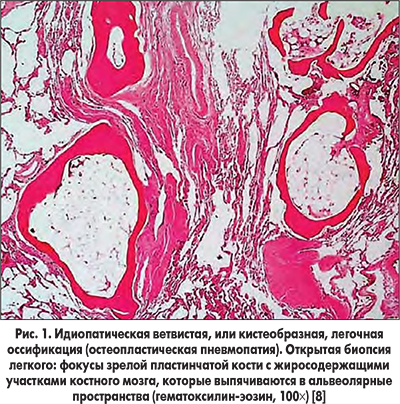
Ветвистая форма характеризуется наличием ветвистых костных образований с элементами костного мозга, расположенных в интерстиции, которые могут выпячиваться в альвеолярные пространства [7] (рис. 1). Ветвистая форма обычно характерна для идиопатической оссификации – остеопластической пневмопатии [8].
Остеопластическая пневмопатия чаще наблюдается у мужчин в возрасте старше 60 лет, однако описаны случаи заболевания у женщин и мужчин молодого возраста.
Заболевание часто протекает без клинических проявлений и выявляется случайно при рентгенологическом обследовании. Много случаев данной патологии диагностируется при аутопсии. У части больных остеопластическая пневмопатия проявляется одышкой преимущественно инспираторного характера и кровохарканьем, спонтанными пневмотораксами. Течение болезни хроническое, медленно прогрессирующее. Формируется рестриктивный тип нарушений легочной вентиляции с уменьшением диффузионной способности легких [1, 6, 9].
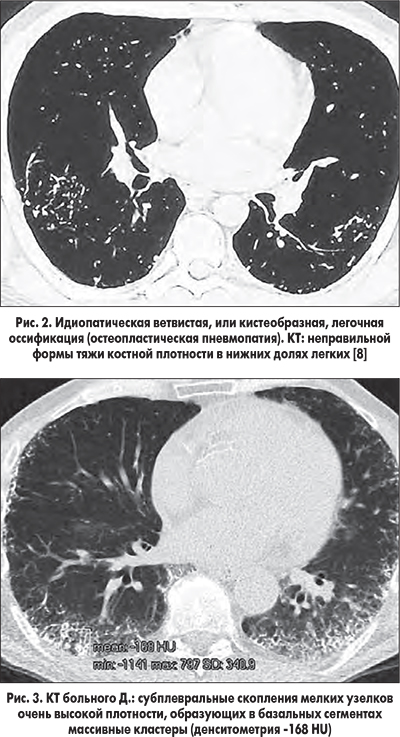 Остеопластическая пневмопатия редко диагностируется при обзорной рентгенографии легких. Если патологические изменения присутствуют, то они, как правило, локализованы в нижних долях в виде ретикуло-узелковых теней. При компьютерной томографии (КТ) определяются более специфические неправильной формы тяжи с разветвлениями костной плотности, расположенные в нижних долях легких [5] (рис. 2).
Остеопластическая пневмопатия редко диагностируется при обзорной рентгенографии легких. Если патологические изменения присутствуют, то они, как правило, локализованы в нижних долях в виде ретикуло-узелковых теней. При компьютерной томографии (КТ) определяются более специфические неправильной формы тяжи с разветвлениями костной плотности, расположенные в нижних долях легких [5] (рис. 2).
Диагностика остеопластической пневмопатии трудна, так как заболевание может протекать длительное время бессимптомно.
Такие клинические проявления болезни, как одышка, кровохарканье, спонтанный пневмоторакс, могут иметь место и при многих других интерстициальных заболеваниях легких.
В связи с отсутствием патогномоничных клинических и рентгенологических признаков заболевания достоверная диагностика возможна только на основании гистологического исследования тканей, полученных при хирургической биопсии легких [1].
Лечение больных остеопластической пневмопатии симптоматическое.
Клинический случай
Пациент Д., 1951 года рождения, житель Черкасской области, наблюдается в ГУ «Национальный институт фтизиатрии и пульмонологии им. Ф.Г. Яновского НАМН Украины» (далее – НИФП) на протяжении трех лет.
В июле 2014 года во время проведения профилактического осмотра на рентгенограмме органов грудной полости были выявлены патологические изменения в легких, в связи с чем пациент был направлен в НИФП для уточнения диагноза.
Жалоб при поступлении в НИФП не предъявлял. Хронических заболеваний органов дыхания в анамнезе нет. Имеет стаж курения около 20 пачко-лет, на протяжении последних 10 лет не курит. В течение 40 лет работал инженером на гидроэлектростанции, имел постоянный контакт с парами масла турбинного трансформатора.
На протяжении 15 лет наблюдается кардиологом по поводу ишемической болезни сердца, принимает антиагреганты (комбинацию ацетилсалициловой кислоты и гидроксида магния), при необходимости – антиангинальные средства. В 2011 году перенес оперативное вмешательство по поводу аневризмы брюшного отдела аорты.
Объективно: состояние удовлетворительное. Пациент нормостенического телосложения, удовлетворительного питания. Кожа и видимые слизистые чистые, сыпи и гиперемии нет. Периферические лимфатические узлы не увеличены. Частота дыхания – 20/мин.
Перкуторный звук – ясный легочный. Аускультативно: над легкими дыхание везикулярное, в базальных отделах с обеих сторон выслушиваются трескучие хрипы. Частота сердечных сокращений – 88 уд/мин. Артериальное давление – 140/90 мм рт. ст. Тоны сердца приглушены, шумов нет. Живот мягкий, печень не увеличена. Периферических отеков нет.
Результаты клинического и биохимического анализов крови и мочи – без особенностей.
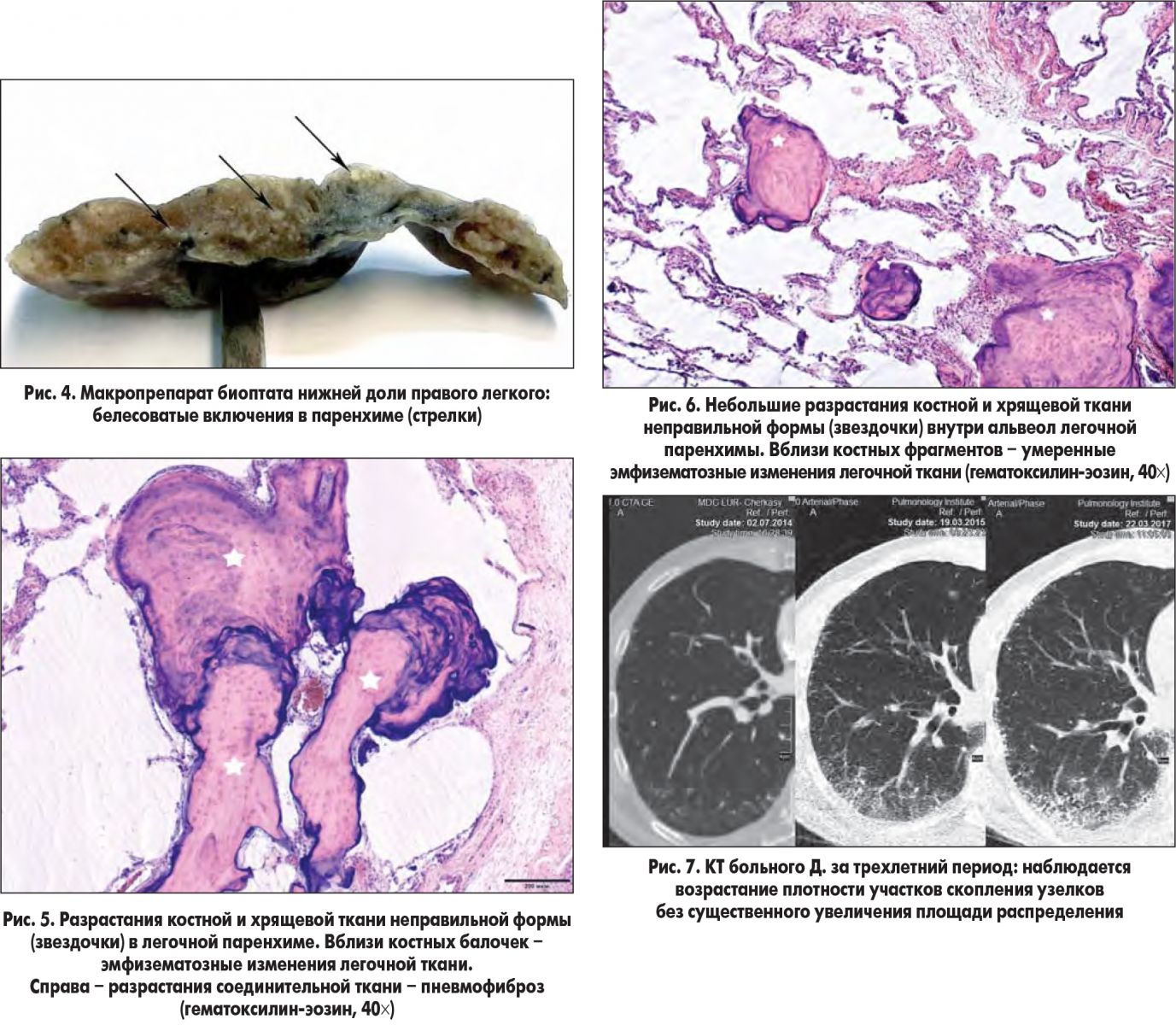
КТ (рис. 3) показала: на всем протяжении легочных полей, за исключением сегментов верхних долей, субплеврально определяются мелкие узелки очень высокой плотности, которые в базальных сегментах образуют массивные скопления (плотность кластера узелков -168 HU). Медиастинальные и бронхопульмональные лимфатические узлы не увеличены.
Больному проведена открытая биопсия – краевая резекция нижней доли правого легкого. На рисунке 4 представлен макропрепарат: на разрезе отчетливо видны плотные белесоватые включения.
На рисунках 5 и 6 представлены микрофотографии гистологических препаратов биоптата легкого.
Заключение патогистологического исследования биоптата: диффузная мелкоузелковая пульмональная оссификация.
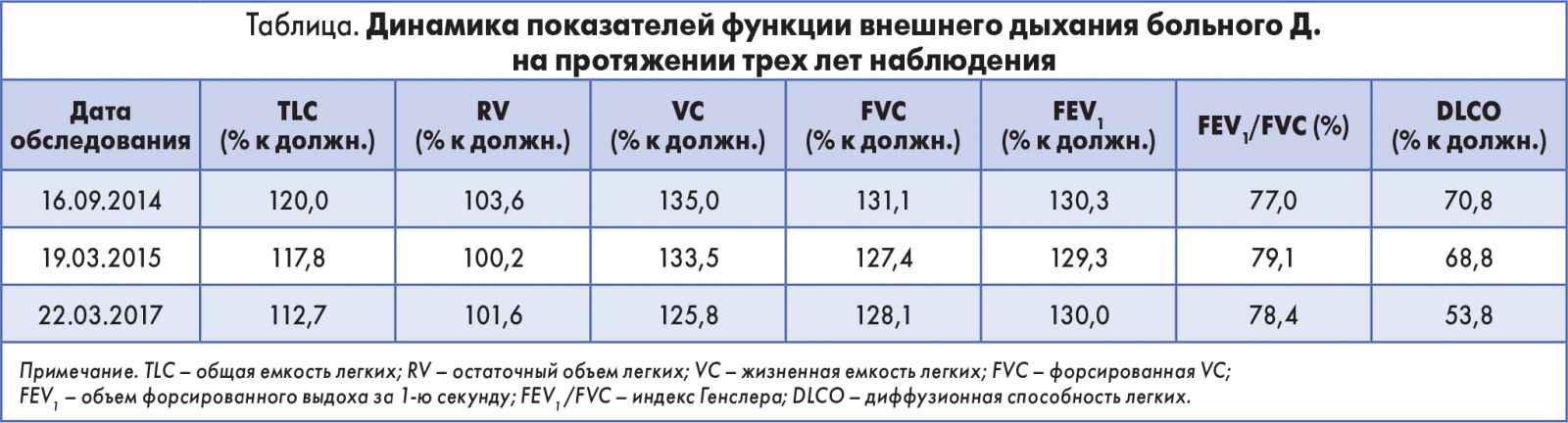
Результаты исследования функции внешнего дыхания (таблица): вентиляционная функция и диффузионная способность легких не нарушены.
Клинический диагноз: остеопластическая пневмопатия, узелковая форма.
В марте 2015 и 2017 года были проведены контрольные обследования пациента. Клинических проявлений заболевания по-прежнему не было. На рисунке 7 представлена динамика данных КТ за трехлетний период.
Как видно на рисунке 7, на протяжении трех лет наблюдения отмечается прогрессирование процесса в легких – значительное увеличение плотности участков поражения паренхимы.
Показатели бодиплетизмографии и спирометрии сохранялись практически на прежнем уровне (таблица), поскольку увеличения площади поражения паренхимы не наблюдалось. Вместе с тем отмечалось существенное снижение диффузионной способности легких.
Больному было рекомендовано приехать в НИФП через год для проведения контрольного обследования.
Литература
1. Редкие интерстициальные заболевания легких / Под ред. В.К. Гаврисюка. – Киев, 2012. – 148 с.
2. Azuma A. Familial clustering of dendriform pulmonary ossification / A. Azuma, H. Miyamoto, T. Usuki et al. // Sarcoidosis Vasc. Diffuse Lung Dis. – 2003. – Vol. 20. – P. 152-154.
3. Buja L.M. Pulmonary parenchymal ossific nodules in idiopathic hypertrophic subaortic stenosis / L.M. Buja, W.C. Roberts // Am. J. Cardiol. – 1970. – Vol. 25. – P. 710-715.
4. Galloway R. Pulmonary ossific nodules in mitral valve disease / R. Galloway, E.J. Epstein, N. Coulshed // Br. Heart J. – 1961. –
Vol. 23. – P. 297-307.
5. Gevenois P.A. Disseninated pulmonary ossification in end-stage pulmonary fibrosis: CT demonstration / P.A. Gevenois, M. Abehsera, C. Knoop et al. // AJR Am. J. Roentgenol. – 1994. – Vol. 162. – P. 1303-1304.
6. Joines R.W. Dendriform pulmonary ossification: Report of two cases with unique finding / R.W. Joines, V.L. Roggli // Am.J. Clin. Pathol. – 1989. – Vol. 91. – P. 398-402.
7. Ndimbie O.K. Dendriform pulmonary ossification / O.K. Ndimbie, C.R. Williams, M.W. Lee // Arch. Pathol. Lab. Med. – 1987. –
Vol. 111. – P. 1062-1064.
8.Poletti V. Rare Infiltrative Lung Diseases: A Challenge for Clinicians / V. Poletti, U. Costabel, G.L. Casoni et al. // Respiration. – 2004. –
Vol. 71. – P. 431-443.
9. Rajjoub S. A case report of idiopathic pulmonary ossification / S. Rajjoub, R.B. Altmeyer // W.V. Med. J. – 1998. – Vol. 94. – 143-145.
10. Whitaker W. Pulmonary ossification in patients with mitral stenosis / W. Whitaker, A. Black, A.J.N. Warrack // J. Fac. Radiol. – 1955. – Vol. 7. – P. 29-34.
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 3 (40), жовтень 2017 р.