2 листопада, 2017
Противовирусная терапия у пациентов с гриппом

Вирусы гриппа остаются наиболее распространенной причиной респираторных инфекций и приводят к высокой заболеваемости и смертности, особенно среди детей раннего возраста, пожилых людей и лиц с ослабленным иммунитетом. Широко распространены три типа вируса гриппа: А, В и С (при этом грипп С встречается редко). Вирусы типов B и C распространены в основном у людей, тогда как тип A, наиболее часто встречаемый, поражает людей и разные виды млекопитающих, в том числе свиней, а также птиц [1].
Введение
Первые сведения о возникновении пандемий гриппа датируются 1700-ми годами. Самая смертоносная из них, ставшая причиной 675 тыс. смертей в США, имела место в 1918 г. [1]. Последняя на сегодня пандемия (2009), вызванная вирусом гриппа H1N1 (также известным как свиной грипп), унесла 12 469 жизней в США [2]. В конце 2016 г. уровень госпитализации составил 3,1 на 100 тыс. населения, причем наибольший процент среди них – лица в возрасте 65 лет и старше [3].
Профилактика является ключевым компонентом в снижении уровней смертности и госпитализации, связанных с гриппом. Однако согласно совокупным данным Национального исследования иммунизации США и системы наблюдения за факторами риска только 41,7% населения проходили сезонную вакцинацию от гриппа в 2015-2016 гг. [4]. Таким образом, более половины населения США в сущности не получало профилактической помощи.
Патофизиология
Вирусы гриппа A и B имеют сходные структуры – это одноцепочечные РНК-вирусы, состоящие из восьми сегментов гена, инкапсулированных и покрытых белками гемагглютинина (НА), нейраминидазы (NA) и матрицы [1]. Белок HA распознает клетку-хозяина и присоединяется к ней, после чего вирусная РНК внедряется в эндосому, высвобождая свои вирусные частицы в ядро клетки-хозяина для репликации [5, 6]. Вирус гриппа A сначала реплицируется в носоглотке и в конечном итоге перемещает репликацию в верхний и нижний дыхательные пути. Зараженные лица выздоравливают в течение недели после появления симптомов; это связано с тем, что вирусная репликация медленно снижается и прекращается по меньшей мере через 7 дней после начала болезни [1, 7].
Грипп A делится на две подгруппы на основе поверхностных белков HA и NA. Существует 18 различных HA-белков и 11 NA-белков, и каждый вирус гриппа A состоит из одного поверхностного белка НА и одного поверхностного белка NA [8]. Вирусные мутации, возникающие в процессе репликации различных белков HA и NA и их комбинаций, связаны с двумя различными механизмами [8].
Во-первых, может возникнуть антигенный дрейф, при котором вирус создает небольшие генетические изменения во время репликации. Эти изменения приводят к появлению вируса, который очень похож на исходный, при этом оба имеют одни и те же антигенные свойства. Со временем изменения делают вирус неузнаваемым для человеческих антител [9]. Второй механизм, известный как антигенный шифт, вызывает выраженное изменение вируса гриппа А [9]. Новый вирус имеет отличающиеся от исходного антигенные свойства и различные HA и/или NA-белки [9]. Антигенный шифт стал одной из причин пандемии гриппа 2009 г. [9].
После заражения иммунная система создает антитела против поверхностных белков HA и NA вируса [1]. Вакцина аттенуированного, или живого, вируса вводится в организм для производства антител против антигенов гриппа [10, 11]. Антигенный шифт и дрейф РНК-содержащего вируса гриппа учитываются при разработке прогностической вакцины против инфекции [10]. Исследователи используют данные, собранные в предыдущие годы, и тенденции, чтобы определить, какие три или четыре вирусных штамма должны быть включены в состав сезонной вакцины [11, 12].
Разработкой вакцин занимаются центры по контролю и профилактике заболеваний (CDC). Была разработана система эпиднадзора для отслеживания прогрессирования вируса гриппа каждый год, чтобы помочь в разработке вакцин. Собранная информация включает данные о местоположении и сроках вирусной активности, типах и подтипах гриппа, любых антигенных изменениях или мутациях, сообщения о гриппоподобных заболеваниях, госпитализациях, связанных с гриппом, и смертях от гриппа [13]. В течение сезона 2016-2017 гг. чаще всего сообщалось о гриппе A (H3N2), за которым следует грипп A (H1N1pdm09); однако также сообщалось о некоторых типах вируса гриппа B [3].
Вакцинация является эффективной мерой профилактики гриппа. Так, ее эффективность против гриппа А достигает 70-90% [1]. Однако при непрерывных небольших изменениях, вызванных антигенным дрейфом, вакцинированный человек все еще может заразиться вирусом гриппа [9].
Клиника
Симптомы, связанные с вирусом гриппа, напоминают симптомы бактериальных инфекций и простуды; дифференциальный диагноз является важным фактором при уходе за пациентами. В отличие от простуды, симптомы гриппа обычно резкие, первые признаки – внезапная лихорадка (38-40 °C) и кашель [14]. Кашель обычно сухой и надсадный, вызывающий дискомфорт в груди. Дополнительными симптомами являются выраженная миалгия, артралгия, слабость, недомогание, снижение аппетита и головная боль. Заложенность носа, чихание и боль в горле чаще распространены у пациентов с острой респираторной вирусной инфекцией, а тяжелый сухой кашель и слабость свойственны обычно гриппу [14].
Для гриппов А и В диагноз, как правило, устанавливается при посеве из носоглотки или носа. Диагностические экспресс-тесты гриппа (RIDT) обнаруживают вирусные антигены и входят в число наиболее часто используемых диагностических методов, результаты которых доступны быстро (<15 мин). Однако чувствительность теста (от 50 до 70%) приводит к частым ложно негативным результатам. Следует также обратить внимание, что диагностический материал для RIDT следует собирать в первые 3-4 дня (не позже) с момента появления симптомов [15, 16].
Тест обратной транскрипционной полимеразной цепной реакции остается золотым стандартом для диагностики гриппа благодаря его высокой специфичности и чувствительности [16]. В дополнение к мазкам из носоглотки могут быть использованы горловые мазки, бронхиальный смыв и мокрота. Образцы из нижних дыхательных путей могут быть использованы для диагностики и позже 4-го дня с момента появления симптомов, однако для получения результатов может потребоваться от 1 до 8 ч [15].
После постановки диагноза гриппа следует рассмотреть возможные нефармакологические и фармакологические методы лечения, направленные на уменьшение симптомов и непосредственно сокращение продолжительности и тяжести заболевания.
Лечение гриппа
Нефармакологические методы
При гриппе рекомендуют постельный режим, изоляцию от других лиц и активную дегидратацию. Усиленное потребление жидкости необходимо во время болезни, чтобы предотвратить осложнения от обезвоживания. Ацетаминофен или ибупрофен можно использовать для снятия лихорадки, головной боли и мышечных болей. Тем не менее некоторые пациенты могут воспользоваться антивирусным лечением [17-19].
Фармакологические методы
Антивирусные препараты с активностью против вирусов гриппа являются важным дополнением к вакцинации. Озельтамивир, ингаляционные занамивир и IV-перамивир являются рекомендуемыми в настоящее время средствами для лечения гриппа
[20-22]. Эти препараты являются селективными ингибиторами нейраминидазы, проявляют активность против гриппа A и гриппа B.
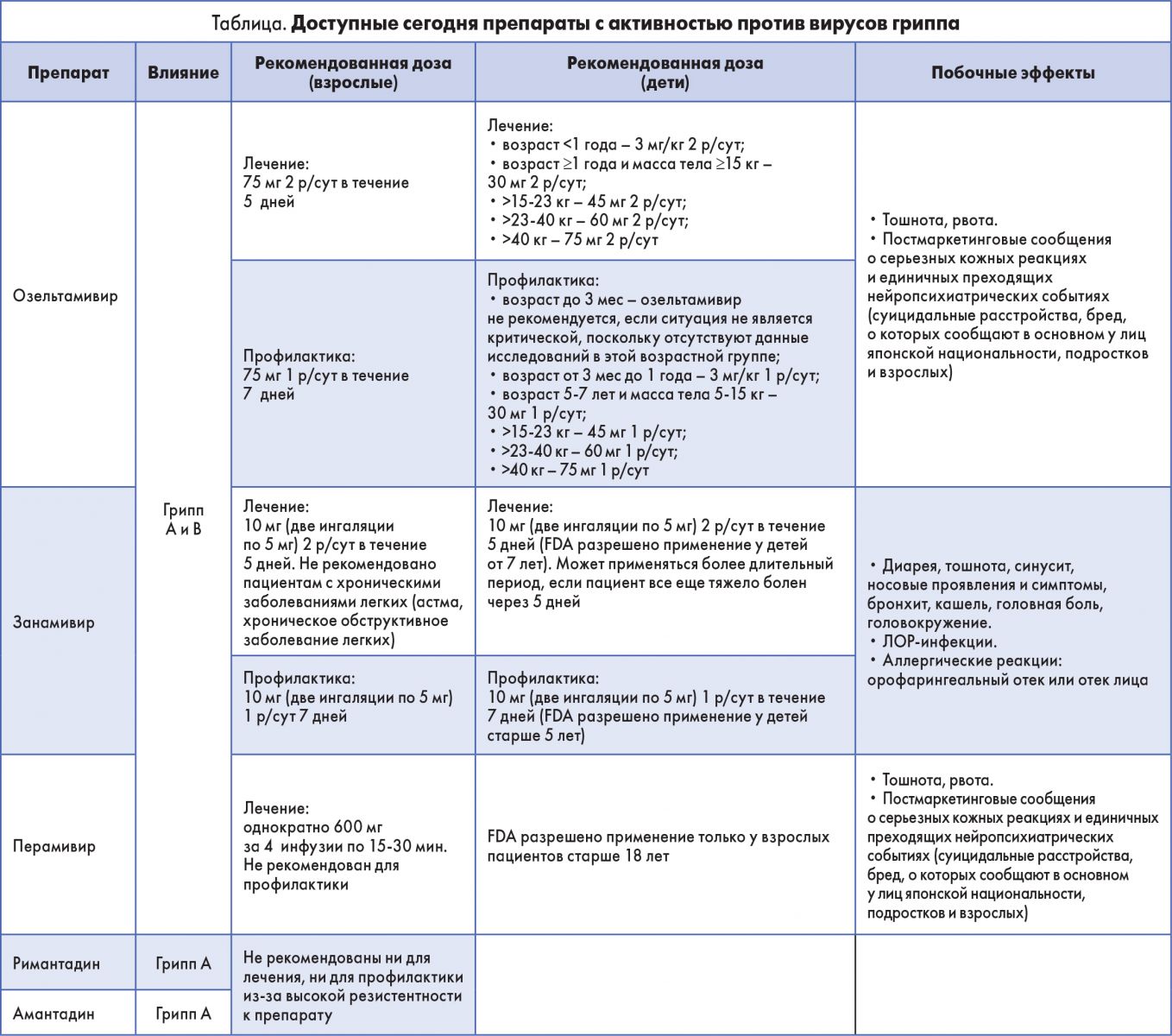
Блокируя нейраминидазу, они предотвращают высвобождение вирусных частиц из инфицированных клеток, тем самым уменьшая вирусную агрессию. Все названные препараты могут использоваться для лечения, но только озельтамивир и занамивир могут использоваться и для лечения, и для профилактики. Дозы этих лекарств для химиопрофилактики ниже, чем дозы для лечения, однако продолжительность приема больше (табл.) [20-23]. Озельтамивир и занамивир разрешены для применения у взрослых и детей; перамивир не был одобрен Управлением по контролю качества продуктов питания и лекарственных средств США (FDA) для использования у детей [19, 23].
Помимо ингибиторов нейраминидазы, доступны два других продукта: амантадин (Симметрел) и римантадин (Флумадин), оба из которых являются противораковыми агентами адамантана с активностью против вирусов гриппа А. Эти агенты оказывают ингибирующее действие на подтипы вируса гриппа А (H1N1, H2N2 и H3N2) в начале вирусного репликативного цикла. Тем не менее они больше не рекомендуются для лечения и профилактики гриппа из-за повышенных показателей резистентности (>99%) к типам вируса гриппа H3N2 и H1N1 [19, 23].
Вопросы фармакотерапии
Раннее начало лечения вышеуказанными противовирусными препаратами может сократить продолжительность симптомов гриппа до 3 дней и снизить риск развития осложнений [24]. Наибольшее клиническое преимущество проявляется, когда антивирусное лечение начинается в течение 48 ч после начала болезни. Также важно правильно идентифицировать пациентов, которые соответствуют параметрам как для профилактики, так и для лечения, чтобы они получали правильную дозировку и выдерживали нужную продолжительность терапии [19].
Профилактический прием противовирусных препаратов следует начать у взрослых и детей в возрасте от 1 года и старше, которые подвергаются высокому риску развития осложнений гриппа и которым вакцинация против гриппа противопоказана, недоступна или, как ожидается, имеет низкую эффективность (например, из-за значительно ослабленного иммунитета) [18, 19]. Противовирусные препараты в профилактическом аспекте могут рассматриваться для применения в популяции в целом, когда вакцинация еще не была проведена, но уже зафиксированы случаи гриппа.
Профилактическую терапию также следует проводить невакцинированным взрослым, включая работников здравоохранения, и детям в возрасте ≥1 года, которые находятся в тесном контакте с лицами с высоким риском развития осложнений гриппа в периоды эпидемической активности, а также всем вакцинированным и невакцинированным лицам в учреждениях, которые могут усиливать распространение вспышек гриппа [19].
Противовирусное лечение должно быть начато у всех лиц с лабораторно подтвержденной или сильно подозреваемой инфекцией вируса гриппа с высоким риском развития осложнений [19]. К таким относятся:
• дети в возрасте до 2 лет (дети в возрасте <5 лет считаются подверженными высокому риску, однако самый высокий риск – в возрасте <2 лет при максимальной смертности и смертности среди младенцев в возрасте <6 мес);
• взрослые в возрасте старше 65 лет;
• лица с хроническим легочным заболеванием (включая астму), с сердечно-сосудистыми заболеваниями (кроме наличия у пациента одной лишь гипертонической болезни), с почечной, печеночной, гематологической патологией, с метаболическими нарушениями (включая сахарный диабет) или с неврологическими и неврогенными состояниями (включая нарушения работы головного мозга, спинного мозга и нарушения нейро-мышечной передачи, такие как эпилепсия/судороги, инсульт, интеллектуальная отсталость, задержка развития средней тяжести, мышечная атрофия, повреждения спинного мозга);
• лица с иммуносупрессией, в том числе вызванной лекарствами или ВИЧ-инфекцией;
• беременные женщины или те, которые родили менее чем 2 нед назад;
• лица моложе 19 лет, получающие долгосрочную терапию аспирином;
• американские индейцы / уроженцы Аляски;
• люди с ожирением (индекс массы тела – >40);
• жители домов престарелых и других учреждений хронического ухода.
Пациентам, которым требуется госпитализация по причине гриппа, независимо от того, вакцинированы они или нет, без учета характера основного заболевания должны быть назначены противовирусные препараты. Амбулаторные больные с высоким риском осложнений, у которых не наблюдается положительной динамики в болезни, при положительном результате теста на грипп могут признаваться кандидатами на назначение противовирусных препаратов. То же самое относится к амбулаторным пациентам, которые не подвергаются повышенному риску, но хотят сократить продолжительность заболевания или находятся в тесном контакте с кем-то с высоким риском осложнений, связанных с инфекцией гриппа [19].
При подборе соответствующего противовирусного препарата для профилактики или лечения пациента следует рассмотреть местные особенности распространения инфекции в популяции в течение всего сезона гриппа. Озельтамивир, занамивир и перамивир были антивирусными препаратами, рекомендованными для сезона гриппа в 2016-2017 гг. [19]. FDA в августе 2016 г. одобрило к применению значительно более дешевый генерик озельтамивира [25].
Пациентам на искусственной вентиляции легких или критическим пациентам озельтамивир можно вводить через назогастральную или орогастральную (NG/OG) трубку. Порошок из капсул следует растворить в 20 мл воды для инъекций и впрыснуть через трубку NG/OG, затем добавить 10 мл воды для инъекций [20].
Неотложные состояния
Противовирусная терапия может быть дефицитной во время пандемий. В США, например, законом о Проекте биозащиты от 2004 г. предусмотрено, что при выявлении угрозы общественному здоровью при отсутствии лицензионного или запатентованного продукта специальный уполномоченный может выдавать разрешение на чрезвычайное использование противовирусных препаратов [26]. Если недоступны коммерчески приготовленная пероральная суспензия, подходящая по возрасту дозировка или другие антивирусные продукты, производитель рекомендует смешивать озельтамивир в суспензию 6 мг/мл для индивидуального использования в чрезвычайных ситуациях.
Выводы
Практикующие врачи должны прежде всего уметь быстро идентифицировать среди зараженных гриппом пациентов тех, кто имеет высокий риск развития осложнений, чтобы снизить риски летальных исходов. Некоторым больным может потребоваться профилактическая противовирусная терапия. Препараты для лечения гриппа и профилактики одинаковы, и лечащим врачам следует контролировать правильность применяемой дозировки.
Литература
1. CDC. CDC estimates of 2009 H1N1 influenza cases, hospitalizations and deaths in the United States. www.cdc.gov/h1n1flu/estimates_2009_h1n1.htm. Accessed December 29, 2016.
2. CDC. Weekly US influenza surveillance report: 2016-2017 season, week 51 ending December 24, 2016. www.cdc.gov/flu/weekly/weeklyarchives2016-2017/Week51.htm. Accessed March 8, 2017.
3. Santibanez T.A., Kahn K.E., Zhai Y. et al. Flu vaccination coverage, United States, 2015-2016 influenza season. www.cdc.gov/flu/fluvaxview/coverage‑1516estimates.htm. Accessed March 3, 2017.
4. Luo M. Influenza virus entry. Adv. Exp. Med. Biol. 2012; 726: 201-221.
5. Lakadamyali M., Rust M.J., Zhuang X. Endocytosis of influenza viruses. Microbes Infect. 2004; 6: 929-936.
6. CDC. Influenza (flu): information for schools. www.cdc.gov/flu/school/qa.htm. Accessed December 30, 2016.
7. CDC. Types of influenza viruses. – www.cdc.gov/flu/about/viruses/types.htm. Accessed January 14, 2017.
8. CDC. How the flu virus can change: «drift» and «shift». www.cdc.gov/flu/about/viruses/change.htm. Accessed December 30, 2016.
9. Hunt R. Vaccines: past successes and future prospects. Virology. www.microbiologybook.org/lecture/vaccines.htm. Accessed January 14, 2017.
10. Sedova E.S., Shcherbinin D.N., Migunov A.I. et al. Recombinant influenza vaccines. Acta Naturae. 2012; 4: 17-27.
11. CDC. Selecting viruses for the seasonal influenza vaccine. www.cdc.gov/flu/about/season/vaccine-selection.htm. Accessed January 14, 2017.
12. Thompson W.W., Comanor L., Shay D.K. Epidemiology of seasonal influenza: use of surveillance data and statistical models to estimate the burden of disease. J. Infect. Dis. 2006; 194 (suppl 2): S82-S91.
13. Montalto N.J. An office-based approach to influenza: clinical diagnosis and laboratory testing. Am. Fam. Physician. 2003; 67: 111-118.
14. CDC. Influenza signs and symptoms and the role of laboratory diagnostics. www.cdc.gov/flu/professionals/diagnosis/labrolesprocedures.htm.Accessed January 14, 2017.
15. Vemula S.V., Zhao J., Liu J. et al. Current approaches for diagnosis of influenza virus infections in humans. Viruses. 2016; 8: 96.
16. CDC. Influenza (flu) treatment. www.cdc.gov/flu/consumer/treatment.htm. Accessed December 22, 2016.
17. Fiore A.E., Fry A., Shay D. et al. Antiviral agents for the treatment and chemoprophylaxis of influenza – recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm. Rep. 2011; 60: 1-24.
18. Harper S.A., Bradley J.S., Englund J.A. et al. Seasonal influenza in adults and children – diagnosis, treatment, chemoprophylaxis, and institutional outbreak management: clinical practice guidelines of the Infectious Diseases Society of America. Clin. Infect. Dis. 2009; 48: 1003-1032.
19. Oseltamivir. Lexi-Comp Online. Hudson, OH: Lexi-Comp, Inc; 2016. https://online.lexi.com. Accessed December 9, 2016.
20. Zanamivir. Lexi-Comp Online. Hudson, OH: Lexi-Comp, Inc; 2016. https://online.lexi.com. Accessed December 9, 2016.
21. Аnamivir. Lexi-Comp Online. Hudson, OH: Lexi-Comp, Inc; 2016. https://online.lexi.com. Accessed December 9, 2016.
22. Peramivir. Lexi-Comp Online. Hudson, OH: Lexi-Comp, Inc; 2016. https://online.lexi.com. Accessed December 9, 2016.
23. CDC. Influenza antiviral medications: summary for clinicians. www.cdc.gov/flu/professionals/antivirals/summary-clinicians.htm. Accessed March 8, 2017.
24. Cooper N.J., Sutton A.J., Abrams K.R. et al. Effectiveness of neuraminidase inhibitors in treatment and prevention of influenza A and B: systematic review and meta-analyses of randomized controlled trials. BMJ. 2003; 326: 1235.
25. The FDA approves first generic version of widely used influenza drug, Tamiflu.www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationfor-PatientsandProviders/ucm514854.htm. Accessed January 13, 2017.
26. CDC. Antiviral emergency use authorization. www.cdc.gov/flu/professionals/antivirals/antiviral-emergency-use.htm. Accessed December 17, 2016.
US Pharmacist. 2017, 42 (4): 32-36.
Сокращенный перевод с англ. Юлии Иванченко
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 3 (40), жовтень 2017 р.