9 листопада, 2017
Антибіотикорезистентність як глобальна проблема: фокус на респіраторні інфекції
Згідно з даними Всесвітньої організації охорони здоров’я (ВООЗ) швидке зростання стійкості мікроорганізмів до антибактеріальних препаратів загрожує підірвати основи охорони здоров’я, закладені протягом останніх 50 років.
Як наслідок, ВООЗ визначила антибіотикорезистентність однією з головних загроз людству, також було розроблено документ «Глобальна стратегія ВООЗ щодо стримування стійкості».
Антибіотикорезистентність як загроза безпеці людства
За даними Центрів з контролю і профілактики захворювань США, щороку не менш ніж 2 млн мешканців цієї країни інфікуються бактеріями, резистентними до антибіотиків, приблизно 23 тис. таких хворих помирають унаслідок резистентних інфекцій. У Європі, за оцінками експертів, річна кількість летальних наслідків інфекцій, спричинених резистентними патогенами, приблизно така ж, як у США, а глобальний показник обчислюється сотнями тисяч. Інфекції, зумовлені резистентними збудниками, можуть розвинутися в будь-якої людини, навіть у здорових дорослих у розквіті сил. І хоча ступінь ризику істотно варіює, фактично ніхто на 100% не захищений від цих інфекційних агентів. Крім того, у випадку антибіотикорезистентних збудників значно збільшується вартість терапії. Так, за оцінками Європейського центру з профілактики та контролю захворювань, тільки в країнах ЄС додаткові збитки від резистентних до антибіотиків бактерій сягають 1,5 млрд євро на рік.
В огляді щодо стійкості до протимікробних препаратів, який підготували британські експерти під керівництвом Jim O’Neill 2014 року, йдеться про те, що якщо антибіотики втрачатимуть ефективність такими ж темпами, що й сьогодні, то у 2016-2050 рр. резистентні інфекції обійдуться світовій економіці в 100 трлн доларів. За умови збереження нинішніх тенденцій до 2050 р. антибіотикорезистентність буде причиною смерті 10 млн осіб щороку (рис.).
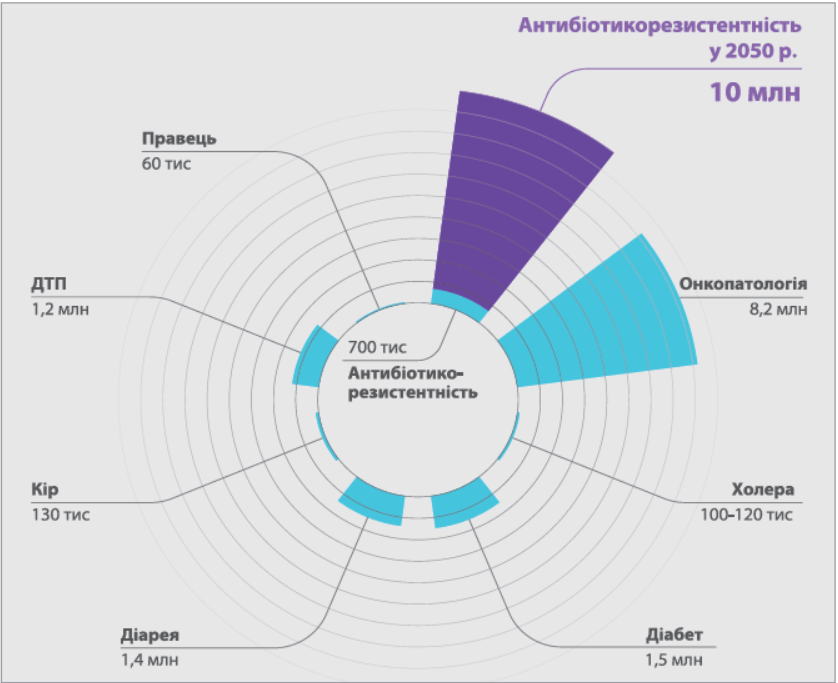
Причини зростання антибіотикорезистентності
Одними з найважливіших причин є доступність антибіотиків населенню в багатьох країнах світу і висока частота самолікування, що нерідко є неадекватним. Так, за даними Європейського центру з профілактики та контролю захворювань, 40% європейців переконані, що антибіотики ефективні при застуді і грипі.
Недостатня обізнаність клініцистів щодо правил раціональної антибіотикотерапії, а іноді й нездатність встояти перед наполегливими проханнями пацієнтів і їхніх батьків призводять до невиправданих або неадекватних призначень антибактеріальних препаратів. Відсутність просвітницької роботи з пацієнтами (роз’яснень необхідності завершення повного курсу антибіотикотерапії тощо) стає причиною дострокового припинення лікування. Усе це сприяє формуванню та поширенню резистентних штамів мікроорганізмів.
У державах з перехідною економікою, зокрема в Україні, є локальні додаткові фактори ризику зростання антибіотикорезистентності, до яких, наприклад, належить широке використання більш дешевих і не завжди якісних генеричних антибактеріальних препаратів, що пришвидшує селекцію резистентних штамів мікроорганізмів.
Роль лікаря у вирішенні проблеми антибіотикорезистентності
Призначаючи антибактеріальний препарат, кожен лікар має пам’ятати про те, що перед ним стоїть два важливих завдання – тактичне (вибір засобу з максимальним терапевтичним і мінімальним токсичним потенціалом) і стратегічне (зменшення ризику селекції і поширення в популяції резистентних штамів бактерій).
Робоча група Міжнародного товариства антимікробної терапії сформувала 10 рекомендацій для лікарів загальної практики з метою мінімізації ризику селекції і поширення резистентних мікроорганізмів (2011).
1. Призначати антибіотик лише за наявності відповідних показань і пам’ятати, що в разі вірусних інфекцій ці лікарські засоби неефективні.
2. Обирати адекватний клінічній ситуації протимікробний препарат.
3. Враховувати фармакокінетичний/фармакодинамічний профіль антибіотиків і призначати максимально короткий з можливих курс лікування.
4. Сприяти підвищенню комплаєнсу пацієнтів, щоб вони повністю завершували курс лікування.
5. Комбінувати антибіотики тільки в разі потреби.
6. Уникати використання протимікробних препаратів низької/сумнівної якості.
7. Переконувати пацієнтів не застосовувати антибіотики на власний розсуд.
8. Дотримуватися заснованих на даних доказової медицини практичних рекомендацій щодо лікування тих чи інших захворювань.
9. Використовувати можливості мікробіологічної лабораторії.
10. При емпіричному призначенні антибактеріальних препаратів брати до уваги тенденції регіональної антибіотикорезистентності.
Раціональна антибіотикотерапія інфекцій дихальних шляхів
На особливу увагу заслуговує той факт, що переважна кількість антибіотиків у світі використовується для лікування респіраторних інфекцій.
За результатами епідеміологічних досліджень, найчастіше збудниками позалікарняних респіраторних інфекцій є S. pneumoniae, H. influenzaе, M. catarrhalis, M. pneumoniae і С. pneumoniae. Виходячи з цього, для емпіричної терапії позалікарняних інфекцій дихальних шляхів рекомендовані β-лактами, макроліди і респіраторні фторхінолони. Чи є вони рівнозначним вибором? Зазвичай ні.
Перш за все слід пам’ятати про те, що респіраторні фторхінолони вважаються альтернативними засобами, які недоцільно призначати як стартову терапію неускладнених респіраторних інфекцій. Це пояснюється тим, що деякі класи антибіотиків мають більший потенціал у селекції резистентних штамів, ніж інші. Так, при широкому використанні глікопептидів, цефалоспоринів і фторхінолонів відзначається підвищення частоти виявлення метицилінрезистентного стафілокока (MRSA).
У зв’язку із цим у переважній більшості випадків позалікарняних інфекцій дихальних шляхів лікування починають з β-лактамів або макролідів. До переваг класу макролідів відносять здатність проникати всередину клітин і обумовлену цим високу активність відносно атипових збудників, а також наявність додаткових неантимікробних властивостей (протизапального й імуномодулюючого ефектів). Не слід забувати і про те, що β-лактами не активні стосовно атипових патогенів, натомість можливість участі останніх у розвитку респіраторних інфекцій досить висока (в середньому 10-15%). Макроліди здатні впливати як на внутрішньоклітинних (атипових) збудників, так і на типову мікрофлору.
У розрізі проблеми антибіотикорезистетності варто відзначити два ключові механізми резистентності збудників (переважно стрепто- і стафілококів) до дії макролідів – модифікацію мішені (метилювання рибосом) та ефлюкс (активне виведення з клітини). Цікаво, що за наявності резистентності до 14- і 15-членних макролідів за рахунок модифікації мішені мікроорганізми можуть зберігати чутливість до 16-членних препаратів. Резистентність за механізмом ефлюксу також частіше розвивається до 14- і 15-членних макролідів.
Серед 16-членних макролідів на особливу увагу заслуговує спіраміцин. Завдяки особливостям хімічної будови препарат забезпечує надійний зв’язок із 50s-субодиницею рибосоми (відразу з 3 доменами), а отже, стійкий протимікробний ефект. Спектр антибактеріальної активності спіраміцину охоплює всі значимі респіраторні патогени, включно зі Streptococcus spp. (у тому числі S. pneumoniae і S. pyogenes), Staphylococcus spp. (крім MRSA), C. diphtheriae, H. influenzaе, M. catarrhalis, B. pertussis, M. pneumoniae, С. pneumoniae, L. pneumophila та ін. Незважаючи на те що спіраміцин є одним з найстаріших представників класу, резистентність до нього не вища, а за деякими даними – навіть нижча (як у дослідженнях ПеГАС ІІ і ПеГАС ІІІ), ніж до новіших макролідів. Можливо, це пов’язано з особливостями розвитку резистентності патогенів до різних макролідів, які ми вже згадували.
Фармакодинамічні особливості спіраміцину забезпечують його високу клінічну ефективність. Так, при помірній активності in vitro клінічна ефективність цього антибіотика значно вища. Цей феномен отримав назву парадоксу спіраміцину, а пояснюється він тим, що зазначений макролід створює високі тканинні (паренхіма легенів, мигдалини та ін.) і внутрішньоклітинні концентрації (особливо в нейтрофілах і макрофагах), демонструє найменше зв’язування з білками плазми, забезпечує постантибіотичний ефект (9 год), має імуномодулюючі властивості та знижує адгезивність стрепто- і стафілококів (Smith C. R., 1988; Bergone-Berezin E., 1996).
Варто відзначити і високий профіль безпеки макролідів, особливо спіраміцину. Препарат виводиться двома шляхами (печінкою і нирками), тож немає потреби в корекції дози за наявності недостатності цих органів; не виявляє кардіотоксичної дії; не викликає фототоксичності; характеризується низьким алергенним потенціалом і найнижчим серед макролідів потенціалом міжлікарських взаємодій.
На українському фармацевтичному ринку спіраміцин представлений єдиним лікарським засобом – оригінальним препаратом Роваміцін® виробництва відомої європейської компанії Sanofi. Це автоматично знімає проблему використання неякісних генериків, які не тільки знижують можливість досягнення терапевтичного успіху, а й, як зазначалося вище, сприяють селекції резистентних штамів збудників.
Який би антибіотик лікар не обрав для терапії бактеріальної респіраторної інфекції, завжди слід пам’ятати про необхідність дотримуватися рекомендацій щодо тривалості лікування. Як занадто короткі, так і дуже тривалі курси асоціюються з підвищенням ризику селекції резистентних штамів. Зазвичай курс лікування препаратом Роваміцін® – 5-7 днів, але цей термін може подовжуватися у випадку інфекцій, спричинених атиповими мікроорганізмами.
Об’єднання зусиль на глобальному рівні
Знаменною подією минулого року стало підписання Sanofi й іншими провідними міжнародними фармацевтичними, діагностичними та біотехнологічними компаніями спільної декларації про реалізацію всеосяжних заходів проти інфекцій, резистентних до терапії. Декларацію було ухвалено на Всесвітньому економічному форумі в Давосі (Швейцарія), на сьогодні її підписали майже 100 фармацевтичних компаній.
Представники фарміндустрії закликають уряди всіх країн вийти за рамки заяв про наміри і у співпраці з компаніями вжити конкретних заходів на підтримку інвестицій у розробку антибіотиків, засобів діагностики, вакцин та інших продуктів, що мають життєво важливе значення для профілактики і лікування резистентних інфекцій. Разом із тим у декларації встановлюються зобов’язання сторін щодо подальших дій у сфері проблем лікарської резистентності. Компанії зобов’язуються зменшити вплив виробництва антибіотиків на довкілля; сприяти належному використанню нових та наявних антибактеріальних засобів, у тому числі за рахунок дотримання рекомендацій щодо застосування цих препаратів; продовжувати і розширювати науково-дослідні розробки зі створення нових молекул; підтримувати ініціативи, спрямовані на забезпечення доступу до антибіотиків для всіх мешканців планети незалежно від рівня доходів.
Насамкінець хочемо звернутися до читачів з проханням не залишатися осторонь від вирішення такої серйозної проблеми, як антибіотикорезистентність. Це дійсно реальна загроза для людства. Робіть усе можливе з того, що залежить особисто від вас. Лише у цьому разі шанс не програти битву інфекціям отримає все людство. Допомагаючи пацієнтам сьогодні, пам’ятайте про майбутнє!
Підготував Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 19 (416), жовтень 2017 р.


