11 листопада, 2017
Еволюція таргетної терапії пацієнтів з меланомою: фокус на комбінацію вемурафенібу та кобіметинібу
Останніми десятиліттями захворюваність на меланому поширювалася, особливо у віковій групі людей старше 50 років. Хоча більшості пацієнтів хворобу діагностують на локалізованій стадії, коли можливе ефективне лікування шляхом хірургічної резекції, залишається багато пацієнтів, в яких дисемінована меланома наявна на момент встановлення діагнозу або розвивається після початкового лікування. Історично прогноз у пацієнтів з меланомою IV стадії був поганим, половина хворих вмирали протягом 8-10 міс після встановлення діагнозу. Проте наразі лікування метастатичної меланоми швидко еволюціонує, що дозволило збільшити виживаність. Значною мірою цього вдалося досягти завдяки більш чіткому розумінню патогенезу захворювання, зокрема, відкриттю того, що головним сигнальним шляхом розвитку меланоми є MAPK (мітоген-активована протеїнкіназа).
Сигнальний шлях MAPK при метастатичній меланомі
MAPK є комплексним сигнальним шляхом, в якому задіяні RAS (сімейство малих G-протеїнів) і три протеїнкінази (RAF, MEK, EPK). Онкогенна активація цього шляху може бути наслідком мутацій будь-якого його компонента або промоторів. Зазвичай важливі медіатори MAPK стимулюються активацією RAS з подальшою низхідною взаємодією між серин-треоніновими кіназами, BRAF та CRAF. У клітинах з «диким» (тобто немутантним) геном BRAF BRAF-кіназа активується формуванням гомо- чи гетеродимерів з іншими ізоформами RAS, такими як ARAF та CRAF. У клітинах з мутантним BRAF BRAF-кіназа залишається постійно активованою у мономерному стані, при цьому активність кінази підвищується більше ніж у 400 разів. В умовах активації RAF відбувається взаємодія між низхідними кіназами MEK (MEK1 і MEK2); це ініціює фосфорилювання MEK, що своєю чергою полегшує активуюче фосфорилювання ERK і, відповідно, стимулює онкогенез.
Активація ERK спричиняє ангіогенез, міграцію і проліферацію клітин, одночасно пригнічуючи апоптоз, що сприяє росту злоякісних клітин. У патогенезі меланоми цей сигнальний каскад відбувається найчастіше внаслідок активуючих мутацій BRAF, які наявні приблизно у 50% усіх меланом шкіри пізніх стадій. Найбільш поширеною мутацією BRAF є однонуклеотидна мутація – заміна тиміну на аденін у позиції 1799 в активуючому сегменті домену кінази, що своєю чергою призводить до заміни глутамату на валін у кодоні 600 (V600E). Ця точкова мутація ідентифікується у 80% мутацій BRAF. Наступною за частотою мутацією є заміна двох нуклеотидів, гуаніну та тиміну, на аденін у позиціях 1798 та 1799 відповідно, що спричиняє заміну лізину на валін у кодоні 600 (V600K). Мутації у V600 підвищують активність кінази та зазвичай не супроводжуються іншими онкогенними мутаціями, зокрема мутаціями генів NRAS та KIT.
Вемурафеніб
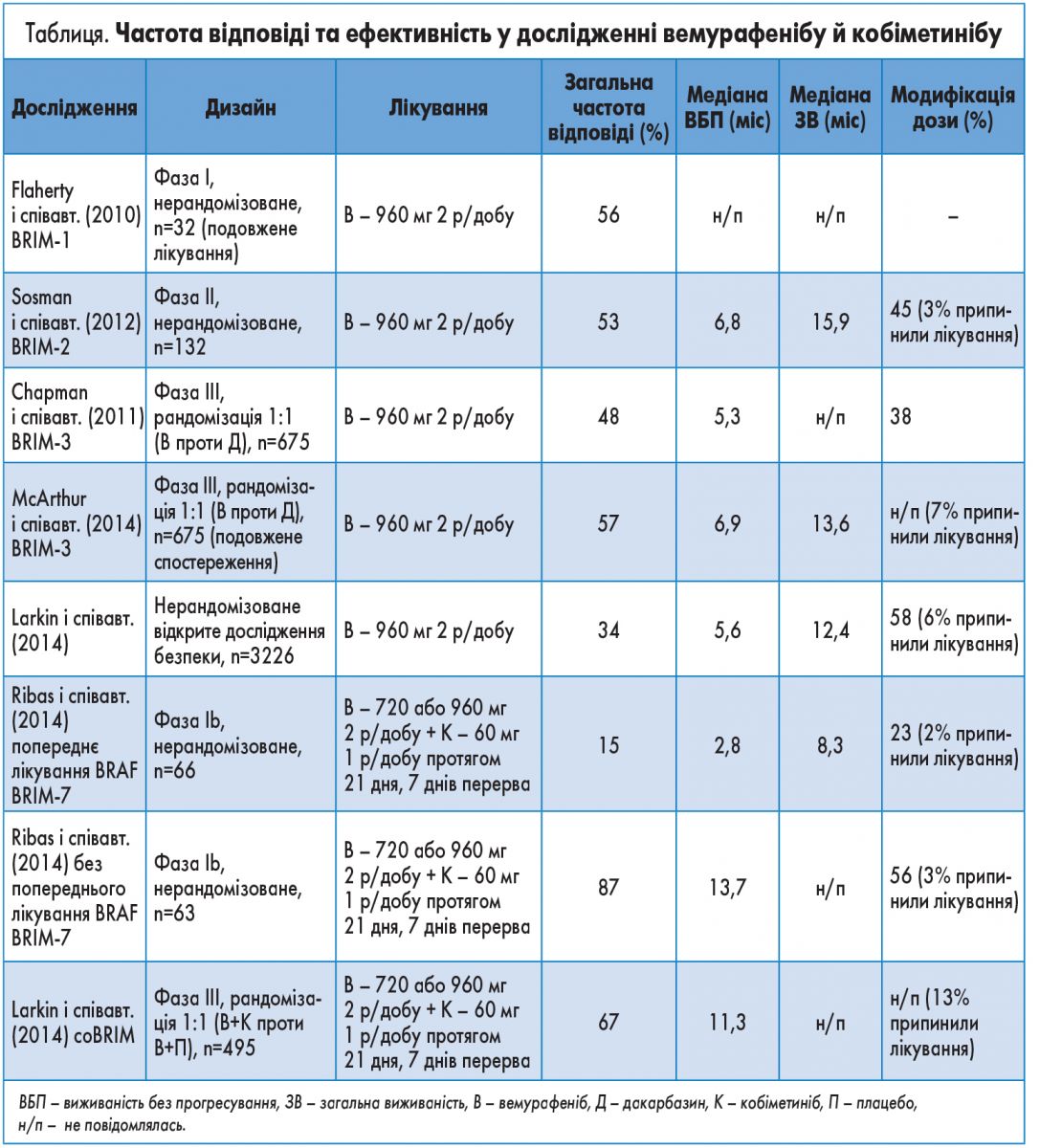
Після невдалої спроби пригнічення BRAF мультикіназним інгібітором сорафенібом був розроблений вемурафеніб – потужний інгібітор кіназ з високою специфічністю до АТФ-зв’язувального карману активованої мутантної BRAF-кінази, зокрема варіанту V600E. Вемурафеніб є першим селективним зворотним інгібітором BRAF-кінази V600. У дослідженні I фази (BRIM‑1) на підставі фармакокінетики, фармакодинаміки, безпеки та ефективності було встановлено, що максимальною дозою вемурафенібу, яка добре переноситься хворими, є доза 960 мг 2 р/добу. У подовженій фазі цього дослідження у 32 пацієнтів з мутаціями BRAF V600E вемурафеніб забезпечив безпрецедентну виживаність – 56%.
У дослідженні II фази (BRIM‑2) частота відповіді на препарат склала 56% (у тому числі 6% повної відповіді); медіана загальної виживаності (ЗВ) становила 15,9 міс, медіана виживаності без прогресування (ВБП) – 6,7 міс. В обох дослідженнях вемурафеніб мав подібний профіль безпеки. Найчастішими побічними ефектами були шкірна токсичність (фоточутливість, висип та ін.), артралгія, загальна слабкість, алопеція і безсимптомне підвищення трансаміназ. У дослідженні BRIM‑2 45% учасників потребували зниження дози, 64% – тимчасового припинення лікування через побічні ефекти. Середня доза вемурафенібу становила 1740 мг/добу, що складає 91% від запланованої дози 1920 мг/добу.
У подальшому монотерапія вемурафенібом вивчалася в міжнародному дослідженні BRIM‑3, в якому 675 пацієнтів з меланомою, які мали мутацію V600 (у тому числі 20 пацієнтів з нетиповими мутаціями, наприклад V600K та V600D), рандомізували для лікування вемурафенібом або дакарбазином до прогресування захворювання. Частота відповіді й токсичність вемурафенібу були такі самі, як у попередніх дослідженнях. Дослідження BRIM‑3 також показало, що пацієнти з нетиповими мутаціями BRAF, зокрема V600K, також отримують користь від лікування вемурафенібом з частотою відповіді 40%. Запланований проміжний аналіз продемонстрував значне покращення ОВ у групі вемурафенібу; препарат знижував відносний ризик (ВР) смерті на 63%, ризик смерті або прогресування – на 74% (р<0,001). Подальше спостереження показало значно більшу медіану ЗВ (13,6 проти 9,7 міс; р=0,0008) та ВБП (6,9 проти 1,6 міс; р<0,0001) у групі вемурафенібу порівняно з групою дакарбазину.
Кобіметиніб
Активність вемурафенібу характеризується швидкою початковою відповіддю, у багатьох пацієнтів пухлина значно зменшується в розмірах уже після 14 днів лікування. На жаль, у більшості хворих, лікованих BRAF-інгібітором, рано чи пізно розвивається резистентність. Альтернативним підходом до лікування є MEK-інгібітори, проте переведення пацієнтів з резистентністю до BRAF-інгібітора на монотерапію MEK-інгібітором не має значної терапевтичної користі. Отже, для подолання резистентності доцільною є комбінована таргетна терапія BARF- та MEK-інгібіторами.
Кобіметиніб – потужний селективний інгібітор MEK1/2, який зберігає свою активність стосовно фосфорильованої MEK. У багатоцентровому дослідженні Ib фази (BRIM‑7) оцінювали безпеку, переносність та активність кобіметинібу в комбінації з вемурафенібом. У дослідження включали як пацієнтів, в яких захворювання прогресувало на вемурафенібі, так і хворих з мутацією BRAF V600, які раніше не отримували BRAF- або MEK-інгібіторів.
Після початкової фази, під час якої визначали безпечні дози препаратів, для наступного етапу були відібрані дві когорти пацієнтів, які отримували вемурафеніб 720 або 960 мг 2 р/добу + кобіметиніб 60 мг/добу (21 день лікування, 7 днів перерва).
Було встановлено, що пацієнти, які раніше не отримували BRAF-інгібітор, продемонстрували кращу відповідь (87%, зокрема 10% повна відповідь) і клінічні результати (ВБП 13,7 міс; 1-річна виживаність 83%) порівняно з пацієнтами з нещодавнім прогресуванням на тлі анти-BRAF-терапії (загальна відповідь 15%, жодного випадку повної відповіді; ВБП 2,8 міс; 1-річна виживаність 32%). Імовірно, це пов’язано з гетерогенністю пухлини, яка виникає під час лікування BRAF-інгібітором.
Окремі субклони з різними механізмами резистентності можуть діяти паралельно, підвищуючи активність сигнального шляху MAPK, що не можна подолати додаванням MEK-інгібітора. Серед гетерогенної популяції пухлинних клітин відбувається селекція субпопуляцій, які не чутливі до пригнічення MAPK і, відповідно, мають перевагу щодо виживаності. Отже, комбіноване інгібування BRAF і MEK є найбільш ефективним у разі використання вже на старті терапії; це дозволяє відтермінувати селективний тиск, який може спричинити різноманітні геномні та, можливо, епігенетичні зміни.
Комбінація вемурафенібу та кобіметинібу в подальшому вивчалась у міжнародному багатоцентровому дослідженні III фази coBRIM. Раніше не лікованих пацієнтів (n=495) з нерезектабельною місцеворозповсюдженою меланомою IIIC або IV стадії рандомізували на терапію вемурафенібом 960 мг 2 р/добу + кобіметиніб 60 мг 1 р/добу (21/7) або вемурафенібом 960 мг 2 р/добу + плацебо. Частота об’єктивної відповіді була значно вищою в групі комбінованої терапії порівняно з контрольною групою (68 проти 45%; р<0,001), так само як і частота повної відповіді (10 проти 4%). Медіана тривалості відповіді в групі комбінованої терапії не була досягнута, натомість у контрольній групі вона склала 7,3 міс.
Після 14,2 міс спостереження медіана ВБП у групі комбінованої терапії становила 12,3 міс порівняно з 7,2 міс у контрольній групі (ВР 0,58); медіана ЗВ після 18,5 міс спостереження дорівнювала 22,4 та 17,4 міс відповідно (ВР 0,70; р=0,005).
Побічні реакції в групі комбінованої терапії були переважно легкими або помірними (1-2 ступеня); найчастіше повідомлялося про фоточутливість, висип, діарею, підвищення рівня печінкових трансаміназ або креатинфосфокінази. Після 4 міс лікування багато побічних реакцій зникали; найважчі прояви токсичності зазвичай спостерігались у перші 28 днів терапії. Важливо, що комбіноване лікування вемурафенібом і кобіметинібом асоціювалося зі зниженою частотою вторинного плоскоклітинного раку шкіри. Крім того, було встановлено, що підвищений рівень лактатдегідрогенази є негативним прогностичним фактором.
Таким чином, комбінація вемурафеніб + кобіметиніб чітко продемонструвала значне покращення відповіді та ЗВ пацієнтів з меланомою з мутацією BRAF V600. Результати дослідження coBRIM свідчать, що монотерапію інгібітором BRAF або MEK більше не можна вважати стандартом першої лінії лікування.
Список літератури знаходиться в редакції.
Стаття друкується в скороченні.
Medina T.M., Lewis K.D. The evolution of combined molecular targeted therapies to advance the therapeutic efficacy in melanoma: a highlight of vemurafenib and cobimetinib. Onco Targets Ther, 2016 Jun 22; 9: 3739-52.
Переклав з англ. Олексій Терещенко
Тематичний номер «Онкологія» № 4 (50), жовтень 2017 р.