15 листопада, 2017
Профилактика резистентной артериальной гипертензии: как достичь целевого уровня артериального давления у пациентов с коморбидной патологией?
По материалам XVIII Национального конгресса кардиологов, 20-22 сентября, г. Киев
Резистентная артериальная гипертензия (АГ) – серьезная проблема для клинициста. Однако частота истинной резистентной АГ не так уж высока, гораздо чаще врачам приходится сталкиваться с недостаточным контролем артериального давления (АД) из-за низкой приверженности к терапии или неадекватного лечения АГ.

О том, как улучшить комплайенс и достичь целевого АД у пациентов с коморбидной патологией, рассказал заведующий отделом артериальной гипертензии ГУ «Национальный институт терапии им. Л. Т. Малой НАМН Украины», доктор медицинских наук, профессор Сергей Николаевич Коваль.
– По мнению экспертов Американской ассоциации сердца (American Heart Association, AHA), критерием резистентной АГ является неэффективность одновременного приема ≥4 препаратов (включая хлорталидон и спиронолактон).
Распространенность резистентной АГ в популяции, по разным данным, составляет 10-35%. Однако далеко не все случаи неконтролируемой АГ связаны с резистентностью. Среди причин псевдорезистентной АГ лидирующие позиции занимают субоптимальная/неадекватная терапия и низкая приверженность пациентов к лечению.
Низкий комплайенс – это скрытый фактор риска неблагоприятных сердечно-сосудистых событий. В исследовании Jung и соавт. (2013), в котором проводился масс-спектрометрический анализ метаболитов антигипертензивных препаратов в моче у пациентов с резистентной АГ, было показано, что 53% больных резистентной АГ не были привержены назначенной терапии, из них 30% совсем не принимали препараты. В израильском исследовании Weitzmanet и соавт. (2014) участвовали 172 432 пациента с АГ. Неконтролируемая АГ наблюдалась у 36% больных. Из них 20% не назначались максимальные дозы, 9% не использовали диуретики, 48% употребляли <3 препаратов, 20% не принимали препараты совсем. И только в 2,2% случаев патология отвечала критериям резистентной АГ.
! Суммируя эти данные, можно заключить, что ≥20% пациентов с неконтролируемой АГ вообще не используют назначенные препараты, а проблема отсутствия контроля АД часто связана не с резистентностью, а с низким комплайенсом.
Чем выше приверженность к антигипертензивной терапии среди пациентов, тем большее количество больных достигает целевых значений АД.
Это наглядно показано в работе B. Waeber и соавт. (2014).
В нашей стране наблюдается парадоксальная ситуация: комплайенс составил почти 60%, превышая таковой в Германии, Финляндии и Нидерландах, а вот целевых значений АД достигают только 10% пациентов. Объясняется эта ситуация все теми же двумя причинами: либо было назначено неадекватное лечение, либо больные не принимают рекомендованные им препараты.
Приверженность к антигипертензивной терапии напрямую зависит от количества таблеток, которые необходимо употреблять ежедневно. Если частота их приема 4 раза в день, комплайенс едва превышает 50%, использование препарата 1 раз в день увеличивает приверженность к лечению до 75-80% (Mancia G. et al., 2015). Современные подходы к антигипертензивной терапии требуют комбинированного лечения у пациентов с АГ 2-3 степени. Это значит, что для достижения целевого АД может потребоваться ежедневный прием 2-4 препаратов. В исследовании ALLHAT 24% больных, исходно получавшим диуретик, 41% пациентов, изначально принимавшим ингибитор ангиотензинпревращающего фермента (АПФ), и 31% участников, в качестве стартовой терапии употреблявшим блокатор кальциевых каналов, потребовалось назначение ≥3 препаратов для контроля АД (Wright J. T. et al., 2005). В испытании ACCOMPLISH для достижения контроля АД к концу наблюдения у 32% больных АГ появилась необходимость добавления третьего препарата к начальной терапии (Jamerson K. et al., 2007); на момент завершения исследования SCOPE 49% больных находились на поликомпонентной (≥3) терапии (Lithell H. et al., 2003); в испытании INVEST примерно половина больных АГ в сочетании с ИБС к концу двухлетнего наблюдения принимали ≥3 препаратов (Pepine J. et al., 2003). В исследовании STITCH необходимость трехкомпонентной терапии регистрировалась примерно у половины больных неосложненной и нетяжелой АГ.
Становится понятным, что сократить количество принимаемых препаратов для повышения комплайенса нельзя. Но можно уменьшить число принимаемых таблеток, используя фиксированные комбинации антигипертензивных средств. Метаанализ 9 исследований, в которых сравнивалось назначение комбинаций в фиксированной форме или в виде отдельных компонентов, показал, что использование фиксированных комбинаций позволяет улучшить комплайенс на 26% (Bangalore S. et al., 2007) и значительно уменьшить затраты на лечение (Ambrosioni Е., Borghi C., 2014).
! Трехкомпонентная комбинация антигипертензивных препаратов – ингибитора АПФ, тиазидоподобного диуретика и блокатора кальциевых каналов дигидропиридинового ряда длительного действия – является, согласно современным представлениям, наиболее перспективной (Mancia G. et al., 2014; Barghi C. et al., 2017). Сочетание трех компонентов в одной таблетке усиливает антигипертензивное действие, снижает частоту побочных эффектов, а также упрощает режим приема, что, несомненно, повышает приверженность пациентов к лечению и значительно удешевляет его (Лутай М. И., 2016).
Одним из таких препаратов является Ко-Амлесса® – фиксированная трехкомпонентная комбинация периндоприла, индапамида и амлодипина. Лекарственное средство Ко-Амлесса® показано пациентам с АГ 2-3 степени в качестве базовой терапии, при неконтролируемой и резистентной АГ, пациентам с коморбидной патологией (СД, метаболический синдром, ИБС, заболевания периферических артерий, ХБП, хроническое обструктивное заболевание легких, СОАС).
Ко-Амлесса® имеет 4 варианта дозирования, что облегчает подбор необходимой дозы для пациента:
1. Периндоприла терт-бутиламин – 4 мг;
индапамид – 1,25 мг;
амлодипин – 5 мг.
2. Периндоприла терт-бутиламин – 4 мг;
индапамид – 1,25 мг;
амлодипин – 10 мг.
3. Периндоприла терт-бутиламин – 8 мг;
индапамид – 2,5 мг;
амлодипин – 5 мг.
4. Периндоприла терт-бутиламин – 8 мг;
индапамид – 2,5 мг;
амлодипин – 10 мг.
На базе нашей клиники было выполнено собственное исследование эффективности препарата Ко-Амлесса® у пациентов с АГ и абдоминальным ожирением. Все участники были разделены на две группы: в основной – пациенты получали фиксированную комбинацию периндоприла, индапамида и амлодипина Ко-Амлесса®, в группе сравнения – нефиксированную комбинацию периндоприла, индапамида и амлодипина в виде трех разных препаратов. Результат оценивали через 3 и 6 месяцев от начала терапии.
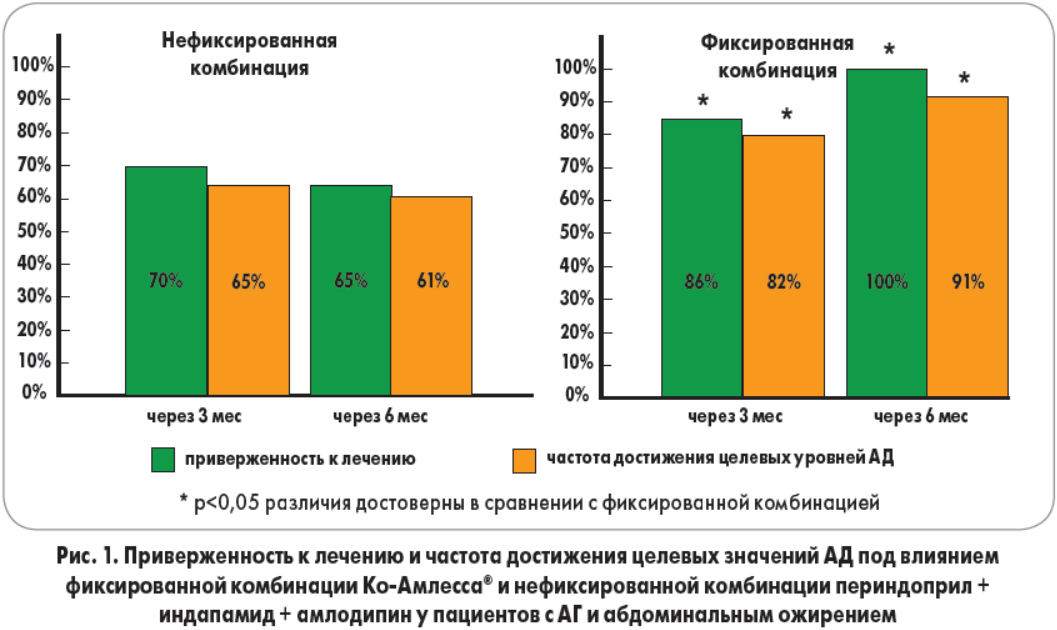
Целевых значений АД через 3 и 6 месяцев достигли 65 и 61% пациентов соответственно, принимавших нефиксированную комбинацию, и 82 и 91% больных, которые получали препарат Ко-Амлесса®.
! Уровни приверженности к лечению фиксированной комбинацией Ко-Амлесса® были значительно выше, чем в группе сравнения (рис 1.). Этим можно объяснить лучшую эффективность лечения в основной группе.
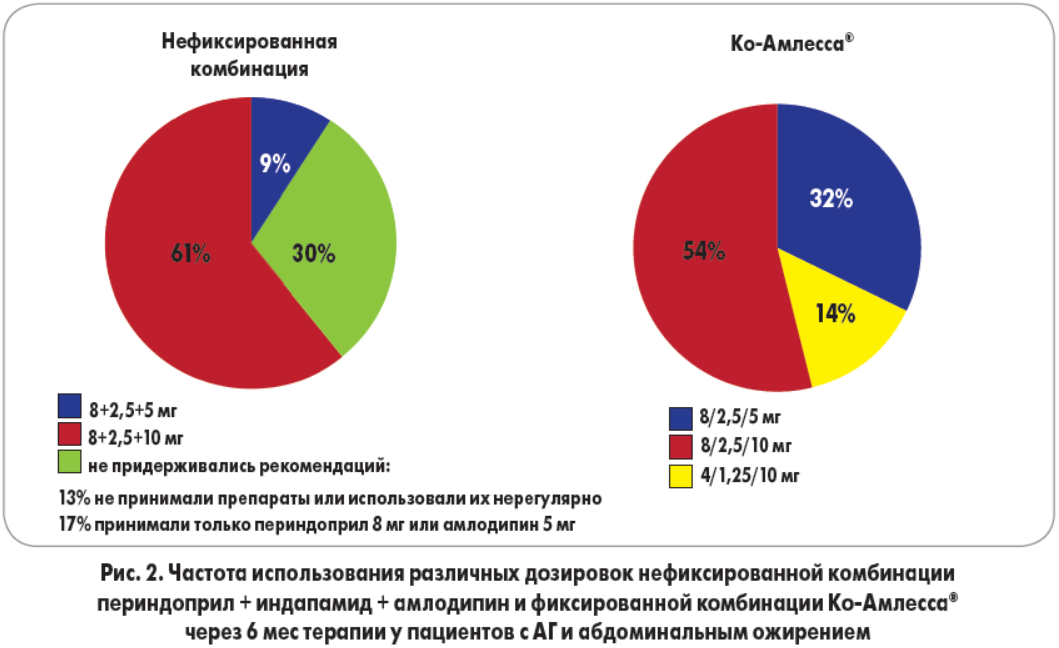
Пациентам, принимавшим нефиксированную комбинацию антигипертензивных препаратов, требовались более высокие дозы для достижения целевого АД. Почти треть больных из этой группы вообще не употребляли назначенное лечение, еще столько же – использовали препараты нерегулярно или самостоятельно сокращали терапию до 1-2 препаратов в день (рис. 2).
Данные суточного мониторирования АД подтвердили более высокую эффективность антигипертензивной терапии в основной группе. Так, у пациентов, принимавших препарат Ко-Амлесса®, среднесуточное САД было в среднем на 10 мм рт. ст., а среднесуточное ДАД – приблизительно на 5 мм рт. ст. ниже, чем в группе сравнения.
Таким образом, для достижения целевого уровня АД у пациентов с неконтролируемой АГ необходимо улучшать приверженность к терапии. Хорошим способом повышения комплайенса является применение фиксированных комбинаций, имеющих доступную стоимость. Фиксированная комбинация периндоприла, индапамида и амлодипина Ко-Амлесса® может быть рекомендована пациентам, которые не достигают целевых значений АД на фоне приема 2 антигипертензивных средств, а также лицам, получающим ≥3 антигипертензивных препаратов, на фоне сниженного уровня переносимости и недостаточного комплайенса. Лечение препаратом Ко-Амлесса® — эффективно потому, что удобно.
Медична газета «Здоров’я України 21 сторіччя» № 20 (417), жовтень 2017 р.