17 листопада, 2017
Синдром раздраженного кишечника
Синдром раздраженного кишечника (СРК) является хроническим, иногда инвалидизирующим заболеванием. Как правило, этот диагноз устанавливается при отсутствии структурных или биохимических изменений, но имеющиеся доказательные данные свидетельствуют, что патофизиологические нарушения могут объяснять клинические проявления, а СРК вряд ли является этиологически однородным состоянием либо исключительно психиатрической (соматосенсорной) патологией.
Римские критерии IV, созданные на основе консенсусного соглашения мультидисциплинарной группы экспертов по функциональным гастроинтестинальным заболеваниям, представляют современные стандарты диагностики СРК. В соответствии с этими критериями СРК диагностируется на основании рецидивирующей абдоминальной боли, связанной с дефекацией или изменением частоты/формы каловых масс (табл.). Вздутие является распространенным сопутствующим симптомом. Симптомы должны быть хроническими, возникать не реже одного раза в неделю, беспокоить пациента в среднем на протяжении предыдущих 3 мес с продолжительностью не менее 6 мес.

СРК оказывает неблагоприятное влияние на качество жизни и производительность труда. Распространенность СРК в США оценивается в 7-16%, наиболее часто эта патология диагностируется у женщин и лиц молодого возраста. Прямые затраты, ассоциированные с СРК, в США, по самым скромным подсчетам, оцениваются в ≥1 млрд долларов. Таким образом, точная диагностика СРК, минимизация числа инвазивных процедур, подбор эффективного лечения играют важную роль в усилиях, направленных на уменьшение социальных и экономических последствий этого заболевания.
Классификация
В соответствии с Римскими критериями IV СРК классифицируется на четыре подтипа (СРК с диареей, СРК с констипацией, смешанный СРК с наличием констипации и диареи, неклассифицируемый СРК) с учетом жалоб пациентов на наличие плотных/комковатых или неоформленных/водянистых каловых масс. Обоснование для выделения этих подтипов состоит в увеличении гомогенности пациентов, принимающих участие в клинических исследованиях, создании рекомендаций по эффективной диагностике и терапии, расширении знаний о потенциальных патофизиологических механизмах заболевания.
Диагностика
Национальное руководство по лечению СРК утверждает, что при наличии у пациента симптомов, соответствующих Римским критериям IV и отсутствии симптомов тревоги (табл.), врачу следует диагностировать СРК, не прибегая к дополнительным исследованиям. Однако проведенный опрос свидетельствует, что представители здравоохранения и врачи, оказывающие первичную медицинскую помощь, как правило, настаивают на проведении подтверждающих исследований и не склонны следовать положительной диагностической стратегии по сравнению с экспертами в данной области. Тем не менее результаты исследований, проводимых для исключения органической патологии у пациентов с симптомами СРК, немногочисленны.
Обязательное проведение рутинных анализов крови не поддерживается данными доказательной медицины, хотя клиницисты часто рекомендуют выполнить клинический анализ крови (КАК) и определить уровень С-реактивный белка (СРБ) для исключения ВЗК. Руководство по лечению целиакии рекомендует проводить скрининг этой патологии у лиц с симптомами СРК посредством серологического исследования. Эта рекомендация поддерживается данными недавнего метаанализа, продемонстрировавшего, что распространенность целиакии, подтвержденной биопсией, значительно возрастает у пациентов с любым подтипом СРК по сравнению с контрольной популяцией, не имевшей СРК. Целесообразность дополнительных исследований определяется вариантом СРК. Диагностический алгоритм приведен на рисунке.
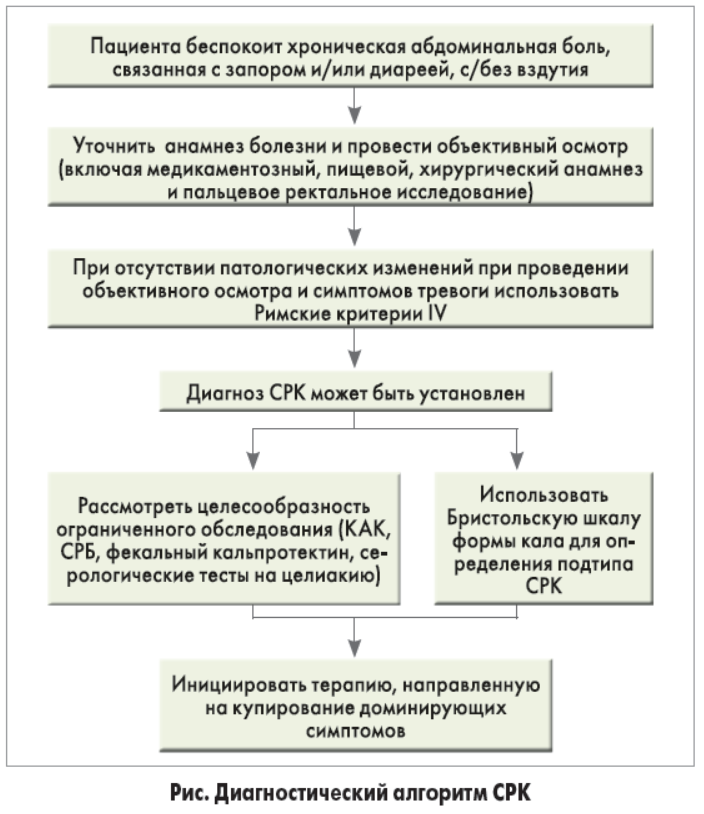
У пациентов с СРК-подобными симптомами и преобладанием хронической констипации следует рассмотреть вероятность наличия обструктивной дефекации (дисфункции тазового дна), т. к. это состояние хорошо отвечает на биологическую обратную связь. Такой симптом, как необходимость ручного пособия, является недостаточным основанием для диагностики обструктивной дефекации, но ректальное обследование с целью выявления парадоксального сокращения ануса при натуживании, может быть целесообразным; для подтверждения диагноза используется аноректальная манометрия. Если в ходе тазового/ректального осмотра с последующим ультразвуковым исследованием (трансабдоминальным/трансвагинальным) у постменопаузальных женщин, предъявляющих жалобы на запор, боль в нижних отделах живота, вздутие или увеличение живота в размерах, обнаруживается опухолевидное образование, то следует исключить рак яичников, поскольку это редкое заболевание может являться основной причиной появления указанных симптомов.
У больных СРК с диареей или диареей и констипацией дифференциация между органической и функциональной гастроинтестинальной патологией только на основании симптомов может быть несколько затруднительной. У пациентов с указанными подтипами СРК целесообразно определить фекальный кальпротектин, т. к. данное исследование позволит дифференцировать СРК и ВЗК с высокой точностью (высокой чувствительностью и специфичностью). Определение фекального кальпротектина может стать альтернативой бессистемной колоноскопии, имеющей низкую диагностическую ценность. В кросс-секционном исследовании, в котором приняли участие больные СРК с диареей / смешанным вариантом заболевания, перенесшие колоноскопию (n=466), не было выявлено ни одного случая колоректального рака, ВЗК диагностированы у <2% пациентов. Метаанализ продемонстрировал, что у >1 из 4 больных СРК с диареей обнаруживаются признаки хологенной диареи при проведении исследования с 23-селено‑25-гомотаурохолевой кислотой, предполагающим введение 75-селен-гомохолитаурина (желчной кислоты, меченной радиоактивным изотопом селена) и последующее сканирование всего тела при помощи гамма-камеры через 7 дней, однако это исследование не проводится в США. Биохимический анализ крови (определение 7α-гидрокси‑4-холестен‑3-она, предшественника желчных кислот) становится доступным в клинической практике.
Таким образом, СРК не является диагнозом исключения. Применение положительного диагностического подхода поддерживается данными, демонстрирующими стабильность диагноза СРК на протяжении длительного динамического наблюдения; последующее развитие органической гастроинтестинальной патологии у таких пациентов происходит довольно редко. Другие доказательства целесообразности использования данного подхода получены в датском рандомизированном контролированном исследовании (РКИ), в котором приняли участие пациенты с вероятным СРК (n=302). В этом исследовании положительный диагностический подход, основанный на симптомах, сравнивался с подходом, при котором органическая патология исключалась при помощи расширенных анализов крови, кала, ректороманоскопии. Два подхода не отличались по качеству жизни, симптомам СРК, удовлетворенности пациентов, однако стоимость обследования была ниже при использовании положительной диагностической стратегии.
Разработка точного неинвазивного диагностического теста для исключения структурных изменений при наличии симптомов СРК пока остается несбыточной мечтой. Исследования сфокусировались на разработке новых биомаркеров (физиологические механизмы, гены, белки, метаболиты) для подтверждения диагноза. В метаанализе, оценивавшем все вышеописанные диагностические подходы, эффективность определения биомаркеров не превышала результативность симптоматических критериев. В недавнем исследовании сравнивалась точность двух сывороточных биомаркеров (антител к бактериальному токсину, продуцируемому Campylobacter jejuni, и винкулина), позволяющих дифференцировать СРК от ВЗК с высокой специфичностью (92% для C. jejuni и 84% для винкулина), но низкой чувствительностью (44% для C. jejuni и 33% для винкулина). Эти результаты требуют подтверждения. Некоторые биомаркеры (определение колоректального транзита или концентрации желчных кислот в фекалиях) могут использоваться для установления подтипов СРК, что позволит индивидуализировать таргетную терапию.
Патофизиология
Как правило, СРК рассматривается как нарушение взаимодействия кишечника с головным мозгом в связи с сопутствующими психиатрическими заболеваниями и психологическими состояниями, особенно тревожностью и депрессией. Данный факт не объясняется поведением, направленным на поиск медицинской помощи, а действительно неразрывно связан с кишечными симптомами. Несмотря на то что чрезмерная реакция на стресс с увеличением уровня циркулирующего кортикотропин-рилизинг фактора имеет место у больных СРК, спровоцированным тяжелой травмой (жестоким обращением с детьми), блокирование кортикотропин-рилизинг фактора не приводило к появлению значимого терапевтического эффекта. Примерно в половине случаев СРК возникает в кишечнике, а не в головном мозге; сначала появляются симптомы СРК, а психологический дистресс развивается несколько позже. Тот факт, что пробиотики способны изменить обработку сигнала в головном мозге, также подтверждает нарушение взаимодействия кишечника с ЦНС.
После перенесенного острого бактериального, протозойного и вирусного гастроэнтерита у 10-20% инфицированных пациентов СРК-подобные симптомы продолжают персистировать. Лицам со 2 фенотипом Т-хелперных клеток свойствен более высокий риск. Патофизиология постинфекционного СРК, по-видимому, отличается от таковой при СРК, вызванном неинфекционными причинами. Например, пациентам с постинфекционным СРК свойственно латентное воспаление кишечника, сопровождающееся инфильтрацией толстого и тонкого кишечника тучными клетками. Остается неясным, может ли специфическая персистирующая инфекция спровоцировать развитие СРК, хотя есть данные, подтверждающие, что кишечный спирохетоз ассоциирован с ранее недиагностированной стертой эзонофилией толстого кишечника и СРК с диареей.
Кишечный микробиом может изменяться при СРК, хотя типичные признаки и причины еще не установлены. Проспективное исследование, в котором участвовали 110 пациентов с СРК, продемонстрировало, что тяжесть СРК ассоциирована с различными изменениями фекальной микробиоты (уменьшением микробного разнообразия, снижением распространенности метанобактерий и превотелл). Пристеночный микробиом отличается от микробиома каловых масс, а перекрестная контаминация при проведении эндоскопической биопсии может являться фактором, объясняющим гетерогенность данных, полученных в различных исследованиях. Газопродуцирующие бактерии могут индуцировать ответный интестинальный рефлекс посредством растяжения кишечной стенки, что ведет к неадекватной релаксации диафрагмы, выпячиванию и видимому вздутию живота. Коррекция диеты быстро изменяет микробиом, однако объясняет ли данный факт эффективность диетотерапии у некоторых больных СРК, остается пока неизвестным.
Описаны изменения сенсорной (интестинальная гиперчувствительность) и двигательной (быстрый интестинальный транзит при СРК с диареей или замедленный интестинальный транзит при СРК с констипацией) функции, хотя ни одно из них не является патогномоничным. Проницаемость кишечной стенки может изменяться у некоторых больных СРК, особенно у пациентов с диареей. Это может частично объяснить, почему при СРК наблюдается активация иммунной системы, изменяющая локальный выброс серотонина, а также сенсорную и моторную функции. Неизвестно, является ли активация иммунной системы более выраженной у женщин или у мужчин, уменьшается ли она с возрастом, но теоретически данный факт может объяснить эпидемиологию СРК. Биологические маркеры активации иммунной системы тощей кишки, вероятно, возникающие вследствие изменения барьерной функции кишечника, коррелируют с тяжестью диареи и депрессии. Кроме того, у больных СРК может быть повышен уровень циркулирующего фактора некроза опухоли, высокие концентрации которого достоверно коррелируют с тревожностью. Эти наблюдения подтверждают, что кишечное воспаление непосредственно обусловливает появление психологического дистресса.
Особенно важно изучать кластеры СРК в семьях, необходимы также генетические изыскания и исследования, проводимые на ранних этапах жизни. Обнаружена специфическая мутация в гене натриевых каналов (SCN5A), вероятно, объясняющая 2% случаев СРК. Мексилетин корригировал многие дефекты натриевых каналов in vitro и нормализовал опорожнение кишечника у больных СРК с констипацией in vivo. Врожденная недостаточность сахаразы-изомальтазы может представлять собой другое объяснение семейного кластерного фенотипа СРК. Исследователи наблюдали изменение экспрессии генов на слизистой тонкого кишечника, принимающих участие в транспорте ионов железа, барьерной и иммунной функциях, работе тучных клеток. Проявления СРК, возникшего в кишечнике после инфекционного гастроэнтерита, подобны симптомам СРК, появившегося сначала в головном мозге после тяжелой и жизнеугрожающей травмы. Это наблюдение в конечном итоге может изменить парадигмы лечения, определив первоначальные цели терапии СРК.
Лечение
Гетерогенность СРК, даже при выделении индивидуальных подтипов, затрудняет разработку алгоритма лечения, подходящего для всех пациентов. Эффективность давно известных лекарственных средств и диетических рекомендаций анализировалась в различных исследованиях, в которых использовались конечные точки, не рекомендуемые Управлением по контролю качества продуктов питания и лекарственных средств США (FDA) в настоящее время; результативность недавно синтезированных препаратов оценена в широкомасштабных РКИ с конечными точками, одобренными FDA.
Модификация диеты
Многие больные СРК указывают на наличие специфических диетических тригерров, провоцирующих появление симптомов заболевания. Увеличение доли пищевых волокон является традиционной терапией первой линии у пациентов с СРК, но нерастворимые волокна, такие как отруби, могут усиливать абдоминальную боль и вздутие живота. Систематический обзор и метаанализ 7 плацебо-контролируемых исследований (n=499) доказал эффективность растворимых волокон (оболочки семян подорожника обыкновенного) в лечении СРК.
Возрождается интерес к использованию диетотерапии в лечении СРК. Признание того факта, что ферментированные олиго-, ди- и моносахариды, а также полиолы (FODMAP), содержащиеся в косточковых плодах, овощах, лактозосодержащих продуктах, искусственных подсластителях, обостряют симптомы заболевания у некоторых пациентов по причине ферментации и наличия осмотического эффекта, способствовало применению диеты с низким содержанием FODMAP-продуктов в качестве способа лечения СРК. В перекрестном РКИ, сравнивавшем FODMAP-диету с привычным местным рационом, отмечено уменьшение выраженности основных симптомов СРК, а также вздутия и боли при использовании первого подхода. В двух рандомизированных исследованиях, сравнивавших FODMAP-диету с традиционными диетическими рекомендациями (принимать пищу небольшими порциями, избегать приема нерастворимых волокон, жирной пищи и кофеина), продемонстрировано отсутствие значимых различий между указанными подходами. Однако в одном из этих исследований отмечены значительное уменьшение интенсивности абдоминальной боли, вздутия, нормализация частоты и консистенции стула, исчезновение ургентных позывов при использовании FODMAP-диеты.
Некоторые пациенты связывают появление симптомов СРК с употреблением глютена, несмотря на отсутствие иммунологических, серологических и гистологических маркеров целиакии. В одном небольшом РКИ часть больных СРК с отрицательными результатами тестов на целиакию, не отвечавших на безглютеновую диету, продолжала соблюдать диету, а другим рекомендовали употреблять глютенсодержащие маффины и хлеб. В итоге 68% пациентов, получавших глютен, сообщили о плохом контроле над симптомами заболевания, тогда как в группе плацебо этот показатель составил 40% (р<0,001). В другом исследовании, в котором сравнивалась комбинация FODMAP и безглютеновой диеты с исключением только FODMAP-продуктов, продемонстрировано отсутствие дополнительных преимуществ ограничения глютена и не выявлено данных, поддерживающих эту теорию. Несмотря на то что диетотерапия ассоциирована с низким риском, она быстро и значимо изменяет кишечный микробиом; долгосрочные последствия этих изменений не известны.
Спазмолитики и масло мяты перечной
У некоторых пациентов имеют место нарушения гастроинтестинальной моторики и сократимости гладкой мускулатуры. В метаанализе 23 РКИ, анализировавших эффективность спазмолитиков (n=2154), показано превосходство гиосцина, пинаверия, отилония над плацебо, несмотря на небольшое количество больных в этих подгруппах. Ни один из перечисленных препаратов не доступен в США. Одно последовательное исследование результативности пинаверия, в котором приняли участие больные СРК с диареей (n=427), подтвердило эффективность этого препарата в уменьшении абдоминальной боли и улучшении консистенции стула через 4 нед по сравнению с плацебо.
Масло мяты перечной, обладающее спазмолитическими свойствами, способствует релаксации гладкой мускулатуры посредством блокады кальциевых каналов; по данным одного метаанализа, его эффективность превосходит таковую плацебо.
Стимуляторы кишечной секреции
Любипростон и линаклотид являются новыми препаратами, которые воздействуют на интестинальные энтероциты, повышая секрецию жидкости в просвет кишечника за счет увеличения секреции хлоридов и бикарбонатов, а также ускоряя гастроинтестинальный транзит. Оба препарата одобрены FDA для лечения СРК с констипацией. Любипростон, производное простагландина, воздействует на белок натриевых каналов. Обобщенный анализ результатов двух больших рандомизированных исследований (n=1171) показал, что у 18% пациентов, получавших любипростон, выраженность клинических проявлений уменьшилась, тогда как в группе плацебо этот показатель составил 10% (р=0,001). Влияние препарата на интенсивность абдоминальной боли в этих двух исследованиях признана статистически значимой, но умеренной; при его использовании у 8% больных может возникать тошнота.
Линаклотид представляет собой плохо абсорбируемый 14-аминокислотный пептид, воздействующий на рецепторы гуанилатциклазы С. Кроме ускорения гастроинтестинального транзита, препарат ингибирует активность болевых волокон. В 3 исследованиях ІІ фазы (n=1604) частота ответа (определенная как уменьшение абдоминальной боли на ≥30% или увеличение частоты опорожнения кишечника на ≥1 акт) в каждой из работ в группе линаклотида составила 33% по сравнению с 14% и 21% в группе плацебо. Диарея развивалась почти у 20% пациентов, принимавших этот препарат, хотя показатель исключения из исследования по причине диареи был достаточно низким – 5%. Плеканатид, другой агонист гуанилатциклазы С, одобрен FDA в январе 2017 г. для лечения хронической идиопатической констипации; исследования ІІІ фазы с участием больных СРК с констипацией, принимавших этот препарат, завершены.
Лекарства, воздействующие на 5-гидрокситриптаминовые рецепторы 3 типа
В патофизиологии СРК отводится большое значение патологической экспрессии 5-гидрокитриптамина (5-НТ). Лекарства, воздействующие на 5-НТ рецепторы 3 типа, замедляют кишечный транзит. В одном метаанализе доказано превосходство алосетрона над плацебо у больных СРК с диареей в уменьшении выраженности клинических проявлений заболевания (4 исследования; n=1732), снижении интенсивности абдоминальной боли или дискомфорта (6 исследований; n=2830). Нежелательные явления, ассоциированные с приемом этого препарата, одобренного в США для применения у женщин, страдающих СРК с диареей, включают запор и ишемический колит (редко).
Ондансетрон, использующийся в качестве антиэметического препарата уже на протяжении 30 лет, имеет хороший профиль безопасности. В перекрестном рандомизированном исследовании (n=98) доказано, что лечение ондансетроном способствовало нормализации консистенции стула с частотой ответа 80% по сравнению с 41% в группе плацебо; интенсивность абдоминальной боли не уменьшалась.
Препараты, воздействующие на опиоидные рецепторы
Опиоидные рецепторы расположены по всему гастроинтестинальному тракту; лекарства, воздействующие на них, уменьшают восприятие боли и замедляют интестинальный транзит. Лоперамид действует исключительно на µ-опиоидные рецепторы и часто используется для лечения СРК с диареей, хотя доказательства его эффективности немногочисленны. Элуксадолин – это новый препарат, действующий на δ-, κ- и µ-опиоидные рецепторы. В 3 рандомизированных исследованиях ІІ фазы (n=2427) этот препарат превосходил плацебо в лечении СРК с диареей с частой ответа 27% по сравнению с 17% в группе плацебо (р<0,001). Однако интенсивность абдоминальной боли не изменялась. Задокументировано 5 случаев панкреатита (0,3%), 8 случаев спазма сфинктера Одди (0,5%); пациенты, ранее перенесшие холецистэктомию, имели более высокий риск развития нежелательных явлений. Препарат одобрен FDA для лечения СРК с диареей, но не рекомендован пациентам с алкогольной зависимостью или панкреатобилиарной патологией.
Антибиотики и пробиотики
Эффективность минимально абсорбирующегося антибиотика рифаксимина изучалась в 3 рандомизированных исследованиях ІІ фазы, в которых приняли участие больные СРК, в том числе не имевшие признаков констипации (n=1260). По данным обобщенного анализа, рифаксимин превосходил плацебо в уменьшении выраженности типичных симптомов заболевания и вздутия (р<0,001 в обоих случаях), хотя его эффективность была умеренной. Другое большое проспективное исследование доказало, что повторная терапия рифаксимином является безопасной и результативной. Несмотря на то что рифаксимин одобрен FDA для лечения СРК с диареей, рецидивы заболевания у пациентов, ответивших на терапию этим препаратом, достаточно типичны; механизмы действия препарата окончательно не изучены, изменения кишечного микробиома отсутствуют.
Пробиотики являются ослабленными бактериями или бактериальными продуктами, оказывающими полезное влияние на организм хозяина. Метаанализ показал, что штаммы бифидобактерий могут быть полезными как в уменьшении выраженности проявлений заболевания, так и в снижении интенсивности абдоминальной боли (n=501), Lactobacillus plantarum (штам DSM 9843) превосходил плацебо в общей оценке ответа на лечение (данные 3 РКИ; n=314).
Противовоспалительные препараты
Воспалительный процесс низкой активности, наблюдающийся у некоторых больных СРК, в частности у лиц с постинфекционным вариантом СРК, явился основанием для проведения исследований с использованием противовоспалительных препаратов. В ходе рандомизированных исследований преднизолон и препараты 5-аминосалициловой кислоты не смогли продемонстрировать превосходство над плацебо.
Антагонисты рецепторов гистамина
Активация тучных клеток, локализованных на слизистых оболочках, приводящая к выбросу триптазы и гистамина, обусловливает возникновение висцеральной гиперчувствительности у больных СРК. В небольшом плацебо-контролируемом исследовании эбастин, антагонист Н1-рецепторов, способствовал уменьшению висцеральной гиперчувствительности: 46% больных отметили снижение выраженности симптомов заболевания по сравнению с 13% больных, получавших плацебо (р=0,004).
Антидепрессанты и психологическая терапия
Антидепрессанты и психологическая терапия могут улучшить состояние больных СРК в связи с центральной ролью оси «головной мозг – кишечник» в развитии заболевания и патологического восприятия центральной боли. Результаты одного метаанализа показали, что трициклические антидепрессанты превосходили плацебо (11 рандомизированных исследований; n=744). Трициклические антидепрессанты обладают антихолинергическими свойствами и замедляют интестинальный транзит. Эти препараты также превосходят плацебо в купировании абдоминальной боли. Эффективность других антидепрессантов, включая селективные ингибиторы обратного захвата серотонина, остается неясной.
По данным метаанализа, психологическая терапия (когнитивная бихевиоральная терапия и гипнотерапия) может оказывать положительное влияние на состояние больных, но ее эффективность иногда переоценивается в связи отсутствием слепого метода в некоторых исследованиях, а также использованием листа ожидания для получения активного вмешательства в качестве группы сравнения. В рандомизированном исследовании доказано, что эффективность гипнотерапии сопоставима с таковой FODMAP-диеты; дополнительные преимущества комбинации гипнотерапии с FODMAP-диетой по сравнению с монотерапией гипнозом не выявлены.
Дополнительная и альтернативная терапия
Многие пациенты с СРК недовольны эффективностью традиционной медикаментозной терапии и прибегают к другим формам лечения. Преимущества фитопрепаратов окончательно не выяснены, поскольку было проведено небольшое количество исследований. Эффективность зверобоя обыкновенного и STW5 (комбинации нескольких растительных экстрактов) изучалась у больных СРК. STW5 доказал свое превосходство над плацебо, а зверобой обыкновенный – нет. Есть сообщения, что мелатонин может уменьшать абдоминальную боль у пациентов с СРК.
Персонифицированный подход к терапии
Эффективные отношения между доктором и больным, требующие особого сопереживания со стороны врача, увеличивают удовлетворенность пациента проведенным лечением и уменьшают количество последующих консультаций. Уверенность, разъяснение и положительный диагноз являются основными шагами в лечении. Мы рекомендуем начинать лечение с модификации диеты (медленное увеличение количества растворимых волокон, если пациент страдает СРК с констипацией, или временное использование FODMAP-диеты, если пациент страдает СРК с диареей / смешанным вариантом). Мы также рекомендуем увеличить физические нагрузки и уменьшить влияние стрессовых факторов. Можно добавить пробиотик, особенно при выраженном вздутии. Боль можно купировать назначением спазмолитика или трициклического антидепрессанта, диарею – лоперамидом или секвестрантом желчных кислот (холестиполом), констипацию – полиэтиленгликолем. Линаклотид или любипростон могут помочь больным с констипацией; алосетрон, элуксадолин или рифаксимин будут эффективны при диарее.
Рефрактерный СРК ухудшает качество жизни; больные рефрактерным СРК нуждаются в повторных консультациях. Несмотря на проведение медикаментозной терапии, как правило, основной проблемой является болевой синдром, часто обнаруживается психическое заболевание. Полное излечение рефрактерного СРК, как правило, невозможно, но вполне реально научить пациентов жить с симптомами. В этом случае идеальным является мультидисциплинарный командный подход. Следует избегать назначения опиатов, поскольку их применение увеличивает риск развития наркотического кишечного синдрома (вариант опиоидиндуцированной дисфункции кишечника, возникающий при увеличении дозы опиодов для купирования рецидивирующей абдоминальной боли). Сочетание препаратов, воздействующих на кишечник, и лекарств с центральным механизмом действия в комбинации с психологической терапией является ключевым в уменьшении выраженности симптомов. Больные с жалобами, трудно поддающимися лечению, могут нуждаться в трансплантации фекальной микробиоты. Эффективность этого подхода в лечении СРК остается неизвестной, хотя в настоящее время проводятся рандомизированные исследования.
Статья печатается в сокращении.
Ford A.C., Lacy B.E., Talley N.J. Irritable Bowel Syndrome
N Engl J Med 2017; 376:2566-2578. June 29, 2017DOI: 10.1056/NEJMra1607547.
Перевела с англ. Татьяна Можина
Медична газета «Здоров’я України 21 сторіччя» № 20 (417), жовтень 2017 р.


