30 листопада, 2017
Канефрон® Н при лечении рецидивирующего цистита у женщин детородного возраста: рандомизированное контролируемое исследование

Цистит – инфекционно-воспалительный процесс в стенке мочевого пузыря, локализованный в основном в слизистой оболочке. Обычно он сопровождается инфекцией нижних мочевыводящих путей (ИНМП) [1]. Цистит – это неприятное заболевание, но он никогда не приводит к необратимым изменениям в мочевом пузыре или к летальному исходу [2].
Типичными признаками цистита являются обременительные частые позывы к мочеиспусканию. У пациенток может отмечаться также боль в нижней части живота, гематурия и неотложные позывы к мочеиспусканию. Кроме того, моча может быть мутной и иметь неприятный запах.
Escherichia coli (E. coli) – основной патоген, вызывающий цистит в 85% случаев внебольничных и в 50% случаев внутрибольничных ИНМП. При инфекциях мочевого пузыря обычно применяют антибиотикотерапию (АБТ) [1, 3]. Если симптомы легкие, антибактериальное средство может быть назначено после получения результатов бактериологического посева мочи.
У мужчин с нормальным строением мочевыводящих путей ИНМП возникают редко [4]. Что же касается женской популяции, у 1/3 женщин <24 лет в течение жизни отмечался хотя бы 1 эпизод ИНМП, требующий назначения АБТ. Примерно 50% женщин в течение жизни хотя бы раз страдали циститом, из них более чем у половины отмечались 1-2 рецидива. В большинстве случаев рецидивные эпизоды возникают в результате полового контакта, а также могут быть связаны с применением спермицидов, но в некоторых случаях исходные причины неизвестны. Рецидивные эпизоды можно предотвратить путем профилактического применения антибиотиков, хотя при этом существует риск развития резистентности [5, 6].
Лекарственные средства растительного происхождения можно применять для предотвращения развития антибиотикорезистентности, в частности при долговременной профилактике эпизодов рецидивирующего цистита. Одним из таких препаратов является Канефрон® Н («Бионорика СЕ», Германия). Это фиксированная и стандартизованная комбинация лекарственных растительных компонентов (травы золототысячника, корня любистка лекарственного и листьев розмарина), действующих против инфекции и воспаления в мочевыводящих путях. Препарат in vitro оказывает бактерицидное и бактериостатическое действие на различные уропатогены, ингибирует адгезию бактерий к уротелию, улучшает уродинамику и подавляет воспалительные реакции [7, 8]. Улучшения в уродинамике связаны с мягким диуретическим действием [9] и снятием спазмов [10].
Канефрон® Н продемонстрировал высокую эффективность при профилактике хронических/рецидивирующих инфекций и воспалительных патологий мочевыводящих путей [10]. Авторы представляют первое рандомизированное долговременное исследование применения препарата Канефрон® Н для профилактики рецидивных эпизодов цистита у женщин детородного возраста.
Методы
Целью исследования было изучить действие препарата растительного происхождения Канефрон® Н на клиническое течение острого рецидивирующего цистита (ОРЦ), вызванного E. coli, у женщин детородного возраста. В ходе открытого рандомизированно-контролируемого исследования стандартная терапия фторхинолонами (офлоксацин), применяемая в контрольной группе, сравнивалась с применением стандартной терапии в сочетании с препаратом Канефрон® Н.
В исследовании участвовали 90 женщин в возрасте 18-45 лет. У всех пациенток был диагностирован ОРЦ, вызванный E. coli (частота эпизодов составляла 1-2 каждые 6 мес или 3 р/год). Пациентки проходили обследование и лечение в ГУ «Институт урологии НАМН Украины».
Исследование проводилось в соответствии с принципами Хельсинской декларации и было одобрено местным Комитетом по вопросам этики. При включении в исследование применялись следующие методы обследования:
• биохимический анализ крови и общий анализ мочи;
• стандартный бакпосев мочи и тест на восприимчивость к антибактериальным препаратам;
• ультразвуковое исследование мочевого пузыря и почек;
• определение показателя тяжести симптомов ИНМП (табл. 1).
Критериями невключения в исследование являлись:
• нарушение развития мочеполовой системы;
• внутриклеточные патогены, передающиеся половым путем, и патогены, не принадлежащие к E. coli;
• индивидуальная непереносимость компонентов препарата Канефрон® Н;
• камни, нарушающие уродинамику, коралловидный уролитиаз;
• сахарный диабет 1 или 2 типа;
• гематурия, хроническое заболевание почек и другие патологии мочевыделительной системы, способствующие повышению риска рецидива;
• общий показатель тяжести ИНМП по 3 основным симптомам ≤3 или ≥9 баллов (табл. 1);
• связь цистита с половой активностью (посткоитальный цистит).
 Участников случайным образом распределили в исследуемую (n=45) и контрольную группу (n=45). Пациентки обеих групп в течение 7 дней получали АБТ (офлоксацин 200 мг 2 р/сут) по результатам посева мочи. Кроме того, им были даны общие рекомендации по профилактике цистита (употреблять достаточное количество жидкости, не допускать переохлаждения и т. д.). В дополнение к стандартной терапии пациентки в исследуемой группе применяли Канефрон® Н (2 таблетки 3 р/день в течение 3 мес).
Участников случайным образом распределили в исследуемую (n=45) и контрольную группу (n=45). Пациентки обеих групп в течение 7 дней получали АБТ (офлоксацин 200 мг 2 р/сут) по результатам посева мочи. Кроме того, им были даны общие рекомендации по профилактике цистита (употреблять достаточное количество жидкости, не допускать переохлаждения и т. д.). В дополнение к стандартной терапии пациентки в исследуемой группе применяли Канефрон® Н (2 таблетки 3 р/день в течение 3 мес).
После первичного обследования все пациентки проходили контрольное обследование на 7-й день, а затем через 3, 6 и 12 мес; при возникновении рецидивного эпизода обследование проводилось безотлагательно. В каждый контрольный момент времени регистрировались следующие симптомы цистита: боль в мочевом пузыре, жжение и острая боль при мочеиспускании, неотложные позывы к мочеиспусканию и учащенное мочеиспускание маленькими порциями.
Пиурия контролировалась в течение 12 мес. При каждом обследовании проводился подсчет бактерий E. coli в культуре, рецидивы цистита регистрировались в течение периода последующего наблюдения, составлявшего 12 мес.
Критериями рецидивных эпизодов острого цистита были повторяющиеся симптомы ИНМП и положительный результат бакпосева мочи.
Чтобы не допустить искажения результатов из-за ошибок в технике забора мочи, образцы мочи для бакпосева при остром цистите отбирались с помощью катетера НелатонFr 6. Через 3, 6 и 12 мес отбиралась средняя порция мочи без применения катетера.
Все результаты выражались в абсолютном значении и, при необходимости, в процентном отношении. Статистические сравнения проводились с применением t-критерия Стьюдента с двусторонним 95% ДИ, p≤0,05.
Результаты
Частота основных симптомов цистита (боль в мочевом пузыре, жжение и острая боль при мочеиспускании; неотложные позывы к мочеиспусканию; учащенное мочеиспускание маленькими порциями) в целом не отличалась в исследуемой и в контрольной группах (табл. 2), что подтверждает сопоставимость групп. Через 7 дней лечения в обеих группах улучшились все 4 симптома, хотя наблюдалась тенденция к более значительному улучшению в исследуемой группе по сравнению с контрольной. Единственная статистически значимая разница между двумя группами отмечалась в отношении неотложных позывов к мочеиспусканию.
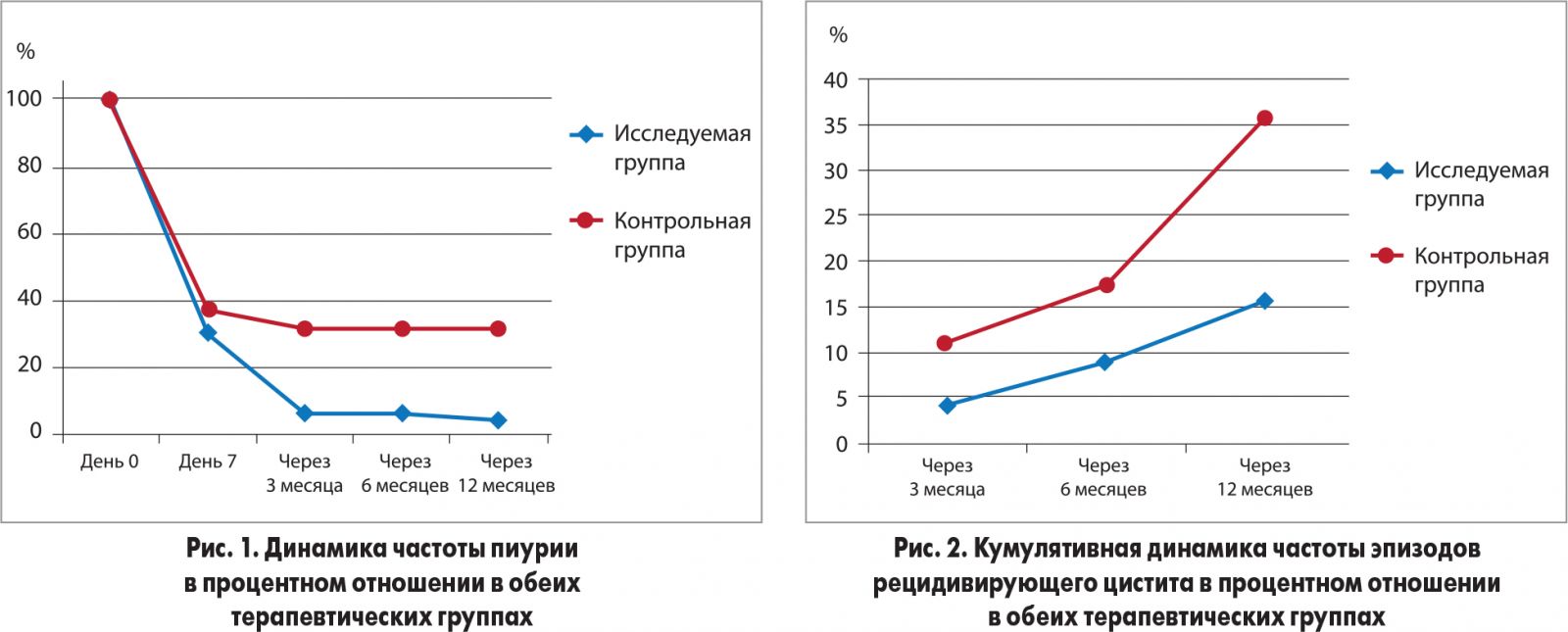
Пиурия (≥6 лейкоцитов в поле видимости микроскопа) изначально фиксировалась у всех пациенток обеих групп. В дальнейшем пиурия чаще отмечалась в контрольной группе (рис. 1). Эта разница была статистически значимой через 3 мес (31,1 по сравнению с 6,7%, p≤0,05), через 6 мес (31,1 по сравнению с 6,6%, p≤0,05) и через 12 мес (31,1 по сравнению с 4,4%, p≤0,05). Каждые 3 мес разница между группами оставалась неизменной.
Результаты посева на E. coli анализировались отдельно при наличии бактериурии (титр E. coli ≥103 КОЕ/мл) и при отсутствии бактериурии.
Изначально бактериурия наблюдалась у всех пациенток в обеих группах (100%). В дальнейшем количество пациенток с бактериурией было стабильно более низким в исследуемой группе по сравнению с контрольной. Эта разница была статистически значимой через 3 и через 12 мес (табл. 3).
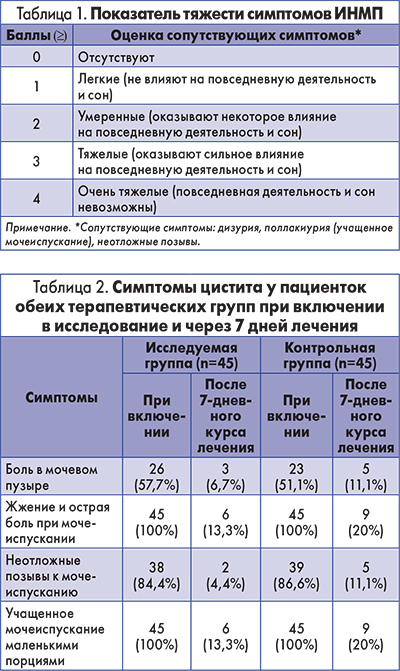
Частота рецидивных эпизодов острого неосложненного цистита была стабильно более низкой в исследуемой группе (рис. 2). Эта разница была статистически значимой через 6 мес (8,9 vs 7,8%) и через 12 мес (15,5 vs 35,5%).
В течение 12 мес средний показатель тяжести симптомов ИНМП при рецидивных эпизодах цистита составлял 6 баллов в контрольной группе и 3 балла – в исследуемой.
Комментарий
Данное рандомизированно-контролируемое исследование было проведено с участием женщин детородного возраста, страдающих рецидивирующим циститом с острыми эпизодами. Пациентки в исследуемой группе получали такую же терапию, как и пациентки в контрольной группе, но дополнительно принимали препарат растительного происхождения Канефрон® Н (2 таблетки 3 р/день в течение 3 мес).
В течение первых 7 дней лечения симптомы цистита улучшились в обеих группах. Наблюдалась тенденция к лучшим результатам в исследуемой группе по сравнению с контрольной, но разница была статистически значимой только относительно неотложных позывов к мочеиспусканию (4,44 vs 11,1%).
Через 3, 6 и 12 мес после завершения АБТ пиурия была значительно менее выраженной в исследуемой группе (рис. 1). В этот период более низким был также показатель наличия бактериурии (табл. 3). Наконец, в исследуемой группе отмечалась более низкая частота рецидивных эпизодов острого цистита через 6 и 12 мес (рис. 2).
В течение 12 мес средний показатель тяжести симптомов ИНМП при рецидивных эпизодах цистита составлял 6 баллов в контрольной группе и 3 балла – в исследуемой. Это может свидетельствовать о том, что тяжесть рецидивов в исследуемой группе была менее выраженной, чем в контрольной.
Эти эффекты могут быть связаны с фармакологической активностью препарата Канефрон® Н, в том числе с его диуретическим, спазмолитическим, противовоспалительным, антибактериальным и нефропротекторным действием [10]. Учитывая вариабельность хемотипов лекарственных растений и методов производства препаратов растительного происхождения, важно отметить, что Канефрон® Н представляет собой фиксированную комбинацию экстрактов лекарственных растений (травы золототысячника, корня любистка и листьев розмарина), где особое внимание уделяется вопросу стандартизации и воспроизводимости ингредиентов.
Сложнее объяснить разницу показателей между группами через 6 и 12 мес после лечения, когда пациентки больше не принимали Канефрон® Н. Можно предположить, что физиологический эффект, оказываемый препаратом Канефрон® Н (например, уменьшение воспаления), длится дольше, чем немедленное действие компонентов препарата растительного происхождения. В любом случае снижение частоты рецидивных эпизодов цистита можно объяснить стойкими положительными изменениями в мочевыводящих путях и, возможно, изменением характера связи между микро- и макроорганизмами. Этот вопрос подлежит изучению в дальнейших фармакокинетических исследованиях.
К ограничениям данного исследования относятся отсутствие маскировки данных для пациенток и врача в ходе всего исследования, характеризации отдельных компонентов препарата растительного происхождения и более глубоких исследований урологической функции.
Выводы
Применение препарата растительного происхождения Канефрон® Н женщинами детородного возраста, страдающими ОРЦ, может снизить частоту рецидивных эпизодов, а также бактериурии и пиурии. Для обобщения результатов необходимы дополнительные исследования, в том числе долговременные, с участием женщин более старшего возраста.
Имеющиеся данные свидетельствуют, что Канефрон® Н представляет собой инновационное эффективное средство для лечения рецидивирующего цистита. Благодаря сложному составу препарата Канефрон® Н риск развития резистентности бактерий может быть более низким, чем при применении АБТ для лечения того же заболевания. Эту возможность также следует изучить.
Список литературы находится в редакции.