3 січня, 2018
Токсические и медикаментозные повреждения печени: основные направления коррекции
По материалам научно-практической конференции «Полиморбидная патология органов пищеварения в практике семейного врача», 9-10 ноября, г. Днепр
Токсические поражения печени все чаще встречаются в практике семейного врача и гастроэнтеролога. Этой проблеме уделялось особое внимание на состоявшейся в Днепре конференции «Полиморбидная патология органов пищеварения в практике семейного врача», ведь именно лекарственно индуцированные поражения печени выходят сегодня на первый план, поскольку пациенты с коморбидностью вынуждены принимать одновременно несколько медикаментозных средств.
 О возможностях коррекции лекарственных поражений печени рассказал директор ГУ «Институт гастроэнтерологии НАМН Украины» (г. Днепр), доктор медицинских наук, профессор Юрий Миронович Степанов.
О возможностях коррекции лекарственных поражений печени рассказал директор ГУ «Институт гастроэнтерологии НАМН Украины» (г. Днепр), доктор медицинских наук, профессор Юрий Миронович Степанов.
– Среди причин токсических повреждений печени выделяют продолжительный прием синтетических медикаментов (цитостатиков, антибиотиков, психотропных веществ), длительное воздействие на организм продуктов бытовой химии, отравление ядовитыми грибами, загрязнение окружающей среды, профессиональные вредности, злоупотребление спиртными напитками. Среди перечисленных выше причин неслучайно на первом месте именно медикаменты. Сегодня достаточно часто пациенты принимают одновременно ≥3-6 лекарственных средств. Как при этом взаимодействуют между собой метаболиты этих лекарств, неизвестно. Некоторые из препаратов даже при использовании в монотерапии оказывают токсическое действие на паренхиму печени.
! По данным американских исследователей, лекарственные средства являются причиной желтухи в 2-5% случаев у стационарных больных, 40% гепатитов у пациентов старше 40 лет, 25% случаев фульминантной (острой) печеночной недостаточности.
К основным механизмам медикаментозного повреждения печени относят прямое токсическое действие препарата на клетки печени (встречается редко), токсическое действие метаболитов лекарственных средств и иммуноаллергическое поражение паренхимы печени, спровоцированное приемом лекарств (Полунина Т. Е., 2005). Основной системой метаболизации лекарственных средств в печени служит система ферментов цитохрома Р450. Идентифицированы по меньшей мере 50 изоферментов системы Р450, однако на самом деле их, несомненно, больше. У человека метаболизм лекарств обеспечивают цитохромы, относящиеся к трем семействам: P450-I, P450-II, P450-III. В процессе метаболизации лекарств образуются токсичные метаболиты, которые повреждают гепатоциты и приводят к их гибели. Когда два активных средства конкурируют за один участок связывания на ферменте, метаболизм препарата с меньшей аффинностью замедляется и срок его действия увеличивается. Это ведет к более продолжительному воздействию токсичного вещества на гепатоцит. К примеру, этанол индуцирует синтез Р450-II-Е1 и тем самым увеличивает токсичность парацетамола. Токсичность парацетамола повышается и при лечении изониазидом, который также индуцирует синтез Р450-II-Е1 (Полунина Т. Е., 2005).
На молекулярном уровне одним из важнейших (и в целом универсальных) механизмов повреждения гепатоцитов является перекисное окисление липидов под действием свободных радикалов. Помимо этого, гепатоциты могут повреждаться путем денатурации клеточных белков, истощения запасов АТФ, дисфункции митохондрий, блокады транспортной РНК, нарушения гомеостаза кальция и разрушения цитоскелета.
Одна из серьезных проблем, интерес к которой с каждым годом возрастает, – гепатотоксичность фитопрепаратов и диетических добавок. Сеть по изучению гепатотоксических эффектов лекарственных средств (Drug Induced Liver Injury Network – DILIN) сообщает, что примерно 20% случаев лекарственных поражений печени вызваны приемом фитопрепаратов и диетических добавок (Navarro V. J., Barnhart H. et al., 2014). По другим данным, их доля в структуре причин лекарственных поражений печени достигает 73% (Bessone F., Hernandez N., 2013). Вместе с тем частота обращений пациентов по поводу таких побочных эффектов составляет <1% от числа произошедших случаев. Наиболее сложной представляется ситуация в плане диагностики и лечения поражений печени мультикомпонентными фитопрепаратами и диетическими добавками. В таких случаях практически не представляется возможным установить причинно значимый токсический агент. В Украине ситуация не лучше, чем в западных странах. В результате дерегуляции рынка диетических добавок в нашей стране фактически отсутствует контроль за их оборотом. В этой связи ответственность за побочные эффекты приема таких средств ложится на врачей, которые их рекомендуют, или пациентов, принимавших их самостоятельно.
Для восстановления структуры и функции гепатоцитов рационально использование эссенциальных фосфолипидов (ЭФЛ). Хорошо известно, что клеточные мембраны в среднем на 75%, а мембраны митохондрий на 92% состоят из ЭФЛ. От состава фосфолипидов мембран зависит их текучесть, проницаемость, рецепторная и ферментативная активность связанных с мембраной белков, а также физиологическая активность простагландинов и тромбоксанов, которые синтезируются из мембранных фосфолипидов. Фосфолипиды также принимают участие в процессах молекулярного транспорта, делении и дифференцировке клеток; стимулируют активность различных ферментных систем.
ЭФЛ обладают широким спектром гепатопротекторных эффектов:
- за счет встраивания в мембраны клеток печени повышают их стабильность, уменьшают апоптоз гепатоцитов;
- обеспечивают цитопротекторное действие (уменьшают свободнорадикальное повреждение и перекисное окисление липидов);
- улучшают физиологические показатели мембраны (текучесть и проницаемость);
- ускоряют регенерацию клеток печени;
- повышают интенсивность процессов детоксикации;
- имеют иммуномодулирующие свойства;
- замедляют трансформацию звездчатых клеток в коллагенпродуцирующие, повышают активность коллагеназы, обеспечивая тем самым антифибротический эффект;
- улучшают липидный обмен, проявляют гипохолестеринемическую активность;
- стабилизируют состав желчи.
При встраивании молекул насыщенных жирных кислот в мембрану клетки формируются локальные участки, через которые осуществляется пассивная диффузия ионов по градиенту концентрации – потеря ионов калия клеткой и накопление натрия и кальция. Дисбаланс катионов приводит к нарушению функции клеток. ЭФЛ способны восстанавливать целостность мембран и прекращать разрушение клеток (Вялов С. С., 2013).
Одним из препаратов ЭФЛ на украинском рынке является Энерлив®. Препарат выпускается в мягких желатиновых капсулах, каждая из которых содержит 300 мг обогащенных соевых фосфолипидов с высоким содержанием (≥76%) полиненасыщенного фосфатидилхолина. Благодаря этому Энерлив® в полной мере проявляет присущие ЭФЛ гепатопротекторный, гипохолестеринемический, антифибротический эффекты.
Энерлив® использовался нами в собственных исследованиях, проведенных на базе ГУ «Институт гастроэнтерологии НАМН Украины» с целью оценки влияния терапии ЭФЛ на функциональное состояние печени у пациентов с вирусным гепатитом С и неалкогольной жировой болезнью печени (НАЖБП). Как при вирусном гепатите С, так и в случае НАЖБП лечение ЭФЛ (Энерлив®) сопровождалось улучшением субъективных, объективных и клинико-лабораторных симптомов.
В динамике лечения препаратом Энерлив® у пациентов с вирусным гепатитом С отмечены снижение частоты жалоб на боль в правом и левом подреберьях, чувство тяжести и распирания в этих областях, а также уменьшение интенсивности болевого синдрома. Проявления диспепсического синдрома также уменьшились, гораздо реже пациентов беспокоили горечь во рту, вздутие живота, изжога. Данные физикального обследования продемонстрировали положительное влияние ЭФЛ на болевой синдром и размеры печени. Болезненность в правом и левом подреберьях отмечалась реже в 2,8 (p<0,01) и 3,7 раза (p<0,02) соответственно, болезненность в эпигастрии беспокоила в 4 раза реже (p<0,05), чем до лечения.
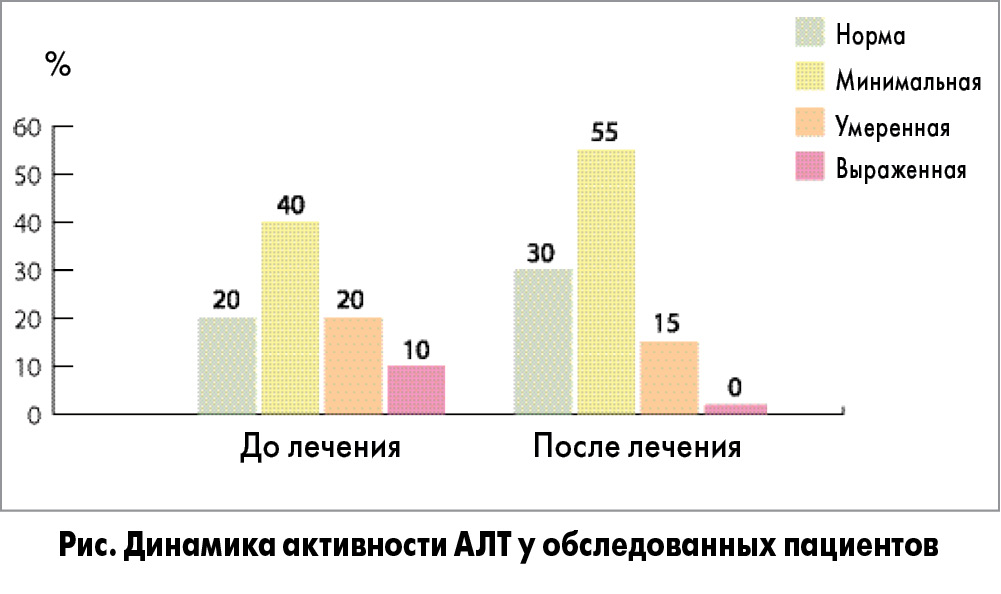 При анализе влияния ЭФЛ на функциональное состояние печени было установлено снижение активности показателей цитолиза – аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ) в 1,8 (р<0,01) и 1,2 раза соответственно. Кроме того, выявлена тенденция к улучшению показателей, характеризующих синдром холестаза. Степень выраженности цитолитического синдрома среди пациентов с повышенными уровнями АЛТ снизилась в среднем в 1,2 раза за счет отсутствия высокой активности фермента (рис.).
При анализе влияния ЭФЛ на функциональное состояние печени было установлено снижение активности показателей цитолиза – аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ) в 1,8 (р<0,01) и 1,2 раза соответственно. Кроме того, выявлена тенденция к улучшению показателей, характеризующих синдром холестаза. Степень выраженности цитолитического синдрома среди пациентов с повышенными уровнями АЛТ снизилась в среднем в 1,2 раза за счет отсутствия высокой активности фермента (рис.).
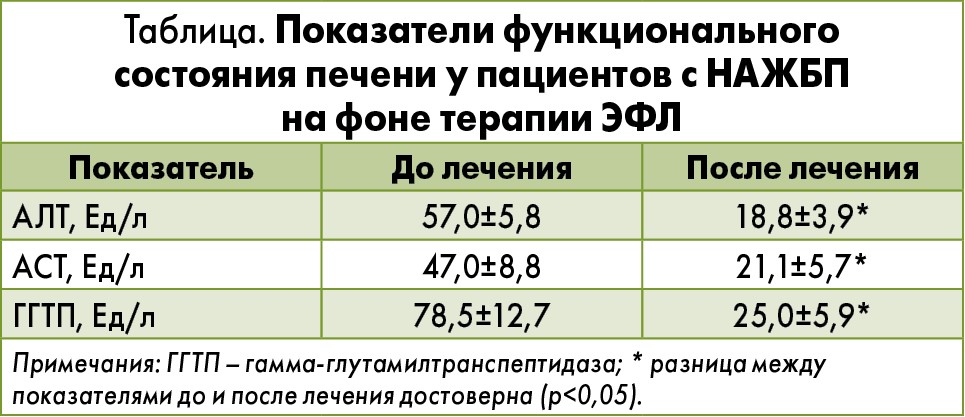
В другом нашем исследовании использование ЭФЛ у пациентов с диффузными заболеваниями печени (НАЖБП) также способствовало значительному улучшению функционального состояния печени (табл.).
 Принципиально важным моментом является положительное воздействие ЭФЛ на показатели жесткости и степень стеатоза печени. Пациентам проводили эластометрию с функцией САР™. В основе этого метода лежит реакция материала на сжатие: чем выше плотность печени, тем быстрее распространяются и отражаются испускаемые датчиком волны.
Принципиально важным моментом является положительное воздействие ЭФЛ на показатели жесткости и степень стеатоза печени. Пациентам проводили эластометрию с функцией САР™. В основе этого метода лежит реакция материала на сжатие: чем выше плотность печени, тем быстрее распространяются и отражаются испускаемые датчиком волны.
Для оценки жесткости паренхимы печени использовались такие эластометрические критерии: <7,1 кПа соответствует стадии фиброза F0-F1; 7,1-8,7 кПа – стадии F1-F2; 8,7-9,5 кПа – F2; 9,5-12,5 кПа – F3; 12,5-14,5 кПа – F3-F4; >14,5 кПа – стадии фиброза F4 по шкале METAVIR.
В проведенном нами исследовании терапия ЭФЛ способствовала достоверному уменьшению жесткости печени с 6,0±2,3 до 4,8±1,7 кПа. Эти данные говорят о возможности не только замедления, но и регресса фибротических изменений в печени под влиянием ЭФЛ.
Эластометрия печени с функцией САР™ (controlled attenuation parameter – контролируемый параметр затухания) позволяет количественно рассчитать снижение амплитуды ультразвуковых сигналов в печени, которая зависит от суммарного объема липидных включений в исследуемой части печени и выражается в дБ/м в абсолютных единицах. Возможности данной методики позволяют верифицировать стеатоз печени на ранних этапах развития, когда диагностика при помощи ультразвукового исследования затруднена.
Для оценки степени стеатоза были использованы такие критерии CAP:
<232 дБ/м (степень стеатоза S0) – доля гепатоцитов с жировыми включениями составляет <10%;
233-255 дБ/м (степень стеатоза S1) – доля гепатоцитов с жировыми включениями равняется 11-33%;
256-289 дБ/м (степень стеатоза S2) – доля гепатоцитов с жировыми включениями варьирует в пределах 34-66%;
≥290 дБ/м (степень стеатоза S3) – доля гепатоцитов с жировыми включениями достигает 67-100%.
В результате лечения ЭФЛ степень жировой инфильтрации печени у пациентов с НАЖБП достоверно снизилась с 243,7±44,5 до 214,8±30,2.
Таким образом, токсические поражения печени представляют собой реальную угрозу для пациентов, принимающих несколько лекарственных средств одновременно. В последние годы возрастает обеспокоенность в отношении токсического потенциала фитопрепаратов и диетических добавок.
Использование ЭФЛ – эффективная стратегия гепатопротекции у пациентов с токсическими поражениями печени. В проведенных нами исследованиях Энерлив® продемонстрировал высокую эффективность в лечении пациентов с вирусным гепатитом С и НАЖБП, способность положительно влиять на маркеры цитолиза, степень фиброза и стеатоза печени.
Подготовила Мария Маковецкая
Медична газета «Здоров’я України 21 сторіччя» № 24 (421), грудень 2017 р.


