3 січня, 2018
Клинический случай: патологическая усталость, ночная потливость, генерализованная лимфоаденопатия – ваше мнение?
Представляем вниманию читателей клинический случай, опубликованный в авторитетном издании The New England Journal of Medicine.
K. Heaton (терапевт). 57-летняя женщина амбулаторно наблюдалась в ревматологическом отделении нашего госпиталя с жалобами на усталость, ночную потливость, снижение массы тела, головную и диффузную абдоминальную боль, поражение кожи.
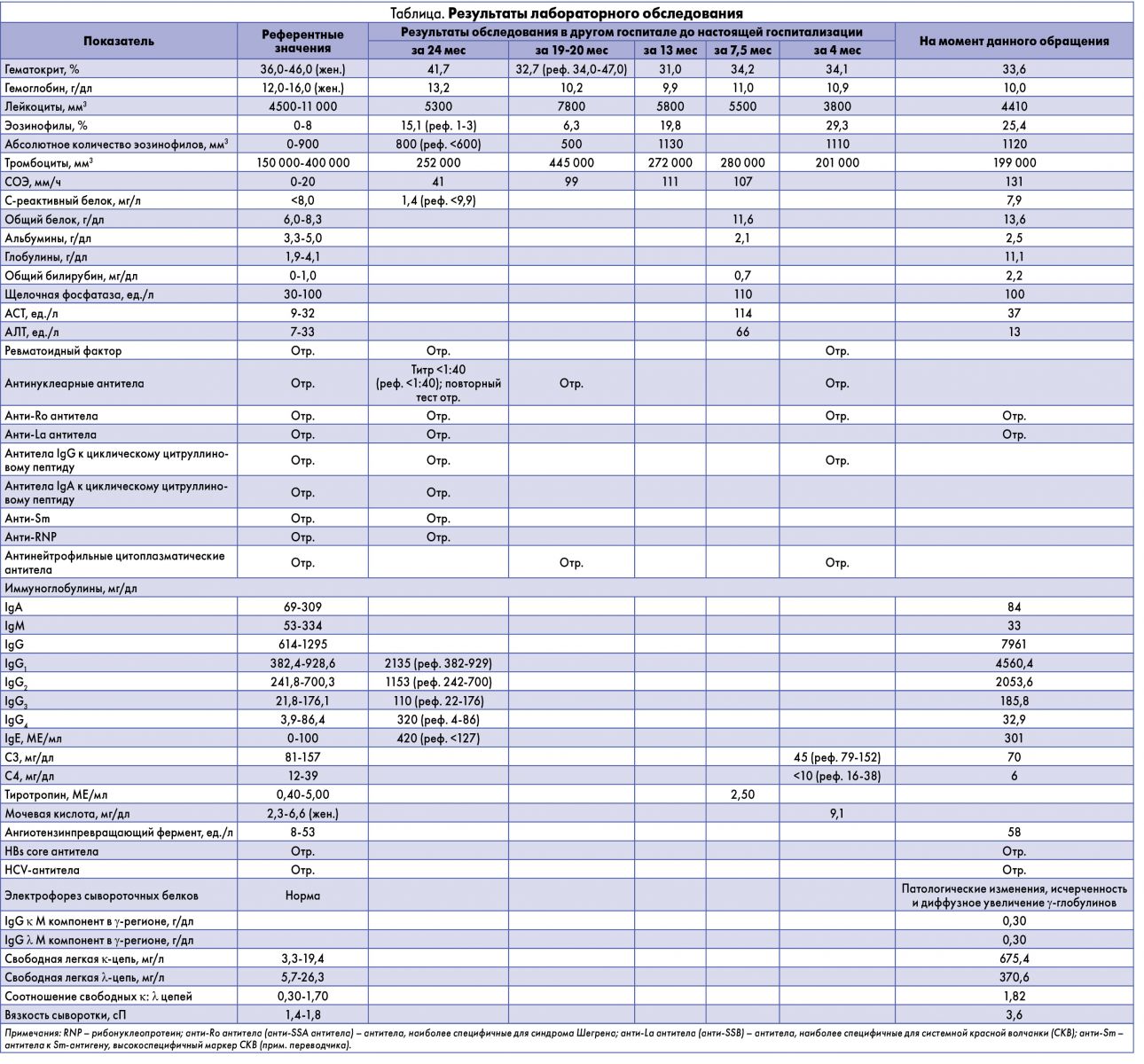
Пациентка чувствовала себя относительно удовлетворительно примерно за 24 мес до данного обращения, когда появился сухой непродуктивный кашель. Результаты лабораторного обследования, выполненные в другой клинике, представлены в таблице.
Двадцать один месяц назад при осмотре терапевтом другого лечебного учреждения пациентка предъявляла жалобы на персистирующий кашель, снижение аппетита и умеренную абдоминальную боль, не имеющую четкой локализации. На момент осмотра ее вес составлял 108,9 кг (5 мес назад исходная масса тела была равна 122,5 кг). Пациентке был назначен ингибитор протонной помпы. В течение следующего месяца возникла усталость и миалгии, затем появились болезненные «красные точки» вокруг щиколоток. Результаты исследования биоптатов кожи соответствовали начальной стадии пурпурозного пигментного дерматита. В клиническом анализе крови зафиксирована периферическая эозинофилия.
За двадцать месяцев до настоящего обращения пациентка обследовалась в другой клинике в связи с персистирующим кашлем; результаты лабораторного обследования приведены в таблице. Рентгенография органов грудной клетки (ОГК) без патологии. При компьютерной томографии (КТ) ОГК, органов брюшной полости (ОБП), малого таза, выполненной с контрастным усилением, зафиксировано легкое диффузное утолщение бронхиальной стенки (данные, указывающие на хроническое воспаление). Умеренно увеличенные лимфатические узлы обнаружены в паракардиальной области, воротах печени, брыжейке тонкой кишки и забрюшинном пространстве.
На протяжении следующего года пациентка неоднократно получала консультации аллерголога, ревматолога, онколога-гематолога, эндокринолога, гастроэнтеролога. Девятнадцать месяцев назад проведена эзофагогастродуоденоскопия и патогистологическое исследование биоптатов антрального отдела желудка; диагностирован легкий хронический и фокальный активный гастрит. Иммуногистохимическое окрашивание на Helicobacter pylori дало отрицательный результат, ворсинки тонкого кишечника без патологических изменений.
A. Sharma. При магнитно-резонансной томографии ОБП, выполненной в другом госпитале 18 мес назад, обнаружено увеличение перипортальных лимфоузлов. Не выявлены локальные изменения печени, поджелудочной железы, почек, селезенки, надпочечников. Отмечена незначительная спленомегалия. Поджелудочная железа не увеличена. Шестнадцать месяцев назад при КТ ОГК, ОБП, малого таза, выполненной с внутривенным введением контрастного вещества, зафиксированы незначительное утолщение бронхиальной стенки, лимфоаденопатия в подмышечных областях (наибольший узел – 2,3 х 1,3 см – локализовался в правой подмышечной области), увеличение правого эпикардиального лимфоузла (1,5 х 1,1 см), гиперплазия лимфоузлов в портокавальной, перипанкреатической, мезентериальной областях (наибольший узел находился в воротах печени – 4,2 х 2,9 см).
К. Heaton. Спустя месяц при патогистологическом исследовании правого подмышечного лимфоузла отмечена сохранность его архитектуры. Обнаружены фолликулярная и паракортикальная гиперплазия наряду с разнотипным плазмоцитозом. Иммуногистохимическое исследование на наличие ДНК вируса герпеса человека 8 типа дало отрицательный результат. Полученные данные характерны для реактивной лимфоаденопатии; доказательства гематологической онкопатологии не выявлены. Пробное лечение пероральным метоклопрамидом, цетиризином, омепразолом, будесонидом, назальным спреем флутиказона, ингаляционным флутиказоном/сальмотеролом не способствовало улучшению состояния. Пациентка продолжала терять вес.
А. Sharma. Тринадцать месяцев назад при позитронно-эмиссионной томографии (ПЭТ) с 18F-фтордезоксиглюкозой (ФДГ), выполненной в другой клинике, обнаружены лимфоузлы с повышенным накоплением ФДГ в подмышечной и паракардиальной областях, а также в области правой внутренней грудной артерии. Печень и селезенка были увеличены и диффузно накапливали ФДГ.
 К. Heaton. При изучении биоптатов и аспиратов костного мозга обнаружен гиперклеточный костный мозг со зрелым трехростковым гематопоэзом, увеличенным количеством эозинофилов, мегакариоцитов, поликлональных плазматических клеток; полученные данные были характерны для реактивного процесса. Проведена биопсия печени для определения генеза гепатоспленомегалии и обнаружения причины накопления ФДГ в печени и селезенке. Патологистологическое исследование биоптата, полученного при толстоигольной биопсии печени, выявило признаки умеренно-выраженного / выраженного портального, перипортального и лобулярного воспаления, в котором доминировали плазматические клетки (с разнотипной экспрессией κ- и λ-легких цепей иммуноглобулинов при иммуногистохимическом окрашивании) и единичные эозинофилы. Также наблюдались пролиферация желчных протоков, локальное повреждение, интраэпителиальные лимфоциты, рассеянные апоптотические гепатоциты; трехцветное окрашивание выявило наличие синусоидального фиброза. Окрашивание на наличие железа дало отрицательный результат. Полученные данные расценены как соответствующие перекрестному синдрому аутоиммунного гепатита и фокального склерозирующего холангита. Начатое лечение преднизолоном было прервано пациенткой по непонятным причинам. В это же время была начата терапия азатиоприном. Зафиксировано снижение интенсивности абдоминальной боли и усталости.
К. Heaton. При изучении биоптатов и аспиратов костного мозга обнаружен гиперклеточный костный мозг со зрелым трехростковым гематопоэзом, увеличенным количеством эозинофилов, мегакариоцитов, поликлональных плазматических клеток; полученные данные были характерны для реактивного процесса. Проведена биопсия печени для определения генеза гепатоспленомегалии и обнаружения причины накопления ФДГ в печени и селезенке. Патологистологическое исследование биоптата, полученного при толстоигольной биопсии печени, выявило признаки умеренно-выраженного / выраженного портального, перипортального и лобулярного воспаления, в котором доминировали плазматические клетки (с разнотипной экспрессией κ- и λ-легких цепей иммуноглобулинов при иммуногистохимическом окрашивании) и единичные эозинофилы. Также наблюдались пролиферация желчных протоков, локальное повреждение, интраэпителиальные лимфоциты, рассеянные апоптотические гепатоциты; трехцветное окрашивание выявило наличие синусоидального фиброза. Окрашивание на наличие железа дало отрицательный результат. Полученные данные расценены как соответствующие перекрестному синдрому аутоиммунного гепатита и фокального склерозирующего холангита. Начатое лечение преднизолоном было прервано пациенткой по непонятным причинам. В это же время была начата терапия азатиоприном. Зафиксировано снижение интенсивности абдоминальной боли и усталости.
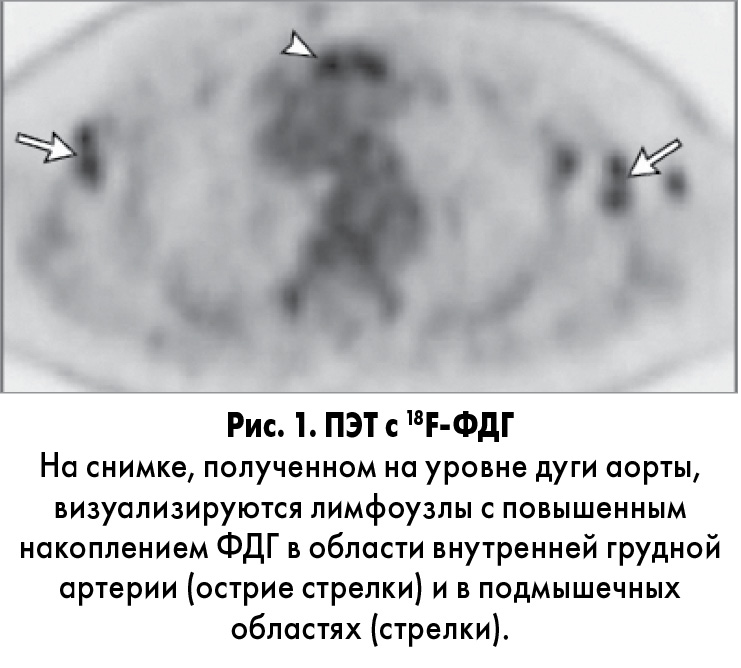
А. Sharma. Семь месяцев назад в другом госпитале была выполнена ПЭТ с ФДГ и КТ для коррекции поглощения излучения (рис. 1).
Зафиксированы спленомегалия, стабильно увеличенные лимфоузлы с повышенным накоплением ФДГ в подмышечной области, около внутренней грудной артерии, ретроперитонеально, в подвздошной и паховой областях. Прикорневая лимфоаденопатия не обнаружена. Отмечено диффузное, умеренное утолщение бронхиальной стенки. Легочные лимфоузлы или затемнение воздушности легких не визуализировались.
 К. Heaton. Месяц спустя был удален паховый лимфоузел. Патогистологическое исследование выявило фолликулярную гиперплазию и разнотипный мастоцитоз в мозговой и синусоидальной области. Выполнено иммуногистохимическое исследование для обнаружения IgG и IgG4; небольшая фракция плазматических клеток была иммунореактивной по отношению к IgG4. За 4 мес до настоящего обращения пациентка была повторно обследована по причине непродуктивного кашля, выраженной усталости, потери массы тела, анорексии, абдоминальной боли, тошноты, рвоты, артралгии, диффузного акне, отечности правого колена и ночной потливости. Зафиксирована дальнейшая потеря веса (до 88,5 кг при исходной массе 122,5 кг). Результаты дополнительных лабораторных исследований приведены в таблице. Два месяца назад появилась сильная, прогрессирующая битемпоральная головная боль. Пациентка была направлена в ревматологическое отделение нашей клиники.
К. Heaton. Месяц спустя был удален паховый лимфоузел. Патогистологическое исследование выявило фолликулярную гиперплазию и разнотипный мастоцитоз в мозговой и синусоидальной области. Выполнено иммуногистохимическое исследование для обнаружения IgG и IgG4; небольшая фракция плазматических клеток была иммунореактивной по отношению к IgG4. За 4 мес до настоящего обращения пациентка была повторно обследована по причине непродуктивного кашля, выраженной усталости, потери массы тела, анорексии, абдоминальной боли, тошноты, рвоты, артралгии, диффузного акне, отечности правого колена и ночной потливости. Зафиксирована дальнейшая потеря веса (до 88,5 кг при исходной массе 122,5 кг). Результаты дополнительных лабораторных исследований приведены в таблице. Два месяца назад появилась сильная, прогрессирующая битемпоральная головная боль. Пациентка была направлена в ревматологическое отделение нашей клиники.
При обследовании в нашей клинике пациентка предъявляла жалобы на ежедневную краниалгию и боль в челюстях при пережевывании пищи. Больную не беспокоили сухость глаз или языка. Пациентка страдала гипертонией, анемией, жаловалась на хроническую посттравматическую боль в левом колене (травма имела место 6 лет назад), перенесла гистерэктомию. Кожные туберкулиновые пробы, выполненные 2,5 года назад, дали отрицательный результат. Медикаментозная терапия включала будесонид, азатиоприн, омепразол, метоклопрамид, лозартан. Напроксен провоцировал появление сыпи; других аллергических реакций или проявлений атопии не было. Пациентка умеренно употребляла спиртные напитки, не курила, не принимала наркотики. Ее мать страдала сахарным диабетом и гипертонией, отец умер от рака толстого кишечника в возрасте 70 лет. Дочь пациентки страдает системной красной волчанкой, трое сыновей и пять родных братьев и сестер здоровы.
При объективном осмотре температура тела составляла 35,1 °C, артериальное давление – 178/96 мм рт. ст., пульс – 114 уд./мин, насыщение кислородом при вдыхании окружающего воздуха – 95%. Рост – 165 см, вес – 87,5 кг, индекс массы тела – 32,1 кг/м2. Верхние веки были приподняты, слезные железы отечны с двух сторон (рис. 2А). Височные артерии набухшие, уплотненные, билатерельно узловаты с сильным пульсом, безболезненны (рис. 2В). Обнаружены двухсторонняя гипертрофия слюнных желез и безболезненный лимфоузел по задней поверхности шеи диаметром до 1 см. При пальпации живота выявлена умеренная болезненность в левом нижнем квандранте, пальпаторно обнаружен нижний полюс селезенки. В правом колене и левой лодыжке отмечен теплый синовиальный выпот. Левая лодыжка болезненна, рядом локализовались области с пальпируемой и непальпируемой пурпурой (рис. 2С). Остальные объективные данные без особенностей. Содержание в крови электролитов, кальция, глюкозы, щелочной фосфатазы и результаты почечных функциональных тестов находились в рамках нормативных значений. Анализ на антитела к вирусам гипатита С и B был отрицательным. Результаты других тестов представлены в таблице.
Рис. 2. Клинические фотографии
Верхнее веко приподнято, отек слезной железы (А). Височная артерия припухлая, узловатая, безболезненная (В). Области с пальпируемой и непальпируемой пурпурой на ногах (С).
Дифференциальный диагноз
P. Monach. При проведении дифференциального диагноза с целью объяснения синдромов, имеющихся у пациентки, было бы идеально определить одно заболевание, которое объясняло все проявления. Однако не существует типичного диагноза, полностью бы их пояснившего; все симптомы, наблюдаемые в этом случае, атипичны. Поэтому необходимо избежать исключения диагноза только на основании наличия одного или нескольких атипичных проявлений. Все это делает данный случай достаточно сложной задачей. Кроме того, некоторые представленные лабораторные данные могут быть неправильно интерпретированы. Наиболее важными клиническими особенностями при проведении дифференциального диагноза, по моему мнению, являются отечность слезных и слюнных желез, поликлональная гипергаммаглобулинемия, гипокомплементемия, плазмоцитоз в биоптатах различных органов. Эти четыре особенности позволят быстро исключить три наиболее вероятных заболевания: гигантоклеточный артериит (ГКА), саркоидоз, эозинофильный гранулематоз с полиангиитом (ЭГсП).
Гигантоклеточный артериит
Наличие головной боли, привычного вывиха нижней челюсти, конституциональных симптомов (симптомов, свидетельствующих о генерализации процесса), пальпаторных изменений височной артерии, увеличение скорости оседания эритроцитов (СОЭ) у пациентов >50 лет свидетельствует о ГКА даже при отрицательных результатах биопсии височной артерии. В то же время многие другие признаки исключают это заболевание, включая абдоминальную боль, сыпь, отечность слезных и слюнных желез, гипергаммаглобулинемию, гипокомплементемию, эозинофилию, плазмоцитоз в лимфоузлах и особенно в печени. Краниалгия – это неспецифический симптом, повышенная вязкость крови также может дать альтернативное объяснение этой жалобе. Пациентка может страдать височным артериитом, но он вряд ли будет гигантоклеточным.
Саркоидоз
Лимфоаденопатия и мультисистемное поражение, включая кожные покровы, печень, легкие, слезные и слюнные железы, характерны для саркоидоза. Также могут наблюдаться артрит, конституциональные симптомы, эозинофилия. Однако гипергаммаглобулинемия и гипокомплементемия не свойственны саркоидозу, а отсутствие гранулем во множественных биоптатах лимфоузлов исключает данный диагноз.
Эозинофильный гранулематоз с полиангиитом
Многие симптомы у данной пациентки характерны для ЭГсП, включая эозинофилию, кашель, абдоминальную боль, конституциональные симптомы, артралгию, миалгию. Типично повышение уровня IgE и IgG4, но гипергаммаглобулинемия, включая другие изотипы IgG, гипокомплементемию и плазмоцитоз, не свойственны. У пациентки нет некоторых проявлений, наиболее характерных для ЭГсП, таких как астма, инфильтраты в паренхиме легких, воспаление придаточных пазух носа и периферическая нейропатия. Наличие плазматических клеток в биоптатах лимфоузлов, печени противоречит диагнозу ГКА, саркоидоза и ЭГсП.
Аутоиммунный гепатит и многоочаговая болезнь Кастлемана
Приблизительно за год до обследования в нашем госпитале была выполнена биопсия печени; полученные результаты позволяли предположить аутоиммунный гепатит. Однако результаты биопсии лимфоузлов напоминали плазматический вариант многоочаговой болезни Кастлемана (МБК). Поликлональная гипергаммаглобулинемия характерна для обоих заболеваний. Уровни С3 и С4 могут быть низкими при тяжелом поражении печени из-за низкой синтетической активности. Высокий уровень С-реактивного белка (CРБ), свойственный МБК, может снижаться при аутоиммунном гепатите. Но другие клинические проявления не могут быть объяснены исключительно аутоиммунным гепатитом. В связи с мультисистемным поражением помимо лимфатических узлов необходимо рассмотреть другие заболевания, сопровождающие или мимикрирующие плазматическую МБК.
Клональные иммунопролиферативные заболевания
У пациентки имеется выраженная лимфоаденопатия и значительное снижение массы тела – два симптома, вызывающие беспокойство в отношении лимфомы. Лимфома и плазмоклеточные опухоли (миелома и плазмоцитома) могут быть ассоциированы с плазматической МБК. В таком случае результаты биопсии крупного лимфатического узла должны представить неопровержимые доказательства лимфомы. Однако некоторые типы лимфомы трудно диагностировать, поэтому необходимо помнить про вероятность этого заболевания при отсутствии альтернативных объяснений.
Синдром Шегрена
Патологические изменения лимфоузлов, наблюдаемые при синдроме Шегрена, могут напоминать картину плазматического варианта МБК. Увеличение слезных и слюнных желез предполагает диагноз синдрома Шегрена в качестве самостоятельного заболевания или в виде составной части перекрестного синдрома с ревматоидным артритом или СКВ. Аутоиммунная патология печени также может быть ассоциирована с синдромом Шегрена. Однако, как правило, основные проявления синдрома Шегрена заключаются в умеренной/выраженной ксерофтальмии или сухости рта и незначительном увеличении желез. У пациентки имеет место значительное увеличение желез при отсутствии ксерофтальмии и сухости полости рта.
IgG4-ассоциированное заболевание
Я полагаю, что клинический синдром, имеющийся у данной пациентки, полностью соответствует IgG4-ассоциированному заболеванию (IgG4-АЗ), хотя некоторые симптомы не типичны для него. Гистологические проявления IgG4-АЗ включают плазмоцитоз и фиброз (различной степени в разных органах); гистологические изменения в лимфоузлах, возникающие при IgG4-АЗ, трудно отличить от таковых, наблюдаемых при плазматической МБК. Многие симптомы у пациентки, включая поликлональную гипергаммаглобулинемию, гипокомплементемию, выраженное увеличение слезных и слюнных желез, вовлечение желчных протоков, кожные проявления, могут быть объяснены IgG4-АЗ. Склерозирующий холангит крупных желчных протоков является наиболее характерной манифестацией IgG4-АЗ, но вовлечение микроскопических желчных протоков тоже может развиваться при этой патологии. Также описано вовлечение кожных покровов, артерий, периартериит крупных артерий. При биопсии кожи плазматические клетки не обнаружены, но анализируемый биоптат мог быть получен из участка поражения с неспецифическим лимфоплазматическим инфильтратом, что привело бы к неспецифическому описанию пурпурозного пигментного дерматита.
Проявлениями, не характерными для IgG4-АЗ, являются ярко выраженные конституциональные симптомы и артрит. Еще одним признаком, противоречащим IgG4-АЗ, может быть отсутствие преобладания IgG4 в биоптатах и подклассах IgG в сыворотке крови. Однако есть вероятность, что зафиксированный уровень IgG4 искусственно занижен, т. к. концентрации IgG1 и IgG2 значительно возросли с течением времени, а уровень IgG4 упал. Известно, что ложно низкая концентрация IgG4 отмечается в 20% случаев IgG4-АЗ, если обследование проводится без адекватного разведения сыворотки. Еще один симптом, который, как полагают, имеет высокую специфичность для IgG4-АЗ, – положительное окрашивание не менее 40% плазматических клеток на IgG4. Но эти признаки могут маскироваться плазмоцитозом с вовлечением множественных изотипов.
Чтобы подтвердить диагноз IgG4-АЗ в данном случае, я хотел бы определить уровень IgG4 после разведения и выполнить биопсию височной артерии. Кроме того, я хотел бы тщательно изучить ранее полученные биоптаты для исключения IgG4-АЗ. Если повторное обследование ранее полученных биоптатов не подтвердит IgG4-АЗ, может потребоваться биопсия слезных, слюнных желез и, возможно, кожных изменений.
J. Stone. Мы рассматривали диагноз МБК, хотя известно, что это заболевание провоцируется интерлейкином-6 и ассоциировано с чрезвычайно высоким уровнем CРБ. У пациентки зафиксирован нормальный уровень CРБ и высокая СОЭ, которая, по нашему мнению, обусловлена высокой концентрацией иммуноглобулинов в крови.
Мы были обеспокоены вероятным ГКА из-за наличия височного артериита, но ГКА очень редко провоцирует появление пурпуры. Мы были поражены значительным увеличением слезных, слюнных желез и гипокомплементемией, эти проявления лишены смысла в контексте ГКА. Мы предполагаем, что IgG4-АЗ является единственно возможным заболеванием, и полагаем, что нормальный уровень IgG4 в сыворотке крови, вероятно, обусловлен эффектом прозоны, который проявляется получением ложно отрицательного результата исследования при избытке антигена. В данном случае избыточным антигеном является IgG4. Для исключения вероятного эффекта прозоны мы попросили персонал лаборатории выполнить серию разведений оригинального образца. Также была проведена биопсия височной артерии.
Клинический диагноз: IgG4-АЗ.
Диагноз P. Monach: IgG4-АЗ.
Патогистологическое обсуждение
R. Nazarian: При изучении гистологических срезов, полученных из биоптата правой височной артерии, обнаружен интенсивный воспалительный инфильтрат с вовлечением адвентиции и комплекса интима-медиа, преимущественно состоявший из лимфоцитов, плазматических клеток и примеси эозинофилов. Окрашивание на CD68 не выявило гранулематозной инфильтрации и специфических макрофагов, локализованных во внутренней эластичной пластинке. При иммуногистохимическом исследовании обнаружено, что большинство CD138+ плазматических клеток были IgG+; более 60% IgG+ плазматических клеток экспрессировали IgG4, при этом 85% поля зрения под большим увеличением приходилось на IgG4+ плазматические клетки (рис. 3). Полученные данные можно интерпретировать в пользу IgG4-ассоциированного васкулита.
Рис. 3. Биоптат правой височной артерии
При окрашивании гематоксилин-эозином биоптата правой височной артерии визуализируется воспалительный инфильтрат, состоящий из лимфоцитов, плазматических клеток, эозинофилов, с вовлечением в патологический процесс адвентиции и комплекса интима-медиа височной артерии (А). При окрашивании по Вергоффу – ван Гизону на эластин отмечается истончение собственной пластики, данные соответствуют повреждению стенки сосуда (В). Иммуногистохимическое окрашивание на CD68 гранулематозного инфильтрата (С). Иммуногистохимическое окрашивание на CD138 (D) демонстрирует преобладание популяции плазматических клеток с иммунореактивностью в отношении IgG (E), соотношение IgG4+ к IgG+ плазматических клеток составило приблизительно 0,60 (F). Полученные данные соответствуют IgG4-ассоциированному васкулиту височной артерии.
Обсуждение терапии
J. Stone. В данном случае лечение началось раньше, чем было получено подтверждение диагноза. В связи с тем, что 15-20% пациентов с ГКА теряют зрение до начала соответствующей терапии, мы немедленно начали лечение преднизолоном. Биопсия височной артерии, которая в конечном итоге подтвердила вероятный диагноз IgG4-АЗ, была выполнена на следующий день.
Эффект прозоны оказался действительно ответственным за иллюзорно низкий уровень IgG4. Когда мы попросили персонал лаборатории развести образец пациентки и повторить исследование, вторичное определение дало иной результат – 226 мг/дл. Мы предположили, что повторное измерение снова дало низкие результаты, и после разведения того же образца в соотношении 1:8000 сывороточный уровень IgG4 оказался 2075 мг/дл.
Мы допускали, что пациентке с исходно высоким уровнем IgG4 потребуется длительный курс лечения. Мы понимали, что длительная терапия преднизолоном может ассоциироваться с побочными эффектами, поэтому назначили пациентке две дозы ритуксимаба и курс преднизолона с постепенным снижением дозировки на протяжении 2 мес. После начала лечения конституциональные симптомы уменьшились, а вес стабилизировался. Проявления височного артериита были быстро купированы, результаты лабораторных исследований улучшились, размеры слезных и слюнных желез значительно уменьшились. Спустя 6 мес плотность сыворотки крови снизилась с 3,6 до 1,9 сантипуаз (нормативные значения 1,4-1,8 сантипуаз), уровень IgG1 понизился с 4560 до 2027 мг/дл (382-929 мг/дл), IgG4 уменьшился с 2075 до 636 мг/дл (4-86 мг/дл). Содержание комплемента в сыворотке крови также нормализовалось. На протяжении нескольких недель сохранялись проявления пурпуры, что послужило причиной для проведения биопсии кожи спустя 1 мес после начала приема глюкокортикоидов. В конечном итоге проявления пурпуры были купированы. Через год после подтверждения диагноза пурпура не беспокоила пациентку в течение 9 мес.
Анатомический диагноз: IgG4-АЗ.
Статья печатается в сокращении.
Полный текст: N Engl J Med. 2017 Feb 23;376(8):
775-786. doi: 10.1056/NEJMcpc1613461
Перевела с англ. Татьяна Можина
Медична газета «Здоров’я України 21 сторіччя» № 24 (421), грудень 2017 р.



.jpg)
.jpg)