21 березня, 2018
Сучасні інгаляційні глюкокортикостероїди в терапії бронхообструктивного синдрому: фокус на флутиказон
Бронхіальна астма (БА) та хронічне обструктивне захворювання легень (ХОЗЛ), попри величезні досягнення респіраторної медицини, залишаються актуальною медико-соціальною проблемою у всьому світі. За даними Всесвітньої організації охорони здоров’я, загальна кількість хворих на БА становить близько 300 млн осіб і до 2025 року збільшиться ще на 100 млн. Водночас на ХОЗЛ страждають 210 млн осіб, а до 2020 року, за прогнозами фахівців, смертність від цієї патології займатиме 3-тє місце серед усіх причин смерті. Незважаючи на те що ці захворювання вважаються самостійними нозологічними одиницями, їх об’єднує наявність бронхообструктивного синдрому (БОС), який є універсальним проявом хронічного запалення дихальних шляхів (ДШ). Пошук оптимальних методів досягнення контролю БА та ХОЗЛ, попередження загострень та смертності є актуальним завданням як в спеціалізованій, так і в загальній медичній практиці.
Проблеми сучасної терапії загострень БА та ХОЗЛ
Незважаючи на прогрес у клінічній фармакології бронхолітиків та протизапальних препаратів, сьогодні спостерігається зростання кількості тяжких форм і частоти загострень БА та ХОЗЛ, а також збільшення соціально-економічного навантаження на національні системи охорони здоров’я всіх країн світу без виключення (Global Strategy for Diagnosis, Managementand Prevention of COPD (GOLD)-2017, 2018). Наразі ми маємо досить великий арсенал препаратів для лікування БА та ХОЗЛ, у тому числі – в період загострень, проте не можемо говорити навіть про часткову перемогу в цьому питанні. Ситуацію, що склалася, певною мірою відображає щорічна публікація таких широковідомих і важливих документів, як гайдлайни GINA (Global Initiative for Asthma) та GOLD, адже саме постійна потреба в оновленні знань про етіологію, патогенез і засоби ефективного контролю БА та ХОЗЛ свідчить про актуальність питання для світового респіраторного та алергологічного товариств. У чому ж полягає проблема контролю над БОС?
Сьогодні дуже поширеною є думка про те, що однією з основних причин виникнення такої ситуації є повсюдна недооцінка лікарями й хворими тяжкості стану чи наявності загострення як БА, так і ХОЗЛ. У цьому сенсі показовими й цікавими є результати дослідження, проведеного у 2006 році J.M. Fitzgerald і співавт. за участю 893 хворих на БА та 463 лікарів. Так, було встановлено, що кількість пацієнтів із контрольованою астмою за об’єктивними показниками досягала 47% порівняно з кількістю таких пацієнтів за суб’єктивною оцінкою самих хворих і лікарів (97 і 90% відповідно). При цьому понад 50% пацієнтів успішність контролю визначали за частотою та кількістю використання медикаментів і рівнем якості життя. Щодо лікарів, то 30% із них брали до уваги відсутність нічних симптомів, близько 20% оцінювали проміжки часу між загостреннями, і тільки 1% із них керувався критеріями офіційних клінічних рекомендацій. Автори дослідження зробили висновок, що, незважаючи на розробку і вдосконалення методів лікування астми у відповідності до міжнародних рекомендацій, лікарі не використовують їх у повному обсязі. До того ж непокоєння авторів рекомендацій GINA та GOLD викликає низький рівень порозуміння між лікарями та пацієнтами, що страждають на БА та ХОЗЛ. Ця проблема набула глобального характеру, що пояснюється наявністю певних труднощів у лікуванні «хронічних» пацієнтів. Досить важко переконати їх у необхідності постійного прийому базисних препаратів, а також пояснити важливість вчасного інформування лікуючого лікаря про перші ознаки загострення чи втрати контролю над симптомами хвороби. Проблема ефективної терапії бронхообструктивних захворювань ускладнюється ще й тим, що хворі, а іноді й лікарі не завжди об’єктивно оцінюють тяжкість стану. Згідно з даними масштабного дослідження AIR, проведеного в США, Західній Європі та Японії, від 50 до 75% хворих на легку БА (2 денних і 2 нічних симптоми на місяць) потребували частішого застосування швидкодіючих фармакологічних препаратів, що свідчило про неповний контроль захворювання внаслідок недостатньо об’єктивної оцінки свого стану (K.F. Rabeetal, 2004). Схожа ситуація спостерігається і в лікуванні ХОЗЛ. За даними, отриманими L. Langsetmo і співавт. (2008), приблизно у 50% випадків загострень ХОЗЛ пацієнти взагалі не звертаються за медичною допомогою. При цьому кожне наступне загострення ХОЗЛ асоціюється з підвищенням ризику смерті, особливо впродовж першого тижня після погіршення респіраторних симптомів (S. Suissaetal, 2012).
Отже, лікування БА та ХОЗЛ пов’язано з переліком певних проблем, з-посеред яких однією з провідних є неадекватна оцінка стану хворого, причому як самим пацієнтом, так і лікарем. Змінити ситуацію на краще можна завдяки більш повному використанню лікарями сучасних інструментів контролю над захворюванням, задекларованих на сторінках рекомендацій GINA та GOLD. Украй важливим є також своєчасне діагностування наявності загострення БА чи ХОЗЛ та адекватне купірування бронхообструктивного і запального синдромів; це є ефективним методом запобігання не тільки виникнення загострень у майбутньому, але й випадків смерті від наслідків хвороби.
Місце ІГКС у терапії БА та ХОЗЛ: загальна характеристика
Загальними рисами БА та ХОЗЛ є наявність хронічного запального процесу в ДШ. Схожість патогенетичних процесів при цих нозологіях зумовлює й подібні підходи до лікування, а саме – застосування таких протизапальних і бронхолітичних засобів, які дозволяють успішно й оперативно встановлювати контроль над запаленням та розвитком бронхоконстрикції.
Наразі найефективнішими протизапальними препаратами для терапії БА та ХОЗЛ (у тому числі – загострень) є інгаляційні глюкокортикостероїди (ІГКС). Успішне багаторічне використання цієї групи препаратів докорінно змінило тактику й розширило можливості лікування БА та ХОЗЛ. Обґрунтуванням необхідності застосування ІГКС є їхня виражена протизапальна активність. Це дуже важлива характеристика для базисної терапії та незамінна – для екстреної. Адже призначення ІГКС у період загострення БА та ХОЗЛ надає можливість забезпечити контроль над БОС завдяки купіруванню запалення у ДШ шляхом зниження запальної інфільтрації, зменшення кількості еозинофілів і мастоцитів, продукції цитокінів і медіаторів запалення. Використання ІГКС може також сприяти відновленню пошкодженої структури бронхіального епітелію, що є важливим фактором профілактики майбутніх загострень.
Як відомо, ІГКС є препаратами вибору за наявності так званого еозинофільного запалення, характерного першочергово для БА. При цьому в пацієнтів із ХОЗЛ ключова роль у запаленні ДШ належить макрофагам і нейтрофілам. На відміну від еозинофілів ці клітини менш чутливі до дії ІГКС, хоча у свій час було доведено, що застосування цієї групи препаратів призводить до достовірного зменшення кількості нейтрофілів та лімфоцитів у ДШ (R. Jenetal, 2012). Існує думка, що стероїдна резистентність хронічного запалення ДШ у хворих на ХОЗЛ є причиною використання більш високих доз ІГКС, ніж при БА.
Разом із тим необхідно підкреслити, що під час загострення ХОЗЛ спостерігається збільшення кількості еозинофілів. Тобто навіть ті пацієнти, у яких ефективність ІГКС як базисної терапії виявилась обмеженою, потребують призначень інгаляційних кортикостероїдів у період загострень.
Таким чином, ІГКС – дуже важливий компонент більшості базисних схем лікування БА та ХОЗЛ. При цьому ефективність ІГКС у лікуванні останнього поза періоду загострення може бути обмеженою через превалювання нейтрофільного запалення над еозинофільним. Однак збільшення кількості еозинофілів у хворих на ХОЗЛ у період загострення є вагомою причиною для того, щоб вважати ІГКС препаратами вибору для купірування БОС у разі як БА, так і ХОЗЛ.
Ефективність ІГКС: від чого залежить?
Терапія за допомогою ІГКС на тлі БОС покращує або нормалізує функцію легень, зменшує потребу в бронхолітиках і, у більшості випадків, усуває необхідність використання системних ГКС. При цьому клінічна ефективність терапії ІГКС залежить від активної речовини, дози, форми й засобу доставки препарату в ДШ, терміну початку й тривалості лікування, тяжкості перебігу або загострення БА та ХОЗЛ, комплаєнсу хворого. Загалом ГКС являють собою ліпофільні молекули, які легко проникають крізь клітинну мембрану в цитоплазму, де зв’язуються з цитоплазматичними ГКС-рецепторами, внаслідок чого знижується синтез цитокінів, хемокінів, ферментів і рецепторних білків, залучених до патогенезу як БА, так і ХОЗЛ.
Час настання клінічного ефекту від ІГКС залежить від кількох факторів, і одним із найважливіших є ліпофільність. Ліпофільні препарати здатні швидше проникати крізь фосфоліпідні мембрани клітин ДШ і мають більш високу спорідненість до ГКС-рецепторів. (P.H. Ratneretal, 2006). Сьогодні в рутинній клінічній практиці широко застосовується сучасний ліпофільний представник покоління ІГКС – флютиказону пропіонат (ФП).
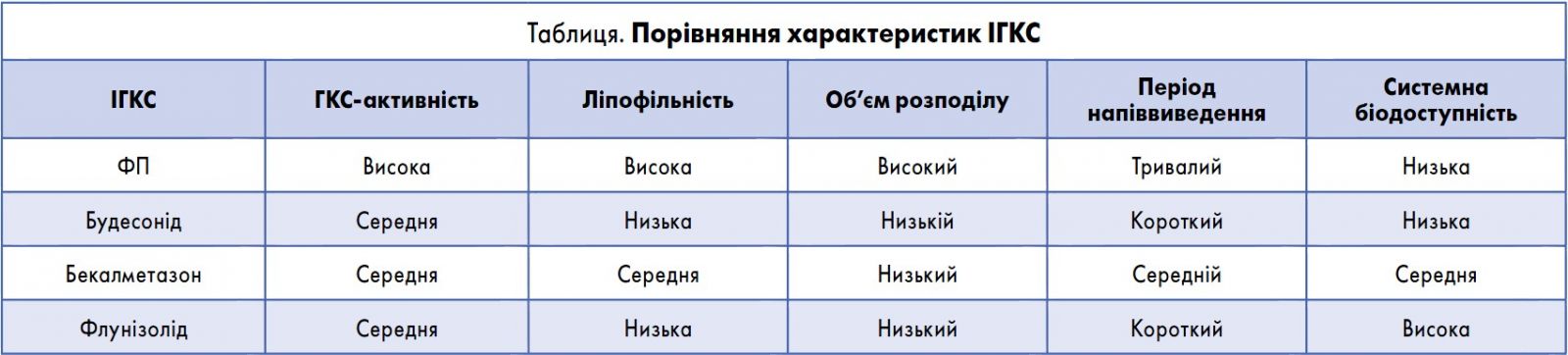
Відомо, що місцева протизапальна активність і можливі системні ефекти ІГКС визначаються спорідненістю (афінністю) до ГКС-рецепторів. Ключовою перевагою ФП у цьому сенсі є набагато більша афінність і тривалий зв’язок із ГКС-рецепторами порівняно з аналогами (Н. Derendorf, 1997) (табл.).
Слід зазначити, що при інгаляції з використанням дозованого аерозольного інгалятора в легені потрапляє лише близько 20% номінальної дози ІГКС, тоді як 80% осідає в ротовій порожнині, а потім проковтується. Саме ці «20%» не дозволяють широко застосовувати ІГКС у період загострень, коли є потреба в швидкому ефекті та високих концентраціях. Натомість вважається, що застосування системних ГКС не тільки пришвидшить, а й підвищить ефективність лікування БОС. Проте використання системних ГКС (особливо у високих дозах) може мати численні негативні наслідки у вигляді побічних явищ, що виникають на тлі ін’єкційного чи перорального прийому стероїдних препаратів. До того ж не варто забувати, що «… всмоктування ліків через слизову оболонку дихальних шляхів відбувається в 20 разів швидше, ніж при прийомі таблетованих форм…» (Г.Д. Тарасова, 2007). Отже, таблетовані форми ГКС як засоби купірування БОС за наявності сумнівних переваг водночас мають доведені серйозні недоліки. І хоча системні ГКС завжди вважалися стандартом надання допомоги при загостреннях БОС, у дослідженні G.J. Rodrigo і співавт. (2005) було продемонстровано, що повторне застосування інгаляційного ФП має рівноцінну клінічну ефективність та більшу безпечність у порівнянні із довенним введенням системного ГКС. При цьому терапевтична перевага інгаляційного ФП була особливо значущою в пацієнтів із більш тяжкою формою бронхообструкції. Схожі результати продемонструвало дослідження, яке було здійснене С.С. Солдатченко, С.Г. Донич та І.П. Ігнатоніс. Автори показали, що терапія тяжких загострень БА небулізованим флютиказоном (2-4 мг/добу) рівноцінна лікуванню системними стероїдами за дією на функціональні параметри, а за впливом на клінічні показники та зменшення ризику побічних ефектів навіть перевершує їх.
Можливості підвищення ефективності використання ФП у рутинній клінічній практиці
Згідно з оновленими міжнародними рекомендаціями визначення БА та ХОЗЛ як гетерогенних захворювань враховує ключову роль хронічного запалення ДШ та БОС у патофізіології цих захворювань і залишає ці фактори найважливішими мішенями для фармакотерапії. ФП можна вважати сьогодні одним із найактивніших протизапальних препаратів у терапії БОС. Так, ФП внесений до усіх міжнародних (GINA‑2017, GOLD‑2018) і національних (накази МОЗ України № 128, № 555, № 868) стандартів і входить до переліку життєво необхідних препаратів.
У міжнародних настановах небулізований ФП рекомендований як альтернатива системним ГКС у лікуванні загострень бронхообструктивних захворювань. У нашій країні в щоденній клінічній практиці для терапії загострень та досягнення контролю БА та ХОЗЛ широко використовується небулізований ФП (Небуфлюзон®, ФК «Юрія-Фарм»). Застосування препарату за допомогою небулайзера забезпечує високий показник потрапляння ФП у легені (близько 85-90% від використаної дози в залежності від небулайзера доставки, що використовується). Для ФП, який має практично нульову біодоступність та, відповідно, високий профіль безпеки, ефективність лікування визначається тільки типом пристрою доставки препарату й технікою проведення інгаляції. Доведено, що застосування інгаляційних препаратів для терапії БОС через небулайзер веде до суттєвого й швидкого покращення легеневої функції (рівень доказів А). Важливою перевагою небулайзерної терапії є легкість використання та доступність процедури як в умовах лікувального закладу, так і вдома.
Важливо також пам’ятати, що потрапляння лікарських речовин при небулайзерній терапії відбувається пасивно, а значить, необхідність робити глибокий вдих нівелюється, що є важливим позитивним фактором у разі лікування дітей, літніх та малоконтактних пацієнтів.
Отже, використання небулайзера не тільки забезпечує високу ефективність лікування БОС під час загострення БА та ХОЗЛ, а й дозволяє лікуватися в комфортних умовах, не витрачаючи при цьому зайвих коштів.
Висновки
- Адекватна терапія загострень бронхообструктивних захворювань залишається актуальною проблемою і для пацієнта, і для лікаря.
- На сьогодні ІГКС – це золотий стандарт терапії БА та ХОЗЛ, адже раннє призначення й тривале застосування цих препаратів допомагає знизити ризик смертності та кількість загострень.
- Сучасні компресорні небулайзери доставки дозволяють підібрати оптимальне поєднання діючої речовини та інгалятора для кожного пацієнта з БА або ХОЗЛ.
- Клас ІГКС представлений різними препаратами, що різняться за своєю протизапальною активністю, своїми фармакокінетичними і фармакоекономічними характеристиками, профілем безпеки.
- За всіма наведеними характеристиками ФП має безумовні переваги, які були доведені в ході багаторічних масштабних клінічних досліджень, а це, звичайно, має важливе значення в загальній та спеціалізованій медичній практиці.
Підготувала Олена Риженко
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 1 (42), лютий 2018 р.