10 травня, 2018
Современные подходы к лечению хронической идиопатической крапивницы

Крапивница – одно из самых распространенных аллергических заболеваний, которому подвержены практически все возрастные категории. Согласно статистическим данным, у 15-20% населения земного шара в течение жизни наблюдается по крайней мере один эпизод крапивницы [2].
Данная патология может встречаться в любом возрасте, но чаще всего заболевание проявляет себя в период от 30 до 50 лет. Случаи возникновения крапивницы у взрослых впервые после 70 лет чрезвычайно редки. Согласно наблюдениям, крапивница у женщин встречается примерно в 2 раза чаще, чем у мужчин. Специалисты предполагают, что виновниками данного явления становятся гормоны, но официального исследования, выявляющего зависимость предрасположенности к крапивнице у женщин и мужчин вследствие различного гормонального фона, до сих не проводилось.
Крапивница является одной из самых сложных и неоднозначных проблем современной практической медицины. Это обусловливает высокую обращаемость пациентов с данным заболеванием к специалистам различного профиля: дерматологам, аллергологам, педиатрам, врачам общей практики и др. Крапивница негативно влияет на качество жизни пациентов, затрагивая практически все сферы деятельности людей. На фоне выраженного кожного зуда, сопровождающего заболевание, у больных отмечается снижение внимания, ухудшается сон, существенно нарушается трудоспособность. Косметические дефекты, возникающие вследствие высыпаний и отеков, ухудшают эмоциональное состояние пациентов, ограничивают их социальную активность, что создает трудности в межличностных отношениях, общении с друзьями, одноклассниками, коллегами по работе. Несмотря на многочисленные методы, рекомендуемые современными согласительными документами в диагностическом алгоритме крапивницы, причину заболевания, особенно его хронических форм, удается выявить редко [1].
Известно, что у 80-95% больных хронической крапивницей (ХК) диагностируется идиопатическая форма, что создает объективные трудности в лечении этих пациентов и ухудшает прогноз заболевания в целом [1]. Симптомы пациентов с ХК характеризуются не только кожными высыпаниями и зудом, но и различными нарушениями общего состояния организма, его функциональных способностей и качества жизни: более низкая физическая активность, физический дискомфорт, нарушения сна, пониженное эмоциональное благополучие, психические и ментальные нарушения, снижение работоспособности, интереса к организации досуга [19]. При этом ХК в значительной степени оказывает влияние на показатели качества жизни наравне с атопическим дерматитом и псориазом, но меньше, чем у пациентов со стенокардией [17, 18]. В опросном исследовании качества жизни (опросник CU-Q2oL) около 80% пациентов с ХК сообщали о значительной усталости и отсутствии концентрации в дневное время, около 54% – жаловались на проблемы со сном [20].
Терапия ХК по-прежнему остается значительной медико-социальной проблемой, поскольку заболевание проявляется чаще у людей трудоспособного возраста и характеризуется выраженным снижением качества жизни [1, 2]. Пациенты страдают от изнуряющего зуда и кожных уртикарных высыпаний, что не может не отражаться на их психологическом статусе [1]. В тяжелых случаях симптомы сопровождаются отечным компонентом. Кожные высыпания возникают не реже трех раз в неделю и исчезают бесследно в течение 24 ч, что затрудняет прогноз ремиссий и выздоровления. Широкая распространенность (0,1-1% в популяции) и сложный контингент пациентов требуют дальнейшего усовершенствования схем лечения и гибкого индивидуального подхода в рамках развития персонализированной терапии. Это нашло отражение в международных рекомендациях по лечению ХК [24, 25].
Антагонисты Н1-гистаминовых рецепторов в настоящее время являются единственной патогенетически обоснованной группой препаратов, рекомендованной для лечения больных крапивницей [24, 25]. Основной медиатор – гистамин, высвобождаясь из гранул тучных клеток, воздействует на Н1-гистаминовые рецепторы кожи и вызывает зуд. При взаимодействии с Н1-рецепторами на посткапиллярных венулах гистамин индуцирует высвобождение оксида азота, который стимулирует продукцию циклического гуанозинмонофосфата (цГМФ), что приводит к вазодилатации, повышению сосудистой проницаемости и возникновению отека. Проведенные исследования по применению антигистаминных препаратов последнего поколения для лечения различных форм крапивницы обладают высоким уровнем доказательности, в связи с этим современные отечественные и зарубежные руководства рекомендуют именно эту группу препаратов в качестве терапии первой линии в лечении любой формы крапивницы [5, 6, 9, 10].
При выборе конкретного антигистаминного препарата II поколения необходимо руководствоваться в первую очередь эффективностью и безопасностью. Кроме того, следует учитывать, что в рамках препаратов II поколения в настоящее время выделяют так называемые активные метаболиты, применение которых может обеспечить прогнозируемый терапевтический эффект, а также более адекватную переносимость препарата, что особенно важно при наличии у больных с ХК сопутствующей патологии.
Известно, что цетиризин – смесь двух стереоизомеров (левоцетиризина и декстроцетиризина), из которых только левоцетиризин обладает антигистаминным действием. Левоцетиризин по сродству к Н1-гистаминовым рецепторам оказывается в два раза сильнее цетиризина, применяется в два раза меньшей дозе, чем цетиризин, и, кроме того, практически не метаболизируется в организме, что снижает риск побочных действий и лекарственных взаимодействий [3, 4]. Левоцетиризин влияет на гистаминозависимую стадию аллергических реакций: уменьшает проницаемость сосудов, миграцию эозинофилов и высвобождение медиаторов воспаления, устраняя экссудацию и зуд [3, 4].
Показания к назначению левоцетиризина: хроническая идиопатическая крапивница, аллергический ринит, в том числе круглогодичный. Левоцетиризин обладает отличной фармакокинетикой. После приема одной дозы препарата внутрь его действие развивается в ближайшие 15 мин и сохраняется на протяжении целых суток (24 ч) [9, 10].
Сродство (аффинность) левоцетиризина к Н1-рецепторам в 600 раз превышает сродство к другим (холинергическим, мускариновым, серотониновым) рецепторам, и он практически не имеет антихолинергического и антисеротонинового действия [16]. Левоцетиризин не проникает через гематоэнцефалический барьер, поэтому в терапевтических дозах не оказывает седативного действия [7]. Рекомендуемая суточная доза левоцетиризина для взрослых и детей старше 6 лет составляет 5 мг (1 таблетка). При хронических аллергических заболеваниях курс лечения может длиться до 12 мес.
Уникальными свойствами левоцетиризина является его способность ингибировать инфильтрацию еозинофилами, ключевыми клетками аллергического ответа поздней фазы. Левоцетиризин блокирует кожный ответ на тромбоцитактивирующий фактор, важный медиатор хемотаксиса в поздней фазе аллергического ответа и уменьшает образование пузыря и эритемы этим фактором [8]. Также левоцетиризин уменьшает уровни лейкотриенов. Он не ингибирует активацию тучных клеток, таким образом, другие клетки, кроме тучных, с наибольшей вероятностью эозинофилы, возможно, базофилы и макрофаги, обеспечивают продукцию этих лейкотриенов.
Известно, что гистамин сам по себе не влияет на продукцию LTC4, следовательно, цетиризин может блокировать антиген-индуцированный синтез LTC4, таким образом смягчая острый аллергический ответ. В изолированном кожном эксперименте цетиризин демонстрировал независимое противовоспалительное, противоаллергическое действие, такое как подавление поздней фазы инфильтрации эозинофилами и базофилами. Механизм действия цетиризина заключается в контроле адгезии эозинофилов на эндотелий путем модулирования экспрессии ICAM-1 (молекулы-1 межклеточной адгезии) [8].
В исследованиях на моделях крапивницы были показаны преимущества цетиризина и его метаболита левоцетиризина наряду с фексофенадином; наименьший эффект подавления кожной реакции имел лоратадин. Только в одном исследовании был использован наиболее широкий спектр антигистаминных препаратов, причем применялись они в разовых дозах и при коротком 5-дневном курсе. Вместе с тем, были подтверждены преимущества левоцетиризина и цетиризина в подавлении гистамин-индуцированной кожной реакции, а сравнительный ряд составлен следующий: левоцетиризин > цетиризин > фексофенадин 180 мг = фексофенадин 120 мг > лоратадин = дезлоратадин [12, 13]; аналогичные сравнения подтверждаются и в других обзорах [23].
В случае неэффективности лечения ХК антигистаминными препаратами II поколения в течение 2-4 нед больному назначают препараты альтернативной линии терапии (табл. 1).
Таблиця 1. Сравнение Европейских и Американских рекомендаций по лечению крапивницы [24, 25]
Одним из альтернативных методов лечения ХК является сочетанное назначение антигистаминных препаратов II поколения с антилейкотриеновыми лекарственными средствами. Эффективность антилейкотриеновых препаратов у больных ХК связана с селективной блокадой ими лейкотриеновых рецепторов LTC4, LTD4, и LTЕ4,, которые участвуют в патогенезе формирования крапивницы, высвобождаясь из активированной тучной клетки. В отличие от гистамина, являющегося преформированным медиатором, лейкотриены образуются в ходе метаболизма арахидоновой кислоты под действием фермента 5-липооксигеназы и являются вторичными медиаторами, синтезируемыми de novo. Обсуждаемые медиаторы могут поддерживать и усиливать уртикарную реакцию у больных ХК за счет вазодилатации и повышения проницаемости сосудов.
В настоящее время известны две группы антилейкотриеновых препаратов: зафирлукаст (аколат) и монтелукаст (сингуляр). Однако, по данным проведенных исследований, основанных на принципах доказательной медицины, было выявлено, что наиболее выраженным положительным эффектом в лечении ХК обладает комбинация монтелукаста и антигистаминных препаратов II поколения, в то время как оценка эффективности применения зафирлукаста у аналогичных пациентов с ХК показала сопоставимость полученных результатов с плацебо. Кроме того, в целом ряде исследований показано, что наиболее значимый терапевтический эффект при назначении подобной комбинации препаратов наблюдается у пациентов, страдающих ХК в сочетании с бронхиальной астмой и/или непереносимостью нестероидных противовоспалительных средств, что может рассматриваться как терапия выбора у указанной категории больных [15, 21, 22].
Таким образом, современный подход к лечению крапивницы предусматривает целый комплекс терапевтических мероприятий, включающий элиминацию этиологических и триггерных факторов, провоцирующих заболевание, лечение сопутствующей патологии, а также проведение фармакотерапии с применением высокоэффективных и безопасных антигистаминных препаратов, а при необходимости – и альтернативных медикаментозных средств.
Одним из примеров эффективной фиксированной комбинации современных блокаторов Н1-гистаминовых рецепторов и модификатора лейкотриенов в одной таблетке является комбинация левоцетиризина и монтелукаста (препарат Аллергинол плюс, производитель Бафна Фармасьютикалс Лтд., Индия). Одна таблетка содержит монтелукаста натрия 10,5 мг, эквивалентно монтелукасту 10 мг, левоцетиризина дигидрохлорида 5 мг.
Материалы и методы исследования
В исследование включено 64 пациента с хронической идиопатической крапивницей в возрасте 18-60 лет обоих полов: мужчин – 21, женщин – 43. У всех пациентов продолжительность заболевания составляла более 6 нед.
28 пациентов, которые получали в комплексной терапии Аллергинол плюс 1 раз в сутки на протяжении 30 дней, составили І группу; 17 пациентов, получавших в комплексной терапии один из блокаторов Н1-гистаминовых рецепторов ІІ поколения (лоратадин, дезлоратадин или фексофенадин) 1 раз в сутки на протяжении такого же времени, – ІІ группу; 19 больных, получавших левоцетиризин в течение 30 дней, – ІІІ группу.
У 17 (64,2%) пациентов І группы, 11 (67,7%) – ІІ группы и 12 (63,2%) – ІІІ группы отмечалась сопутствующая патология желудочно-кишечного тракта, а именно хронический холецистоангиохолит, дискинезия желчевыводящих путей или дисбиоз кишечника. Этим пациентам в комплексную терапию были назначены желчегонные препараты и пробиотики. Всем больным была назначена гипоаллергенная диета.
Группы больных были сопоставимы по полу, возрасту, тяжести, продолжительности заболевания, выраженности клинических и функциональных симптомов хронической идиопатической крапивницы.
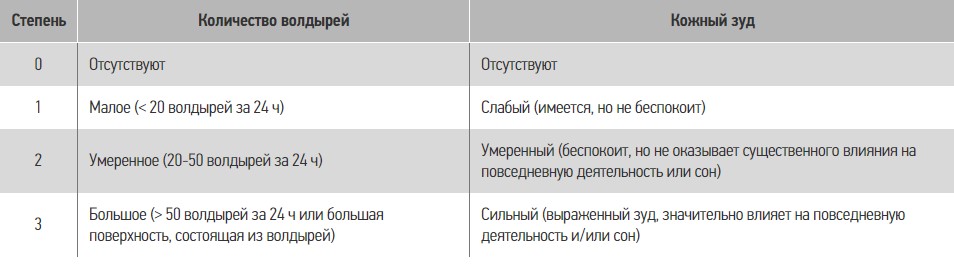
Основные и второстепенные показатели, которые оценивали в ходе исследования: ОАК (лейкоциты, эозинофилы, СОЭ), биохимический анализ крови (АЛТ), показатели АД, ЧСС. Для оценки степени тяжести крапивницы мы использовали балльную шкалу – Индекс активности крапивницы 7 (urticaria activity score – UAS7), которая представляет собой суммарную оценку основных симптомов заболевания (количество высыпаний и интенсивность зуда) самим пациентом или его представителями каждые 24 ч в течение 7 последовательных дней (табл. 2) [11, 14, 24]. Сумма баллов за сутки – от 0 до 6, за неделю – максимум 42. Чем больше сумма баллов, тем хуже качество жизни пациента. Эта балльная оценка активности не может быть использована для оценки активности физической крапивницы и изолированных ангиоотеков. Терапевтическую активность определяли по следующим критериям: 1 – полное излечение, 2 – значительное улучшение, 3 – улучшение, 4 – без изменений, 5 – ухудшение.
Таблиця 2. Оценка активности крапивницы в баллах для определения степени тяжести ее течения по шкале UAS7
Результаты и их обсуждение
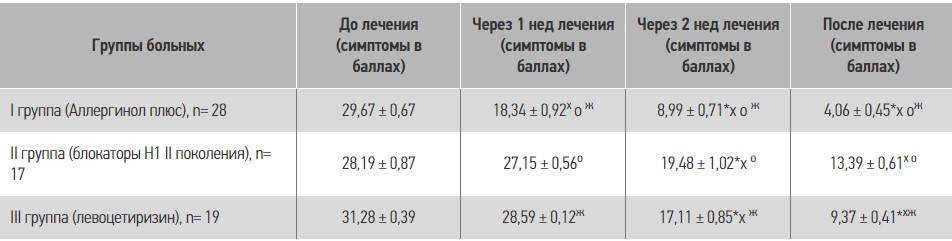
Результаты клинической эффективности лечения больных хронической идиопатической крапивницей приведены в таблице 3 и на рисунке 1.
Таблиця 3. Результаты клинической эффективности лечения больных хронической идиопатической крапивницей
Примечания: * разница результатов до, в процессе и после лечения достоверная (р < 0,05); х разница между группами достоверная (р < 0,05); о разница между І и ІІ группой достоверная (р < 0,05); ж разница между І и ІІІ группой достоверная (р < 0,05).
Рис. 1. Результаты клинической эффективности лечения пациентов с хронической идиопатической крапивницей
Как видно из вышеприведенных данных, результаты уменьшения симптомов крапивницы были значительно выше при применении Аллергинола плюс уже после первой недели лечения, и такая же тенденция сохранялась к окончанию лечения (рис. 2, 3). Было также учтено уменьшение суммарного балла симптомов хронической идиопатической крапивницы на 50%. Под влиянием Аллергинола плюс это происходило в среднем на 5-6-й день, во ІІ группе – на 11-12-й день, а под влиянием только левоцетиризина (ІІІ группа) – на 8-9-й день.
Размеры самых крупных высыпаний во всех группах до лечения составляли 57,9 ± 4,6 мм в диаметре в І группе, 55,4 ± 5,7 мм – во ІІ группе и 58,1 ± 4,2 мм – в ІІІ группе. Уже через 1 сутки размеры этих же высыпаний в І группе (под влиянием Аллергинола плюс) составили 13,1 ± 2,4 мм, а во ІІ и ІІІ группах (под влиянием одного из других блокаторов Н1 ІІ поколения) – 28,6 ± 3,2 мм и 26,4 ± 2,5 мм соответственно. Как показывают эти результаты, сочетание левоцетиризина и монтелукаста (Аллергинол плюс) значительно сильнее угнетает кожную аллергическую реакцию, чем другие антигистаминные препараты без монтелукаста.
Рис. 2. Пациентка с хронической идиопатической крапивницей до лечения
Рис. 3. Пациентка через 7 дней после применения препарата Аллергинол плюс
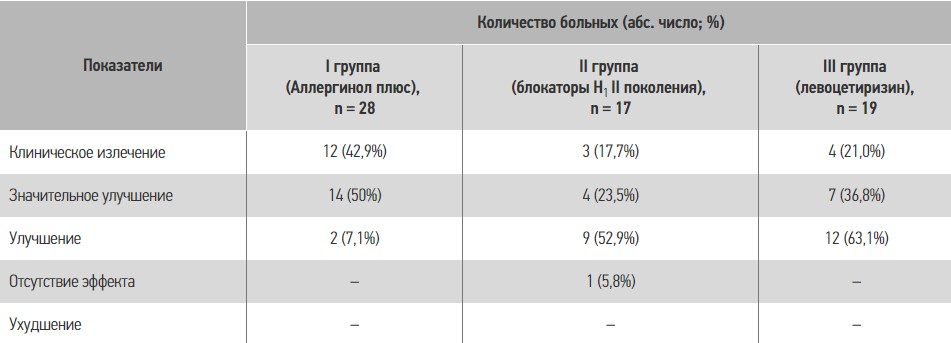
В таблице 4 приведены результаты лечения продолжительностью 30 суток пациентов с хронической идиопатической крапивницей.
Таблиця 4. Результаты лечения пациентов с хронической идиопатической крапивницей
Таким образом, проведенные исследования эффективности лечения больных ХК Аллергинолом плюс в течение 30 дней продемонстрировали значительное улучшение состояния пациентов в виде прекращения кожного зуда, уменьшения количества высыпаний, размеров крупных высыпаний. Указанные положительные эффекты сопровождались улучшением ночного сна, восстановлением дневной активности, приводили к повышению качества жизни пациентов. Причем результаты лечения были выше в группе пациентов, получавших Аллергинол плюс, чем в группах других блокаторов Н1-гистаминовых рецепторов.
Всем пациентам проводились общеклинические исследования. В таблице 5 приведены данные общеклинических методов исследования.
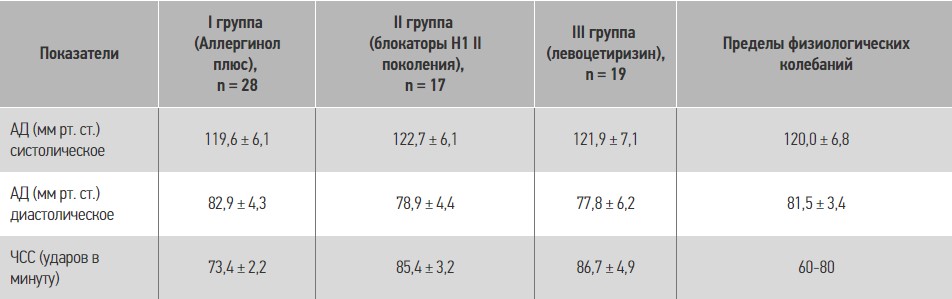
Таблиця 5. Показатели артериального давления (АД) и частоты сердечных сокращений (ЧСС) у пациентов с хронической идиопатической крапивницей во время лечения
Примечания: * разница результатов между основной и контрольной группами достоверна (р < 0,05); х разница между пределами физиологических колебаний достоверна (р < 0,05).
Как известно, применение блокаторов Н1 ІІ поколения и их метаболитов не влияет на изменения АД и не увеличивает частоту сердечных сокращений. Как видно из таблицы 5, комплексное применение левоцетиризина и монтелукаста (Аллергинол плюс) тоже не приводит к достоверным изменениям этих показателей. Все показатели находились в пределах физиологических колебаний.
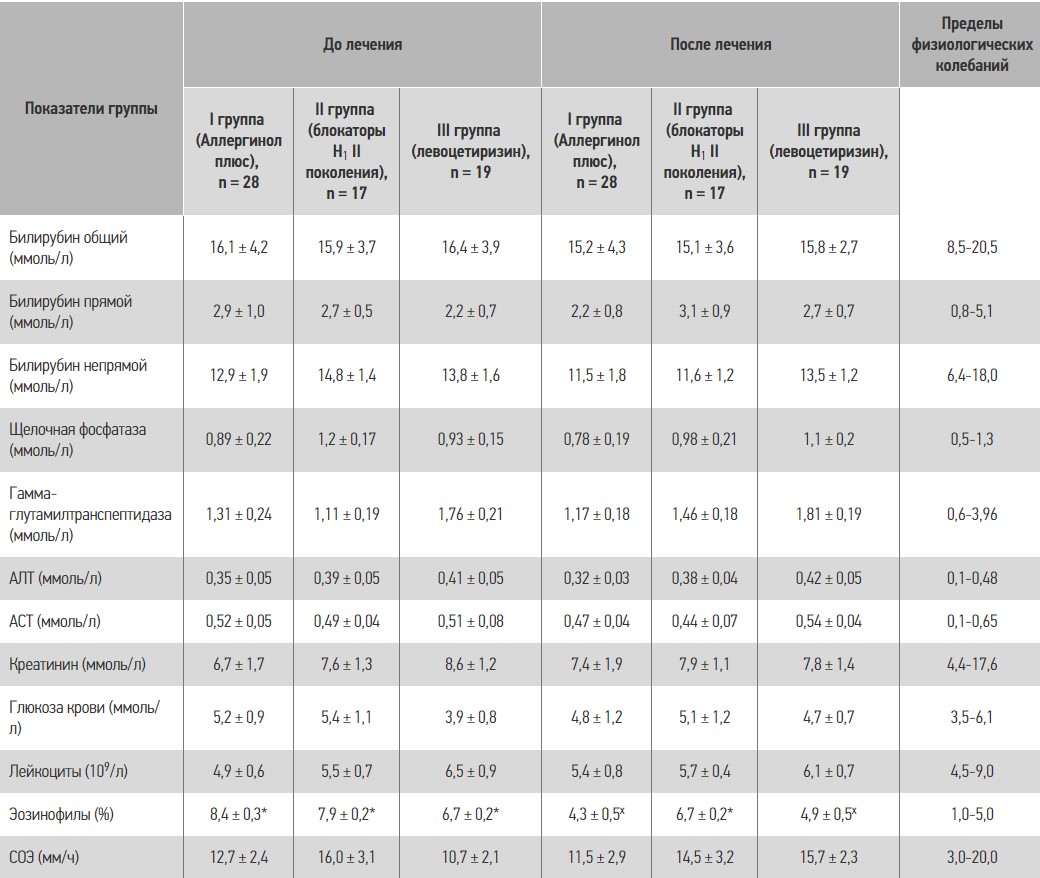
В таблице 6 приведены результаты общеклинических и биохимических показателей крови у пациентов с хронической идиопатической крапивницей до и после лечения. Как видно из таблицы, биохимические показатели крови у больных с ХК достоверно не отличались от нормы, то есть применение антигистаминных препаратов II поколения не вызывает изменений со стороны таковых. Комплексное применение левоцетиризина и монтелукаста (Аллергинол плюс) в течение 30 дней также не приводит к достоверным изменениям этих показателей. В результатах общего анализа крови обращает на себя внимание повышение уровня эозинофилов. Под влиянием левоцетиризина и Аллергинола плюс показатель достигал нормальных значений, под влиянием других антигистаминных (ІІ группа) этот показатель снижался, но нормальных показателей не достигал. Побочных эффектов у пациентов, принимавших в течение 30 дней Аллергинол плюс, мы не наблюдали ни в одном случае.
Таблиця 6. Динамика биохимических и общеклинических показателей крови у пациентов с хронической идиопатической крапивницей до и после лечения
Примечания: * достоверная разница (р < 0,05) между показателем и пределами физиологических колебаний; хдостоверная разница между данными до и после лечения.
Таким образом, результаты работы демонстрируют высокую клиническую эффективность комплексного препарата Аллергинол плюс, включающего комбинацию левоцетиризина и монтелукаста. Это позволяет применять Аллергинол плюс в комплексном лечении вышеупомянутых пациентов. Приведенные данные подтверждают тот факт, что эффекты Аллергинола плюс не ограничиваются блокадой Н1-гистаминовых рецепторов, а также способны блокировать симптомы, которые обусловлены факторами поздней фазы аллергической реакции.
Выводы
1. Аллергинол плюс (монтелукаст + левоцетиризин) обладает высоким сродством к Н1-рецепторам и дополнительной способностью блокировать позднюю фазу аллергической реакции. Препарат продемонстрировал высокую клиническую эффективность при лечении хронической идиопатической крапивницы.
2. Аллергинол плюс не влияет на показатели артериального давления и частоты сердечных сокращений, а также биохимические показатели крови.
3. Применение препарата Аллергинол плюс позволяет уменьшить проявления или достичь ремиссии хронической идиопатической крапивницы, что позволяет использовать его для базисной терапии этих заболеваний.
4. Применение Аллергинола плюс в комплексной терапии больных с хронической идиопатической крапивницей позволяет значительно улучшить клиническое течение заболевания и качество жизни больных.
5. Препарат Аллергинол плюс хорошо переносится пациентами.
Список литературы
1. Горячкина Л. А., Кашкина К. П. Клиническая аллергология и иммунология. Руководство для практикующих врачей. М.: Миклош, 2009. С. 222-271.
2. Патерсон Р., Грэммер Л. К., Гринбергер П. А. Аллергические болезни: диагностика и лечение: Пер. с англ. Под ред. акад. РАМН А. Г. Чучалина. М.: Медицина, 2000. С. 454-483.
3. Трусова О.В, Коростовцев Д. С. Левоцетиризин (Ксизал). Характери-стика препарата и опыт клинического применения. Аллергология. 2006. № 2. С. 25-31.
4. Agraval D. K. Pharmacology and clinical efficacy af desloratadine as an antiallergic and antiinflamatory drug. Exp. Invest. Drugs. 2001;10(3):547-560.
5. Asero R. Chronic anremitting urticaria: is the use of antihistamine sabove the licensed dose effective? A preliminary study of cetirizine at licensed and above – licensed doses. British societty for immunology, Clinical and Experimental Dermatology. 2006;32:34-38.
6. Bhan Anant. Updozing of antihistamines to improve control of chronic urticarial. Indian J. Dermatol. Venerol. Leprol. 2010;76:61-63.
7. Chen C. Physicochemical, pharmacological and pharmacokinetic properties of the zwitterionic antihistamines cetirizine and levocetirizine. Curr. Med. Chem. 2008;15(21):2173-2191.
8. Devalia J. L. et al. A randomized, double-blind, crossover comparison among cetirizine, levocetirizine, and ucb 28557 on histamine-induced cutaneous responses in healthy adult volunteers. Allergy. 2001;56:50-57.
9. Kapp A., Pichler W. J. Levocetirizine is an effective treatment in patients suffering from chronic idiopathic urticaria: a randomized, double-blind, placebo-controlled, parallel, multicenter study. Int. J. Dermatol. 2006;45:469-474.
10. Kapp A., Wedi B. Chronic urticaria: clinical aspects and focus on a new antihistamine, levocetirizine. J. Drugs Dermatol. 2004;3:632-639.
11. Khan D. A. Chronic urticaria: Standard management and patient education. In: UpToDate, Waltham, MA. Available at http://www.uptodate.com/contents/chronic-urticaria-standardmanagement-and-patient-education? topicKey=ALLRG% 2F8106&elapsedTimeMs=6&view=print&d%E2%80%A6.
12. Kruszewski J, Kłos K, Sułek K. Inhibition of histamine-induced wheel after a recommended single dose administration of 10 mg cetirizine, 5 mg desloratadine, 120 and 180 mg fexofenadine, 5 mg levocetirizine and 10 mg loratadine–a randomized, double-blind, placebo controlled trial. Pol Merkur Lekarski. 2006;21(125):443-448.
13. Kłos K, Kruszewski J, Kruszewski R, Sułek K. The effect of 5-days of cetirizine, desloratadine, fexofenadine 120 and 180 mg, levocetirizine, loratadine treatment on the histamine-induced skin reaction and skin blood flow–a randomized, double-blind, placebo controlled trial. Pol Merkur Lekarski. 2006;21(125):449-453.
14. Hide M. Urticaria. Therapy of Skin Diseases: A Worldwide Perspective on Therapeutic Approaches and Their Molecular Basis. Ed. Krieg T, Bickers DR, Miyachi Y. Springer. 2010;247-62.
15. Lorenzo G. D., Pacor M. L., Mansueto P. L. et. al. Is there a role for antileukotrienes in urticaria? Clinical and Experimental Dermatology. 2006;31:327-334.
16. Grant A. J., Riethuisen J.-M., Moulaert B., De Vos C. A double-blind, randomized, single-dose, crossover comparison of levocetirizine with ebastine, fexofenadine, loratadine, mizolastine, and placebo: suppression of histamine-induced wheal-and-flare response during 24 hours in healthy male subjects. Ann. Allergy Asthma Immunol. 2002;88:190-197.
17. Grob JJ, Gaudy-Marqueste C. Urticaria and quality of life. Clin Rev Allergy Immunol. 2006;30(1):47-51.
18. Grob J-J, Revuz J, Ortonne J-P, et al. Comparative study of the impact of chronic urticaria, psoriasis and atopic dermatitis on the quality of life. Br J Dermatol. 2005;152:289-295.
19. O’Donnell BF, Lawlor F, Simpson J, et al. The impact of chronic urticaria on quality of life. Br J Dermatol. 1997:136:197-201.
20. Perkowska J, Kruszewski J, Gutkowski P, et al. Occurrence of sleep-related breathing disorders in patients with chronic urticaria at its asymptomatic or oligosymptomatic stages. Adv Dermatol Allergol. 2016; XXXIII(1):63-67.
21. Riccioni G., Di Ilio C., Conti P. et. al. Advances in therapy with antileukotriene drugs. Ann. Clin. Lab. Sci. 2004;34:379-387.
22. Sanada S., Tanaka T., Yoshikazu Kameyoshi Y., Hide M. The effectiveness of montelukast for the treatment of anti-histamine-resistant chronic urticari. Archives of Dermatological Research September. 2005;297(3):134-138.
23. Wolthers OD. Bilastine: A New Nonsedating Oral H1 Antihistamine for treatment of allergic rhinoconjunctivitis and urticaria. BioMed Research International. 2013. Article ID626837, 6 p.
24. Zuberbier T., Asero R., Bindslev-Jensen C. et. al. EAACI/GA2LEN/EDF/WAO guideline: definition, classification and diagnosis of urticaria. Allergy. 2009;64:1417-1426.
25. Zuberbier T., Aberer W., Asero R et al.The EAACI/GA2LEN/EDF/WAO Guideline for the definition, classification, diagnosis and managment of urticaria: The 2017 Revision and Update. Allergy. 2018, Jan 15. doi: 10.1111/all.13397.].
СУЧАСНІ ПІДХОДИ ДО ЛІКУВАННЯ ХРОНІЧНОЇ ІДІОПАТИЧНОЇ КРОПИВ’ЯНКИ
Л.С. Осипова1,2, В.І. Літус1, В.І. Аверіна2, Л.В. Кузнецова1
1 Національна медична академія післядипломної освіти ім. П.Л. Шупика. 2 Клінічна лікарня «Феофанія» Державного управління справами
Резюме
В статті приведений огляд досліджень та дані власних досліджень щодо ефективності та безпеки застосування левоцетиризину та монтелукасту у пацієнтів, які потерпають від хронічної ідіопатичної кропив’янки, а також дані про ефективність комбінованого препарату Алергінол плюс. Сприятлива фармакокінетика, високий профіль безпеки роблять комбіновані препарати привабливими в широкій медичній практиці для лікування даної патології.
Ключові слова: хронічна ідіопатична кропив’янка, левоцетиризин, монтелукаст, Алергінол плюс, лікування.
Current approaches for the treatment of chronic idiopathic urticaria
L.S. Osipova1,2, V.I. Litus1, V.I. Averina2, L.V. Kuznetsova1
1 Shupyk National Medical Academy of Postgraduate Education. 2 Feofaniya Clinical Hospital
Abstract
The article presents an overview of studies and data of own studies on the efficacy and safty of levocetirizine and montelukast in patients suffering from chronic idiopathic urticaria, and data about efficacy fixed combination drug – Allerginol plus. Favorable pharmacokinetics, a high safety profile make fixed combination drug appealing to the wide medical practice for the treatment of this pathology.
Keywords: chronic idiopathic urticaria, levocetrizin, montelukast, Allerginol plus, treatment.