28 травня, 2018
Рецидивирующие инфекции мочеполовых путей у женщин: насколько многообещающим является использование пробиотиков?
Инфекции мочеполовых путей
Инфекции мочеполовых путей (ИМП) представляют собой острые бактериальные заболевания мочевыводящего тракта, по поводу которых ежегодно за медицинской помощью обращается около 8 млн пациентов. ИМП очень характерны для женщин: бактерии колонизируют влагалище и восходящим путем распространяются в мочевую систему. Согласно имеющимся данным, 1 из 3 женщин перенесет ИМП в возрасте до 26 лет. У 25-30% взрослых женщин, перенесших первый эпизод ИМП, развивается рецидив заболевания.
Факторы риска, ассоциированные с возрастанием риска рецидива ИМП у женщин, включают: обструкцию мочевыводящих путей, катетеризацию мочевого пузыря, нейрогенную дисфункцию, беременность, использование спермицидов, диафрагмы или антихолинергических средств. ИМП, как правило, диагностируются на основании обнаружения микроорганизмов в количестве ≥105 КОЕ/мл в средней порции мочи. Основным микроорганизмом, вызывающим ИМП, является Escherichia coli, также заболевание могут спровоцировать Staphylococcus saprophyticus, Enterococcus faecalis, иногда Klebsiella pneumoniae и Proteus mirabilis.
Рецидивирующие ИМП у женщин
В своем исследовании Mabeck установил, что почти у половины женщин, у которых неосложненная ИМП разрешилась самостоятельно, впоследствии в течение 1 года развился рецидив заболевания. Рецидивирующие ИМП у женщин и в определенных популяциях пациентов (перенесших травму спинного мозга, с нейрогенным мочевым пузырем или постоянным мочевым катетером) представляют собой распространенную и значимую проблему для системы здравоохранения во всем мире. Рецидив ИМП проявляется симптоматической ИМП, манифестирующей учащенным мочеиспусканием, дизурией или болезненным опорожнением мочевого пузыря; в большинстве случаев он связан с реинфицированием первоначальными бактериальными штаммами здоровых женщин, не имеющих анатомической или функциональной патологии мочевыводящих путей с клинически разрешившейся ИМП. В одном исследовании сообщалось, что около 27% молодых женщин, обучавшихся в колледже, в течение 6 мес после первого эпизода ИМП перенесли по крайней мере 1 культурально подтвержденный рецидив и 2,7% – 2 рецидива в течение этого же времени. В исследовании Ikaheimo и соавт. установлено, что среди женщин 17-82 лет, перенесших E. coli-ассоциированный цистит, у 44% в течение 1 года развился рецидив заболевания; 53% женщин были старше 55 лет и 36% являлись молодыми пациентками; впоследствии оказалось, что пожилые женщины более склонны к рецидиву заболевания. Несмотря на то что данный факт не подтвержден документально, предполагается, что 10-15% женщин >60 лет страдают частыми рецидивами ИМП. К сожалению, широкомасштабные популяционные исследования с целью определения особенностей частых рецидивов у женщин с ИМП не проводились. Высказывалось предположение, что подавляющее большинство рецидивов цистита связано с повторным инфицированием штаммами, содержащимися в фекалиях, которые после элиминации из мочевого тракта снова колонизируют его и провоцируют рецидив заболевания, а также, что данные штаммы, внедряясь в эпителий мочевого пузыря, ускользают от защитных сил организма хозяина и поэтому вызывают рецидив ИМП. Повторные эпизоды ИМП часто развиваются в связи с рецидивом или повторным инфицированием. С клинической и терапевтической точки зрения необходимо различать рецидив и реинфицирование, поскольку подавляющее большинство пациентов, как полагают, подвержено именно рецидивам, хотя они, как правило, связаны с повторным инфицированием. Реинфекцией называется повторный эпизод ИМП, вызванный штаммами, отличающимися от тех, которые спровоцировали предшествующую ИМП, его трудно отличить от рецидива. Клинически рецидив часто определяется как повторный эпизод ИМП, если он вызван теми же штаммами микроорганизмов, которые инициировали предшествующую ИМП, и возник в течение 2 нед после завершения лечения первоначального эпизода. Он считается реинфекцией, если возникает спустя >2 нед лечения предшествующего ИМП. Исключительным случаем является следующая ситуация: после терапии культуральный анализ мочи не обнаруживает роста микроорганизмов, а повторный эпизод ИМП вызывается этими же организмами; в этом случае его следует рассматривать как реинфекцию, поскольку большинство из них развивается в течение первых 3 мес после первоначального эпизода (за исключением данных некоторых исследований). В исследовании, проведенном с участием студенток колледжа, страдавших неосложненным циститом и получавших разнообразные антибактериальные препараты, установлено, что рецидив заболевания (персистирование инфекции) развивался только в 6% случаев (возникал в течение 1 нед после начала лечения), тогда как в других случаях имели место осложняющие факторы и около 80% повторных эпизодов представляли собой реинфицирование, возникая спустя несколько месяцев. Антибиотикопрофилактика такими препаратами, как триметоприм/сульфаметоксазол, нитрофурантоин, фторхинолоны, ассоциирована со снижением частоты рецидивов с 2-3 случаев на 1 пациента в год до 0,1-0,2 случая на 1 пациента в год, однако приводит к росту резистентности патогенов. Появление проблем с резистентностью, таких как бета-лактамазы расширенного спектра и карбапенемрезистентная E. coli, оправдывает необходимость изучения новых препаратов, имеющих меньшее количество нежелательных явлений и, вероятно, подходящих для длительной антимикробной профилактики.
Пробиотики
Нобелевский лауреат Илья Мечников в начале 1900 г. предположил, что высокая средняя продолжительность жизни болгарских крестьян обусловлена употреблением ферментированных молочных продуктов. Он также отметил положительную роль некоторых бактерий, в отношении которых впоследствии было высказано мнение, что их введение в организм хозяина может способствовать многообещающим результатам в замещении ими вредоносных микробов. Позднее они получили название «пробиотики». Термин «пробиотики» происходит от греческого слова, означающего «для жизни», впервые его использовали в 1960 г. Lilly и Stillwell.
Продовольственная и сельскохозяйственная организация и Всемирная организация здравоохранения позже охарактеризовали пробиотики как «живые микроорганизмы», которые при введении в адекватных количествах приносят пользу организму хозяина. Наиболее часто в пробиотических препаратах используются различные штаммы бактерий Lactobacillus, Bifidobacterium, Escherichia, Enterococcus, Bacillus и Streptococcus, а также некоторые непатогенные штаммы E. coli и штаммы грибов рода Saccharomyces. Штаммы, способные имплантироваться внутрь организма и переносить неблагоприятные условия, считаются идеальными пробиотиками и привлекают к себе наибольшее клиническое внимание. Пробиотические организмы усиливают иммунитет организма посредством увеличения синтеза иммуноглобулина А (IgA) и активности других клеток, секретирующих иммуноглобулин, в слизистых оболочках, стимулируя местное высвобождение интерферона и облегчая транспорт антигенов к лимфоидным клеткам, что способствует увеличению поглощения антигенов в пейеровых бляшках.
Почему пробиотики?
Флора кожных покровов и слизистых оболочек совместно с нормальной бактериальной флорой выступает в качестве серьезного барьера инфекционному началу; защита организма хозяина обеспечивается за счет баланса между непатогенными комменсалами и патогенными бактериями. В иммуноскомпрометированном организме, а также у тех, кто получает антибиотикотерапию, нарушается естественная защитная биопленка из бактерий и поверхностных клеток. Это справедливо для пациентов, инфицированных ВИЧ, у которых уменьшается колонизация урогенитального тракта лактобактериями, что приводит к распространению ВИЧ в мочевыводящих путях.
Нарушение естественной флоры делает пациентов склонными к тяжелым инфекционным заболеваниям, которые могут вызываться различными патогенными микроорганизмами. Стратегия восстановления бактериальной флоры, поддерживающей организм хозяина, включает использование пробиотиков.
Существуют две основные научные концепции, ассоциированные с пробиотиками:
- Во-первых, это теория конкуренции, в соответствии с которой живые микроорганизмы, принимаемые перорально или применяемые в области наружных половых органов, тормозят избыточный рост патогенной флоры и восстанавливают окружающую среду, устойчивую к инфекциям. Более того, пробиотики могут оказывать синергетическое действие с антибиотиками.
- Вторая, наименее спорная, основывается на модуляции иммунной системы, в соответствии с которой живые микроорганизмы, как известно, влияют на продукцию иммуноглобулинов, изменяя иммунную защиту организма и способствуя выработке специфического иммунного ответа против патогенных бактерий.
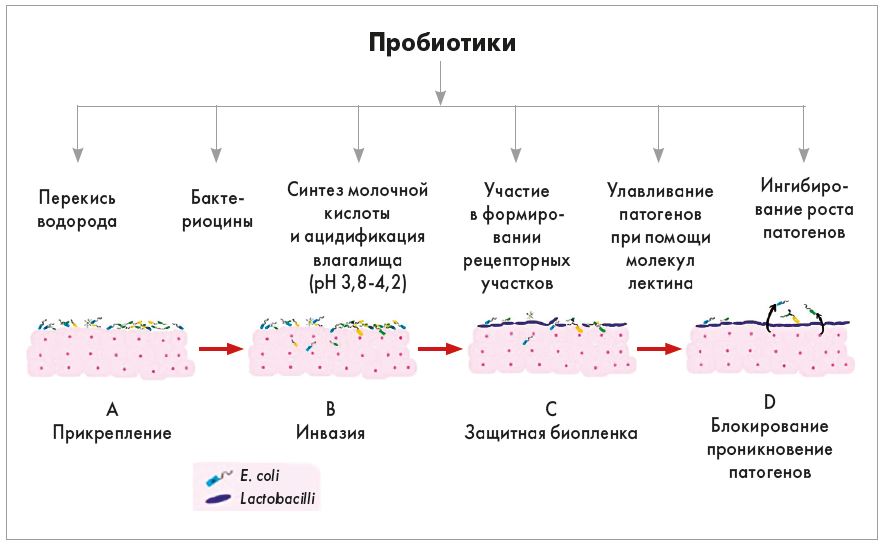
Понятие «дружественные бактерии» часто используется в качестве альтернативного термина для пробиотиков и широко применяется в настоящее время вместо химиотерапевтических агентов в йогуртах и пробиотических напитках. Штаммы Lactobacillus и Bifidobacterium являются потенциальными кандидатами для пробиотической терапии. Они, как правило, считаются безопасными. Пробиотики используются благодаря их протекторным свойствам, таким как антимикробное, антиоксидантное, антидиарейное, антиканцерогенное, антилипидемическое, а также возможности применения при непереносимости лактозы, они помогают в лечении и профилактике заболеваний. Пробиотики оказывают благоприятное влияние посредством различных протекторных механизмов в поддержании кислотного рН, синтезе бактериоцинов, перекиси водорода, предупреждении колонизации патогенными микроорганизмами, наличия антимикробной активности, деградации токсинов и стимуляции иммунной системы организма хозяина (рис.).
Рис. Механизм действия лактобактерий в кишечной микрофлоре человека
В урогенитальной микрофлоре здоровых женщин доминируют штаммы лактобактерий; уменьшение численности лактобактерий у пациентов, перенесших ИМП, бактериальный вагиноз и многие другие генитальные инфекции, включая кандидоз, привлекло пристальное внимание к этим бактериям. Лактобациллы представляют собой грамположительные палочковидные бактерии, факультативные или облигатные анаэробы, которые обычно весьма требовательны к окружающим условиям. Они предпочитают кислую среду и помогают создавать ее, продуцируя молочную и другие кислоты. Как правило, лактобактерии не провоцируют возникновение заболеваний и уже более 100 лет считаются непатогенными представителями интестинальной и урогенитальной флоры.
Исследования пробиотиков
Учитывая способность некоторых пробиотических штаммов балансировать состав интестинальной микробиоты, улучшать функционирование слизистого барьера и восстанавливать здоровье влагалища, были проведены многочисленные исследования для изучения эффективности пробиотиков у пациентов с ИМП. В нескольких исследованиях рассматривалось влияние перорального приема пробиотика на состояние больных ИМП; доказано, что пероральный прием является более эффективным, чем применение вагинальных суппозиториев. Проведены небольшие исследования, в которых пробиотики назначались при конкрементах в почках, спровоцированных тонкокишечной гипероксалурией, рецидивирующем кандидозном вульвовагините, ИМП. В других исследованиях получены обнадеживающие результаты у пациентов с нейрогенным мочевым пузырем, в которых в качестве пробиотика использовались штаммы непатогенной E. coli. В исследовании, выполненном Darouiche и соавт., изучалась эффективность топического применения пробиотиков у пациентов с нейрогенным мочевым пузырем и применялись полезные штаммы E. coli. Авторы отметили снижение частоты рецидивов ИМП у пациентов, у которых удалось достичь успешной колонизации мочевого пузыря. Кроме того, снизилась частота симптоматических ИМП у больных, пользовавшихся мочевыми катетерами, обработанными пробиотиками, по сравнению с катетерами, обработанными антибактериальными средствами. В пилотном исследовании женщинам назначали лактобактерии в виде вагинальных суппозиториев, что способствовало уменьшению случаев E. coli-ассоциированных ИМП с 5,0±1,6 до 1,3±1,2 эпизода (р<0,0007) на протяжении 12 мес.
В исследовании, предполагавшем пероральный прием пробиотика, содержавшего два штамма (Lactobacillus rhamnosus и L. reuteri), постменопаузальных женщин (n=280) рандомизировали для приема пробиотика или проведения стандартной антибактериальной терапии рецидива ИМП. Лечение продолжалось на протяжении 12 мес с последующим 3-месячным наблюдением. В другом исследовании, проведенном в США, пременопаузальных женщин (n=100) рандомизировали для приема плацебо или топических лактобактерий (L. crispatus) во влагалищной капсуле в течение 3 мес с последующим 6-месячным наблюдением. Ни в одном из этих исследований не сравнивалась эффективность пре- и постменопаузальной терапии пробиотиками, на основании чего было сделано заключение, что применение пробиотиков не предполагает полной эрадикации инфекционного начала, но уменьшает частоту рецидивов и предупреждает развитие бактериальной резистентности к антиымикробным препаратам. В недавнем рандомизированном двойном слепом исследовании сравнивалась эффективность вагинальных таблеток, содержащих лактобациллы, и рН таблеток в отношении здоровья влагалища и синтеза воспалительных цитокинов. Авторы пришли к выводу, что вагинальные таблетки, содержащие лактобациллы, способны излечить вагинальную инфекцию и уменьшить активность воспалительного процесса во влагалище.
В недавнем метаанализе, выполненном Grin и соавт., анализировались результаты применения пробиотиков у пременопаузальных женщин с рецидивами ИМП. Ученые сделали вывод, что пробиотические штаммы лактобактерий являются безопасными и эффективными в профилактике рецидива ИМП у взрослых женщин, но перед принятием какого-либо окончательного решения необходимо проведение рандомизированных контролированных исследований, поскольку представленная в данном метаанализе популяция была небольшой. В 2011 г. Stapleton и соавт. представили результаты рандомизированного плацебо-контролированного исследования II фазы, в котором пременопаузальных женщин с рецидивом ИМП (n=100) рандомизировали для интравагинального введения пробиотика L. crispatus в течение 10 нед; они сообщили о значительном сокращении частоты рецидивов ИМП у участниц, у которых удалось достичь высокой концентрации L. crispatus во влагалище, по сравнению с женщинами из группы плацебо с недостоверным уменьшением ИМП. Авторы установили, что L. crispatus ассоциирована со снижением симптоматических ИМП.
Учитывая огромную нагрузку на пациентов, а также научные и экономические проблемы, связанные с рецидивами ИМП, изучение пробиотиков имеет потенциально решающее значение как для пациентов, так и для клинической науки. Лабораторные и клинические исследования живых микроорганизмов открыли большую область для проведения углубленных научных изысканий и испытаний.
С эволюционной точки зрения живые микроорганизмы обеспечили организму человека такие важные функции, как пищеварение и модуляция иммунной системы. Человеческому организму нет необходимости разрабатывать эти функции, он использует флору микроорганизмов в качестве метаболического органа, настроенного на особенности его физиологии и расположенного на его наружных поверхностях. Бактериальная флора кишечника весит приблизительно 1-2 кг и считается метаболически такой же важной, как и печень.
Поскольку живые микроорганизмы, используемые в качестве пробиотиков, часто изолированы от человеческой флоры, исследования специфических пробиотиков могут помочь понять роль этих бактерий в экосистеме человеческого организма.
Выводы
Рецидивы ИМП являются серьезной проблемой у женщин всех возрастов. Частое и неизбирательное применение антибиотиков привело к развитию выраженной антибиотикорезистентности, что, в свою очередь, явилось основанием для изучения новых терапевтических средств, предназначенных для профилактики и снижения частоты возникновения рецидива ИМП. Несмотря на многообещающие перспективы, имеющихся литературных данных недостаточно, чтобы рекомендовать использование пробиотиков для профилактики рецидивов ИМП, поскольку широкомасштабных клинических исследований не проводилось. Недавние исследования показали, что пробиотические штаммы лактобактерий являются эффективными и безопасными средствами для профилактики рецидивов ИМП, но пока не могут рекомендоваться для широкого применения в связи с отсутствием доказательств, полученных в крупномасштабных клинических исследованиях. Работы, проанализированные нами, подтверждают что суппозитории, содержащие лактобактерии, могут безопасно применяться: незначительные нежелательные явления возникали у небольшого количества пациентов. Мы также обнаружили отсутствие серьезных нежелательных явлений, вызываемых лактобактериями, в исследованиях, проведенных с участием здоровых пременопаузальных женщин, что подтверждает целесообразность проведения дополнительных клинических исследований.
До завершения дальнейших исследований следует рассматривать целесообразность применения суппозиториев, содержащих пробиотические штаммы лактобактерий, но пока их не следует настоятельно рекомендовать. Пробиотики могут считаться безопасной альтернативой антимикробным препаратам для профилактики ИМП у женщин высокого риска при наличии резистентности к антибиотикам.
Статья печатается в сокращении.
Gupta V. et al. Recurrent urinary tract infections in women: How promising is the use of probiotics? 2017. DOI: 10.4103/ijmm.IJMM_16_292
Перевела с англ. Лада Матвеева
Медична газета «Здоров’я України 21 сторіччя» № 9 (430), травень 2018 р.