4 червня, 2018
Пембролізумаб в ад’ювантній терапії меланоми III стадії
Меланома III стадії становить новоутворення будь-якої товщини з розповсюдженням у регіонарні лімфатичні вузли. Стандартним лікуванням таких хворих є видалення первинної пухлини та всіх регіонарних лімфатичних вузлів. Для зменшення ризику рецидиву після хірургічного втручання застосовують ад’ювантну терапію. Відповідно до настанов NCCN (січень 2018 р.), в ад’ювантній системній терапії меланоми можна використовувати інтерферони, біохіміотерапію (поєднання препаратів інтерферону, інтерлейкіну-2 та хіміотерапії) та інгібітори імунних контрольних точок [1].
Пембролізумаб (Кітруда®, MSD) – це препарат гуманізованих моноклональних антитіл проти PD-1 (білка клітинної смерті 1), інгібітор імунної контрольної точки, який блокує зв’язування PD-1 з лігандами PD-L1 та PD-L2 і таким чином відновлює здатність імунної системи атакувати та знищувати ракові клітини. Пембролізумаб є першим протипухлинним препаратом, схваленим Управлінням з контролю якості харчових продуктів і лікарських препаратів США (FDA) для лікування пацієнтів з нерезектабельними і метастатичними солідними пухлинами з певними генетичними аномаліями незалежно від локалізації чи гістологічного типу новоутворення.
 Раніше на підставі результатів дослідження KEYNOTE-006 пембролізумаб був схвалений для застосування при нерезектабельній і метастатичній меланомі. Метою міжнародного багатоцентрового дослідження III фази KEYNOTE-054 було порівняти ефективність пембролізумабу та плацебо в ад’ювантній терапії у пацієнтів з видаленою меланомою III стадії з високим ризиком рецидиву (рис. 1).
Раніше на підставі результатів дослідження KEYNOTE-006 пембролізумаб був схвалений для застосування при нерезектабельній і метастатичній меланомі. Метою міжнародного багатоцентрового дослідження III фази KEYNOTE-054 було порівняти ефективність пембролізумабу та плацебо в ад’ювантній терапії у пацієнтів з видаленою меланомою III стадії з високим ризиком рецидиву (рис. 1).
У дослідженні KEYNOTE-054 брали участь пацієнти віком від 18 років з гістологічно верифікованою меланомою шкіри IIIA, IIIB або IIIC стадії за класифікацією AJCC (2009). Основними критеріями включення були:
- повністю видалені первинне вогнище та метастази в регіонарних лімфатичних вузлах;
- хороший функціональний стан (ECOG 0-1);
- високий ризик рецидиву меланоми;
- відсутність аутоімунних захворювань, неконтрольованих інфекцій, потреби в системному введенні кортикостероїдів і попередньої системної терапії меланоми;
- наявність матеріалу метастатично ураженого лімфатичного вузла для визначення експресії PD-L1.
Пацієнтів рандомізували 1:1 для проведення внутрішньовенних інфузій пембролізумабу 200 мг або плацебо через кожні 3 тижні до отримання 18 доз (приблизно 1 рік), розвитку рецидиву захворювання, неприйнятної токсичності, істотного відхилення від протоколу або відкликання інформованої згоди.
Первинною кінцевою точкою була безрецидивна виживаність (БРВ) у загальній популяції та в пацієнтів з PD-L1-позитивними пухлинами (експресія PD-L1 у >1% пухлинних клітин за даними імуногістохімії). Вторинні кінцеві точки включали виживаність без віддалених метастазів, загальну виживаність, безпеку та якість життя. БРВ визначали як час від рандомізації до першого рецидиву (локального, регіонарного чи віддаленого) або смерті.
У дослідження залучили 123 клінічні центри у 23 країнах, які з серпня 2015 по листопад 2016 року відібрали для участі 1019 пацієнтів. Середній вік хворих становив 54 роки, переважали чоловіки.
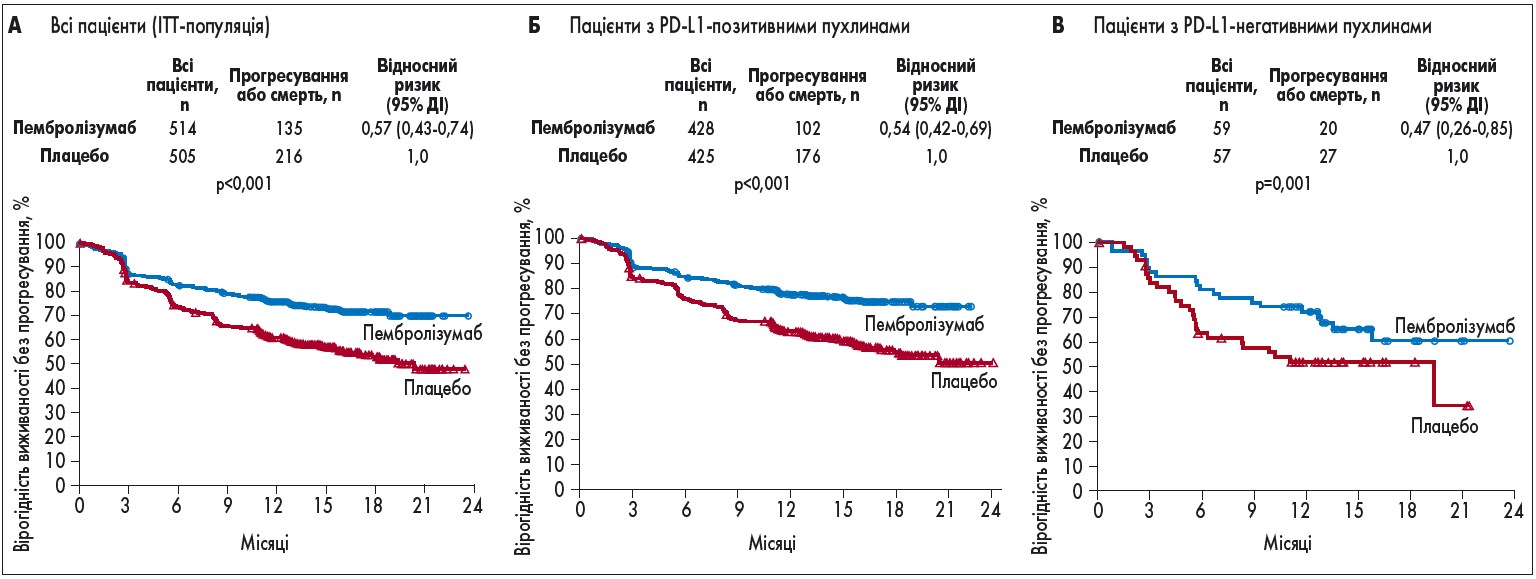
Рис. 2. Виживаність без прогресування в загальній популяції та залежно від статусу PD-L1
У загальній популяції (ITT; пацієнти, які отримали принаймні 1 дозу досліджуваного препарату) 12-місячна БРВ становила 75,4% у групі пембролізумабу та 61,0% у групі плацебо (рис. 2А). Це означає, що введення пембролізумабу сприяло зниженню ризику рецидиву або смерті на 43% (р<0,001). Після 18 міс різниця між групами стала ще помітнішою: БРВ становила 71,4 та 53,2% при лікуванні пембролізумабом або плацебо відповідно.
У підгрупі 853 пацієнтів з PD-L1-позитивними пухлинами 12-місячна БРВ дорівнювала 77,1% у групі пембролізумабу та 62,6% у групі плацебо (рис. 2Б). У цих пацієнтів застосування пембролізумабу сприяло зниженню ризику рецидиву або смерті на 46% (р<0,001). Так само високу ефективність пембролізумаб продемонстрував і в підгрупі хворих з PD-L1-негативними пухлинами (рис. 2В).
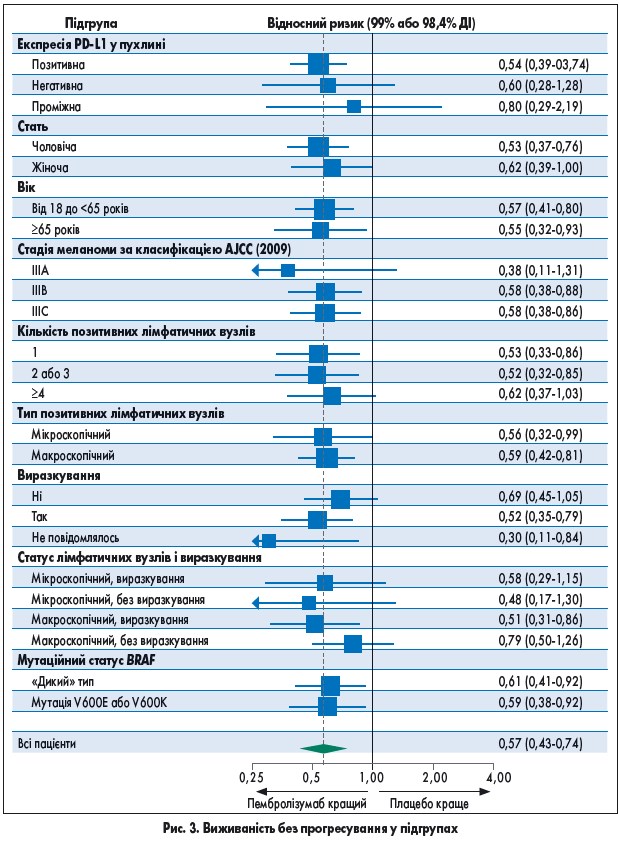 Значне підвищення БРВ при лікуванні пембролізумабом спостерігалося в усіх підгрупах, сформованих з урахуванням початкових характеристик (рис. 3). Зокрема, користь від застосування пембролізумабу статистично не відрізнялась у пацієнтів з меланомою IIIA, IIIB чи IIIC стадії, мікро- або макроскопічним ураженням лімфатичних вузлів, наявністю чи відсутністю виразкування. Статус BRAF, стать та індекс маси тіла не мали будь-якого впливу на різницю БРВ між групами пембролізумабу та плацебо (рис. 3).
Значне підвищення БРВ при лікуванні пембролізумабом спостерігалося в усіх підгрупах, сформованих з урахуванням початкових характеристик (рис. 3). Зокрема, користь від застосування пембролізумабу статистично не відрізнялась у пацієнтів з меланомою IIIA, IIIB чи IIIC стадії, мікро- або макроскопічним ураженням лімфатичних вузлів, наявністю чи відсутністю виразкування. Статус BRAF, стать та індекс маси тіла не мали будь-якого впливу на різницю БРВ між групами пембролізумабу та плацебо (рис. 3).
Втома/астенія та діарея спостерігалися з однаковою частотою в обох групах. Небажані події 3-5 ступеня тяжкості, пов’язані з лікуванням, реєстрували у 14,7% пацієнтів групи пембролізумабу та 3,4% – групи плацебо.
Імунозалежні небажані події частіше відзначали при лікуванні пембролізумабом (37,3% проти 9,0%), більшість таких подій мали 1 або 2 ступінь тяжкості. Серед 43 імунозалежних подій 3-4 ступеня тяжкості, які спостерігали у 36 (7,1%) пацієнтів групи пембролізумабу, 34 події повністю минули з нормалізацією стану, зокрема 21 – упродовж 2 міс після введення останньої дози пембролізумабу.
Таким чином, у пацієнтів з видаленою меланомою III стадії ад’ювантна терапія пембролізумабом значно подовжує БРВ і добре переноситься. Введення пембролізумабу зменшувало ризик рецидиву або смерті на 43% в загальній популяції, на 46% – у пацієнтів з PD-L1-позитивною пухлиною та на 53% – у хворих з PD-L1-негативною пухлиною. Отже, для призначення пембролізумабу як ад’ювантної терапії у хворих на меланому не потрібно визначати PD-L1 статус пухлини.
На думку професора Брайана Гастмана, співавтора настанов з лікування меланоми NCCN, результатів дослідження KEYNOTE-054 щодо БРВ буде достатньо, щоб FDA схвалило використання пембролізумабу в ад’ювантній терапії пацієнтів з меланомою [2]. Порівнюючи ефективність пембролізумабу та ніволумабу (ще одного анти-PD-1-препарату, що застосовується при меланомі), Б. Гастман зазначив, що ці препарати є дуже подібними, проте лікування пембролізумабом є більш зручним для пацієнтів у зв’язку з меншою частотою інфузій – кожні 3 тижні замість 2. Крім того, попри те що ніволумаб схвалений FDA для ад’ювантної терапії всіх пацієнтів з меланомою III стадії, його застосування у пацієнтів з меланомою IIIA стадії не вивчалося. Натомість пембролізумаб продемонстрував зіставну користь у пацієнтів з меланомою IIIA, IIIB та IIIC стадії.
Результати дослідження KEYNOTE-054 були опубліковані в онлайн-версії New England Journal of Medicine [3] та представлені на щорічному конгресі Американської асоціації з вивчення раку [4].
Література
- Melanoma. NCCN Clinical Practice Guidelines in Oncology. Version 2.2018 – January 19, 2018.
- The Benefits of Adjuvant Immunotherapy in Melanoma. www.cancertherapyadvisor.com. Published April 26, 2018. Accessed May 21, 2018.
- Eggermont A.M.M. et al. Adjuvant pembrolizumab versus placebo in resected stage III melanoma. N Engl J Med. 2018 Apr 15. doi: 10.1056/NEJMoa1802357 [Epub ahead of print].
- Eggermont A.M.M. et al. Pembrolizumab versus placebo after complete resection of high-risk stage III melanoma: efficacy and safety results from the EORTC 1325-MG/Keynote 054 double-blinded phase III trial. Oral presentation at: 2018 American Association for Cancer Research Annual Meeting; April 14-18, 2018; Chicago, IL.
Підготував Олексій Терещенко
Тематичний номер «Онкологія» № 2 (53), травень 2018 р.